多重实时荧光定量PCR分析转基因烟草外源基因拷贝数
2017-09-27余婧邹颉付强郭玉双林世锋赵杰宏
余婧,邹颉,付强,郭玉双,林世锋,赵杰宏
贵州省烟草科学研究院,烟草行业烟草分子遗传重点实验室,贵州省贵阳市龙滩坝路29号 550081
多重实时荧光定量PCR分析转基因烟草外源基因拷贝数
余婧,邹颉,付强,郭玉双,林世锋,赵杰宏
贵州省烟草科学研究院,烟草行业烟草分子遗传重点实验室,贵州省贵阳市龙滩坝路29号 550081
【目的】采用多重实时荧光定量PCR方法在一个反应内同时检测转基因烟草中插入外源基因35S、NOS、NPT II的拷贝数。【方法】将转基因阳性参照烟草基因组DNA经梯度稀释,通过多重荧光定量PCR反应同时获得烟草内源参照基因NR、外源基因35S、NOS、NPT II的相关性标准曲线方程,将待测株系外源基因的Ct值代入标准曲线方程后估算其拷贝数。【结果】获得了上述4个基因的标准曲线,其R2均接近于1,相关性较高。在检测的六个转基因株系中初筛到3株3个外源基因均为单拷贝的株系。【结论】可使用该方法对转基因烟草外源基因插入拷贝数进行估算,为获得稳定遗传材料提供初筛依据。
转基因烟草;多重实时荧光定量PCR;外源基因;拷贝数
1983年,第一株转基因烟草问世[1],烟草作为植物分子生物学研究的模式植物,30多年来,人们对烟草的转基因研究从未停歇,包括将烟草自身基因进行超量表达以验证其基因功能[2-4],外源基因在烟草中表达后的功能验证[5-7]等,这些研究均需使用转基因技术。然而,无论是内源基因的过表达或外源基因的转入和表达,转基因植物中插入基因的拷贝数是影响其表达水平及遗传稳定性的主要因素,外源基因的拷贝数过多会导致基因沉默或不能稳定表达。因此,通常应筛选出含有拷贝数为1~2个,最好是单拷贝外源基因的转基因植株[8-9]。
检测外源基因拷贝数主要采用Southern blot技术,该方法稳定、可靠,但其价格昂贵、程序复杂、耗时较长、需要大量高纯度DNA,灵敏度相对较低,且对实验技术条件要求较高[10]。近年来,研究人员开始利用实时荧光定量PCR检测外源基因拷贝数,该方法经PCR反应获得样品Ct值并制作标准曲线,根据起始模板数的相关性方程,将样品的Ct 值代入该方程便可计算目的基因的起始模板数,将其与内源参照基因起始模板数作比较,便可估算出基因组中外源基因的拷贝数[11]。目前,已有多篇关于实时荧光定量PCR检测转基因植物中外源基因拷贝数的报道,但均为单重荧光定量PCR[12-15],即内源基因及外源基因需分别做二次标准曲线,待测样品内、外源靶标的检测也在不同PCR管内进行,这对于定量要求较高的定量PCR而言,易受加样误差的影响。多重PCR技术是在同一PCR管中同时加入多对引物,只需1次反应便能同时检测2种以上靶标序列[16],该方法已用于动物源成分检测[17]、转基因作物检测[18]、食品中细菌的检测[19]等,而用多重实时荧光定量PCR检测转基因烟草外源基因拷贝数的相关文献未见报道。
本研究建立了一种使用多重实时荧光定量PCR分析转基因烟草外源基因拷贝数的方法,该体系在一次PCR反应内便完成了以烟草内源硝酸还原酶基因NR[20]为内参基因、外源基因35S启动子、终止子NOS及卡那霉素抗性标记基因NPT II标准曲线的制备及待测样品Ct值的检测工作,并根据Ct值及公式测算了外源基因拷贝数。由于本研究在1个反应内便能获得上述4个基因的Ct值,这可消减内参基因与目的基因在不同PCR反应间产生的加样误差。另外,对3个外源基因拷贝数同时进行检测,可排除部分可能发生基因重排而未稳定遗传的株系。因此,该方法可用于估算转基因烟草外源基因插入拷贝数,为初筛并获得稳定遗传材料提供技术支撑。
1 材料与方法
1.1 实验材料
转基因烟草株系T31为阳性参照株系,其遗传转化载体由pBI121改造,该载体含有外源基因35S、NOS、NPT II,T31种子经卡那霉素抗性测试已稳定遗传至T6代;A1-A6待测单株为T5代转基因材料;阴性对照为贵烟1号。上述材料于贵州省烟草科学研究院人工气候室种植,T31取群体叶片,A1-A6取单株叶片用于DNA提取。
1.2 实验试剂
植物基因组DNA提取试剂盒购自天根生化科技(北京)有限公司,用于荧光定量PCR的Premix Ex Taq™(Probe qPCR)购自宝生物工程(大连)有限公司。
1.3 实验设备
ViiA 7 实时荧光定量PCR仪(美国ABI公司);NanoDrop 2000超微量分光光度计(美国Thermo Fisher公司);离心机(德国Eppendorf公司);C1000 Touch PCR仪( 美 国BIO-RAD公 司);ChemiDocXRS凝胶成像系统(美国BIO-RAD公司)。
1.4 实验方法
1.4.1 定性PCR检测
引物序列、反应体系及条件参照余婧等[16],引物由上海捷瑞生物工程有限公司合成。
1.4.2 烟草基因组DNA提取
采用试剂盒提取烟草基因组DNA用于荧光定量PCR测试,提取方法参照试剂盒使用说明书。待测样品DNA经NanoDrop 2000测定浓度及纯度后统一用ddH2O稀释至100 ng/μL,用于制备标准曲线的T31 DNA测定浓度后备用。本研究中所提取DNA的OD260/OD280比值均在1.80~1.90之间。
1.4.3 Southern印迹杂交
阳性参照株系T31外源基因35S启动子Southern印迹杂交参照J.萨姆布鲁克等[21],基因组DNA经EcoRI、HindIII、NdeI、TaqI四组酶酶切。待测株系基因组DNA经HindIII酶切,对外源基因NPT II进行Southern印迹杂交。
1.4.4 定量PCR标准曲线制备
用ddH2O按2倍浓度梯度稀释T31的基因组DNA制作标准曲线,标准曲线设置5个点,3次重复获得标准曲线。
1.4.5 多重定量 PCR反应体系及条件
20μL PCR反应体系(4个靶标的引物及探针均加入同一PCR管中):Premix Ex Taq 10μL,探针10 μM,上下游引物各 10 μM,50×ROX Dye II 0.4 μL,DNA 2 μL;PCR反 应条 件:95℃ 30s;95℃5s,60℃ 34s,40个循环。引物及探针见表1,由上海捷瑞生物工程有限公司合成。

表1 多重定量PCR引物、探针序列Tab.1 Multiplex real-time PCR primer and probe sequence
1.4.6 转基因烟草外源基因拷贝数估算
定量PCR结束后,获得标准曲线及待测样品Ct值,根据NR及35S、NOS、NPT II的Ct值并依据公式X0/R0=10[(Ct,X-IX)/SX]-[(Ct,R-IR)/SR](其中Ct,X为外源基因的 Ct 值,IX 为外源基因标准曲线的截距,SX为外源基因标准曲线的斜率;Ct,R为内参基因的Ct值,IR为内参基因标准曲线的截距,SR为内参基因标准曲线的斜率),拷贝数即根据X0/R0的平均值进行估算[24]。
2 结果与分析
2.1 转基因阳性植株定性PCR检测
为确保参试样品为转基因阳性,提取待测植株叶片DNA为模板进行多重定性PCR扩增目的基因35S、NOS、NPT II。扩增产物经2%琼脂糖凝胶电泳(图1),A1-A6号样品均带有目的基因35S(345bp)、NOS(199bp)、NPT II(490bp)特异性扩增片段,初步确定6个单株均为转基因阳性单株,另外,内源参照基因NR(137bp)扩增条带单一,特异性好,表明DNA提取质量附合PCR检测要求。
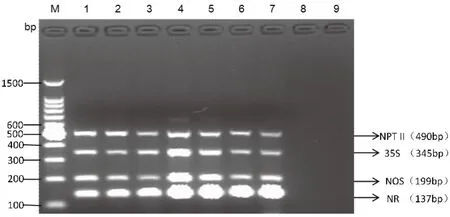
图1 多重PCR定性检测电泳结果Fig.1 Results of multiplex qualitative PCR detection
2.2 阳性参照株系35S Southern印迹拷贝数检测
为避免2个拷贝所在片段大小相同的巧合,分别采用EcoR I、HindIII、NdeI、TaqI四组酶对阳性参照株系T31基因组DNA进行酶切。插入基因35S经四组酶切的Southern结果均有杂交目的条带(图2),这表明35S已被整合到T31阳性参照株系基因组中,且为单拷贝插入。
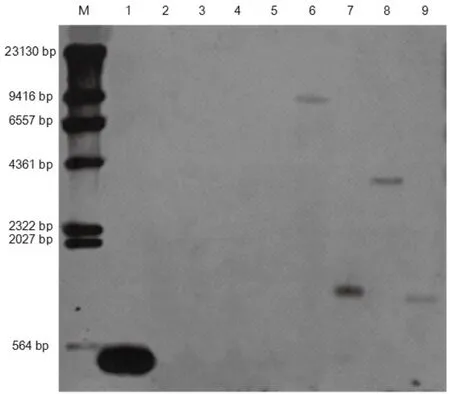
图2 阳性参照株系T31 35S启动子插入拷贝数Southern检测结果Fig.2 Southern detection results for 35S promoter insertion copy number of the positive reference plants T31
2.3 标准曲线制作及待测样品Ct值
T31基因组DNA测定浓度后直接用ddH2O 2倍稀释后制作3组重复标准曲线(本研究T31 DNA初始浓度为170 ng/μL),以模板起始拷贝数对数为X轴,以Ct值为Y轴,在一次PCR反应中同时获得到了内源参照基因NR及外源基因35S、NOS、NPT II的扩增曲线(图3)及标准曲线(图4),四条标准曲线扩增效率在99.565%~102.748之间,相关系数R2在0.997~0.999之间,相关性较好,可用于目的基因拷贝数的检测。在待测样品Ct值的测试中,4个基因Ct值的标准偏差在0.02~0.17之间,相对标准偏差在0.10%~0.84%之间,说明Ct值重复性良好,阳性参照株系、对照株系及各待测单株Ct值见表2。

图3 多重荧光定量PCR扩增曲线Fig.3 Multiplex real-time PCR amplification curve
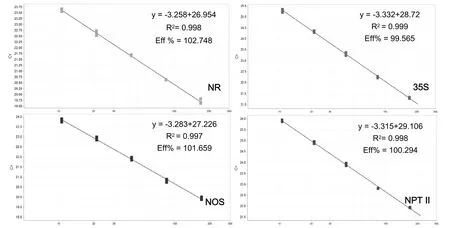
图4 多重荧光定量PCR标准曲线Fig.4 Multiplex real-time PCR standard curve

表2 各株系扩增靶标Ct值Tab.2 Ct value of target gene
2.4 待测株系外源基因插入拷贝数的估算
以阳性株系T31外源基因35S的Southern检测结果及符合高世代稳定遗传的标准为参照,以T31的35S、NOS、NPT II插入拷贝数均为1来比较、估算待测基因拷贝数。按1.4.6中公式X0/R0=10[(Ct,X-IX)/SX]-[(Ct,R-IR)/SR]估算外源基因拷贝数,实验中,以A3样品为例,跟据内源基因NR及外源基因35S、NOS、NPT II的标准曲线(图4),将A3样品Ct值(表2)代入公式计算三个外源基因 的 拷 贝 数:35S0=10[(21.11-28.72)/-3.332]-[(20.42-26.954)/-3.258],NOS0=10[(19.14-27.226)/-3.283]-[(20.42-26.954)/-3.258],NPT II0=10[(21.45-29.106)/-3.315]-[(20.42-26.954)/-3.258]计算出35S0=1.9,NOS0=2.9,NPT II0=2.0,即A3样品35S、NOS、NPT II插入拷贝数的估算值分别为1.9、2.9、2.0。在对待测样品A1-A6各外源基因拷贝数的估算中(表3),A1、A3二个单株部分外源基因插入拷贝数为2~3个拷贝,这表明A1、A3为外源基因多拷贝插入,而A4拷贝数估算值不到1,这可能由于外源基因发生了重排、丢失,为不稳定遗传[25]。A2、A5、A6三个单株三个外源基因插入拷贝数估算值均1,为单拷贝。
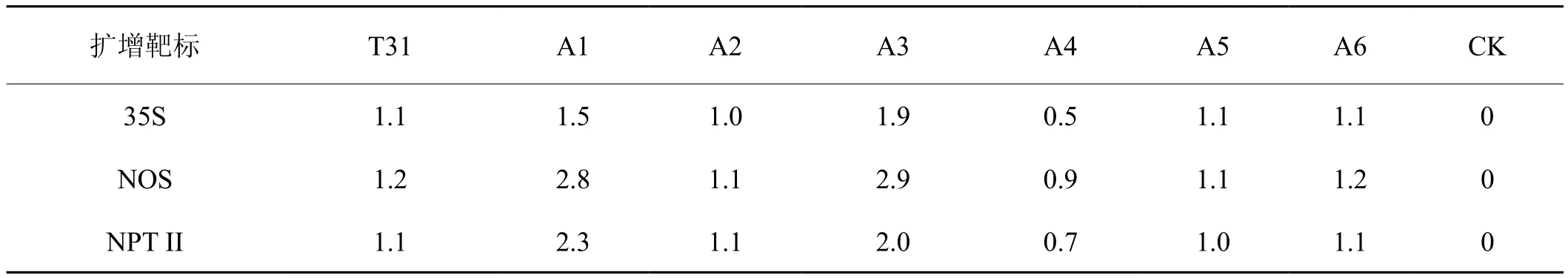
表3 外源基因插入拷贝数估算Tab.3 Estimation of exogenous gene insertion copy number
2.5 待测株系NPT II Southern印迹杂交拷贝数检测
为了验证经多重荧光定量PCR所估算的外源基因插入拷贝数与Southern杂交的结果是否一致,对各株系的外源基因NPI II进行了Southern印迹检测,结果表明(图5),株系A2、A4、A5、A6中NPT II基因的Southern印迹检测拷贝数为1个,其中A4在定量PCR中估算值不足1个拷贝,A4可能为杂合株,并未稳定遗传。而株系A1、A3中NPT II基因的Southern印迹检测拷贝数为2个,这与定量PCR中所估算的NPT II基因的插入拷贝数一致。
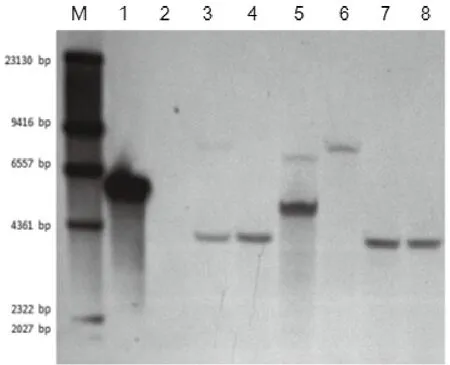
图5 待测株系NPT II插入拷贝数Southern检测结果Fig.5 Southern detection of NPT II insertion copy number
3 讨论
本研究建立了一种多重实时荧光定量PCR,该方法通过一次PCR反应便可同时获得烟草内源参照基因NR,外源基因35S、NOS、NPT II的标准曲线,并通过标准曲线及待测样品Ct值计算出待测样品外源基因拷贝数。根据文献报道[26],用实时荧光定量PCR检测外源基因拷贝数,其阳性参照植株必须是纯度为100%的转基因植物样品,本研究选取了本实验室高世代稳定遗传材料T31作为转基因阳性参照株系,在Southern测试中,T31外源基因35S的插入拷贝数为1,因此,实验以T31的35S、NOS、NPT II插入拷贝数均为1来比较、估算出待测样品3个外源基因的拷贝数。苏慧慧等[12]指出转基因植物中同一单株不同外源基因拷贝数不一致,这可能是发生了基因重排或缺失,因此,我们的多重荧光定量PCR特意对3种外源基因的拷贝数同时进行估算,能有效排除因外源基因的重排或缺失而造成植株遗传不稳定的可能性。值得提出的是,我们后期特意对A1-A6后代种子萌发进行卡那霉素抗性测试,单拷贝单株A2、A5、A6萌发率为100%,而A1、A3、A4均为80%左右,这表明该3个株系可能由于外源基因多拷贝插入或重排、缺失,并未稳定遗传,这与我们估算的外源基因是否为单拷贝结果一致。因此,本方法可用于转基因烟草外源基因插入拷贝数的估算,为初筛并获得稳定遗传材料提供技术支撑。
[1]赵彦平,赵春海.植物转基因育种的分析与研究[J].生物技术通报,2011(3):72-77.ZHAO Yanping, ZHAO Chunhai.Research and analysis of transgenic breeding in plants[J].BIOTECHNOLOGY BULLETIN ,2011(3):72-77.
[2]Mi SL, Hwang S.Cyc07, enhances arsenite tolerance by reducing As levels in Nicotianatabacum, and Arabidopsis thaliana[J].Plant Biotechnology Reports, 2012, 6(4):391-395.
[3]李洋,李明,岳玮,等.烟草NtHCT基因对次生代谢物质绿原酸和类黄酮合成的影响[J].中国烟草学报,2015,21(6):127-131.LI Yang, LI Ming, YUE Wei, et al.Effect ofNtHCTgene on synthesis of chlorogenic acid and fl avonoid in tobacco[J].ActaTaba cariaSinica,2015,21(6):127-131.
[4]张兴坦.烟草MAPK基因的功能研究[D].重庆大学,2015.ZHANG Xingtan.Functional Characterization of Nicotianatabacum MAPK genes[D].Chongqing University, 2015.
[5]Cai R, Zhao Y, Wang Y, et al.Overexpression of a maize WRKY58,gene enhances drought and salt tolerance in transgenic rice[J].Plant Cell, Tissue and Organ Culture (PCTOC), 2014, 119(3):565-577.
[6]Zhou M, Wu L, Liang J, et al.Cold-induced modulation of CbICE53 gene activates endogenous genes to enhance acclimation in transgenic tobacco[J].Molecular Breeding, 2012, 30(4):1611-1620.
[7]Xu Q, Nan G, Ruan M, et al.Ectopic expression of the PttKN1,gene induced altered leaf morphology and hormonal levels in transgenic tobacco[J].Journal of Plant Biochemistry and Biotechnology, 2015, 24(2):197-203.
[8]Weng H, Pan A, Yang L, et al.Estimating number of transgene copies in transgenic rapeseed by real-time PCR assay withHMG I/Y as an endogenous reference gene[J].Plant Molecular Biology Reporter, 2004, 22(3):289-300.
[9]王海慧, 田源, 白国辉,等.转基因植物遗传稳定性影响因素的研究现状[J].贵州农业科学, 2013, 41(9):5-8.WANG Haihui, TIAN Yuan, BAI Guohui,et al.Advances in influencing factors of genetic stability of transgenic plants[J].Guizhou Agricultural Sciences,2013, 41(9):5-8.
[10]罗滨,陈永康,王莹.植物外源基因拷贝数及插入位点的检测方法与技术[J].河南师范大学学报(自然版),2012,40(6):111-116.LUO Bing, CHEN Yongkang, WANG Ying.Methods and techniques for estimating the copy number and fl anking sequences of exogenous gene in transgenic plants[J].Journal of Henan Normal University(Natural Science Edition),2012,40(6):111-116.
[11]李敏, 汪洋, 张银萍,等.TaqMan探针与SYBR Green实时定量PCR法检测转基因植物外源基因拷贝数的差异分析[J].安徽农业大学学报, 2012, 39(4):568-570.LI Min, WANG Yang, ZHANG Yinping,et al.Variance analysis between TaqMan probe and SYBR Green real-time quantitative PCR for determining the copy number of transgene in transformed plants[J].Journal of Anhui Agricultural University, 2012,39(4):568-570.
[12]苏慧慧,李涛,谢雯琦,等.基于实时荧光定量PCR对转基因樱桃番茄外源基因拷贝数的检测[J].分子植物育种,2015,13(2):345-354.SU Huihui, LI Tao, XIE Wenqi, et al.Detecting exogenous gene copy numbers of exogenous gene in transgenic tomato based on fluorescent quantitative real-time PCR[J].Molecular Plant Breeding,2015,13(2):345-354.
[13]Yang X.Analysis of the copy number of exogenous genes in transgenic cotton using real-time quantitative PCR and the 2-△△CTmethod[J].African Journal of Biotechnology, 2012, 11(23):6226-0233.
[14]甄贞,段俊枝,于艳波,等.转基因小麦B73-6-1外源基因拷贝数的确定[J].河南农业科学,2016,45(4):19-22.ZHEN Zhen, DUAN Junzhi, YU Yangbo,et al. Determination of exogenous gene copy number for transgenic wheat B73-6-1[J].Journal of Henan Agricultural Sciences,2016,45(4):19-22.
[15]韩强,刘瑞芳,陆玲鸿,等.实时荧光PCR检测转基因大豆外源基因的拷贝数[J].核农学报, 2016, 30(4):646-653.HAN Qing, LIU Ruifang, LU Linghong, et al.Dectection of transgene copy number in transgenic soybean by real-time fluorescence quantitative PCR[J].Journal of Nuclear Agricultural Sciences,2016, 30(4):646-653.
[16]余婧,郭玉双,林世锋,等.多重PCR技术快速检测烤后烟叶转基因成分[J].生物技术通报, 2015, 31(7):64-68.YU Jing, GUO Yushuang, LIN Shifeng, et al.A multiplex PCR for rapid detection of genetically modi fi ed ingredient in fl ue-cured tobacco[J].BIOTECHNOLOGY BULLETIN,2015, 31(7):64-68.
[17]Iwobi A, Sebah D, Kraemer I, et al.A multiplex real-time PCR method for the quanti fi cation of beef and pork fractions in minced meat[J].Food Chemistry, 2015, 169(169):305-313.
[18]Samson, Cristina M, Gulli, et al.Multiplex real-time PCR assays for simultaneous detection of 'maize; MON810 and GA21 in food samples[J].Food Control, 2013, 30(2):518-525.
[19]Feng C, Mansouri S, Bluhm B H, et al.Multiplex real-time PCR assays for detection of four seedborne spinach pathogens.[J].Journal of Applied Microbiology, 2014, 117(2):472-84.
[20]Bindler G, Borne F D, Gadani F et al.Task Force Genetically Modi fi ed Tobacco-Detection Methods [C]// CORESTA.1999.
[21]J.萨姆布鲁克, D.W.拉塞尔.分子克隆实验指南(第三版)[M].科学出版社, 2002.Sambrook J J, Russell D W.Molecular cloning: a laboratory manual(Third Edition) [M].Academic press, 2002.
[22]中国国家标准化管理委员会.GB/T 24310-2009《烟草及烟草制品转基因检测方法》[S].北京:中国标准出版社,2009.Standardization Administration of the People's Republic of China.GB/T 24310-2009 Tobacco and tobacco products-detecting method of genetically modified organism contents[S].Beijing: China Standards Press, 2009.
[23]Wang F, Zhang X, Feng J, et al.Establishment of a quadruplex real-time PCR for screening of genetically modi fi ed tomatoes[J].European Food Research and Technology, 2014, 238(4):683-690.
[24]王爱民.实时荧光定量PCR(TaqMan)法测定外源基因的拷贝数[J].广西植物, 2009, 29(3):408-412.WANG Aiming.Estimating copy number of transgenic gene by real-time fl uorescent quantitative PCR(TaqMan)[J].Guihaia,2009,29(3):408-412.
[25]金万梅, 潘青华, 尹淑萍,等.外源基因在转基因植物中的遗传稳定性及其转育研究进展[J].分子植物育种, 2005, 3(6):864-868.JIN Wanmei, PAN Qinghua, YIN Shuping, et al.Progress of the genetic stability and breeding behavior of foreign gene in genetically modified plants[J].Molecular Plant Breeding, 2005,3(6):864-868.
[26]刘海礁, 王哲, 李雪君,等.转fps基因烟草纯合系的获得及其特性分析[J].中国烟草学报, 2006, 12(4):41-43.LIU Haijiao, WANG Zhe, LI Xuejun, et al.A method of obtaining fps transgenic homozygous lines in tobacco and the analysis of their characteristics[J].ActaTabacariaSinica,2006, 12(4):41-43.
Detecting copy number of exogenous genes in transgenic tobacco by multiplex RT-PCR
YU Jing, ZOU Jie, FU Qiang, GUO Yushuang, LIN Shifeng, ZHAO Jiehong*
Guizhou Academy of Tobacco Science, Key Laboratory of Molecular Genetics, China National Tobacco Corporation,Guiyang 550081, China
This paper utilized a multiplex real-time PCR assay to simultaneously detect copy number of inserted exogenous gene 35S,NOS and NPT II in transgenic tobacco within one reaction.Gradient dilution was applied to positive reference tobacco genome DNA,and multiplex real-time PCR assay was used to obtain standard curve equation of tobacco endogenuous reference gene NR and exogenous gene 35S, NOS, as well as NPT II.Copy number of exogenous genes was estimated after substituting the Ct values of both endogenuous and exogenous genes of the strains to be tested into the standard curve equation.Results showed that standard curves of the 4 genes were obtained, and all R2 values were close to 1 with relatively high correlation.In the tested 6 transgenic strains, preliminarily screened 3 strains with their 3 exogenous genes were all single copy.This method can be used for the estimation of copy number of inserted exogenous genes in transgenic tobacco, so as to provide preliminary screen basis for obtaining stable genetic materials.
transgenic tobacco; multiplex RT-PCR; exogenous genes; copy number
余婧,邹颉,付强,等.多重实时荧光定量PCR分析转基因烟草外源基因拷贝数[J].中国烟草学报,2017, 23(4)
中国烟草总公司贵州省公司科技项目(201604);贵州省科技支撑计划农业攻关科技计划项目(黔科合NY[2013]3020号);贵州省科学技术基金(黔科合J字[2014]2117号)
余 婧(1983—),硕士,助理研究员,主要从事烟草分子生物学研究工作, Email:yujingbio@126.com
赵杰宏(1978—),博士,研究员,主要从事烟草分子生物学研究工作,Email: zhaojiehong@126.com
2017-03-02;< class="emphasis_bold">网络出版日期:
日期:2017-06-02
:YU Jing, ZOU Jie, FU Qiang, et al.Detecting copy number of exogenous genes in transgenic tobacco by multiplex RT-PCR [J].Acta Tabacaria Sinica, 2017, 23(4)
*Corresponding author.Email:zhaojiehong@126.com
