羧甲基纤维素钠对低酯果胶凝胶流变特性及凝胶形成的影响
2017-09-22曾瑞琪苗钟化李苇舟张甫生赵欣郑炯
曾瑞琪,苗钟化,李苇舟,张甫生,2,赵欣,郑炯,2*
1(西南大学 食品科学学院,重庆, 400715) 2(重庆市特色食品工程技术研究中心,重庆,400715) 3(重庆第二师范学院 重庆市功能性食品协同创新中心,重庆,400067)
羧甲基纤维素钠对低酯果胶凝胶流变特性及凝胶形成的影响
曾瑞琪1,苗钟化1,李苇舟1,张甫生1,2,赵欣3,郑炯1,2*
1(西南大学 食品科学学院,重庆, 400715) 2(重庆市特色食品工程技术研究中心,重庆,400715) 3(重庆第二师范学院 重庆市功能性食品协同创新中心,重庆,400067)
为探究羧甲基纤维素钠(sodiuncarboxy methyl cellulose,CMC)在低酯果胶凝胶形成过程中的作用,以低酯果胶为原料,在pH 5.5下加入不同用量的CMC,考察复配后果胶凝胶的流变学性能,并对其凝胶形成进行了动力学分析。结果表明,CMC/低酯果胶复配体系是典型的假塑性流体,随着CMC添加量的增大,CMC/低酯果胶复配体系的黏度系数K增大,流体系数n减小。CMC的加入还能提高凝胶体系的黏性与弹性,当CMC的添加量为0.8%时,果胶凝胶体系的假塑性最强。同时,CMC还能提高凝胶形成速度,CMC添加量为0.8%时,SDR曲线和G′曲线明显上升,表现出较快的凝胶速度和较强的凝胶强度,当添加量大于0.8%时,凝胶形成速度下降。
羧甲基纤维素钠;低酯果胶;流变特性;凝胶形成速度;动力学分析
果胶是一种由D-半乳糖醛酸聚合而成的高分子植物多糖,广泛存在于植物的细胞壁及细胞间质中,是人体膳食纤维的主要成分。果胶可由苹果、柑橘、柠檬等水果的果皮,通过酶解提取[1-3]。果胶因具有良好的凝胶及增稠能力而在食品领域中被广泛应用。但由于单一果胶溶于水后性能较差,使得果胶无法在面包,饼干等固体食物中大量使用[4]。近年来,一些学者将多糖、蛋白质等大分子物质与果胶混合制备凝胶,并测定复合物的流变学性能,盛林杰等[5]研究了卵磷脂对低酯苹果果胶的流变性能的影响,结果表明加入0.4%的卵磷脂时会加快果胶凝胶形成速度,并提高凝胶强度,当添加量大于0.4%时凝胶形成速度降低且凝胶强度下降;PICOUT等[6]研究了氧化淀粉对低酯果胶凝胶特性的影响,发现在钙离子浓度较低时,添加一定量的氧化淀粉,会使5℃条件下形成的果胶凝胶的弹性性能增强,而较高钙离子与氧化淀粉的同时存在则会使得同温度下的果胶凝胶强度下降;MARTIN等[7]的研究表明,乳清蛋白与低酯果胶混合时,混合凝胶体系会发生相分离且果胶与蛋白竞争钙离子,如要获得较强的凝胶则需配比合适的果胶、蛋白与钙离子。
羧甲基纤维素钠(sodiuncarboxy methyl cellulose,CMC)是离子型纤维素胶的主要代表产品,是一种阴离子型线性高分子物质。CMC具有良好的使结构膨松、增稠、吸水、稳定、凝胶化等作用,可替代明胶、琼脂、海藻酸钠等因而被广泛应用于食品行业[8-9]。将CMC加入低酯果胶中,以提高果胶凝胶强度,控制水分流动,用于果酱、面包、饼干等食品可以提高产品质量和增强其稳定性,且CMC不被人体消化吸收,可促进肠胃蠕动,减轻结肠压力,添加到食品中可起保健作用,适合于高血压、动脉硬化、冠心病患者食用[10]。目前,有研究将CMC与果胶混合后制成复合涂膜液应用于冷鲜肉保鲜[11],或探究CMC与面筋蛋白作用后的特性[12],以及将CMC与黄原胶复合后加到酸乳饮料中[13],但有关CMC/低酯果胶复合凝胶流变学特性的研究鲜有报道。因此,本研究以低酯果胶为原料,考察不同用量的CMC对果胶流变学特性及凝胶形成过程的影响,为CMC/低酯果胶复配体系的应用提供理论依据和实验支撑。
1 材料与方法
1.1材料与试剂
低酯果胶(食品级,酯化度20%),广州鸿易食品添加剂有限公司;羧甲基纤维素钠(食品级),杭州普修化工产品有限公司;柠檬酸(分析纯),成都市科龙化工试剂厂;CaCl2(分析纯),成都市科龙化工试剂厂;NaOH(分析纯),成都市科龙化工试剂厂。
1.2仪器与设备
FA2004A电子分析天平,上海精天电子仪器有限公司;HH-8数显恒温水浴锅,常州澳华仪器有限公司;AR-G2旋转流变仪,美国TA公司。
1.3实验方法
1.3.1 样品制备
在刘贺等[14]的方法上稍有改动。配制质量分数为2%的果胶溶液,加入质量浓度为12.5 g/L的柠檬酸2 mL,搅拌均匀,用1mol/L的NaOH溶液调节pH值为5.5,向果胶溶液中加入0.2%、0.4%、0.6%、0.8%、1.0%的CMC,充分溶解后形成CMC/低酯果胶复合溶液,为避免预凝胶形成,在80℃条件下缓慢加入30%CaCl2溶液1mL。复合果胶配制好后,冷却静置,在4℃冰箱中保存24 h后用流变仪测定流变特性。
1.3.2 流变特性的测定
参照张倩钰等[15]的方法。采用平板-平板测量系统,平板直径40 mm,设置间隙1 mm,用一次性滴管滴加样品,用刮板除去平板外多余样品,表面涂硅油以防止水分蒸发,每次测试均需更换样品。
静态剪切流变的测定:在25℃条件下,测量剪切速率从0~300 s-1递增,再从300s-1~0递减过程中剪切应力和黏度的变化情况。采用Power-law模型对数据点进行回归拟合,拟合系数R2表示方程拟合精度。Power-law方程表示如下:
σ=Kγn
(1)
式中:σ,剪切应力,Pa;K,黏度系数,Pa·sn;γ,剪切速率,s-1;n,流体指数。
动态黏弹性的测定:在温度25 ℃条件下,扫描应变值为0.5%,振荡频率设定从0.1~10 Hz,保留时间180 s,测定样品储能模量G′、损耗模量G″以及损耗正切角tanδ随角频率的变化。
动态温度扫描测定:温度以5 ℃/min的速度从25 ℃升高到80 ℃,再以5 ℃/min的速度从80 ℃降温到25 ℃,应变0.5%,频率1 Hz,保留时间180 s,记录整个过程中储能模量G′、损耗模量G″随时间和温度的变化情况。
1.3.3 凝胶形成速度的计算
在整个凝胶形成过程 中,储能模量的变化可以用凝胶结构发展平均速率(average structure developing rate,SDRa)表示[16],SDRa是凝胶形成时与储能模量和时间有关的参数计算公式(2):

(2)
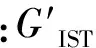
1.4数据处理
所有实验均重复3次,使用Origin 9.0进行相关图表的绘制和数据处理。
2 结果与分析
2.1CMC对低酯果胶凝胶流变特性的影响
2.1.1 静态剪切流变特性的测定
图1表示添加不同量CMC的果胶凝胶体系剪切应力与剪切速率变化的关系。
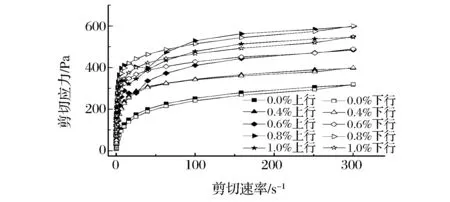
图1 CMC/低酯果胶复配体系剪切应力随剪切速率变化曲线Fig.1 Curves of shear force of CMC/low-methoxyl pectin mixed system with shear rate
由图1可知,CMC添加量从 0增加到1.0%时,体系的剪切应力也逐渐增大,当CMC的添加量达到0.8%时,体系剪切应力也达到最大,当添加量再增加时复配体系剪切应力降低。且随着剪切速率的增加体系的黏度逐渐降低,表现出典型的剪切变稀的非牛顿流体的特性。与单一果胶凝胶相比,添加CMC的果胶凝胶体系的黏度增加,这可能是因为CMC本身具有较高的黏度,与果胶复配后线性大分子链彼此之间相互缠结,使得由分子相对运动引起的流动变得困难,体系的流动阻力增大,从而使得体系剪切难度增大。而当加入CMC的量大于0.8%时,果胶与CMC缠结点减少,分子结构被拉直取向,流动阻力降低,从而使表观黏度下降[17]。这一结果与周爱梅等[18]对海藻酸钠-高甲氧基果胶复合体系凝胶特性的研究结果相类似。
根据Power-law模型对数据点进行拟合,如表1所示,所有的决定系数均在0.94以上,表现出较高的拟合精度。曲线流体指数n小于1,表示凝胶体系为典型的假塑性流体,添加CMC后,混合凝胶体系的稠度系数K升高,表明CMC的加入使果胶凝胶体系的粘稠性增大,且流体指数也随着添加量的增大而减小,体系表现出更强的假塑性。当添加CMC的量为0.8%时,体系具有最大的黏度系数和最小的流体指数,这说明体系的黏度和假塑性达到最大。这可能是因为,CMC和果胶与水之间存在的氢键大量增加,形成了紧密和稳定的三维空间结构,使得体系的黏度升高。当CMC的添加量大于0.8%时,稠度系数和流体指数呈下降趋势,可能是由于过多的CMC使得果胶凝胶分子间的间隙变大,果胶分子间弱结合力形成的交联结构受到影响,流动性能变强。
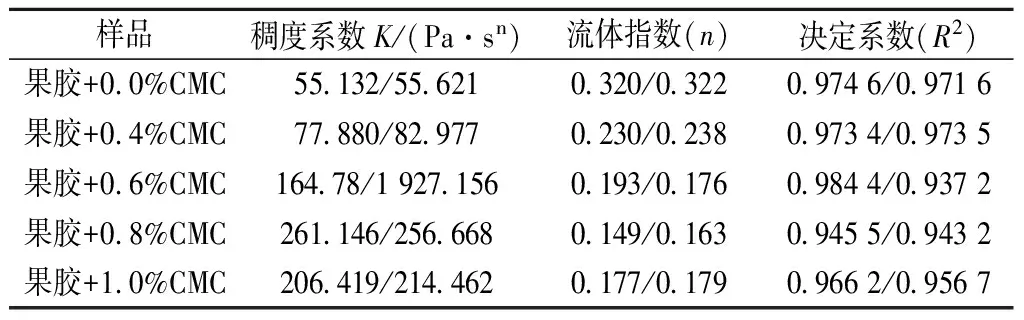
表1 CMC/低酯果胶复配体系Power-law方程拟合参数
注:“/”前数据为上行线拟合数据,“/”后数据为下行线拟合数据。
2.1.2 动态黏弹性的测定
果胶凝胶的黏弹性可以通过动态流变学的特性来描述,凝胶体系的动态黏弹性不仅能反应与产品的实际相关关系,同时还能表征果胶与CMC之间的三维网络结构[19]。储能模量G′可以用来反应样品的弹性,损耗模量G″反应样品的黏性[20]。较强的凝胶储能模量将远大于损耗模量,由图2-A可以看出,所测样品的G′均大于相应的G″,表明该复合体系在扫描频率范围内表现为胶体行为,G′随着扫描频率的增加逐渐增大,表现出弱凝胶动态流变学特征。与单一果胶凝胶相比,随着CMC添加量的增加,复合体系的储能模量也不断加大,表明CMC的添加使得果胶体系内部的分子链段间的缠结点增多,凝胶体系网络结构增强。同时,复合体系的损耗模量也相应增加,体系的黏性性能加强。这一结果与郭肖[18]对刺槐豆胶复配凝胶特性的研究类似。
损耗正切值tanδ是G″与G′的比值,tanδ的比值越大则体系的黏性比例越大,流动性越强,比值越小体系的弹性比例越大,表现出固体的特征[21]。由图2-B可以看出,随着CMC的添加量的增大,体系的tanδ值逐渐减小,CMC/低酯果胶复配体系的流动性变弱,弹性增强,当CMC的添加量达到0.8%时,凝胶体系表现出最强的弹性性能,可能与CMC加入后,CMC与果胶都具有的羧基与钙离子形成类似“蛋盒”结构,将水包裹在网络结构中,使得水的流动在很大程度上被阻止,同时,CMC的加入使整个凝胶在相对有限的空间中聚集,形成更加致密的网络结构,提高了CMC/低酯果胶凝胶的弹性强度。由于CMC为线性阴离子,当加入更高含量的CMC后,CMC与果胶之间的静电相互作用增大,分子之间的排斥作用大于疏水相互作用,果胶分子间的间隙增大,三维结构强度减弱,果胶的伸展和滑动能力增强,导致体系的弹性性能下降。利用加入适量的CMC使果胶凝胶强度增大的特性,可使果胶能在面包、饼干、果冻等食品中更好地应用。
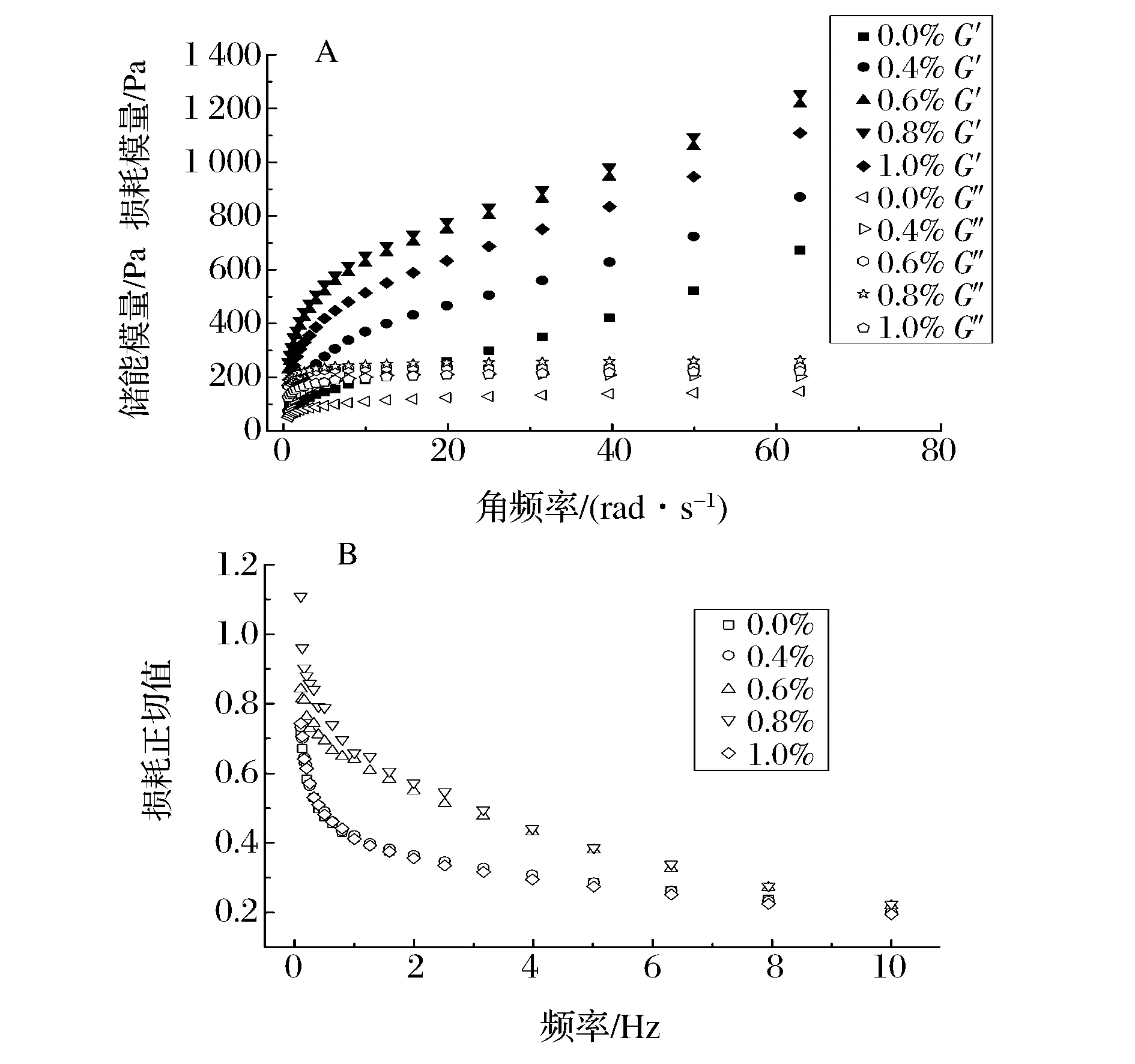
图2 CMC/低酯果胶复配体系动态模量(A)及损耗正切值(B)随角频率/频率变化曲线变化曲线Fig.2 Curves of dynamicmodylus and tanδ with angular frequency/frequency of CMC/low-methoxyl pectin mixed system
2.2CMC对低酯果胶凝胶形成的影响
2.2.1 CMC对凝胶储能模量的影响
图3-A表示为温度与凝胶体系储能模量的关系。由图3-A可知,随着温度的升高,储能模量不断减小,体系的弹性性能降低,可能是由于较高温度会使果胶的内部凝胶结构发生巨大的变化[22]。温度升高,体系分子运动加剧,果胶之间的相互联结被打乱,凝胶强度遭到破坏,弹性性能发生改变,而有较高储能模量的温度对应体系内部有序结构的形成,凝胶强度的增加。添加CMC的果胶凝胶与单一的果胶凝胶体系相比有着相对较高的储能模量,在CMC添加量为0.6%~0.8%时增加显著,而添加量大于0.8%后,体系的储能模量急剧下降。适量的CMC能够使果胶凝胶分子间交联作用加强,由于CMC分子中存在较多羟基,增加凝胶分子间氢键的形成,使凝胶结构致密,不易被温度破坏,当添加量再加大时,果胶分子变大,三维网络结构变得稀松,强度下降。
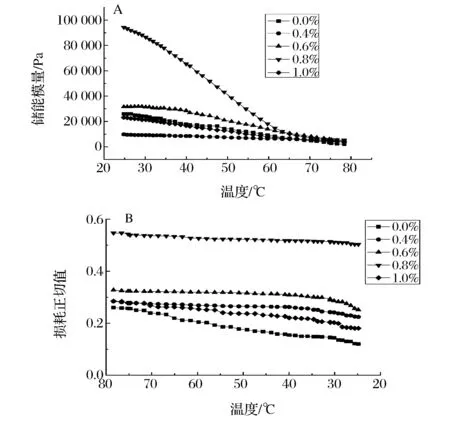
图3 CMC/低酯果胶复配体系动态模量(A)及损耗正切值(B)随温度变化曲线Fig.3 Curves of dynamicmodylus and tanδ with temperature of CMC/low-methoxyl pectin mixed system
2.2.2 凝胶形成速度
SDRa可以表征整个凝胶冷却过程中G′的变化,因此采用凝胶结构形成速度SDR分析凝胶过程具有实际意义[23],将dG′/dt定义为临界结构温度,即凝胶形成时首次剧烈增大的外推温度。图4-a为单一果胶凝胶体系,由图4-a可以看出,温度从80 ℃开始降低,G′略有增加,但G″增加幅度较小,几乎与时间变化曲线重合。表明该过程中只有小部分果胶聚集,凝胶形成速率增长缓慢,当温度降低至46 ℃时,G′开始迅速增大,增加至16 366 Pa占最终G′的63%,表明凝胶网络结构已初步建立,这主要是因为温度下降,果胶与钙离子间的强静电交联作用以及少部分的疏水作用[23]。自45 ℃开始,凝胶形成速率逐渐加大,直到34 ℃时到达最大,表明在这一温度范围内,凝胶结构正以较为稳定的速率建立,在这一阶段中主要是钙离子与果胶进一步形成交联以及果胶分子间氢键的形成[24]。
图4-b为CMC添加量为0.4%的果胶凝胶形成速率曲线。当CMC添加量为0.4%时,随着温度的降低,体系的储能模量呈现升高趋势,凝胶化在60 ℃时开始加速,直到40 ℃时凝胶形成速度到达最大值,当温度下降到40 ℃后,凝胶化速率降低,可能是由于温度降低,分子热运动减慢,果胶羟基氢键的桥联减弱,果胶钙缔合由短缔合区向长缔合区转变,即聚合加深[25]。
图4-c为CMC添加量0.6%时,果胶凝胶形成速度曲线,当温度一开始下降凝胶形成速度即呈现增长趋势,在50~43 ℃时凝胶形成速度的增长趋势最大,当温度在43 ℃时,凝胶形成速度达最大值,G′增加至25 324 Pa,占最终G′的80%,表明此时凝胶结构已大部分建立,随着温度继续降低,凝胶形成速度呈下降趋势,表明CMC/低酯果胶复配凝胶体系结构的建立趋于完善。这一过程中,可能包括果胶与钙离子的相互作用速度加快,CMC分子中的羟基使果胶-果胶、果胶-羧甲基纤维素钠、果胶-羧甲基纤维素钠-果胶间的相互联结作用加强,形成氢键的方向增多,凝胶网络结构形成速度加快。
图4-d为CMC添加量为0.8%时果胶凝胶形成速度曲线。由图4-d可知,当温度下降至70 ℃时,果胶凝胶形成速度迅速增加,G′也迅速增加,与单一的果胶体系以及添加少量CMC的混合体系相比,凝胶速度与G′明显增加,在50 ℃时凝胶形成速度达到最大值,凝胶形成温度升高,在50 ℃时,体系的G′增加至38 697 Pa,高于上述所有凝胶体系G′,弹性性能显著增加,这可能与CMC添加量的增加使得混合体系中氢键形成进一步增多、果胶之间的疏水性及果胶与钙离子的交联增大有关。此外,CMC将水分子牢牢锁住,迅速降低体系的流动性,同时使CMC/低酯果胶体系结构更加致密。当温度继续下降,凝胶速度开始减慢,表明凝胶形成已基本完成,这与0.4%和0.6%CMC结果相似。
图4-e为添加量1.0%CMC的果胶凝胶形成速度曲线。与添加量为0.8%时相比,随着CMC添加量的进一步增加,凝胶形成速度最大值出现温度降低,G′值也明显减小,这可能与CMC添加量过多,其分子中较多的羧基与果胶竞争钙离子,使得果胶与钙离子的桥联减少,导致果胶形成的凝胶结构不牢固,凝胶强度减弱。这与盛林杰[26]等对适量卵磷脂改善低酯苹果果胶凝胶流变性的研究结果一致。
2.2.3 凝胶形成动力学分析
近年来,较多学者在SWARTZEL等[27-28]提出的动力学模型基础上对果胶凝胶的形成进行动力学分析。该模型融合了经典速率方程、阿伦尼乌斯公式以及时间温度关系即与时间温度以及浓度有关的模型。该模型表示如下:
(3)
式中:G′,储能模量,Pa;n,反应级数;t,时间,s;k0,阿伦尼乌斯常数,Pa/s;Ea,活化能,J/mol;R,气体常数8.314J/(mol·K);T,绝对温度,K。
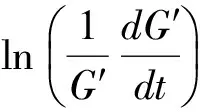
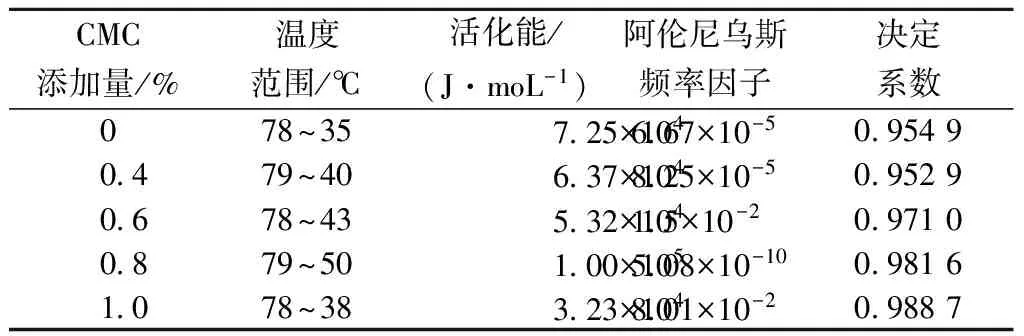
表2 果胶/羧甲基纤维素钠复合凝胶冷却过程中的动力学参数
由表2可以看出,凝胶过程需要的活化能随CMC添加量的不同而有所区别,当添加量为0.8%时需要的活化能最大,当CMC添加量为0.8%时,果胶凝胶体系在较高温度下即开始形成凝胶,这说明在高温时凝胶网络形成需要跨越较高的能量壁垒,而单一的果胶体系或添加较少CMC时凝胶形成温度较低,此时形成凝胶需要的活化能较低,凝胶形成相对容易。这与洪伦波[31]对结冷胶流变行为与凝胶特性的研究结果相似。
3 结论
CMC/低酯果胶复配凝胶体系为典型的假塑性流体,与单一的低酯果胶凝胶相比,CMC/低酯果胶复配体系的稠度系数K随CMC添加量的增加逐渐增大,流体指数n随CMC添加量的增加逐渐减小。动态黏弹和温度扫描测定也发现CMC的加入会使低酯果胶凝胶强度增强,这可能与CMC线性阴离子的分子结构有较大联系,当添加量达到0.8%时,整个CMC/低酯果胶复配体系表现出较好的凝胶性能。综合考虑复配效果,在实际应用中选择CMC添加量为0.8%较为适宜。CMC能显著影响低酯果胶的流变特性,可增大低酯果胶的应用范围,且CMC生产成本相对便宜,在食品生产中适量添加可减少低酯果胶的用量而降低生产成本。但CMC/低酯果胶复配凝胶体系对食品质构、口感、外观等方面的影响还需做进一步研究,以便为CMC/低酯果胶复配体系在食品工业中的应用提供更详细的参考。
[1] 李文德,章克昌.果胶的应用研究进展[J].粮油食品科技,1999,7(4):4-6.
[2] 高建华,戴思齐,刘佳明,等.六种果皮原料果胶的理化及凝胶特性比较[J].农业工程学报,2012,28(16):288-292.
[3] 刘刚,雷激,芮光伟,等.低甲氧基果胶流体质构特性研究[J].食品工业科技,2011,32(1):253-255.
[4] 任梅君,张根义.复合膳食纤维的性质及其应用[J]. 食品工业科技,2012,33(11):165-168.
[5] 赵远航,盛林杰,谌晨,等.卵磷脂/果胶钙凝胶球的制备及性能研究[J].中国新药杂志,2005,24(6):102-109.
[6] PICOUTA D R,RICHARDSONA R K,ROLIN C, et al. Ca2+-induced gelation of low methoxy pectin in the presence of oxidised starch. Part 1. Collapse of network structure[J]. Carbohydrate Polymers,2000,43(2):113-122.
[7] MARTIN BEAULIEUA,TURGEONA L,JEAN-LOUIS DOUBLIER. Rheology, texture and microstructure of whey proteins/lowmethoxylpectins mixed gels with added calcium[J]. International Dairy Journal,2001,11(11):961-967.
[8] 刁静静.食品加工中的增稠剂(六):羧甲基纤维素钠[J].肉类研究,2010,133:66-68.
[9] 黄来发,洪文生,黄恺.食品增稠剂[M].北京:中国轻工业出版社,2000.
[10] 李静,杜柏桥,黄龙,等.羧甲基纤维素钠溶液的流变性质及其在酸性乳饮料中的应用[J].食品科学,2007,28(11):56-59.
[11] 刘莹,谢峰,刘义武,等.果胶/羧甲基纤维素钠复合涂膜液在冷鲜肉保鲜中的应用效果[J].保鲜与加工,2015,15(2):25-28.
[12] 乔聚林,刘传富,董海洲,等. 羧甲基纤维素钠对面团特性及面包品质的影响[J].中国粮油学报,2009,24(4):13-16.
[13] 曹卫春.黄原胶和CMC复配对酸性乳饮料稳定性的影响[D].无锡:江南大学,2006.
[14] 刘贺,徐学明,过世东.酰胺化桔皮果胶凝胶流变学性质研究及动力学分析(Ⅰ)[J].食品与生物技术学报,2008,27(1):38-43.
[15] 张倩钰,徐秋雄,樊巧,等.竹笋膳食纤维对高酯果胶流变及其凝胶质构特性的影响[J].食品与发酵工业,2016,42(7):91-95.
[16] KASTNER H, EINHORN-STOLL U, SENGE B. Structure formation in sugar containing pectin gels-Influence of Ca2+on the gelation of low-methoxylated pectin at acidic pH[J]. Food Hydrocolloids,2012,27(1): 42-49.
[17] CHO M, CHOI W-S, YOU S. Steady and dynamic shear rheology offucoidan-buck wheat starch mixtures[J].Starch,2009,61(5): 282-290.
[18] 周爱梅,郝淑贤,刘欣,等. 海藻酸钠-高甲氧基果胶复合体系凝胶特性的研究[J]. 华南农业大学学报,2003,24(4):75-78.
[19] 吴银琴.不同直链淀粉含量的甘薯淀粉及其与瓜尔胶复配体系性质的研究[D].无锡:江南大学,2014.
[20] FREDERICK H SLIVER, GINO BRADICA, ALFRED TTIA. Elastic energy storage in human articular cartilage: estimation of the elastic modulus for type collagen and changes associated with osteoarthritis[J]. Matrix Biology,2002,21(2):129-137.
[21] 郭肖.刺槐豆胶及其复配胶流变学性质的研究[D].西安:西北师范大学,2013.
[22] PTASZEK P, GRZESIK M. Viscoelastic properties of maize starch and guar gum gels[J].Journal of Food Engineering,2007,82(2):227-237.
[23] LU Lu, LIU Xin-Xing , DAI Lin, et al. Difference in concentration dependence of relaxation critical exponent n for alginate solutions at sol-gel transition induced by calcium cations[J]. Biomacromolecules, 2005, 6(4): 2 150-2 156.
[24] 刘贺,徐学明,过世东.酰胺化桔皮果胶凝胶流变学性质研究及动力学分析(Ⅰ)[J].食品与生物技术学报,2008,27(1):38-43.
[25] CARDENAS A, GOYCOOLEA F M, RINAUDO M. On the gelling behaviour of “nopal” (Opuntiaficusindica) low methoxylated pectin[J]. Carbohydrate Polymers, 2008, 73(2): 212-222.
[26] KASTNER H, EINHORN-STOLL U, SENGE B. Structure formation in sugar containing pectin gels-Influence of Ca2+on the gelation of low-methoxylated pectin at acidic pH[J]. Food Hydrocolloids,2012,27(1): 42-49.
[27] 刘贺,徐学明,过世东.酰胺化桔皮果胶凝胶流变学性质研究及动力学分析(Ⅱ)[J].食品与生物技术学报,2008,27(2):19-24.
[28] 盛林杰,付莹,郭春静,等.适量卵磷脂改善低酯苹果果胶凝胶流变性[J].农业工程学报,2015,31(19):302-307.
[29] SWARTZEL K R. Non-isothermal Kinetic Data Generation for Food Constituents. Food Properties and Computer-aided Engineering of Food Processing Systems[M].Netherlands: Kluwer Academic Publishers, 1989: 99-103.
[30] RHIM J W. Determination of kinetic parameters using linear increasing temperature[J]. Food Science,1989, 54(2): 446-450.
[31] LOPES DA SILVA J A L, GONCO, ALVES M P, et al. Kinetics and thermal behaviour of the structure formation process in HMP/sucrose gelation[J].International Journal of Biological Macromolecules,1995, 17(1): 25-32.
[32] FU J T, RAO M A. Rheology and structure development during gelation of low-methoxyl pectin gels: the effect of sucrose[J]. Food Hydrocolloids,2001, 15(1): 93-100.
[33] 洪伦波.结冷胶流变行为与凝胶特性的研究[D].杭州:浙江工商大学,2007.
Effectofsodiumcarboxymethylcelluloseonrheologicalpropertiesandgelformationoflow-methoxylpectin
ZENG Rui-qi1,MIAO Zhong-hua1,LI Wei-zhou1,ZHANG Fu-sheng1,2,ZHAO Xin3, ZHENG Jiong1,2*
1 (College of Food Science, Southwest University, Chongqing 400715, China) 2(Chongqing Engineering Research Center of Regional Food, Chongqing 400715, China) 3 (Chongqing Collaborative Innovation Center for Functional Food, Chongqing University of Education, Chongqing 400067, China)
In order to investigate the effect of sodiuncarboxy methyl cellulose during gelling of low-methoxyl pectin, different amount of CMC was added to low-methoxyl pectin at pH 5.5, and then the rheological properties of the mixed system were studied. The process of gel formation, and the kinetic analysis of gelling were also studied. The results showed that CMC/low-methoxyl pectin mixed system was a typical pseudoplastic fluid, the consistency coefficient K increased and the fluid index n decreased with the increase of CMC. In addition, CMC improved the viscosity and elasticity of the gel system. When the addition of CMC is 0.8%, the pseudoplasticity of the pectin gel system was the strongest. Meanwhile, the gel formation rate was increased by the addition of CMC. The SDR curve and G 'curve increased obviously, showing faster gelation speed and stronger gel strength when adding CMC at 0.8%. However, the gel formation rate decreased when the addition amount was more than 0.8%.
sodiuncarboxy methyl cellulose; low-methoxyl pectin gels; rheological properties; gel formation rate; kinetic analysis
10.13995/j.cnki.11-1802/ts.013359
本科生(郑炯副教授为通讯作者,E-mail:zhengjiong_swu@126.com)。
重庆市特色食品工程技术研究中心能力提升项目(cstc2014pt-gc8001);中央高校基本科研业务费(SWU20161702001);西南大学本科生创新基金项目(20161702001)
2016-11-08,改回日期:2017-01-04
