头孢地嗪钠含量和有关物测定方法分析
2017-09-21刘敏刘琳琳
刘敏刘琳琳
1.黑龙江中医药大学·北京科信必成医药科技发展有限公司 哈尔滨分公司 150000;
2.北京科信必成医药科技发展有限公司哈尔滨分公司 150000
头孢地嗪钠含量和有关物测定方法分析
刘敏1刘琳琳2
1.黑龙江中医药大学·北京科信必成医药科技发展有限公司 哈尔滨分公司 150000;
2.北京科信必成医药科技发展有限公司哈尔滨分公司 150000
目的:探讨头孢地嗪钠中主要成分的含量测定方法。方法:利用HPLC法进行测定,以十八烷基硅烷键合硅胶为填充剂(250mm×4.6mm,5μm);流动相A为pH3.2醋酸铵溶液,流动相B为乙腈,流速为1.0mL/min,线性梯度洗脱;检测波长254nm;柱温35℃。结果:各杂质峰与主成分峰能完全分离,头孢地嗪钠的检测限为0.056μg/mL,定量限为0.22μg/mL,头孢地嗪钠在0.15¯769.2 μg/mL范围内线性关系良好(r>0.999),80%,100%,120%浓度下各进3个平行样,测得含量的RSD为0.25%。结论:采用HPLC法测定头孢地嗪钠的成分含量具有很好的稳定性,测量结果较为准确,适合相关领域的测定要求。
头孢地嗪钠;含量;测定
作为头孢的第三代抗菌性药品,头孢地嗪钠具有很强的免疫增强作用,能够针对免疫系统疾病有很好的控制作用,这是因为头孢地嗪钠能够在人体内激活巨噬细胞,增强巨噬细胞的杀菌能力,从而抑制细菌的生长和繁殖。对于头孢地嗪钠的含量测定,一般多采用高效液相色谱法进行测定,在此本文就探讨了其具体的测定过程。
1、仪器与试药
1.1 仪器
WatersAlliance2695高效液相色谱仪,2996PDA 检测器;MettlerToledo320pH计;AT260分析天平;Platisil18(250mm4.6mm,5m)色谱柱;Milli-Q超纯水系统。
1.2 试药
乙腈;醋酸铵;甲酸;头孢地嗪钠对照品(含量90.9%),样品,及杂质对照品[7-氨基头孢烷酸(7-ACA)、头孢地嗪母核(3-MTA)、头孢地嗪侧链酸(MMTA)、去乙酰头孢噻肟(DF)、去乙酰氧头孢噻肟(DSF)、头孢噻肟、头孢噻肟内酯(L)]。
2、方法与结果
2.1 色谱条件
色谱柱为Pl18(250mm×4.mm,5μm);流动相A为醋酸铵溶液(取醋酸铵1.9g,2000mL水溶解,甲酸调pH3.2),流动相B为乙腈,线性梯度洗脱,流速为1.0mL/min;检测波长为254nm;柱温35℃;进样量为20μL。

表1 流动相及洗脱程序
2.2 溶液的制备
2.2.1 头孢地嗪钠供试品溶液
取本品适量,精密称定,加乙腈-水(19:81)混合溶液溶解并制成每1mL约含0.5mg的溶液,摇匀,即得。
2.2.2 头孢地嗪钠对照品溶液
取头孢地嗪对照品适量,精密称定,加乙腈-水(19:81)混合溶液溶解并制成每1mL约含0.5mg的溶液,摇匀,即得。
2.2.3 含量测定
精密量取供试品溶液、对照品溶液各20L,分别注入液相色谱仪,记录色谱图;按外标法计算样品中头孢地嗪(C20)含量。
2.2.4 有关物质检测
精密量取对照品溶液1mL,置入100mL量瓶,用乙腈-水(19:81)混合溶液稀释至刻度,摇匀,作为对照溶液;取对照溶液 20L注入液相色谱仪,调节检测器灵敏度,使主成分色谱峰的峰高至少为满量程的10%,再取供试品溶液20L注入液相色谱仪,记录色谱图,头孢地嗪峰和相邻杂质峰的分离度应符合要求。供试品溶液如有杂质峰,按1%自身对照法进行计算。
2.3 分析方法验证
2.3.1 专属性考察
为考察本方法能否有效检测本产品在生产及储存过程中可能产生的杂质,根据其结构特点、合成工艺及贮存条件等,进行了以下强制降解和分离度考察试验。
2.3.1.1 强制降解试验
将样品粉末分别进行高温破坏(60℃,10d),紫外光照破坏(UV254nm,10d),强氧化(35%过氧化氢溶液,15min)、强酸(1mol/L盐酸溶液,100min)、强碱(0.1mol/L氢氧化钾溶液,5min)破坏。结果表明,头孢地嗪钠在碱性和氧化条件下较易降解,光照条件下MMTA和异构体2(HPLC-MS鉴别)均有增加;碱性条件下产生异构体1、异构体3和异构体4(均由HPLC-MS鉴别);酸性条件下杂质L增加。强制降解产生的杂质180食品与药品FoodDrug2015年第17卷第3期均能与主成分完全分离。
2.3.1.2 分离度考察
将头孢地嗪钠与各杂质(主要包括起始原料、中间体、副产物等)的对照品混合溶解后进样,进行分离度考察,以考察本方法能否有效监测生产工艺中产生的杂质。头孢地嗪钠供试品溶液(含头孢地嗪约 0.5mg/mL)、头孢地嗪钠和杂质混合液(含头孢地嗪约0.5mg/mL,各杂质的浓度约0.5~1.5μg/mL)的色谱图见图1。结果显示,各杂质均能得到较好分离。
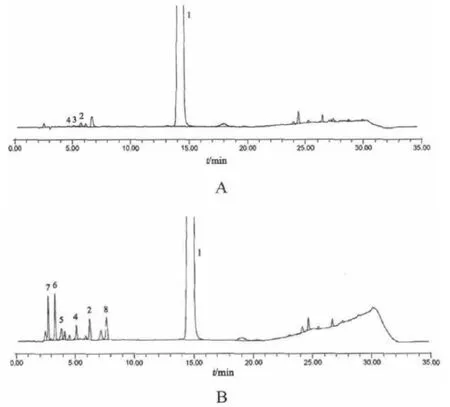
图1 头孢地嗪钠供试品溶液、头孢地嗪钠和杂质混合液的色谱图
上述试验表明,本方法有良好的专属性,适用于头孢地嗪钠在生产和贮存过程中产生的有关物质检测。
2.3.2 检测限和定量限测定
精密称取头孢地嗪钠对照品,用乙腈-水(19:81)混合溶液溶解并稀释,制成含头孢地嗪钠0.044,0.13μg/mL的溶液,重复进样3次。按S/N=3计算,头孢地嗪钠的检测限为0.056μg/mL;按S/N=10计算,头孢地嗪钠的定量限为0.22μg/mL。
2.3.3 线性关系考察
精密称取头孢地嗪钠对照品,用乙腈-水(19:81)混合溶液溶解稀释,制成含头孢地嗪钠0.1479,0.4929,4.929,9.858,24.64,49.29,98.58,218.7,306.9,388.2,411.1,505.4,599.4,619.7,769.2mg/mL系列不同浓度的对照品溶液,以浓度 C(μg/mL)为横坐标,峰面积A为纵坐标做回归直线,见表2。

表2 回归方程
2.3.4 准确度试验
精密称取头孢地嗪钠对照品共9份,用乙腈-水(19:81)混合溶液溶解制得 80%,100%(0.5mg/mL),120%浓度水平的溶液。按2.2.3项方法测定每一样品的含量,结果见表3。

表3 回收率试验结果
2.3.5 精密度和重复性试验
精密称取头孢地嗪钠对照品约50.0mg,共6份,用乙腈-水(19:81)混合溶液溶解,制成每1mL约含0.5mg的溶液,摇匀。进样,记录峰面积,计算头孢地嗪钠响应因子的RSD为0.13%。其中一份溶液连续进6次,记录峰面积。头孢地嗪钠峰面积的RSD为0.2%。结果表明,该方法的精密度良好。
2.3.6 溶液稳定性试验
将头孢地嗪钠分别用流动相(A:B=81:19)、水、乙腈-水(19:81)溶解,室温20℃下放置,分别于80,160,240,320,360,420min进样测定,考察各杂质的变化情况。结果显示,用流动相溶解的样品溶液非常不稳定,杂质增加显著,总杂质增加3.2%。用水和乙腈-水(19:81)溶解的样品溶液比较稳定,总杂质量的变化小于0.1%。鉴于样品在流动相中(A:B=81:19)降解较快,用水溶解时样品溶液虽然稳定,但水的空白峰影响积分,故采用乙腈-水(19:81)溶解样品。
2.3.7 耐用性试验
选用Gemini18(250mm×4.6mm,5μm)色谱柱进行试验,各杂质的保留和分离情况与Platisil柱一致。
3、讨论
从本实验的结果可以看出,采用高效液相色谱法对头孢地嗪钠的成分含量进行测定是十分可行的,且其适应性、专属性、精密度、准确度、线性、耐用性和溶液稳定性均良好;定量限和检测限满足检测需要。
[1]姜晓峰,臧恒昌,薛宗文.头孢地嗪钠含量和有关物测定方法研究[J].食品与药品,2015(3):179-183.
[2]刘锡鲁,王艳芳,张钰.注射用头孢地嗪钠聚合物测定方法的研究[J].疾病监测与控制,2009(1):16-17.
R712+.3
A
1672-5018(2017)02-005-2
