HPLC法检测生物硒醋及老陈醋乳酸和醋酸含量
2017-09-18,,,,,
, ,, , ,
(山西大学生命科学学院,山西太原 030006)
HPLC法检测生物硒醋及老陈醋乳酸和醋酸含量
王兴华,刘菊,谢玉韬,宋佳,张帆,乔沈
(山西大学生命科学学院,山西太原 030006)
本文研究了利用HPLC法测定生物硒醋和老陈醋中乳酸和醋酸的含量,并对其测定条件进行优化。应用以C18为色谱分析柱,检测波长为215 nm,流动相为2.5% NH4H2PO4缓冲液,样品稀释度为30倍,流速为1.0 min/mL,柱温为29 ℃,生物硒醋样品的最佳pH=2.5,老陈醋的最佳pH为2.7时,可以较好的分离、检测生物硒醋和老陈醋中乳酸和醋酸的含量,所有的检测在4 min内完成。同时当其他分析条件一定,pH=2.7时,醋酸和乳酸标样的回归方程分别为y=484.23x-81.373,R2=0.9992、y=441.37x-68.321,R2=0.9979。当pH=2.5时,醋酸和乳酸标样的回归方程分别为y=484.61x+72.201,R2=0.9993、y=389.82x+30.432,R2=0.9991。该检测方法重复性、准确度、精确度的相对标准偏差范围为0.00%~1.07%,其中生物硒醋乳酸和醋酸标品的加标回收率分别为100.00%~110.00%、99.00%~100.83%,老陈醋乳酸和醋酸标品的加标回收率分别为100.00%~101.00%、100.00%~110.00%。此方法重复性好、准确性和精确性好,检测时间短。可以应用于生物硒醋和老陈醋的HPLC法有机酸的定量分析。
HPLC法,生物硒醋,老陈醋,乳酸,醋酸
我国食醋具有悠久的酿造历史,其味酸、醇厚、柔和,是大众生活中的一种重要调味品。食醋中含有一定量的矿物质和维生素和氨基酸[1]。食醋中含有丰富的有机酸,其中有乳酸、醋酸、酒石酸、柠檬酸、琥珀酸等,但含量最高的是醋酸和乳酸,也是影响食醋酸味和品质最重要的两种有机酸。生物硒醋是在传统固态发酵工艺的基础上,加入银杏果、黑苦荞麦、甘草等具有保健功效的物质,是新型保健食醋的代表之一。老陈醋是山西省一种特色的调味料[2],其颜色黑亮透紫,醋香柔酸,是纯粮酿造醋的代表[3]。目前测定有机酸的方法主要有离子色谱法、气相色谱法、碱式滴定法、比色法等[4]。其中离子色谱法由于色谱柱对样品蛋白质的含量有严格的限制[5-6],故不适用于食醋中有机酸的测定;气相色谱法由于有机酸的沸点较高,且食醋中挥发性成分较多,前处理不易控制;碱式滴定法和比色法由于测定过程误差较大,准确性较差。HPLC法是目前测定有机酸最常见的方法[7-10],由于原料使用和制作工艺的差异,采用以前报道的测定方法,应用HPLC法无法较好的分离生物硒醋、老陈醋中的醋酸和乳酸。
因此,建立定量分析生物硒醋和老陈醋中的有机酸的方法是十分必要的。本文研究了食醋样品经过稀释、萃取等预处理过程后,对HPLC法测定生物硒醋和老陈醋中醋酸和乳酸的条件进行优化研究,以期为生物硒醋和老陈醋的酿造工艺、食用品质和药用价值提供一定的理论参考和依据。
1 材料与方法
1.1材料与仪器
老陈醋 山西太原市清徐第四醋厂;生物硒醋 山西银杏食品科技开发有限公司;磷酸二氢铵 分析纯,北京化工厂;磷酸 分析纯,成都市科龙化工试剂厂;甲醇 色谱纯,天津市科密欧化学试剂有限公司;醋酸标品、乳酸标品 色谱纯,Sigma-Aldrich西格玛奥德里奇(上海)贸易有限公司。
STARTER2100型pH计 奥豪斯仪器(上海)仪器有限公司;JA1203N型电子天平 上海奥豪斯仪器有限公司;高效液相色谱仪 大连依利特分析仪器有限公司;Sep-PakC18固相萃取小柱 天津毫津科技有限公司;SC-3616型离心机 安徽中科中佳科学仪器有限公司;移液器 德国Eppendorf股份公司。
1.2实验方法
1.2.1 食醋样品的处理 吸取1 mL生物硒醋和老陈醋分别于10个1 mL的离心管中,以10000 r/min的速度离心20 min后[11-13],吸取各离心管上清液0.6 mL,得生物硒醋和老陈醋上清液总量各6 mL保存于4 ℃的冰箱中备用。
制备的生物硒醋样品和老陈醋样品,用Sep-parkC18固相萃取小柱(250 mg/3 mL)进行处理(萃取小柱先用3 mL甲醇活化,然后用适量超纯水进行平衡)[14],使样品中的色素吸附完全,再将呈无色、透明的样品用针筒式水膜(0.45 μm×0.13 mm)过滤,过滤的样品进行相应梯度的稀释后进入HPLC检测。
1.2.2 HPLC法检测条件的单因素实验 色谱柱:Waters Atlantis T3(150 mm×4.6 mm,5 μm)。
其他条件的选择:在样品稀释度为20倍,进样量为20 μL,流动相为2.0% NH4H2PO4,流动相pH为2.8,流速为0.8 min/mL,柱温为28 ℃的条件下[15],研究不同波长(210、215 nm)对醋样乳酸和醋酸的分离及最大吸收峰的影响;在检测波长为215 nm,其它分析条件不变,比较6种流动相NaH2PO4、KH2PO4、Na2HPO4、K2HPO4、NH4H2PO4、(NH4)2HPO4,对醋样乳酸和醋酸的分离情况;在检测波长为215 nm,其它分析条件不变,研究样品的不同稀释度(1、10、20、30、40、50倍)对醋样乳酸和醋酸这两种有机酸的分离情况;在检测波长为215 nm,其它分析条件不变,研究不同流动相浓度(0.5%、1.0%、1.5%、2.0%、2.5%、3.0%)对醋样乳酸和醋酸这两种有机酸的分离情况;在检测波长为215 nm,其它分析条件不变,研究不同pH(2.5、2.6、2.7、2.8、2.9、3.0)对醋样乳酸和醋酸这两种有机酸的分离情况;在检测波长为215 nm,其它分析条件不变,研究不同流速(0.5、0.6、0.7、0.8、0.9、1.0 min/mL)对醋样乳酸和醋酸这两种有机酸的分离情况;在检测波长为215 nm,其它分析条件不变,研究不同柱温(25、26、27、28、29、30 ℃)对醋样乳酸和醋酸这两种有机酸的分离情况[16-18]。
1.2.3 标准曲线的绘制 分别准确称取40 mg的乳酸标准品、50 mg醋酸标准品于5 mL的离心管中,用移液器精确移取超纯水,使标准品稀释到相应刻度,即浓度分别为8、10 mg/mL作为母液。精确移取乳酸、醋酸母液各50、100、150、200、250、300 μL至1 mL离心管中,用2.5% NH4H2PO4分别将混合酸标准样品稀释到相应刻度,即乳酸的浓度分别为0.4、0.8、1.2、1.6、2.0、2.4 mg/mL,醋酸的浓度分别为0.5、1.0、1.5、2.0、2.5、3.0 mg/mL。在检测波长为215 nm,流动相为2.5% NH4H2PO4缓冲液,样品稀释度为30倍,流速为1.0 min/mL,柱温为29 ℃,pH=2.5和pH=2.7的最佳分析条件下分别进样,进样量为20 μL,并以标品浓度为横坐标,峰面积为纵坐标绘制标准曲线。
1.3数据处理
应用Origin软件计算其HPLC分析法的重复性、准确度、精确度、回收率等的相对标准偏差。
2 结果与分析
2.1检测波长的确定
检测结果发现,当波长为215 nm时,乳酸和醋酸两种有机酸在此处均有最大的吸收峰,波峰稳定且重复性好,不受流动相中其它物质的干扰。所以确定本研究检测波长为215 nm。
2.2流动相的选择
比较六种磷酸盐缓冲液为流动相的目标物分离情况,结果发现,六种磷酸盐缓冲液对生物硒醋和老陈醋乳酸和醋酸的分离有一定的差异。KH2PO4、Na2HPO4、K2HPO4、(NH4)2HPO4这四种磷酸盐分离效果不佳,乳酸和醋酸这两个主峰没有完全分开,出现交叉峰和拖尾峰的现象。NaH2PO4和NH4H2PO4这两种磷酸盐作为流动相时分离效果都比较好,NaH2PO4比NH4H2PO4出峰时间长,乳酸和醋酸分离需要的时间长。NH4H2PO4缓冲液作为流动相时,分离效果好且分析时间短,所以NH4H2PO4选定为流动相。
2.3样品稀释度的选择
生物硒醋和老陈醋中有机酸含量比较多,尤其是乳酸和醋酸含量丰富,且样品食醋的成分复杂。故图谱中出峰杂而多,乳酸和醋酸峰值高且分离效果不好,因受其他物质的影响而不好判断。由于本文只研究样品中具有代表性的乳酸和醋酸,此波长下,样品中的其它物质均不予研究,所以考虑稀释食醋样品,可以让样品中的醋酸和乳酸得到稀释,峰值相应降低,有些含量低的物质可能由于稀释而不出峰或峰值更低,从而可以降低215 nm检测波长处图谱的复杂度,简明分析主要峰。实验结果发现当稀释度达到30倍时,生物硒醋和老陈醋的乳酸和醋酸分离效果好,不受其它杂峰的影响。故选定稀释度为30倍。
2.4流动相浓度的选择
流动相浓度的高低将会影响色谱的分离情况,浓度过高,将会影响到流动柱的灵敏度和寿命,降低组分分析的准确性。浓度过低,可能影响乳酸和醋酸的分离情况,出现拖尾等分离效果差的现象。本实验中NH4H2PO4浓度为2.0%、2.5%和3%的分离效果比较好,但2.5%的浓度出峰效果最好且峰值最高。综合考虑出峰和离子强度对柱子的影响,选用NH4H2PO4缓冲液的浓度为2.5%。
2.5流动相pH的选择
当溶液的pH=3.0,乳酸和醋酸不能很好的分开,逐渐降低磷酸缓冲液的pH,当溶液pH=2.7,老陈醋的乳酸和醋酸可以很好的分开,且分离效果好,但生物硒醋的乳酸和醋酸分离效果不甚好。逐渐降低pH,当pH=2.5时,生物硒醋的乳酸和醋酸的分离效果好,但老陈醋的却不佳。故老陈醋的分析pH选择为2.7,生物硒醋的pH选择为2.5。
2.6流速的选择
当流速0.5 min/mL时,两种食醋的乳酸和醋酸保留时间过长,且分离效果不好。逐渐提高流速时,色谱中乳酸和醋酸的分离效果相差不大,流速越高,保留时间越短。由于高效液相色谱仪最高流速不能超过1.0 min/mL,故生物硒醋和老陈醋的流速选择为1.0 min/mL。
2.7柱温的选择
色谱的柱温是一个重要的操作变数,直接影响到层析柱的选择性、分离效果、检测器的灵敏度和稳定性。温度过高,会导致分离效果和色谱柱使用寿命的下降。温度过低,流动相的粘度增加,导致传递效率降低。当柱温为25 ℃时,生物硒醋和老陈醋的乳酸和醋酸没有完全分开。随着柱温的升高,分离效果愈来愈好。当温度为29 ℃和30 ℃时,两种食醋的乳酸和醋酸的分离效果最佳。但考虑到温度高会影响柱子的寿命和灵敏性。故综合考虑,选用色谱柱的温度为29 ℃。
2.8标准曲线方程
当检测波长为215 nm,流动相为2.5% NH4H2PO4缓冲液,流速为1.0 min/mL,柱温为29 ℃,pH=2.7时,得到醋酸和乳酸的线性方程分别为y=484.23x-81.373(R2=0.9992),y=441.37x-68.321(R2=0.9979)。当检测波长为215 nm,流动相为2.5% NH4H2PO4缓冲液,流速为1.0 min/mL,柱温为29 ℃,pH=2.5时,醋酸和乳酸线性方程分别为y=484.61x+72.201(R2=0.9993),y=389.82x+30.432(R2=0.9991)。
2.9重复性
取生物硒醋和老陈醋样品各6份,预处理后分别在最佳条件下分析检测,即生物硒醋在以C18为色谱分析柱,检测波长为215 nm,流动相为2.5% NH4H2PO4缓冲液,样品稀释度为30倍,流速为1.0 min/mL,柱温为29 ℃,pH=2.5的最佳分析条件下,而老陈醋在以C18为色谱分析柱,检测波长为215 nm,流动相为2.5% NH4H2PO4缓冲液,样品稀释度为30倍,流速为1.0 min/mL,柱温为29 ℃,pH=2.7的最佳分析条件下进样,进行HPLC法检测,对其样品中乳酸和醋酸进行6次平行测定,并计算其相对标准偏差RSD。

表1 重复性实验结果Table 1 The results of repetition test
由表1结果可看出,应用HPLC法平行测定生物硒醋和老陈醋中的乳酸、醋酸含量时,其相对标准偏差范围为0.50%~1.07%,故该方法测定生物硒醋和老陈醋中的乳酸、醋酸含量重复性好,方法可靠。
2.10精密度
对乳酸和醋酸标准品(浓度分别为1.20、1.50 g/100 mL)进行连续5次HPLC分析,分析条件设置同2.9,记录每次进样的保留时间和峰面积,并计算标样乳酸和醋酸在流动相pH为2.7和pH为2.5条件下的相对标准偏差RSD。

表2 精密度实验结果Table 2 The results of precision test
由表2可得出,当检测波长为215 nm,流动相为2.5% NH4H2PO4缓冲液,样品稀释度为30倍,流速为1.0 min/mL,柱温为29 ℃,pH为2.5和2.7时,乳酸、醋酸标准品检测的相对标准偏差范围为0.00%~0.02%,故醋酸、乳酸标品的精密度较高。
2.11稳定性
分别取生物硒醋和老陈醋1 mL,经过预处理过程后,分别在制样不同时间后(1、2、3、4、5 d),在两种食醋的最佳分析条件下对其分别进行HPLC分析,并计算两种醋样的乳酸和醋酸的相对标准偏差RSD。

表3 稳定性实验结果Table 3 The results of stability test

表4 生物硒醋样品中乳酸、醋酸的加标回收率Table 4 The recovery rate of lactic acid and acetic acid in the samples of biological selenium vinegar
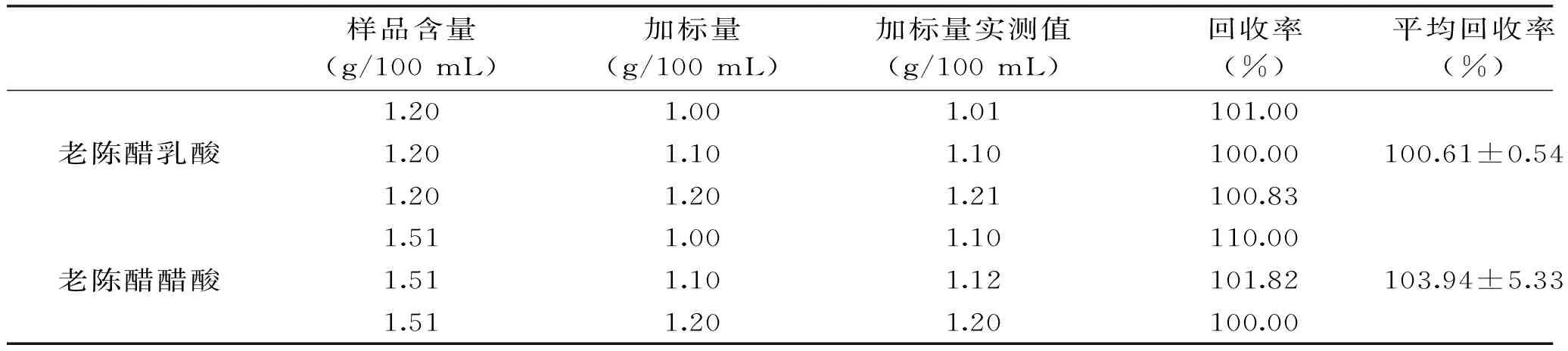
表5 老陈醋样品乳酸、醋酸的加标回收率Table 5 The recovery rate of lactic acid and acetic acid in the samples of vinegar
由表3可看出,在一定时间内,随着时间的延长,生物硒醋和老陈醋中乳酸、醋酸的含量相对稳定,其相对标准偏差范围为0.00%~0.06%,故其测定方法具有较高的稳定性。
2.12加标回收率
取生物硒醋和老陈醋各2份,每份1 mL,其中一份作为本液,另一份加入1 mL乳酸和醋酸的混合酸标准品(其中混合酸标准品的乳酸和醋酸浓度依次为1.00、1.10、1.20 g/100 mL),经过预处理后分别在两种食醋的最佳分析条件下对其进行HPLC分析,并计算其相对标准偏差RSD。
由表4和表5可看出,生物硒醋乳酸和醋酸的加标平均回收率分别为(103.33%±5.77%)、(99.94%±0.92%),老陈醋乳酸和醋酸的加标平均回收率分别为(100.61%±0.54%)、(103.94%±5.33%)。故该分析测定方法具有较高的准确度。
2.13两种食醋样品的高效液相色谱图分析
经过各单因素的条件优化后,得到HPLC法检测生物硒醋中乳酸和醋酸含量的最佳分析条件为:以C18为色谱分析柱,检测波长为215 nm,流动相为2.5% NH4H2PO4缓冲液,样品稀释度为30倍,流速为1.0 min/mL,柱温为29 ℃,pH=2.5。而HPLC法分析检测老陈醋中乳酸和醋酸含量的最佳条件为:以C18为色谱分析柱,检测波长为215 nm,流动相为2.5% NH4H2PO4缓冲液,样品稀释度为30倍,流速为1.0 min/mL,柱温为29 ℃,pH=2.7。两种醋样乳酸和醋酸的检测均在4 min内完成。采用优化后的分析条件,得到两种食醋的高效液相色谱图,如图1~图4所示。其中图1和图2是在上述HPLC法分析检测生物硒醋中乳酸和醋酸含量的最佳条件下得到的分析图谱,图3和图4是在上述HPLC法分析检测老陈醋中乳酸和醋酸含量的最佳条件下得到的分析图谱,由图1和图3可看出,主峰1和主峰2分离完全,不受其它物质的影响且出峰对称稳定,故其乳酸、醋酸的定量分析不受其它物质的干扰,方法准确性高。

图1 老陈醋样品有机酸HPLC分析图谱(pH=2.7)Fig.1 HPLC analysis samples of organic acid of vinegar samples(pH=2.7)注:1代表乳酸峰;2代表醋酸峰;图2~图4同。

图2 标准品的有机酸HPLC分析图谱(pH=2.7)Fig.2 HPLC analysis samples of organic acid of standard samples(pH=2.7)

图3 生物硒醋样品有机酸HPLC分析图谱(pH=2.5)Fig.3 HPLC analysis samples of organic acids of biological selenium vinegar(pH=2.5)

图4 标准品的有机酸HPLC分析图谱(pH=2.5)Fig.4 HPLC analysis samples of organic acid of standard samples(pH=2.5)
3 结论
对生物硒醋和老陈醋的乳酸和醋酸进行HPLC分析,且对其分析条件进行优化,获得最佳优化条件为:以C18为色谱分析柱,检测波长为215 nm,流动相为2.5% NH4H2PO4缓冲液,样品稀释度为30倍,流速为1.0 min/mL,柱温为29 ℃,两种食醋样品分析条件唯一不同的是:生物硒醋样品的最佳pH=2.5,而老陈醋的最佳pH为2.7,所有的检测在4 min内完成。当其他分析条件一定,pH=2.7时,醋酸和乳酸标样的回归方程分别为y=484.23x-81.373(R2=0.9992),y=441.37x-68.321(R2=0.9979)。当pH=2.5时,醋酸和乳酸标样的回归方程分别为y=484.61x+72.201(R2=0.9993),y=389.82x+30.432(R2=0.9991)。使用该方法测定的目标峰对称且稳定性好,一定的稀释倍数可以降低主峰面积过高引起的分析难度,降低其它杂质的干扰,且灵敏度和回收率高。该方法简单、准确性好、精密度高、重复性好、检测时间短,可以应用于生物硒醋和老陈醋的HPLC法的定量分析,准确测定食醋中乳酸和醋酸的含量,为生物硒醋和老陈醋的质量标准提供一定的依据和参考数据。
[1]赵良启,李丽. 我国食醋生产技术的历史、现状与发展趋势:下[J]. 中国调味品,2005,30(2):15-17.
[2]GB 19777-2005,原产地域产品山西老陈醋[S].
[3]GB 19461-2004,原产地域产品独流老醋[S].
[4]薛霞,霍艳敏,王骏,等. 固相萃取-高效液相色谱法测定果醋中7种有机酸[J]. 食品科学,2012,33(14):247-252.
[5]王贵双,唐坤甜,鲁绯,等. 离子交换色谱法测定食醋中有机酸[J]. 中国酿造,2010,28(7):166-169.
[6]成冰,张京芳,徐洪宇,等. 不同品种酿酒葡萄有机酸含量分析[J]. 食品科学,2013,34(12):224-227.
[7]郑战伟,张宝善,祁春燕,等. 醋品中成分检测方法的研究进展[J]. 食品工业科技,2012,33(2):446-447.
[8]莫海涛,杜玉兰,黎庆涛,等. 反相高效液相色谱法测定发酵饮料中有机酸和维生素C的含量[J]. 食品工业科技,2007,28(2):230-231.
[9]Arnetoli M,Montegrossi G,Buccianti A,et al.Determination of organic acids in plants ofSileneparadoxaL. by HPLC[J]. Journal of Agricultural and Food Chemistry,2008,56(3):790-794.
[10]胡小露,刘卉,鲁宁,等. HPLC法同时测定蓝莓汁及其发酵酒中9种有机酸[J]. 食品科学,2012,33(16):229-232.
[11]徐玉涛,李珂珂,王贺新,等. 高效液相色谱法对蓝莓果实中8个有机酸含量的测定[J]. 食品科学,2015,38(16):128-129.
[12]郭燕,梁俊,等. 高效液相色谱法测定苹果果实中的有机酸[J]. 食品科学,2012,33(2):228-230.
[13]孙延芳,梁宗锁,杨开宝,等. 高效液相色谱法分析酸枣中的有机酸和维生素C[J]. 黑龙江农业科学,2011(8):80-81.
[14]Rodrigo S,Ana C P R,Cristiano A B,et al. Validation of HPLC method for simultaneous determination of main organ acids in fruits and juices[J]. Food Chemistry,2012,135(1):150-152.
[15]周萍,罗梁华,胡福良. 高效液相色谱法测定食醋及醋粉中的醋酸和乳酸[J]. 中国调味品,2008,30(7):85-86.
[16]Pilar Flores,Pilar Hellin,Jose Fenoll. Determination of organ acids in fruits and vegetables by liquid chromatography with tandem-mass spectrometry[J]. Food Chemistry,2012,132(2):1049-1052.
[17]余宁华,陆震鸣,许伟,等. 基于主成分分析的中国发酵食醋有机酸含量差异性分析[J]食品与发酵工业,2010,36(10):144-148.
[18]刘凤珠,李晓,王颖颖,水果醋中有机酸成分的分析[J]. 中国农学通报,2010,26(20):94-97.
DeterminationoflacticacidandaceticacidcontentinbiologicalseleniumvinegarandvinegarbyHPLCmethod
WANGXing-hua,LIUJu,XIEYu-tao,SONGJia,ZHANGFan,QIAOShen
(School of Life Science,Shanxi University,Taiyuan 030006,China)
Determination of lactic acid and acetic acid of biological selenium vinegar and vinegar by using HPLC method were studied. C18as chromatographic analysis column,detection wavelength was 215 nm,the mobile phase was 2.5% NH4H2PO4buffer,sample dilution was 30 times,the flow rate was 1.0 min/mL,the column temperature was 29 ℃,the best pH of the biological selenium vinegar was 2.5,while the best pH of the vinegar was 2.7,which could better separation and determination of lactic acid and acetic acid of biological selenium vinegar and vinegar,all testing completed within 4 min. When other analysis conditions were certain,pH was 2.5,the regression equation of acetic acid and lactic acid standard were y=484.23x-81.373,R2=0.9992,y=441.37x-68.321,R2=0.9979,respectively. When pH was 2.5,the regression equations of acetic acid and lactic acid standard were y=484.61x+72.201,R2=0.9993,y=389.82x+30.432,R2=0.9991,respectively. The relative standard deviation of this method was 0.00%~1.07%,standard addition recoveries of biological selenium vinegar lactic acid and acetic acid standard were 100.00%~110.00%,99.00%~100.83% respectively,standard addition recoveries of vinegar lactic acid and acetic acid were 100.00%~101.00%,100.00%~110.00% respectively. The method has good repeatability,accuracy and precision,short detection time,therefore it could be applied in biological selenium vinegar and vinegar.
HPLC method;biological selenium vinegar;vinegar;lactic acid;acetic acid
2017-03-01
王兴华(1958-),男,大学本科,副教授,研究方向:微生物发酵及食品安全,E-mail:xhwang@sxu.edu.cn。
山西省科技厅(20140311021-5);富硒醋生产工艺研究(20130201)。
TS207.3
:A
:1002-0306(2017)16-0247-06
10.13386/j.issn1002-0306.2017.16.047
