吉非替尼小鼠体内药代动力学研究
2017-09-18糜志远汤媛媛
张 佳,糜志远,汤媛媛,李 洁
吉非替尼小鼠体内药代动力学研究
张 佳1,糜志远1,汤媛媛1,李 洁2
(1湖北工业大学生物工程与食品学院,湖北武汉430068;2武昌工学院食品工程学院,湖北武汉430065)
研究吉非替尼在小鼠体内的药动学。方法:小鼠灌胃两种剂量50及32.5mg/kg后用高效液相色谱法(HPLC)测定不同时间的血药浓度。色谱条件为Thermo ODS-2HYPERSIL色谱柱(4.6mm×250mm,5μm),流动相为V(甲醇)∶V(水(0.1%三乙胺))=75∶25体积比,检测波长为330nm,流速为1.0mL/min。用DAS2.0药动学软件处理数据。结果:吉非替尼血清浓度在1.5~6μg·mL-1内线性良好,最低检出质量浓度为20ng· mL-1,高、中、低浓度样品回收率分别为100.06%,99.85%,100.06%。两组剂量的吉非替尼在小鼠体内的药时曲线均符合二室模型,主要药动学参数:半衰期分别为20.49h和20.51h。药时曲线下面积AUC为12.7和8.5mg/(L·h)。表观分布容积Vd为118.2和113.4L·kg-1。平均驻留时间MRT为25.8h。结论:该方法选择性强,方法简单,能够准确测定小鼠给药后的血药浓度,对该药物的临床血药浓度检测和药代动力学研究有一定的参考价值。
吉非替尼;药动学;高效液相色谱法
肺癌是目前致死率最高的肿瘤疾病之一,其中非小细胞肺癌(non-small cell lung cancer,NSCLC)占肺癌发生率的80%以上,其5a生存率小于15%[1],吉非替尼(Gefitinib,又名Iressa)作为一种表皮生长因子受体(epidermal growth factor receptor,EGFR)酪氨酸激酶抑制[2-3],通过抑制肿瘤细胞信号传导,从而抑制肿瘤细胞的增殖与转移,促进其凋亡[4-5],吉非替尼主要是对含铂类化疗失败的晚期非小细胞肺癌(NSCLC)有一定的治疗作用,具有分子靶向性,对正常细胞的毒性小[6-8]。本品在水中溶解性较差(pH=1时微溶于水),并且对光不稳定,据报道,本品在人体内的生物利用度约为59%[9]。
本文主要研究了吉非替尼在小鼠体内的分布随时间的变化,采用高效液相色谱法测定血液中吉非替尼的含量,测定小鼠灌胃(ig)给药后血液中吉非替尼含量的变化,并求得相关药代动力学参数。
1 材料与方法
1.1 材料
1.1.1 药品与试剂 吉非替尼原料(含量99.8%,湖北兴银河化工有限公司,批号:20151210),吉非替尼对照品(自制),肝素钠(国药集团化学试剂有限公司),甲醇(色谱纯,美国Fisher公司),超纯水(自制),三乙胺(色谱纯,天津市科密欧化学试剂开发中心)。
1.1.2 仪器 QL-901型旋涡混合器(江苏海门市麒麟医用仪器厂),TGL-16C型离心机(上海安亭科学仪器厂),美国赛默飞Thermo Ultimate 3000型双三元液相色谱仪,自动进样器(Thermo)
1.1.3 动物 昆明种小鼠(SPF级,体重20±2g),湖北省实验动物研究中心,许可证号:SCXK(鄂)2016-0005。
1.2 方法
1.2.1 溶液配制 准确取干燥至恒重吉非替尼原药,用甲醇制成质量浓度为500μg/mL标准储备液,备用。
取小鼠空白血清0.5mL,加入吉非替尼对照溶液1.0mL,按照上述3血清样品配制方法制备含有吉非替尼的血清样品,20μm微孔滤膜过滤,取续滤液,备用。
取小鼠血浆到已加入0.5mL肝素钠溶液(1000u/mL)的离心管中,6000r·min-1离心10 min,取上清液1.0mL,加入3.0mL甲醇,旋涡振荡0.5min,混匀,6 000r·min-1离心,20μm微孔滤膜过滤,取续滤液20μL注入液相色谱仪,记录色谱图。
1.2.2 实验动物 取小鼠180只,体重(20±2)g,雌雄各半,分为2组,每组90只,每个时间点5只,实验前禁食12h,自由饮水,根据易瑞沙(吉非替尼片)说明书制定本实验给药剂量,第一组灌胃(ig)50 mg/kg,第二组32.5mg/kg,给药后于0.5,1,2,3,4,5,6,8,10,12,15,18,21,24,27,30,36,48h后摘眼球取血1.0mL,提前加入0.5mL 1000u/mL肝素钠抗凝,按前述方法配制血清样品,按照标准曲线法测定各时间点血药浓度。
1.2.3 色谱条件 参考文献[10-11],最终确定色谱条件为Thermo ODS-2HYPERSIL色谱柱(4.6 mm×250mm,5μm),流动相为V(甲醇)∶V(水(0.1%三乙胺))=75∶25[12-13],检测波长为330 nm,流速为1.0mL/min,进样量为20μL,理论塔板数按吉非替尼峰计算大于5000。
1.2.4 方法专属性 吉非替尼对照品溶液、吉非替尼血清样品溶液、空白血清样品等三种溶液,分别取20μl注入液相色谱仪,记录色谱图。
1.2.5 最低检测限与定量限 定量稀释血清样品,使其HPLC图谱中主峰面积的信噪比(S/N)为3.0时样品的进样总量作为最低检测限,S/N为10.0时样品的进样总量作为定量限。
1.2.6 标准曲线 取血清0.2mL,分别加入标准储备液,按照前述步骤配制样品,配制浓度分别为0.2、2、4、6、8μg/mL的溶液,用20μm微孔滤膜过滤,各取续滤液20μL注入液相色谱仪,记录色谱图,以吉非替尼浓度为横坐标,以峰面积为纵坐标做曲线,得到回归方程。
1.2.7 回收率 将吉非替尼对照溶液加入到空白血清中,按照前述标准血清样品配制方法,制备4、5和6μg/mL 3种质量浓度的血清样品,注入液相色谱仪,记录色谱图,结果代入回归方程后得到其对应质量浓度,与标识的血清样品浓度相比即为本方法的相对回收率。
1.2.8 精密度 分别配制吉非替尼浓度为4μg/mL,5μg/mL,6μg/mL的含药血清样品,分别在1 d内测定6组以及连续5d测定其浓度,计算相对标准偏差RSD。
1.2.9 溶液稳定性 配制浓度为4μg/mL,5μg/mL,6μg/mL的含药血清样品,并在0、1、2、3、6h时间点测定,计算RSD。
2 结果
2.1 专属性
三种溶液的HPLC图谱见图1。可见吉非替尼血清样品与吉非替尼对照品溶液主峰出峰时间一致,且空白血清样品在主峰处无色谱峰。
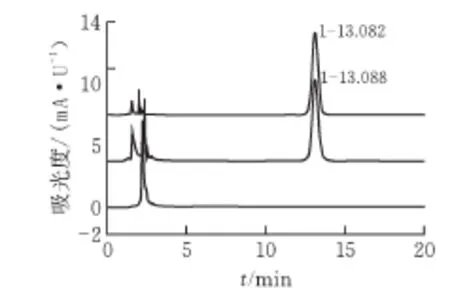
图1 空白血浆、吉非替尼对照溶液和含药血浆样品HPLC图谱
2.2 最低检测限与定量限
最低检测限和定量限分别为2ng和4.8ng,其HPLC图谱如图2所示。
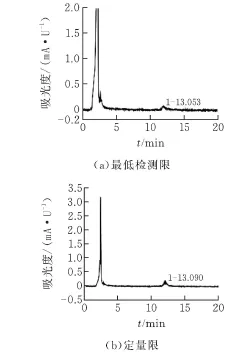
图2 HPLC图谱
2.3 标准曲线
标准曲线(图3)结果表明,在0.2~8μg/mL的浓度范围内,血清样品中吉非替尼浓度与主峰面积呈良好线性关系,可以准确测定血液中吉非替尼含量,得到的标准曲线为y=0.5469x-0.0465,R2=0.9992。
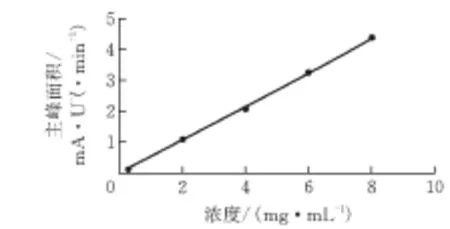
图3 吉非替尼血浆样品标准曲线
2.4 回收率
回收率结果见表1,9份模拟样品平均回收率98.69%。
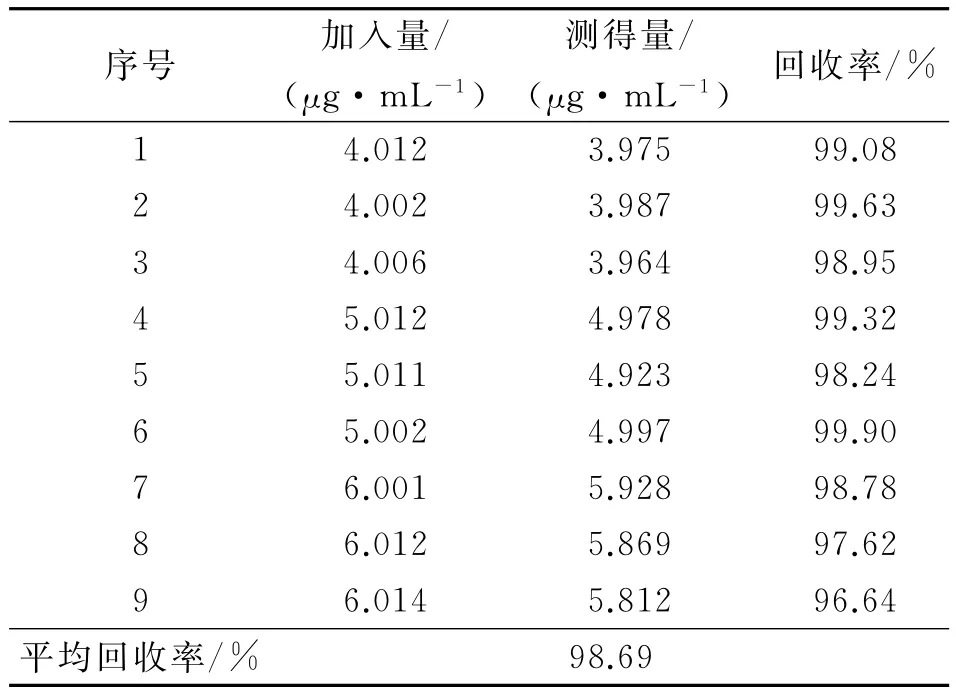
表1 回收率试验结果
2.5 精密度
结果3种质量浓度样品日内精密度(RSD)为3.6%,日间精密度(RSD)为4.9%(d=5),日内精密度与日间精密度(RSD)均小于15%,符合生物样品测定要求。
2.6 溶液稳定性
将3种质量浓度样品溶液分别在0,1,2,3,4,6小时测定,峰面积的RSD为4.12%,表明样品溶液在6h内稳定。
2.7 药时曲线及药代动力学参数
根据各时间点测定的血药浓度绘制药-时曲线,将数据通过DAS2.0程序拟合,根据F检验和AIC值选择适当的房室模型,AIC值越小,拟合度越好,结果表明口服吉非替尼后小鼠体内的动力学符合二室模型。药时曲线见图4。
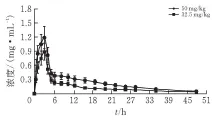
图4 小鼠灌胃两种剂量吉非替尼血液浓度—时间曲线n=5
根据非房室模型统计矩参数的方法,计算主要动力学参数(表2)。
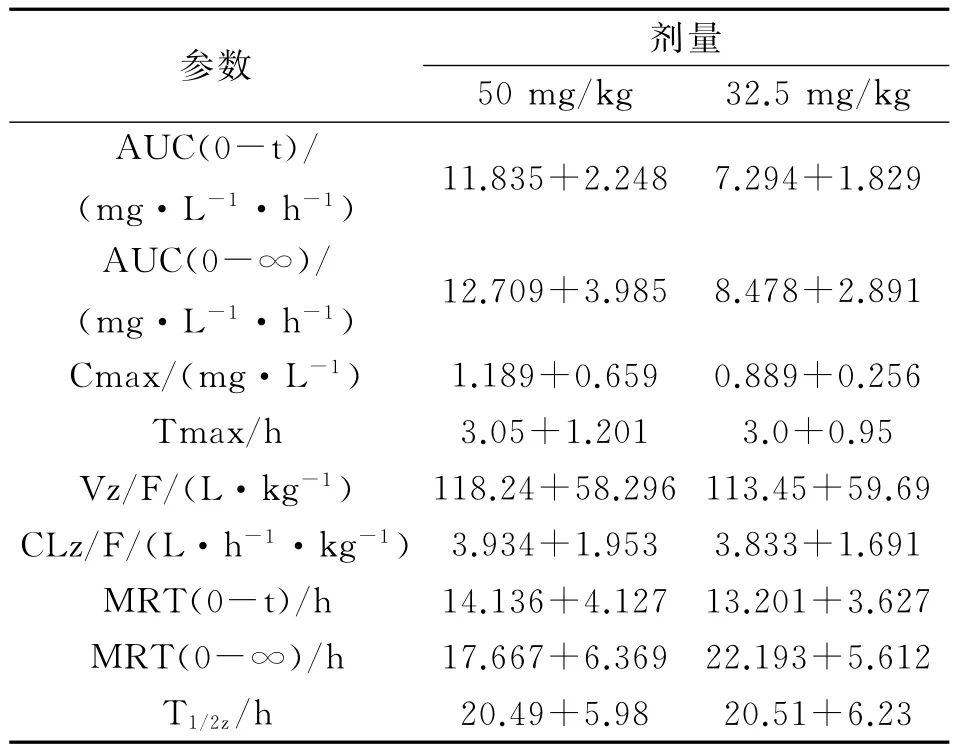
表2 灌胃两种剂量吉非替尼后在小鼠体内的动力学参数(n=5,∞±S)
3 讨论与结论
作为一种具有靶向功能的抗肿瘤药物,吉非替尼在临床上有一定的治疗价值,特别是针对非小细胞肺癌。本实验对吉非替尼在小鼠体内的动力学行为进行了研究。根据本品临床使用剂量(250mg,每天一次),本研究设计试验组剂量为50及32.5 mg/kg两组,和临床使用量相对应;给药途径为灌胃给药,和临床使用途径一致,取样周期为48h,符合一般药代动力学研究的要求。数据经DAS2.0软件处理。结果表明吉非替尼清除相半衰期为约为20h,故临床上设计为1次/d给药;达峰时间(Cmax)比较适中,为3h左右;血浆药物浓度-时间曲线下面积(AUC)与给药剂量成正比。本实验血液样品处理方法为液液萃取法,可以防止测定过程血液中其他成分(特别是蛋白质)的干扰。由于采用高效液相色谱法测定样品含量,方法专属性强,最低检测限为2ng,检测灵敏度较高,回收率试验也证明了该方法的可靠性。
综上所述,该方法选择性强,操作简单,能够准确测定小鼠的血药浓度,对该药物的临床应用有一定的参考价值。
[1] Jemal A,Murray T,Samuels A,et al.Cancer statistics[J].CA Cancer J Clin,2003,53(1):5-26.
[2] 王超,张鑫松,汪泉.六元并五元环母核类EGFR酪氨酸激酶抑制剂的研究进展[J].广东化工,2017,44(340):63-65.
[3] 徐祎春,韩峻松,李跃.肿瘤治疗中小分子激酶抑制剂的研究进展[J].生命科学,2016,28(7):786-792.
[4] Schmidt M,Maurer-gebhard M,Groner B,et al.Suppression of metast-asis formation by a recombinant single chain antibody-toxintargeted to full length and oncogenic variant EGF receptors[J].Oncogene,1999,18(9):1711-1712.
[5] Ciardiello F,Caputo R,Bianco R,et al.Inhibition of growth factor production and angiogenesis in human cancer cells by ZD1839(Iressa),a selective epidermal growth factor receptor tyrosine kinase inhibitor[J].Clin Cancer Res,2001,7(5):1459-1465.
[6] 张骁,张韬.吉非替尼研究进展[J].中国制药信息,2010,26(10):7-12.
[7] 焦海涛,王爱民,田焕娜,等。吉非替尼对敲低ANXA7的HepG2细胞增殖和凋亡的影响[J].中国细胞生物学学报,2015,37(12):1666–1671.
[8] 方利洲,刘凌,张剑青,等.吉非替尼对中、晚期非小细胞肺癌患者血清MMP-7、MMP-9表达的影响[J].基因组学与应用生物学,2016,35(11):2909-2915.
[9] AstraZeneca.IRESSA(gefitinib tablets)instruction[Z].2003.
[10]叶国健,秦凌浩,胡巧红.吉非替尼片含量测定方法考察[J].广东化工,2016,45(319):91-92.
[11]吴丽明,黄国红,李庆国.高效液相色谱法测定吉非替尼的含量[J].当代医学,2011,17(25):23-25.
[12]Jones H K,Stafford LE,Swaisland HC,et al.A sensitive assay forZD1839.(Iressa)in human plasma by liquid-liquid extraction and high performanceliquid chromatography with mass spectrometric detection:validationand use inPhaseⅠclinical trials[J].Journal of Pharmaceutical and BiomedicalAnalysis,2002,29:221-228.
[13]Lionel F,Charline G,Olivier M,et al.A simple HPLCUV method for the simultaneous quantification of gefitinib and erlotinib in human plasma[J].Journal of Chromatography B,2011,879(23):2345–2350.
Study on Pharmacokinetics of Gefitinib in Mice
ZHANG Jian1,MI Zhiyua1,TANG Yuanyuan1,LI Jie2
(1 School of Food and Biological Engineering,Hubei Univ.of Tech.,Wuhan 430068,China,2 School of Food Engineering,Wuchang Institute of Technology,Wuhan 430065,China)
This paper reports a study on the pharmacokinetics of gefitinib in mice.After intragastric administration of gefitinib at two doses of 50and 32.5mg/kg in mice,the plasma concentration at different times were measured by HPLC.The chromatographic conditions were:Thermo ODS-2HYPERSIL column(4.6mm×250mm,5μm)with a mobile phase of methanol-water(0.1%triethylamine)=(75∶25),detection wavelength was at 330nm,the flow rate was 1.0mL/min.Data were processed with DAS2.0pharmacokinetic software.Results show that the concentration of gefitinib was linear in the range of 1.5~6μg·mL-1.The lowest detectable concentration was 20ng·mL-1.The recoveries of gefitinib were 100.06%,99.85%and 100.06%respectively.The pharmacokinetic parameters of gefitinibin two groups of mice,T1/2is 20.49and 20.51h.The area under the curve AUC(mg·L-1·h-1)was 12.7and 8.5.The apparent distribution volume Vd(L·kg-1)was 118.2and 113.4.The average residence time MRT(h)was 25.8.It is concluded that the method has the advantages of high selectivity,simple,accurate and has certain reference value for the clinical blood drug concentration detection and pharmacokinetic study.
Gefitinib;Pharmacokinetics;HPLC
R962
A
[责任编校:张 众]
1003-4684(2017)04-0087-04
2017-05-24
张 佳(1987-),男,陕西眉县人,工学硕士,湖北工业大学实验师,研究方向为药物制剂开发
糜志远(1963-),男,湖北武汉人,湖北工业大学副教授,研究方向为药物开发应用
