基于荧光光谱研究Cryptophane-A对甲烷及氯仿的识别作用
2017-09-16陈慧斐黎学明杨建春
陈慧斐,黎学明,杨建春
(1.重庆大学化学化工学院,重庆 401331;2.重庆大学光电学院,重庆 400044)
基于荧光光谱研究Cryptophane-A对甲烷及氯仿的识别作用
陈慧斐1,黎学明1,杨建春2
(1.重庆大学化学化工学院,重庆 401331;2.重庆大学光电学院,重庆 400044)
超分子主体化合物能够有效地包封小分子,从而形成主-客体化合物,这类化合物在分子识别、信息传递以及超分子材料等方面具有强大的的应用潜力。本文用直接法通过正交试验设计合成cryptophane-A,得到最优组合条件是:60℃和甲酸用量为1524:1下反应5h。通过搭建Y型光纤甲烷传感平台,得出cryptophane-A荧光强度在甲烷浓度从0.1%到3.5%范围内呈线性变化,其荧光强度随甲烷浓度增加而减弱,甲烷与cryptophane-A以接近1比1的比例络合,实验搭建的测量装置甲烷检测限为 0.1%。其中甲烷浓度为1.5%时,荧光恢复时间是荧光猝灭时间的两倍。另外,cryptophane-A与氯仿可发生较为稳定的络合作用。
Cryptophane-A;荧光猝灭;甲烷;氯仿
中性或带电的包合物受到相当大的关注。这类复合物与客体形成特异性非共价键[3],有的已经在广泛应用中被发现,包括分子识别[4]、药物递送[5]、分离和储存[6]、生物感应[7]和催化[8]。这类有机受体,对封装的客体分子具有特定的选择性。例如,手性cryptophane-C能够区分两种对映异构体的CHFClBr[9],水溶性cryptophane-O很容易区分胆碱和乙酰胆碱[10]。X射线确定晶体结构通常为球形cryptophanes[11]。施[12]通过合成cryptophane-M,能特异性识别氯仿。因此,这类超分子对于分子识别有很强的潜力。
甲烷及其氯化物之一的三氯甲烷是一类对安全生产、环境和人体健康有重要影响的气体,其中甲烷气体是煤矿事故的“头号杀手”,也是天然气储运、加工、使用过程中的重要危险源[13-17],而挥发性三氯甲烷则可作用于中枢神经系统,具有麻醉作用,对心、肝、肾有损害,吸入后引起急性中毒[18]。因此监测甲烷及挥发性三氯甲烷的浓度对于煤矿安全生产、天然气安全使用、人体健康具有十分重要的意义。
1 实验方法
1.1 Cryptophane-A的合成
有机试剂均来自于重庆药物与化学试剂公司,其他的化学用品和试剂除了特别提到的均买自Aldrich公司。有机试剂的干燥采用标准实验室操作方法。使用前,实验用品通过重蒸或者重结晶进行前期净化。
Cryptophane-A是由香兰素通过已知合成路径(如图1)进行合成。其中二醛化合物以及二醇化合物的合成产率分别达到80%和90%以上,终产物的产率相对较低,约6%,因此,对最后一步进行正交优化,选取影响因素:反应温度、反应时间以及反应甲酸用量三个因素,各个因素下以现有取值为基础左右浮动数据分别得到三个水平。遵照正交表选取规则,使用三因素三水平的正交表进行试验设计。
因素A,反应温度:40℃,60℃,80℃
因素B,反应时间:1h,3h,5h
因素C,反应物物质的量比:1524:1,1824:1,2124:1

图1 Cryptophane-A合成路线
Fig.1 Synthesis of cryptophane-A
在室温下,对中间产物以及最终产物进行核磁共振分析,实验所得的 cryptophane-A的1 H NMR (CDCl3)数据与文献参考一致。
1.2 Cryptophane-A对甲烷的响应
以抛光p型Si晶片为基片,通过水蒸气辅助法形成多空膜。cyptophane-A成膜溶液配制:称取cryptophane-A 0.01 g, 0.5 g乙基纤维素,溶于10 mL V(二氯乙烷): V(无水乙醇) = 1/1的混合溶剂中,室温搅拌30min后超声处理2 h待用。
1.3 Cryptophane-A溶于不同有机溶剂
取Cryptophane-A固体粉末分别溶解于乙酸乙酯、1,2-二氯乙烷、二氯甲烷、丙酮、1,4-二氧六环、氯仿有机溶剂中配制成浓度为2.0×10-5mol/L的溶液,对新配制的溶液进行荧光光谱检测,超声2h静置后对溶液再次进行荧光检测。365nm紫外灯下溶液分别产生荧光,如图2所示,从左到右依次为乙酸乙酯、1,2-二氯乙烷、二氯甲烷、乙腈、1,4-二氧六环、氯仿。

图2 365nm紫外灯照射下cryptophane-A(2 × 10-5mol·L-1)溶于不同有机溶剂的照片
(a:新配好的溶液, b:超声静置后的溶液)
Fig.2 Picture of cryptophane-A (2 × 10-5mol·L-1) in different solvents irradiated by a hand-held UV lamp at 365 nm
(a. freshly-prepared solution, b. sonicated solution)
1.4 不同浓度氯仿溶液对cryptophane-A(2×10-5mol·L-5)的荧光猝灭作用
为更好地探讨cryptophane-A 与氯仿之间的络合作用,取cryptophane-A溶于1,2-二氧六环溶剂中配制为2×10-5mol·L-1的溶液,考察不同浓度的氯仿溶液对cryptophane-A 的荧光猝灭情况。即配即测,通过对比体积浓度从0%到70%的氯仿溶液荧光光谱,研究不同浓度氯仿溶液对cryptophane-A(2×10-5mol·L-1)的荧光猝灭作用。
2 结果讨论
2.1 极差分析
正交实验极差分析法处理数据。按照分析方法计算出各因素下Kj和kj之后,由每个因素下kj的最大与最小值之差计算得极差Rj,根据Rj的大小排出各因素的主次顺序:2.71>2.52>1.70,因此各因素对试验结果的影响大小排序为A>C>B;另外,根据各因素不同水平下的Kj,得到因素下对试验结果影响较大的水平,对应本实验结果既是A2 、B3和C1,优组合为A2C1B3,即实验优化条件是60℃和甲酸用量为1524:1下反应5h,产率为8.83%。
2.2 Cryptophane-A对甲烷的响应
2.2.1 反应原理
许多物质可用作荧光猝灭剂,其中最广为人知的当属氧气分子,可猝灭多种常见荧光团。在论文中,所合成的cryptophane-A结构在紫外灯照射下均可发出较强紫色荧光,氯仿和甲烷分子分别被用于猝灭这些超分子的荧光。
① 动态猝灭可通过Stern-Volmer方程描述:

(1)
其中,F和F0分别为猝灭发生前后的荧光强度,kq为两种物质键的猝灭系数,τ0是荧光物质在没有猝灭剂存在的情况下的荧光寿命,而[Q]则为猝灭剂的浓度,kq与τ0的乘积可表达为KD,称为猝灭常数,若某一猝灭过程已知为碰撞猝灭,则记为KD,否则记为KSV。
② 静态猝灭原理:动态猝灭是一个很大程度上依赖时间的过程,但静态猝灭则完全是由于新的复合物生成且吸收光返回基态不辐射光子所致。这种过程中,荧光强度与猝灭剂浓度相关,也与猝灭剂和荧光物质的络合系数相关。络合常数Ks可表达为:
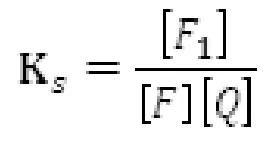
(2)
其中[F1]为络合物浓度,[F]是未络合的荧光物质浓度,[Q]则是猝灭剂浓度,若络合物为费荧光物质,则残留荧光比例可表达为:

(3)
总的荧光物质浓度[F0]=[F]+[F1],带入公式3,则有

(4)
变形得:

(5)
与动态猝灭类似,静态猝灭也被期望为猝灭过程,与动态猝灭不同之处在于,除了与猝灭剂浓度相关外,动态猝灭主要依赖于猝灭常数,而静态猝灭依赖于络合常数。
2.2.2 不同浓度甲烷传感研究

图3 Cryptophane-A在不同浓度甲烷气体中的荧光光谱
Fig.3 Fluorescence spectra of cryptophane-A in methane with different concentrations (v %). From 1 to 9: 0, 0.1, 0.5, 1.0, 1.5, 2, 2.5, 3,3.5

图4 ln(F0/F1) ~ ln[Q]校准曲线Fig.4 Benesi-Hildebrand plot of ln(F0/F1) versus ln[Q]
通过搭建好的Y型光纤检测平台,对浓度为0.1%到3.5%的甲烷与cryptophane-A的络合作用进行考察。增大甲烷浓度则荧光强度呈梯度下降趋势(图3),主峰位置位于438nm附近。实验选取438.11 nm处的数据,考察ln(F0/F1)与ln[Q]相互关系,发现浓度从0.1%到3.5%范围内呈线性变化(图4),通过线性拟合得出直线斜率为0.92622,证明甲烷与cryptophane-A的络合作用以接近1:1的比例进行,截距为-3.54433,计算得到络合常数Ks为0.05%-1。实验所搭建的检测平台的检测限为0.1%。
2.2.3 传感器响应和恢复时间研究
为研究此甲烷传感的响应时间和恢复时间,以氮气为载气,对暴露于1.5%甲烷的响应做了特定研究。荧光猝灭与荧光恢复-时间关系,如图5,光源波长为376nm。

图5 cryptophane-A荧光猝灭与恢复时间图(1.5%甲烷)
Fig.5 Fluorescence quenching and recovery of cryptophane-A versus time(1.5% methane )

图6 荧光猝灭与恢复F0/F-时间关系Fig.6 Fluorescence quenching andrecovery intensity F0 / F versus time
甲烷浓度控制在1.5%时,每隔6s记录一次cryptophane-A的荧光光谱,先通入N2,以排除气室中的空气,只通入N2的cryptophane-A荧光强度处于稳定,随后通入1.5%甲烷气体,荧光强度迅速下降,30 s内达到稳定,荧光猝灭发生在这30s内,对荧光猝灭过程做F0/F与时间t的关系图,如图6(a)。稳定后,将甲烷气体浓度设置为0%,只通入N2,荧光强度开始恢复,60s后荧光强度恢复到甲烷浓度为0%的强度,对荧光猝灭过程做F0/F与时间t的关系图,如图6(b)。荧光猝灭拟合斜率为0.00146,荧光恢复拟合斜率为-0.00112,说明荧光猝灭速度快于荧光恢复的速度,分析原因为,甲烷气体进入cryptophane-A空腔容易,而解析出来相对困难。
2.3 Cryptophane-A对氯仿的响应
2.3.1 Cryptophane-A在不同溶剂中的荧光光谱
采用不同溶剂新配制的溶液,对于cryptophane-A的荧光光谱,如图7(a),没有观察到明显的差异,然而如图7(b),超声2h并静置后,其中尤以氯仿溶液变化最明显,其荧光强度大幅度减弱。另一方面,其他溶剂超声处理后,cryptophane-A溶液的荧光光谱中无明显变化,如图7所示。

图7 不同溶剂cryptophane-A(2 × 10-5mol·L-1)在不同有机溶剂中(a 新配置的溶液,b 超声静置后的溶液)的荧光光谱(激发波长376 nm)
Fig.7 Fluorescence spectra (exited by 365 nm) of cryptophane-A (2 × 10-5mol·L-1) in different solvents (a )freshly-prepared solution(b)sonicated solution)( excitation wavelength:376nm)
2.3.3 Cryptophane-A与氯仿的络合
通过对比体积浓度从0%到70%的氯仿/1,2-二氧六环溶液荧光强度,考察不同浓度的氯仿溶液对2×10-5mol·L-1cryptophane-A 的荧光猝灭情况,如图8(a)为即配即测的不同浓度氯仿溶液荧光光谱,图8(b)为超声静置后不同浓度氯仿荧光光谱。新配置的氯仿溶液浓度越大,cryptophane-A的荧光猝灭则增强,荧光强度依次减弱。但超声处理后的溶液中,不含氯仿的溶液荧光未有明显变化,不同浓度氯仿溶液荧光猝灭均很彻底,荧光基本消失。

图8 cryptophane-A在不同氯仿浓度中的荧光光谱(a 新配置的溶液,b 超声静置后的溶液)
Fig.8 Fluorescence spectra of cryptophane-A in chloroform with different concentrations (v %). From 1 to 9: 0, 0.1, 0.2, 0.3, 0.4 , 0.5, 0.6,0.7 (a )freshly-prepared solution(b)sonicated solution
将体积比换算为摩尔浓度,对cryptophane-A在不同浓度氯仿溶液的荧光强度对浓度进行拟合,以ln(F0/F1)对ln[Q]作图,得到一条直线(图9)。通过线性拟合得出直线斜率为0.73515, 即为cryptophane-A与氯仿的络合比,说明二者以该比例发生络合作用,近似看成一分子空腔内封装一个氯仿分子,可发生较为稳定的络合作用,络合常数KS 通过计算为455.1 M-1。

图9 ln(F0/F1) ~ ln[Q]校准曲线Fig.9 Benesi-Hildebrand plot of ln(F0/F1) versus ln[Q]
3 结论
本文给出了如下结论:
(1)设计三因素三水平的L9(34)正交试验,研究了反应温度、反应时间以及甲酸与反应原料物质的量比三个因素下分别三水平时的反应产率。试验数据处理采用正交实验的极差分析和因素趋势图法,得到的最优组合条件是:60℃和甲酸用量为1524:1下反应5h,优化产率为8.83%。
(2)Cryptophane-A能选择性识别甲烷,甲烷与cryptophane-A的络合比接近1:1,络合常数为0.05%~1%。实验所搭建的检测平台的检测限为0.1%。且甲烷浓度为1.5%时,荧光猝灭时间为30s,荧光恢复时间为60s,且荧光猝灭速度比荧光恢复速度快。
(3)因为甲烷与氯仿不会同时存在,所以cryptophane-A也能用于识别氯仿分子,二者络合比接近1:1,且随氯仿浓度增大,荧光猝灭越强。
[1] Brotin T, Dutasta J P. Cryptophanes and their complexes-present and future[J]. Chem Rev, 2009,109(1):88-130.
[2] Chaffee K E, Fogarty H A, Brotin T, et al. Encapsulation of small gas molecules by cryptophane-111 in organic solution. 1. Size- and shape-selective complexation of simple hydrocarbons[J].Phys Chem A, 2009,113(49):13675-13684.
[3] Diez N M, de la Pena A M, Garcia M C ,et al. Fluorimetric determination of sulphaguanidine and sulphamethoxazoleby host-guest complexation in beta-cyclodextrin and partial least squares calibration[J]. J Fluoresc, 2007,17(3):309-318.
[4] Enoch I V M V, Swaminathan M .Fluorimetric study on molecular recognition of beta-cyclodextrin with 2-amino-9-fluorenone[J]. J Fluoresc,2006,16(4):501-510.
[5] Chen Y, Pang Y, Wu J L, et al. Controlling the particle size of interpolymer complexes through host-guest interaction for drug delivery[J]. Langmuir ,2010,26(11):9011-9016.
[6] Benounis M, Jaffrezic-Renault N, Dutasta J P, et ai. Study of a new evanescent wave optical fibre sensor for methane detection based on cryptophane molecules[J]. Sens Actuators B,2005,107(1):32-39.
[7] Kim B S, Ko Y H, Kim Y, et al. Water soluble cucurbit[6]uril derivative as a potential Xe carrier for Xe-129 NMR-based biosensors[J]. Chem Commun,2008,24:2756-2758.
[8] Marjanska M, Goodson B M, Castiglione F, et al. Inclusion complexes oriented in thermotropic liquid-crystalline solvents studied with carbon-13 NMR[J]. Phys Chem B,2003,107(46):12558-12561.
[9] Chaffee K E, Marjanska M, Goodson B M . NMR studies of chloroform@cryptophane-A and chloroform@bis-cryptophane inclusion complexes oriented in thermotropic liquid crystals[J]. Solid State Nucl Mag,2006,29(1-3):104-112.
[10] Bouchet A, Brotin T, Cavagnat D, et al.Induced chiroptical changes of a water-soluble cryptophane by encapsulation of guest molecules and counterion effects[J]. CheStudy on the Recognition of CH4and CHCl3by cryptophane-A Based on Fluorescence Spectra.m Eur,2010 ,16 (15):4507-4518.
[11] Petrov O, Tosner Z, Csoregh I, et al.Dynamics of chloromethanes in cryptophane-E inclusion complexes: A H-2 solid-state NMR and X-ray diffraction study[J]. J Phys Chem A,2005,109(20):4442-4451.
[12] Shi Y, Li X, Yang J, et al. Efficient encapsulation of chloroform with cryptophane-M and the formation of exciplex studied by fluorescence spectroscopy[J],J Fluoresc, 2010, 21:531-538.
[13] 陈淑华, 罗光荣. 生物有机化学[M]. 成都: 四川大学出版社, 1991.
[14] Lehn J M. Supramolecular chemistry-scope and perspectives molecules, supermolecules, and molecular devices[J]. Angew. Chem. Int. Ed. Engl, 1988, 27(1): 89-112.
[15] 刘 育,尤长城. 超分子化学[M].天津:南开大学出版社, 2001, 320-361.
[16] Beletskaya I, Tyurin V S, Tsivadze A Y, et al. Supramolecular chemistry of metalloporphyrins[J]. Chem Rev, 2009, 109(5): 1659-1713.
[17] 王 宇,唐黎明. 氢键识别超分子聚合物的新进展[J]. 化学进展, 2007, 19(5): 769-778.
[18] 周成合,张飞飞,甘淋玲,等. 超分子化学药物研究[J]. 中国科学B辑:化学, 2009, 39(3): 208-252.
(本文文献格式:陈慧斐,黎学明,杨建春.基于荧光光谱研究Cryptophane-A对甲烷及氯仿的识别作用[J].山东化工,2017,46(14):1-5.)
Study on the Recognition of CH4and CHCl3by Cryptophane-A Based on Fluorescence Spectra
ChenHuifei1,LiXueming1,YangJianchun2
(1.Chemistry and Chemical Engineering School,Chongqing University,Chongqing 401331,China;2.Optoelectronic Engineering School,Chongqing University 400044,China)
The supramolecular host compounds are capable of efficiently encapsulating small molecules to form host-guest compounds, which have potent application potential in molecular recognition, information transfer, and supramolecular materials. In this paper, cryptophane-A was synthesized by orthogonal design, getting that the optimum conditions were as follows: 60 ℃ and the amount of formic acid were 1524: 1 for 5 h. The fluorescence intensity of cryptophane-A was linearly while the methane concentration changed from 0.1% to 3.5%, and the fluorescence intensity decreased with the increase of methane concentration. The ratio of cryptophane-A complexing with chloroform is close to 1:1, and the limit detection of methane concentration is about 0.1% . When the methane concentration is 1.5%, the fluorescence recovery time is twice as long as the quenching time.Also, cryptophane-A complexes stably with chloroform.
cryptophane-A; fluorescence quenching; methane; chloroform
2017-05-16
国家自然科学基金(61271059)
陈慧斐(1991—),女,四川绵阳人,重庆大学化学化工学院研究生在读,主要方向为分析化学以及光纤甲烷传感。
O659.21
A
1008-021X(2017)14-00-01-05
科研与开发
