注射用牡荆素的冻干工艺参数优化
2017-09-08牛海军李晓亮李光辉
牛海军,李晓亮,邵 旭,许 亮,李光辉
(安徽九方药物研究院有限公司,安徽 合肥 230088)
·实验研究·
注射用牡荆素的冻干工艺参数优化
牛海军,李晓亮,邵 旭,许 亮,李光辉
(安徽九方药物研究院有限公司,安徽 合肥 230088)
目的 优化注射用牡荆素的冻干工艺。方法 以外观、复溶性、pH、水分为指标,对冻干工艺中的参数进行优化。结果 优化的冻干工艺为,预冻开始至+25~-40℃,2 h;-40℃,3 h;温度逐渐升至-20℃,再由-20℃逐渐升至25℃。整个升华干燥过程约26 h,在25℃下干燥约5 h。结论 通过优化冻干工艺参数,所得注射用牡荆素的冻干制品外观平整,质地疏松,加生理盐水可迅速溶解分散成澄明溶液。
注射用牡荆素;低共熔点;冷冻干燥;冻干曲线;工艺优化
牡荆素是从山楂叶中提取纯化而得的纯度达99%以上的单一化合物,成分明确,质量可控。牡荆素口服给药生物利用度试验结果表明,灌胃给药后,在大鼠体内几乎无吸收,或吸收后很快被代谢,生物利用度几乎为零[1-5]。注射用牡荆素可通过提高心肌组织抗氧化能力,保护心肌细胞膜,从而保护缺血受损的心肌。牡荆素为黄酮类化合物,其适应证为心血管类疾病,难溶于水,因其口服吸收利用度较低,做成注射制剂较好。注射剂的质量要求较严,包括无菌、无热原、澄明度、渗透压、安全性、稳定性等项目[6-7]。在水性环境中,牡荆素的稳定性、微生物等都不能很好地控制,贮存期短,且进行灭菌处理时也易损害药物活性。冷冻干燥是将需要干燥的药物溶液先预冻成固体,然后在低压低温的环境下,不经过液态,从冻结状态直接升华除去所含水分的一种干燥方式。冻干是低温真空干燥,不会破坏药物活性,且能使微生物失去生物活力,延长贮存期[8-12]。经过冷冻干燥的物品易于长期保存,加水溶解后能恢复到冷冻前的形态,且能保持原有的生物、化学特性[13-15]。对于部分生化药物,因其不稳定的物理、化学特性,冻干已被实践证明为一种非常有效的手段。冷冻干燥的具体过程分为预冻、升华干燥和二次干燥(解析干燥)。本试验中以注射用牡荆素冻干后再分散后的外观、复溶性、pH、水分为考察指标,对注射用牡荆素的冻干工艺进行了考察。现报道如下。
1 仪器与试药
1.1 仪器
PHS-3C型pH酸度计(上海仪电科学仪器股份有限公司);FD5-2.5E型冷冻干燥机(美国西盟国际集团金西盟北京分公司);LC-10AT型液相色谱仪,包括LC-10AT色谱泵、SPD-M10Avp DAD检测器、SIL-10A自动进样器、LCsolution色谱工作站(日本岛津公司)。
1.2 试药
牡荆素原料(合肥七星医药科技有限公司,批号为160802,含量为99.6%);甘露醇(山东天力药业有限公司,批号为160518)。
2 方法与结果
2.1 冻干工艺考察
2.1.1 预冻条件
新产品冻干时,应先测其低共熔点,然后控制冷冻温度在低共熔点以下,以保证冷冻干燥的顺利进行。测定低共熔点的方法有热分析法和电阻法[16-17],根据实际情况,本试验中采用电阻法。配制处方溶液50 mL,置低温冰箱中冷至-50℃,冷冻5 h,取出,记录温度与相应的电阻值,结果见表1,并绘制低共熔点测定曲线(图1)。可见,拐点在-18℃,故低共熔点为-18℃。
制品干燥前必须进行预冻,如不经过预冻而直接抽真空,当压力降至一定程度时,溶于溶液中的气体迅速逸出引起类似“沸腾”现象,部分药液可能会冒出瓶外。预冻温度应低于共熔点10~20℃,因此预冻温度设定为-40℃;预冻时间常用2~3 h,本试验中选择预冻时间为3 h;预冻方法有速冻法和慢冻法,本试验中选择了慢冻法,+25~-40℃预冻2 h,-40℃预冻3 h。这样冻干较实,提高了冻干效率。

表1 低共熔点测定结果

图1 制品温度与电导率关系曲线图
2.1.2 隔板温度与时间
升华干燥时间:升华干燥法有一次升华法和反复升华法。一次升华法适用于低共熔点-10~-20℃的制品,且溶液浓度、黏度均不大,装量厚度在10~15 mm的情况。根据本品性质采用一次升华法,按上述确定的处方和工艺配制溶液,3 mL/瓶灌装于10 mL的西林瓶中,在低于-40℃下预冻3 h,同时将冷凝器温度下降至-45℃以下,启动真空泵,待真空度达到一定数值后,缓缓打开蝶阀,当干燥箱内的真空度达13.33 Pa(0.1 mmHg)以下时关闭冷冻机,通过隔板下的加热系统缓缓加热,供给制品升华过程中所需热量,使冻结产品的温度逐渐升至-20℃,药液中的水分就可升华,再使冻结产品的温度逐渐升至25℃,最后可基本除尽,然后转入在再干燥阶段。整个升华干燥过程约26 h。
再干燥时间:当升华干燥阶段完成后,为尽可能除去残余的水分,需进一步干燥。再干燥温度确定为25℃,时间约10 h。再干燥期间分别在第2,4,6,8,10 h时取样测定水分,结果再干燥5 h后水分基本除尽,达到要求。记录再干燥时间与冻干制品水分的考察结果,详见表2。可见,本品在冻干后外观为疏松块状,复溶后为澄明溶液,pH在要求范围之内,水分到最终也符合要求。
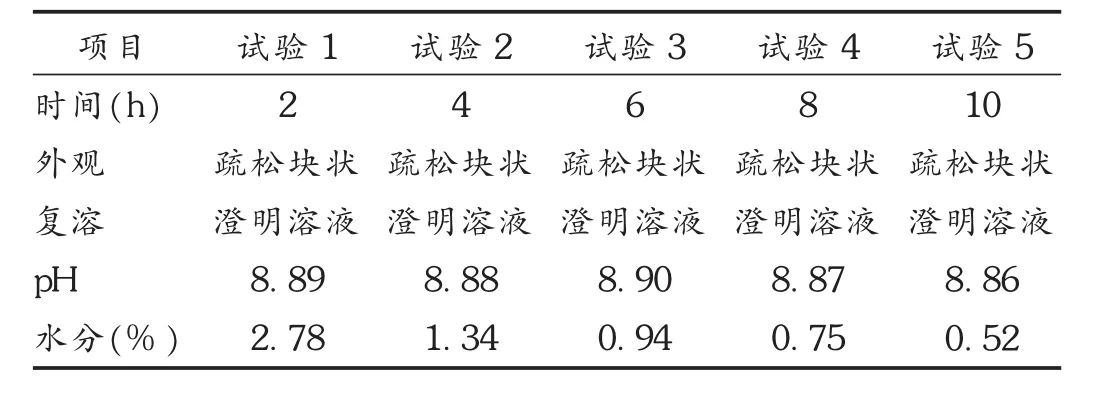
表2 再干燥时间与冻干制品水分的考察结果
2.2 工艺确定
预冻:把分装好的药品放入冻干箱内的隔板上,预冻开始至+25~-40℃,2 h;-40℃,3 h。
升华干燥:将冷凝器温度降至-45℃以下,启动真空泵,待真空度达到一定数值后,缓缓打开蝶阀,当干燥箱内的真空度达13.33 Pa(0.1 mmHg)以下时关闭冷冻机,通过隔板下的加热系统缓缓加热,使冻结产品的温度逐渐升至-20℃,再由-20℃逐渐升至25℃。整个升华干燥过程约26 h。
再干燥:在25℃下干燥约5 h,干燥失重符合规定。
绘制冻干工艺及曲线图[18-19],结果见图2。

图2 注射用牡荆素搁板温度与时间关系
2.3 样品试制
按上述确定的注射用牡荆素冻干工艺条件进行3批样品的试制,并对冻干温度、搁板温度与时间等工艺路线进行记录,确定生产工艺的可行性。结果见表3。可见,按同一处方工艺条件生产的3批样品,各项指标重复性良好,工艺条件可行。3批样品的冻干工艺既能达到满意的结果,又节省了时间,故选用该冻干工艺。
3 讨论
中药注射剂是指以中医药理论为指导,采用现代科学技术和方法,从中药或天然药物的单方或复方中提取的有效物质制成的、可供注入人体内的灭菌溶液、乳状液及供临床用前配置成溶液的无菌粉末或浓溶液。注射剂具有药效迅速,作用可靠,成分较明确,质量相对可控等特点,由于可以从皮内、皮下、肌内、穴位、静脉和脊椎腔等部位给药,为很多药物药效的发挥,尤其是临床治疗、急救和诊断开辟了新途径。
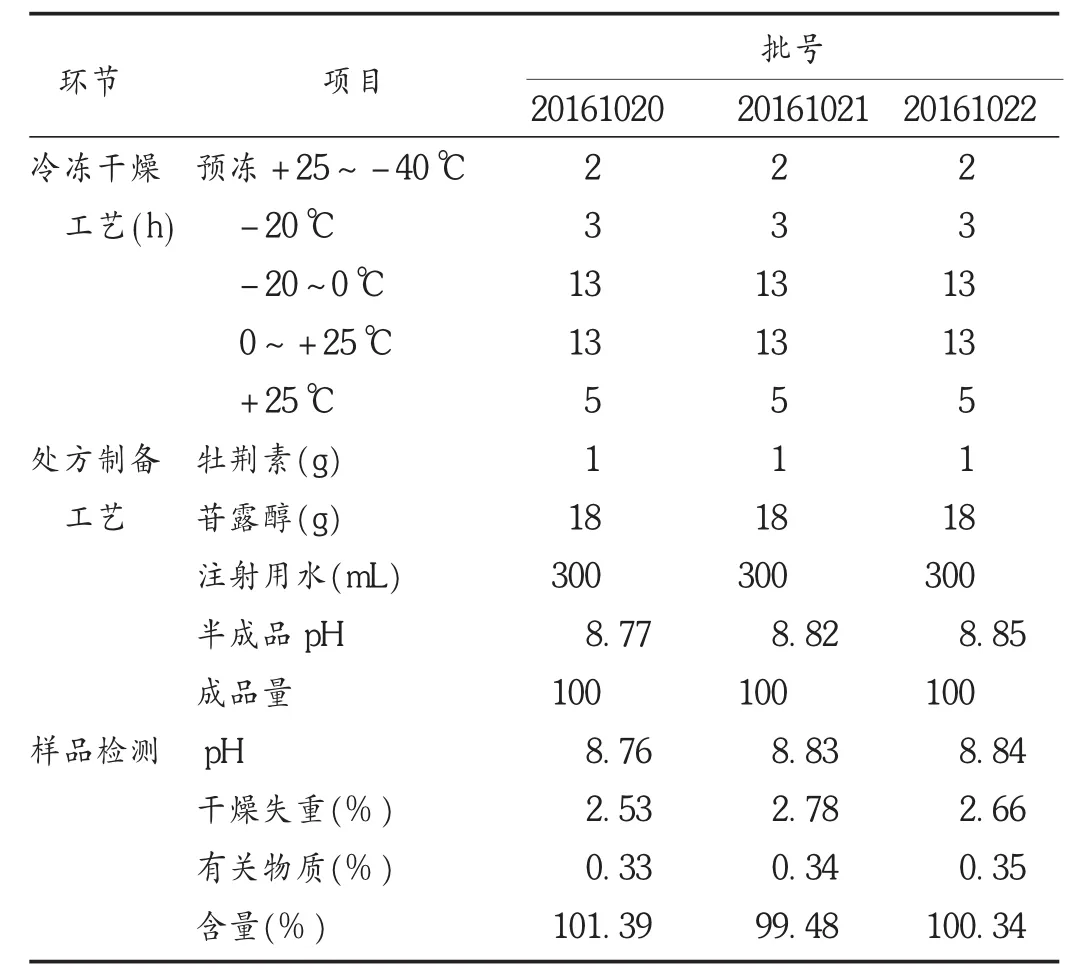
表3 3批样品冻干工艺及结果
牡荆素口服吸收差,因此制成注射剂用于临床。前期笔者对牡荆素小水针试验进行研究,样品溶液灭菌后虽短时间内能保持溶液的稳定性,但长时间放置会出现浑浊,含量降低,保证不了样品质量。鉴于小水针样品稳定性差,说明牡荆素原料制成小水针目前还不可行,故本试验中对牡荆素冻干粉针进行了研究。牡荆素的结构为碳苷,难溶于水,在不同pH水溶液中的溶解度随着pH的增加而增加,pH较高时在溶液中主要以离子形式存在,溶解度增大。工艺中采用为碱溶液调节pH使溶解,pH控制在 8.5±0.5。临床应用时静脉滴注,1次1~2瓶,用250 mL 0.9%氯化钠注射液溶解后使用。采用本品1~2瓶与250 mL不同pH条件及与不同厂家0.9%氯化钠注射液配伍,6 h内性状、pH、含量及有关物质基本稳定,人体血液的pH为7.40±0.05,药物浓度在缓慢滴入血液时,药物被稀释,浓度降低,保证了临床用药的安全性和有效性,为产品上市提供了基础。
冻干过程中最重要的过程参数是制晶的温度和干燥箱内的压力。冻干曲线就是表示冻干过程中产品的温度和压力随时间变化而变化的关系曲线。根据最佳处方,在生产质量管理规范(GMP)冻干粉针剂车间进行了3批中试样品的试生产,并对冻干温度、搁板温度与时间等工艺路线进行记录,3批样品冻干曲线一致,且制得样品均合格,质量稳定。冻干制品中主要残次品有塌陷、干缩、泡坑等,而其影响因素较多,如预冻时间不足,干燥时间上升过快等。通过低共熔点的测定,确定预冻的温度和时间,保证了冻结完全;通过隔板温度上升与时间的关系,确定冻干曲线,保证样品不被溶化,成型率较好。
[1]于 瑶,何金丹,王 振,等.牡荆素调节自噬对小鼠肝缺血/再灌注损伤的保护作用[J].实用器官移植电子杂志,2016,4(1):27-31.
[2]王亚男,彭成凤,甄毅岚,等.注射用牡荆素与葛根素注射液抗大鼠心肌缺血/再灌注损伤量效关系的研究[J].安徽医科大学学报,2015,50(3):314-318.
[3]董六一.牡荆素对心肌缺血/再灌注损伤的保护作用及其作用机制[D].合肥:安徽医科大学,2007.
[4]董六一,邵 旭,江 勤,等.牡荆素对大鼠实验性心肌缺血损伤的保护作用及其机制[J].中草药,2011,42(7):1378-1383.
[5]黄 勇,牟景丽,陈 慧,等.平衡透析法、超滤法结合液质联用技术比较测定注射用复方荭草中黄酮类成分的血浆蛋白结合率[J].中国实验方剂学杂志,2012,18(20):91-96.
[6]杨桂琴.中药注射剂不良反应原因分析[J].内蒙古中医药,2015(6):91.
[7]高 颖,郭 鹏,张静泽,等.中药注射剂的研究进展[J].武警医学院学报,2009,18(3):249-251.
[8]刘文伟,张国泰,田 田,等.真空冻干干燥技术在中药复方制剂生产中的应用[J].中国民族民间医药,2008,17(8):17-20.
[9]李文春,孙永慧,崔仁海,等.中药注射剂工艺中活性炭除热原效果评价[J].中国中医药信息杂志,2014,21(2):80-82.
[10]刘 嘉,刘汉清.冻干技术及其在中药冻干制剂中应用的研究进展[J].中国医药技术经济与管理,2007,1(5):34-42.
[11]郭东杰,顾成波,祖元刚,等.牡荆苷纳米混悬剂冻干粉的制备及表征[J].植物研究,2014,34(4):567-571.
[12]刘苗苗,叶利春,陈立军,等.真空冷冻干燥技术在中药研究中的应用[J].中药材,2014,37(5):909-911.
[13]李月婷,胡 杰,谢玉敏,等.UPLC法同时测定复方荭草冻干粉针中11种指标成分的含量[J].中国新药杂志,2015(5):588-591.
[14]朱咏梅.注射用山楂叶指纹图谱的研究[D].沈阳:沈阳药科大学,2006.
[15]朱思遥.山楂叶冻干粉针及化学成分的研究[D].沈阳:辽宁中医药大学,2006.
[16]黄传伟,梁晓会,范晓逶.冻干物料共晶点、共熔点测定仪的设计[J].医疗卫生装备,2010,31(4):15-17.
[17]崔清亮,郭玉明,程正伟.冷冻干燥物料共晶点和共熔点的电阻法测量[J].农业机械学报,2008,39(5):65-69.
[18]章清扬,丁 宁.关于冻干粉针剂工艺设计的探讨[J].健康必读,2012(4):401.
[19]王继波.浅谈中药冷冻干燥工艺曲线的制订[J].黑龙江科技信息,2010(35):74.
Optimization of Freeze-Drying Process Parameters of Vitexin for Injection
Niu Haijun,Li Xiaoliang,Shao Xu,Xu Liang,Li Guanghui
(Anhui Joyfar Pharmaceutical Research Institute Co.,LTD.,Hefei,Anhui,China 230088)
Objective To optimize the freeze-drying process of vitexin for injection.M ethods The parameters of freeze-drying process were optimized by taking the appearance,solubility,pH and moisture as indexes.Results The optimized freeze-drying process was as follows:pre freezing to +25℃ to -40℃,2 h;-40℃,3 h;the temperature was gradually increased to -20℃,and then gradually increased from -20 ℃ to 25 ℃.The sublimation drying process was about 26 h,and it was dried for about 5 h at 25 ℃.Conclusion By optimizing the parameters of freeze-drying process,the freeze-dried vitexin has smooth appearance and loose texture,it can quickly dissolve and disperse into clear solution in saline.
vitexin for injection;eutectic point;freeze-drying;freeze-drying curve;process optimization
TQ460.6
A
1006-4931(2017)16-0006-03
2017-03-15;
2017-04-17)
10.3969/j.issn.1006-4931.2017.16.002
安徽省重大科技专项项目[15czz04082]。
牛海军,大学本科,副主任药师,主要从事中药新药创制工作,(电话)0551-65399988(电子信箱)niuhaijun.2008@163.com。
