硫脲浸金及置换法从硫脲溶液中回收金研究现状
2017-09-03马方通高利坤
马方通,高利坤,董 方,陈 龙
(1.昆明理工大学 国土资源工程学院,云南,昆明 650093;2.复杂有色金属资源清洁利用国家重点实验室,云南,昆明 650093)
硫脲浸金及置换法从硫脲溶液中回收金研究现状
马方通1,2,高利坤1,2,董 方1,2,陈 龙1,2
(1.昆明理工大学 国土资源工程学院,云南,昆明 650093;2.复杂有色金属资源清洁利用国家重点实验室,云南,昆明 650093)
从电化学和热力学角度介绍了酸性条件下硫脲浸金研究现状,以及用置换法从酸性硫脲浸出液中回收金的基本原理,简要分析了铝、锌、铁、铅置换金的主要影响因素及相应的解决方案,指出了用置换法从酸性硫脲浸出液中回收金过程中存在的问题及改进的方向。
硫脲;浸出;金;置换;现状
金广泛应用于电子制造及航空航天领域[1]。目前,金冶炼原料主要是含金矿物和含金电子废弃物。现阶段,工业上依旧采用比较传统的氰化法提取金。氰化法流程简单,金浸出率高,生产成本低,但使用的浸出剂氰化物具有强毒性,易导致浸出过程和浸出所产生的废水和浸出渣对周围环境带来严重危害[2]。随着环保要求提高,研发高效、环境友好的提金工艺及试剂有重要意义。现阶段的非氰化浸金工艺主要有硫脲法、硫代硫酸盐法、石硫合剂法、卤素及其化合物法、类氰化物法等,其中硫脲法是一种相对较成熟的非氰化浸金工艺[3]。
1 硫脲法浸出金

高温条件下,硫脲的水解反应为

(1)
在含有NaOH的溶液体系中,硫脲易与NaOH发生反应生成Na2S和CNNH2,化学反应[5]为:
(2)

(3)
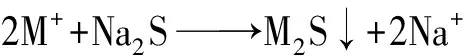
(4)
式中,M+表示溶液中的金属离子。
碱性溶液中,硫脲的分解加大了硫脲消耗量,且硫脲分解产生的S2-很容易与溶液中的金属离子(Ag+、Cu2+、Pb2+等)反应生成沉淀。
为保证硫脲在浸出过程中的相对稳定性,现阶段的硫脲浸出更倾向于在酸性环境下进行。弱酸性条件下,硫脲也会缓慢发生少量分解,其主要反应为

(5)因此,在酸性介质中,为防止硫脲分解以及生成沉淀,浸出过程中溶液pH通常控制在1.0~1.5之间[6-7]。

1.1 硫脲法浸金基本原理
在酸性条件下,Au失去电子形成Au+:

E0=1.68V。
(6)


E0=0.38 V。
(7)

在酸性介质中,二硫甲醚也并非特别稳定,与H+反应被氧化为硫脲:

E0=0.42 V。
(8)
在酸性溶液中,二硫甲脒作氧化剂,金与硫脲发生配合反应[9]:

E0=0.04 V。
(9)
但二硫甲脒会进一步分解[10-11]:

(10)

(11)
该反应是不可逆的,使部分二硫甲脒分解消耗,导致溶液中二硫甲脒浓度降低[12]。由可逆化学反应平衡定理可知,反应向物质浓度降低的方向进行,进而导致溶液中硫脲有不必要的消耗。通过添加亚硫酸抑制该过程的发生,可降低硫脲使用量[13]。

1.1.1 氧气存在条件下硫脲的浸金机制
酸性环境中,硫脲具有还原性。在氧气气氛中,硫脲与金发生反应:

(12)
以氧气作为硫脲浸金氧化剂,当硫脲浓度与溶解氧浓度比约为10/1时,金与硫脲的配合速度达到峰值。常温常压条件下,氧气在溶液中的最大溶解度仅为8.2 mg/L,所以,常规条件下,以氧气作氧化剂时,硫脲对金的浸出率相对较低。
1.1.2 Fe3+存在条件下硫脲的浸金机制
Fe3+是常用氧化剂。在酸性介质中,以Fe3+为氧化剂,金与硫脲之间的反应[16-17]为

E0=0.77 V;
(13)

E0=0.39 V。
(14)
(15)

(16)

(17)
过氧化氢和高锰酸钾的氧化性较强,其电对的标准电极电势较高,导致硫脲的氧化反应进一步增强。
1.2 硫脲浸金工艺的优缺点
硫脲浸金基本上都在酸性介质中进行。酸性体系中,硫脲浸金的优点[20]有:浸出效率高,较大幅度降低了复膜钝化现象的发生;浸出得到的金的配合离子带正电,有利于后续从浸出液中回收金;毒性相对较低;大部分复杂难浸金矿石经预处理后都呈酸性,符合酸性体系条件;干扰少。但硫脲浸金也有缺点[21-22]:酸性溶液中,硫脲选择性大幅度降低,对金浸出率会有一定影响;较强的酸对设备材质稳定性有一定要求;酸性介质中,H+加快了硫脲的分解速度,且溶液中H+浓度与硫脲的分解速度呈正相关;硫脲价格较高且用量大,使生产成本增加;不宜处理碱性矿石、含大量强吸附性杂质(黏土、活性炭等)的矿石。
2 置换法回收硫脲浸出液中的金
从硫脲浸出液中提取金有置换法、溶剂萃取法[23]、离子交换吸附法[24]、活性炭吸附法[25]、加氢还原法[26]、电沉积法[27]等。其中,置换法的置换过程可与硫脲浸金过程同时进行,使硫脲浸金流程得以缩短;置换体系对提高硫脲的稳定性有一定促进作用,可降低硫脲分解率;对金的钝化有一定抑制作用。
硫脲浸出液主要由金配合物、硫脲、氧化剂及其他杂质离子组成。置换法是根据金属的活泼性顺序,利用活泼性较强的金属单质与含有活泼性较弱金属离子的化合物反应得到活泼性较弱金属单质的过程[28]。金、铁、铝、锌、铅的还原反应及所对应的还原电势[29]如下:

E0=1.68 V;
(18)

E0= 0.77 V;
(19)

E0=-0.44 V;
(20)

E0=-0.76 V;
(21)

E0=-1.66 V;
(22)

E0=-0.13 V。
(23)
铁、铝、锌、铅价格低廉,且还原电势相比金的更低,都可以用来置换酸性硫脲浸出液中的金,置换反应[30]为

(24)
式中:Ab+代表金与硫脲的配合离子;B代表比金更活泼、价格更低廉的金属单质,如铁、铝、锌、铅;A代表金单质;Ba+代表被氧化后的贱金属离子。
金和较为活泼的贱金属的标准电极电势差异越大,置换过程越容易进行[31]。随置换过程继续深入,金与硫脲的配合离子浓度降低的同时,贱金属离子浓度升高,直到两者电极电势达到平衡[32-33]。
置换法回收金过程中存在一些问题(一级反应动力学偏离):通过置换得到的金单质会重新溶解返回到浸出液中;贱金属离子与浸出液中的其他离子反应并在贱金属表面形成一层沉淀物,对置换反应有一定影响。
2.1 铝置换法
2.1.1 铝置换法基本原理
铝置换过程中,阴、阳极区发生如下反应[34]:
阳极区,

E0=-1.66 V;
(25)
阴极区,

E0=0.38 V;
(26)
总反应,

E0=2.80 V。
(27)

2.1.2 铝置换法的主要影响因素
1)浸出液中Fe3+对铝置换金的影响
Fe3+是酸性条件下硫脲浸出金的氧化剂,浸出液中会留有大量Fe3+,Fe3+的存在造成浸出体系的氧化还原电势升高,金置换效率下降。在酸性硫脲浸金体系中,Fe3+可以将铝粉置换得到的单质金重新溶解:

ΔG=-57.4 kJ/mol。
(28)
Fe3+/Fe2+的标准电极电势E0=0.77 V,Al3+/Al的标准电极电势E0=-1.66 V,所以,Fe3+容易将铝氧化成Al3+,造成铝粉消耗量增大。反应式为
(29)
随浸出液中Fe3+浓度升高,金回收率明显下降[36]。浸出液中Fe3+浓度为0时,置换时间为75 min,金回收率超过96%;其他条件相同情况下,当体系中Fe3+浓度为0.01 mol/L时,金回收率仅为6.3%。

有F-存在条件下,铝粉置换金的反应为
6SC(NH2)2,
ΔG=-644.1 kJ/mol。
(30)
该反应的ΔG<0 kJ/mol,所以,F-对铝置换法有促进作用。
有F-存在条件下的溶金反应为
Fe2++3F-,ΔG=11.1 kJ/mol。
(31)
该反应的ΔG>0 kJ/mol,且大于反应式(30)的ΔG,所以,F-对置换产物单质金的再次溶解有抑制作用。
2)溶解氧对置换过程的影响
含金配合物溶液中,溶解氧浓度与金的置换效果有一定关系[37]。在溶液中金质量浓度为10 mg/L、SC(NH2)2浓度为0.05 mol/L、有氧存在、置换时间为75 min条件下,金置换回收率仅为73.8%,而相同条件下对浸出液进行脱氧处理后,金可实现100%回收。
溶解氧影响金置换的原因可能为:浸出液中的溶解氧对硫脲的分解具有一定促进作用;置换体系中,溶解氧的存在一定程度上加速了铝表面钝化的发生,在酸性溶液中溶解氧对铝的溶解具有推动作用,易导致铝粉的实际使用量远超理论量。
2.2 铁置换法
2.2.1 铁置换法基本原理
铁置换过程中,阴、阳极区发生如下反应:
阳极区,

E0=-0.44 V;
(32)
阴极区,

E0=0.38 V;
(33)
总反应,

E0=1.2 V。
(34)

2.2.2 浸出液中Fe3+对铁置换金的影响
Fe3+对铁置换金的影响主要有2方面[18]:容易造成浸出体系氧化还原电势明显升高,致使已被置换为单质的金再次溶解;容易与单质铁发生氧化还原反应,降低铁作为置换剂的使用效率,导致置换过程中铁使用量大大增加。
试验过程中,通常采用添加柠檬酸三钠的方法降低Fe3+浓度[39]。柠檬酸三钠的配合能力较强,柠檬酸根离子(cit3-)可以与Fe3+通过两级反应得到配合物Fe(Ⅲ)-cit3-。该过程的基本反应[40]为:

(35)

(36)
体系中Fe3+浓度为0.02 mol/L、置换30 min时,金回收率为59%;而在相同条件下,体系中加入柠檬酸三钠(控制浓度为0.1 mol/L),金回收率达96.5%[36]。
2.3 锌置换法
锌置换过程中,阴、阳极区发生如下反应[41]:
阳极区,

E0=-0.76 V;
(37)
阴极区,

E0=0.38 V;
(38)
总反应,

E0=1.52 V。
(39)
锌粉的还原性较强,置换金的速率较快。单质锌对硫脲体系中金的置换率较高,工艺较成熟,但置换过程在较强的酸性条件下进行,锌容易被氧化并放出氢气。该过程锌消耗量远大于理论量,耗酸量也较大[42]。
2.4 铅置换法

(40)
铅粉与硫脲浸出液中的金配合离子的反应速率较慢,且铅粉在硫酸体系中发生反应

(41)
反应得到的PbSO4以包裹形式附着在铅粉周围,导致铅无法与金配合离子进一步反应[43]。
适当减小铅粉粒度可降低包裹体硬度,提高金置换回收率,但金置换效率仍然偏低,所以,此方法在实际生产中的应用受到限制。S.Ardiwilaga[44]研究表明,浸出体系中添加半胱氨酸,可提高硫脲的稳定性,但不利于金的浸出和置换,而充入一定量氧气则有利于铅对金的置换。
3 结论
置换法在湿法冶金领域较为常用,主要用于获取价值相对较高的贵金属。置换法在金提取过程中的应用相对广泛,可用于从金的氰化法浸出液、硫代硫酸盐法浸出液、酸性硫氰酸盐浸出液中获取单质金。阻碍置换法在工业生产中应用的因素主要有:置换介质价格较高且消耗量远大于理论量;置换介质消耗大量酸,影响酸的浓缩回用,增大生产成本;置换过程在强酸条件下进行,对反应釜有较高要求。因此,需要进一步研发新型高效复合型金属介质,将酸的浓缩回用过程提至置换过程之前,以及研发耐酸的高性能反应釜。
[1] 宋庆双.黄金[J].世界有色金属,2004(11):63-66.
[2] HILSON G,MONHEMIUS A J.Alternatives to cyanide in the gold mining industry:what prospects for the future?[J].Journal of Cleaner Production,2006,14(12/13):1158-1167.
[3] AKCIL A,ERUST C,GAHAN C S,et al.Precious metal recovery from waste printed circuit boards using cyanide and non-cyanide lixiviants:a review[J].Waste Management,2015,45:258-271.
[4] SYED S.Recovery of gold from secondary sources:a review[J].Hydrometallurgy,2012,115/116:30-51.
[5] 郑粟.高稳定性碱性硫脲体系清洁浸金的理论基础研究[D].长沙:中南大学,2006.
[6] 严永谋,孟奇,崔毅琦,等.硫脲浸金技术研究现状[J].黄金,2014,35(2):50-53.
[7] 白静,白建峰,戴珏,等.废旧手机电路板酸性硫脲浸金过程动力学[J].环境工程学报,2016,10(3):1400-1405.
[8] DENG T L,LIAO M X,WANG M H,et al.Enhancement of gold extraction from biooxidation residues using an acidic sodium sulphite-thiourea system[J].Minerals Engineering,2001,14(2):263-268.
[9] YANG X Y,MOATS M S,MILLER J D.The interaction of thiourea and formamidine disulfide in the dissolution of gold in sulfuric acid solutions[J].Minerals Engineering,2010,23(9):698-704.
[10] ÖRGÜL S,ATALAY Ü.Reaction chemistry of gold leaching in thiourea solution for a Turkish gold ore[J].Hydrometallurgy,2002,67(1/3):71-77.
[11] GÖNEN N,KÖRPE E,YIDIRIM Y U.Leaching and CIL processes in gold recovery from refractory ore with thiourea solutions[J].Minerals Engineering ,2007,20(6):559-565.
[12] GÖNEN N.Leaching of finely disseminated gold ore with cyanide and thiourea solutions[J].Hydrometallurgy,2003,69(1/2/3):169-176.
[13] DENG T L,LIAO M X.Gold recovery enhancement from a refractory flotation concentrate by sequential bioleaching and thiourea leach[J].Hydrometallurgy,2002,63(3):249-255.
[14] GROENEWALD T.The dissolution of gold in acidic solutions of thiourea[J].Hydrometallurgy,1976,1(3):277-290.
[15] TREMBLAY L,DESCHNES G,GHALI E,et al.Gold recovery from a sulphide bearing gold ore by percolation leaching with thiourea[J].International Journal of Mineral Processing,1996,48(3/4):225-244.
[16] MURTHY D S R,PRASAD P M.Leaching of gold and silver from Miller Process dross through non-cyanide leachants[J].Hydrometallurgy,1996,42(1):27-33.
[17] MURTHY D S R,KUMAR V,RAO K V.Extraction of gold from an Indian low-grade refractory gold ore through physical beneficiation and thiourea leaching[J].Hydrometallurgy,2003,68(1/3):125-130.
[19] LI J S,MILLER J D.A review of gold leaching in acid thiourea solutious[J].Mineral Processing and Extractive Metallurgy Review,2006,27(3):177-214.
[20] LI J Y,XU X L,LIU W Q.Thiourea leaching gold and silver from the printed circuit boards of waste mobile phones[J].Waste Management,2012,32(6):1209-1212.
[21] BROOY S R L,LINGE H G,WALKER G S.Review of gold extraction from ores[J].Minerals Engineering,1994,7(10):1213-1241.
[22] ZHENG S,WANG Y Y,CHAI L Y.Research status and prospect of gold leaching in alkaline thiourea solution[J].Minerals Engineering,2006,19(13):1301-1306.
[23] 朱萍,古国榜,贾宝琼.P507从酸性硫脲浸金液中回收金[J].过程工程学报,2002,2(2):142-145.
[24] NAKAHIRO Y,HORIO U,NIINAE M,et al.Recovery of gold with ion exchange resin from leaching solution by acidothioureation[J].Minerals Engineering,1992,5(10/11/12):1389-1400.
[25] RICARDO S,FRANCO B,HARMING R,et al.Adsorption of gold from acid thiourea solutions on activated carbon[J].International Journal of Mineral Processing,1988,23(3/4):253-264.
[27] ELENA POISOT-DAZ M,GONZLEZ I,LAOIDUS G T.Electrodeposition of a silver-gold alloy (DOR ) from thiourea solutions in the presence of other metallic ion impurities[J].Hydrometallurgy,2008,93(1/2):23-29.
[28] KARAVASTEVA M.Kinetics and deposit morphology of gold cemented on magnesium,aluminum,zinc,iron and copper from ammonium thiosulfate ammonia solutions[J].Hydrometallurgy,2010,104(1):119-122.
[29] 徐克功.电极电位与氧化还原反应[J].抚州师专学报,1983(2):112-118.
[30] 李瑞卿,王维,吴玉锋,等.废弃印刷线路板中金的回收处理现状[J].稀有金属,2014,38(3):516-526.
[31] 陈世琯.置换过程的电化学和工艺分析(续)[J].上海有色金属,1996,17(2):91-97.
[32] 陈世琯.置换过程的电化学和工艺分析[J].上海有色金属,1996,17(1):36-41.
[33] 吴骏.废电路板硫脲提金[D].上海:东华大学,2008.
[34] REIN R.Cementation of gold onto atomized aluminium from acid thiourea solutions[C]//STRATHDEE G L,KLEIN M O,MELIS L A.The International Symposium on Crystallization and Precipitation.Toronto:[s.n.],1987:297-306.
[35] LEE H Y,KIM S G,OH J K.Cementation behavior of gold and silver onto Zn,Al,and Fe powders from acid thiourea solutions[J].Canadian Metallurgical Quarterly,1997,36(3):149-155.
[36] 王治科,叶存玲,李永芳.氟化物消除铁离子对铝置换硫脲金的负面影响[J].稀有金属,2013,37(3):479-484.
[37] 李永芳.置换法回收硫脲和硫代硫酸盐中的金[D].新乡:河南师范大学,2012.
[38] ZHANG H G,DOYLE J A,KENNA C C,et al.A kinetic and electrochemical study of the cementation of gold onto mild steel from acidic thiourea solutions[J].Electrochimica Acta,1996,41(3):389-395.
[39] OU X X,QUAN X,CHEN S,et al.Photocatalytic reaction by Fe(Ⅲ)-citrate complex and its effect on the photodegradation of atrazine in aqueous solution[J].Journal of Photochemistry and Photobiology A:Chemistry,2008,197(2/3):382-388.
[40] WANG Z K,LI Y F,YE C L.The effect of tri-sodium citrate on the cementation of gold from ferric/thiourea solutions[J].Hydrometallurgy,2011,110(1/2/3/4):128-132.
[41] BIRLOAGA I,VEGLI F.Study of multi-step hydrometallurgical methods to extract the valuable content of gold,silver and copper from waste printed circuit boards[J].Journal of Environmental Chemical Engineering,2015,4(1):20-29.
[42] BEHNAMFARD A,SALARIRAD M M,VEGLIO F.Process development for recovery of copper and precious metals from waste printed circuit boards with emphasize on palladium and gold leaching and precipitation[J].Waste Management,2013,33(11):2354-2363.
[43] 庞朝霞.碘化法浸取金的研究[D].上海:华东理工大学,2012.
[44] ARDIWILAGA S.Effects of cysteine and oxygen on recovery of cemented gold from leach liquors in a thiourea system[J].Minerals Engineering,1999,12(6):645-653.
Situations of Leaching and Replacement of Gold in Acidic Thiourea Solution
MA Fangtong1,2,GAO Likun1,2,DONG Fang1,2,CHEN Long1,2
(1.FacultyofLandResourceEngineering,KunmingUniversityofScienceandTechnology,Kunming650093,China;2.StateKeyLaboratoryofComplexNonferrousMetalResourcesCleanUtilization,Kunming650093,China)
Basic principle of leaching of gold using thiourea and replacement of gold from acidic thiourea leaching solution were introduced based on the electrochemical and thermodynamics mechanism.The main factors influencing replacement of gold from the acidic leaching solution using aluminum,iron,zinc and lead were analyzed and the solutions were proposed.The problems existing in the process and improving direction were pointed out.
thiourea;leaching;gold;replacement;situation
2016-11-24
贵州省科技计划项目(黔科合(GZ字(2014)3014))。
马方通(1991-),男,山东聊城人,硕士研究生,主要研究方向为金属矿选矿。
高利坤(1973-),男,云南曲靖人,博士,副教授,主要研究方向为金属矿选矿。E-mail:likun_gao@126.com。
TF803.21;TF831
A
1009-2617(2017)04-0257-05
10.13355/j.cnki.sfyj.2017.04.002
