黄芩苷镁盐的稳定性研究Δ
2017-09-03许海舰刘一鑫王志轩宋鸿儒刘翠哲承德医学院河北省中药研究与开发重点研究实验室河北承德067000河北北方学院河北张家口07506
许海舰,刘一鑫,王志轩,宋鸿儒,刘翠哲#(.承德医学院河北省中药研究与开发重点研究实验室,河北承德 067000;.河北北方学院,河北张家口 07506)
黄芩苷镁盐的稳定性研究Δ
许海舰1*,刘一鑫1,王志轩1,宋鸿儒2,刘翠哲1#(1.承德医学院河北省中药研究与开发重点研究实验室,河北承德 067000;2.河北北方学院,河北张家口 075061)
目的:研究黄芩苷镁盐的稳定性。方法:考察黄芩苷镁盐在高温(60℃)、高湿(相对湿度90%)、强光照(4 000 lx)及不同温度(20、37、50、60℃)、不同pH(6.80、5.70、4.60、4.30、3.90、3.60、3.20)条件下的稳定性,采用高效液相色谱法测定药物含量。结果:高湿试验表明黄芩苷镁盐在第5天的质量增加了(6.17±0.12)%,第10天质量增加了(6.92±0.05)%。高温、高湿和强光照试验中药物含量在第10天分别为(94.78±0.12)%、(94.79±0.20)%、(94.66±0.15)%(n=3)。在磷酸盐缓冲溶液(pH 6.80)中,仅当温度低于20℃时,黄芩苷镁盐稳定;在纯水(pH 6.76)中,37℃时黄芩苷镁盐稳定性良好。pH稳定性试验表明pH值为4.30时黄芩苷镁盐最稳定。结论:黄芩苷镁盐有一定程度的吸湿性,强光照对其稳定性的影响较高温与高湿更大,其在纯水中的稳定性优于在磷酸盐缓冲溶液中,且在弱酸性条件下较稳定。
黄芩苷镁盐;高温;高湿;强光照;温度;pH;稳定性;高效液相色谱法
黄芩苷(Baicalin)是中药黄芩的主要有效成分之一,属于黄酮类化合物,分子式为C21H18O11。2015年版《中国药典》(一部)规定其在黄芩中的含量不得低于9%。现代药理学研究表明,黄芩苷具有多种药理作用[1-2],临床上主要用于治疗急慢性肝炎、心血管疾病等。目前含黄芩苷的药物剂型主要有片剂、丸剂、胶囊剂和传统汤剂等,亦有单方和复方之别[3]。但除传统汤剂外,其他剂型均是以黄芩提取物的形式入药。根据2015年版《中国药典》(一部)收录内容,黄芩提取物是经水提酸沉,再经碱溶酸沉纯化法制得,市售黄芩苷皆是由此法制备,且应用此法所制得的黄芩苷一直被业界认为是中药黄芩中黄芩苷的原本存在形式[4-5]。
据相关文献报道,黄芩提取物的稳定性不佳、水溶性和脂溶性均较差,口服之后因其有效成分在体内的吸收利用度低,不能发挥稳定可靠的药效,这极大地限制了黄芩苷在临床上的广泛应用[6-7]。为解决这一问题,本课题组前期经过大量试验,证明了黄芩苷在中药黄芩中的原本存在形式为镁盐形式[8]。此形式的黄芩苷化合物水溶性好,在水中的溶解度是黄芩苷的2 225倍,弥补了黄芩苷溶解性差的不足。本研究在前期研究的基础上,研究黄芩苷镁盐在不同条件下的稳定性,对黄芩苷镁盐的进一步开发和应用具有重要意义。黄芩苷和黄芩苷镁盐的结构式见图1。
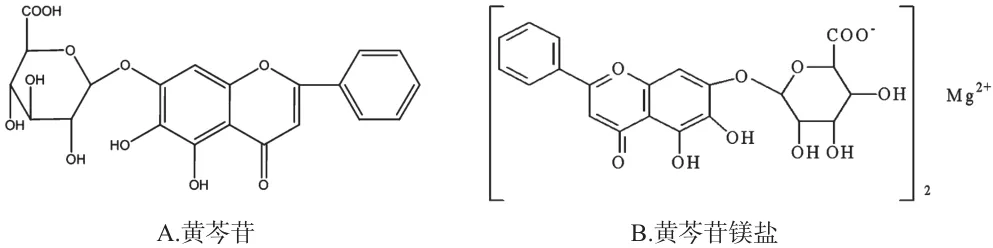
图1 化学结构式Fig 1 Chemical structure
1 材料
1.1 仪器
1260型高效液相色谱(HPLC)仪(美国安捷伦公司);AG-245型电子分析天平(瑞士梅特勒-托利多公司);JA-2003型电子天平(上海精科天平有限公司);X-500型超声波清洗器(昆山市超声仪器有限公司);GT16-3型高速台式离心机(北京时代北利离心机有限公司);pHS-3型酸度计(上海伟业仪器厂)。
1.2 药品与试剂
黄芩苷对照品(中国食品药品检定研究院,批号:110715-201318,纯度:≥98%);黄芩苷镁盐(承德医学院河北省中药研究与开发重点研究实验室自制,批号:20160404,含量:94.8%);甲醇、冰乙酸(天津市科密欧化学试剂有限公司,纯度:≥99.9%);纯水(承德医学院河北省中药研究与开发重点研究实验室自制);其他试剂均为分析纯。
2 方法与结果
2.1 黄芩苷对照品溶液的制备
精密称定黄芩苷对照品5.0 mg,置于10 mL量瓶中,甲醇溶解,定容,超声(频率为50 kHz、功率为100 W,下同)1 min使其充分溶解,制成质量浓度为500 μg/mL的黄芩苷对照品溶液,密封,4℃冰箱贮存,备用。
2.2 黄芩苷镁盐供试品溶液的制备
精密称定黄芩苷镁盐5.0 mg,置于10 mL量瓶中,纯水溶解,定容,超声1 min使其充分溶解,密封,4℃冰箱贮存,备用。
2.3 色谱条件与系统适用性试验
色谱条件参考文献[9]。色谱柱:Discovery C18(250 mm×4.6 mm,5 μm);流动相:甲醇-0.1%冰乙酸(40∶60,V/V);检测波长:278 nm;流速:1.0 mL/min;柱温:30℃;进样量:10 μL。在此色谱条件下,取甲醇空白溶液、“2.1”项下黄芩苷对照品溶液和“2.2”项下的黄芩苷镁盐供试品溶液进样分析。结果在该色谱条件下黄芩苷峰分离度良好,理论板数以黄芩苷峰计不低于3 000,系统适用性良好,色谱图见图2。
2.4 方法学考察
2.4.1 线性关系考察 依次制备质量浓度为10、20、50、100、200、400 μg/mL的黄芩苷对照品系列溶液,按“2.3”项下色谱条件进样测定。以黄芩苷质量浓度(μg/mL)为横坐标(x)、峰面积为纵坐标(y)进行线性回归,得回归方程为y=14 470x+29 231(r=0.999 9)。结果表明,黄芩苷在质量浓度为10~400 μg/mL范围内线性关系良好,定量限为10 μg/mL。
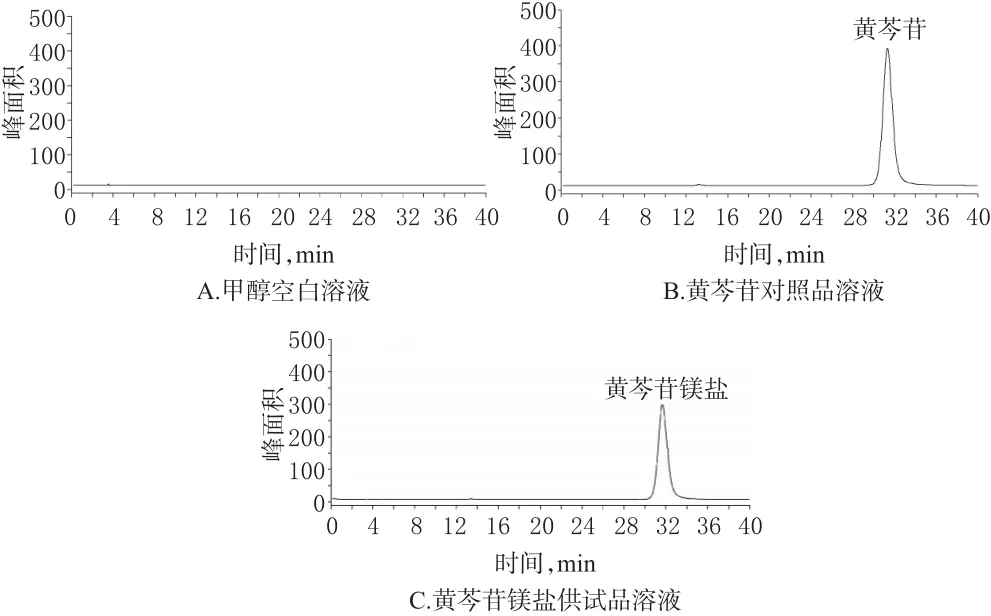
图2 高效液相色谱图Fig 2 HPLC chromatograms
2.4.2 精密度试验 取“2.1”项下黄芩苷对照品溶液适量,按“2.3”项下色谱条件连续进样6次,测定峰面积。结果,黄芩苷峰面积的RSD为0.6%(n=6),表明仪器精密度良好。
2.4.3 重复性试验 取黄芩苷镁盐6份,每份5.0 mg,按“2.2”项下方法操作制备黄芩苷镁盐供试品溶液,按“2.3”项下色谱条件进样测定,记录峰面积。结果,黄芩苷峰面积的RSD为1.34%(n=6),表明本方法重复性较好。
2.4.4 稳定性试验 取“2.2”项下黄芩苷镁盐供试品溶液适量,于0、2、4、8、10、12、24 h时进样测定,记录峰面积。结果,黄芩苷峰面积的RSD为1.7%(n=6),表明样品在24 h内稳定性良好。
2.4.5 加样回收率试验 取适量已知含量的黄芩苷镁盐样品溶液9份,精密加入高、中、低3个浓度(7.69、6.41、5.12 mg/mL)的黄芩苷对照品溶液,按“2.3”项下色谱条件进样测定,记录峰面积,计算含量及加样回收率。结果,黄芩苷的平均加样回收率为96.89%(RSD=1.2%,n=3),表明方法准确度良好。
2.5 黄芩苷镁盐的稳定性考察
2.5.1 温度对黄芩苷镁盐稳定性的影响 精密称定黄芩苷镁盐17.88 mg,共2份,分别用磷酸盐缓冲溶液(pH 6.80)、纯水(pH 6.76)定容至25 mL量瓶中,充分溶解。两种溶液各吸取20 mL至4个安瓿瓶中,密封后分别置于20、37、50、60℃水浴中保温。分别于0、1、2、4、6、8、10、12、14 h取样[10],滤膜滤过,按“2.3”项下色谱条件进样测定,并计算黄芩苷镁盐的含量,结果见图3。
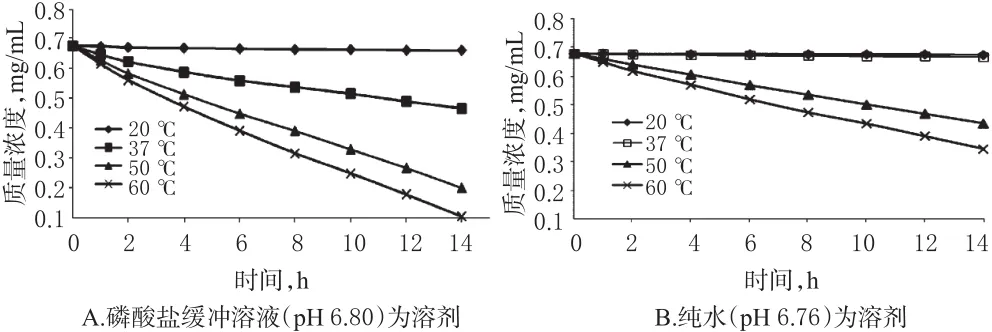
图3 温度对黄芩苷镁盐稳定性的影响Fig 3 Effect of temperature on the stability of baicalin magnesium salt
由图3可知,黄芩苷镁在磷酸盐缓冲溶液中仅当温度低于20℃时稳定,此温度下持续加热14 h,仅有2.3%的黄芩苷镁盐被破坏;而当温度高于20℃时,黄芩苷镁盐极不稳定,50℃下持续加热14 h,仅保留了29.8%的黄芩苷镁盐。黄芩苷镁在纯水中37℃时仍然稳定,此温度下持续加热14 h,仅有1.5%的黄芩苷镁盐被破坏;而50℃下持续加热14 h,仅保留了64.0%的黄芩苷镁盐。
2.5.2 pH对黄芩苷镁盐稳定性的影响 制备pH 6.80的磷酸盐缓冲溶液,分别用NaOH、H3PO4调节pH至3.20、3.60、3.90、4.30、4.60、5.70、6.80,备用。精密称取黄芩苷镁盐10 mg,共7份,用以上各pH磷酸盐缓冲溶液定容至10 mL量瓶中。分别吸取5 mL于安瓿瓶中,密封,置于37℃水浴中持续加热2 h,取样,滤膜滤过,按“2.3”项下色谱条件进样测定并计算含量,结果见图4。
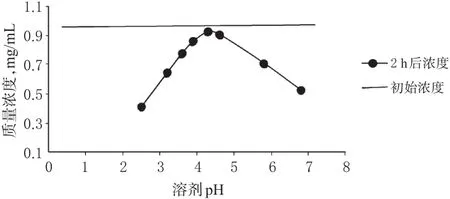
图4 pH对黄芩苷镁盐稳定性的影响Fig 4 Effect of pH on the stability of baicalin magnesium salt
由图4可知,黄芩苷镁盐溶液在pH 4.3下最稳定,持续加热2 h仅2.3%的黄芩苷镁盐被破坏。
2.5.3 高温试验 取3份装有黄芩苷镁盐粉末的培养皿开口置于药品稳定性试验箱中,60℃下放置10 d。于第5天和第10天取样,观察供试品颜色的变化,精密称定取样前后培养皿的质量[11],按“2.2”“2.3”项下方法测定含量,结果见表1。
表1 高温下黄芩苷镁盐的质量变化(±s,n=3)Tab 1 Quality changes of baicalin magnesium salt under high temperature(±s,n=3)

表1 高温下黄芩苷镁盐的质量变化(±s,n=3)Tab 1 Quality changes of baicalin magnesium salt under high temperature(±s,n=3)
时间,d 质量减少,% 05 10含量,% 94.90±0.01 94.84±0.17 94.78±0.12 5.17±0.13 5.89±0.23红外峰无变化无变化无变化
由表1可知,在60℃条件下,随着时间的延长,黄芩苷镁盐的含量逐渐下降,质量逐渐减少。试验过程中观察药物颜色无明显变化。
2.5.4 高湿试验 取3份装有黄芩苷镁盐粉末的培养皿开口置于密闭干燥器中,再将干燥器放入25℃药品稳定性试验箱中,于相对湿度(90±5)%(干燥器底部放置KNO3饱和溶液)放置10 d。于第5天和第10天取样,观察供试品颜色的变化,精密称定取样前后培养皿的质量,按“2.2”“2.3”项下方法测定含量,结果见表2。
由表2可知,90%湿度下,随着时间的延长,黄芩苷镁盐的含量逐渐降低,质量逐渐增加。试验过程中观察药物颜色变化不明显。
表2 高湿下黄芩苷镁盐的质量变化(±s,n=3)Tab 2 Quality changes of baicalin magnesium salt under high humidity(±s,n=3)
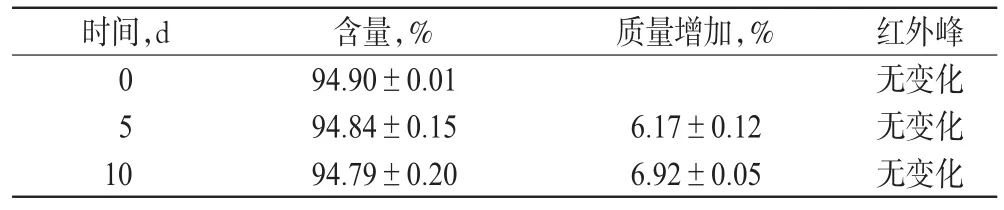
表2 高湿下黄芩苷镁盐的质量变化(±s,n=3)Tab 2 Quality changes of baicalin magnesium salt under high humidity(±s,n=3)
时间,d 质量增加,% 051 0含量,% 94.90±0.01 94.84±0.15 94.79±0.20 6.17±0.12 6.92±0.05红外峰无变化无变化无变化
2.5.5 光照试验 取3份装有黄芩苷镁盐粉末的培养皿开口置于药品稳定性试验箱中,其中放入4只60 W的日光灯,使黄芩苷镁盐距光源15 cm(相当于光照强度4 000 lx),放置10 d。于第5天和第10天取样,观察供试品颜色的变化,精密称定取样前后培养皿的质量,按“2.2”“2.3”项下方法测定含量,结果见表3。
表3 强光下黄芩苷镁盐的质量变化(±s,n=3)Tab 3 Quality changes of baicalin magnesium salt under strong illu mination(±s,n=3)
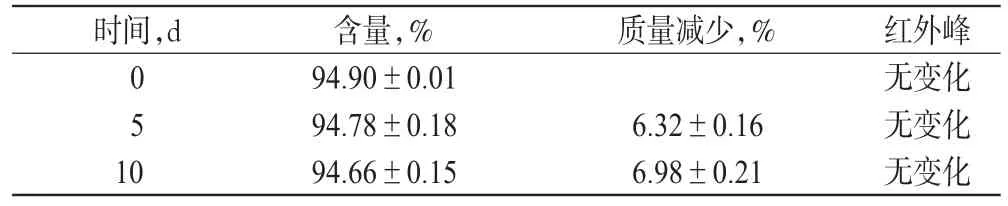
表3 强光下黄芩苷镁盐的质量变化(±s,n=3)Tab 3 Quality changes of baicalin magnesium salt under strong illu mination(±s,n=3)
时间,d 质量减少,% 051 0含量,% 94.90±0.01 94.78±0.18 94.66±0.15 6.32±0.16 6.98±0.21红外峰无变化无变化无变化
由表3可知,4 000 lx光照条件下,随着时间的延长,黄芩苷镁盐的含量明显降低,在第10天质量减少达6.98%。试验过程中观察到药物颜色变化显著,由金黄色变为深黄色。
3 讨论
本研究发现,与pH比较,温度对黄芩苷镁盐溶液的稳定性影响较大,随着温度的升高,其稳定性逐渐降低。同时研究证实黄芩苷镁盐在弱酸性溶液中稳定性较好,在强酸、强碱溶液中的稳定性均不佳。据有关文献报道,黄芩苷在不同溶剂[12]或不同生物样品[13]中的稳定性有差异。黄芩苷镁盐是黄芩苷在中药黄芩中的原本存在形式,其在不同溶剂和不同生物样品中的稳定性与黄芩苷是否相同?有待于进一步研究。
本课题组发现,黄芩苷镁盐在磷酸盐缓冲溶液和纯水中的稳定性具有明显差异:温度为37℃时,黄芩苷镁纯水溶液稳定性良好,但黄芩苷镁磷酸盐缓冲溶液稳定不佳,药物含量明显降低。黄芩苷稳定性研究亦出现相同结果。可能是缓冲溶液中的某些离子对黄芩苷镁盐的稳定性具有一定程度的作用。磷酸盐缓冲溶液中的Na+成为有可能影响黄芩苷镁盐稳定性的关键性因素,但亦不排除磷酸盐缓冲溶液中的H2PO4-及HPO42-对黄芩苷镁盐稳定性的影响[14-15]。目前,造成上述现象的机制尚未见报道,有待于进一步研究证实。
在高温试验中,黄芩苷镁盐质量降低,但颜色变化不明显,表明60℃对黄芩苷镁盐的稳定性无显著影响。但是随着时间的延长或温度的升高,黄芩苷镁盐会发生降解,含量降低。在高湿试验中,黄芩苷镁盐颜色变化不明显,但其质量增加约6%,表明黄芩苷镁盐具有一定吸湿性;同时试验结果显示,90%的湿度对黄芩苷镁盐的含量影响不显著;但是,如果湿度过高,黄芩苷镁盐的含量则会随时间延长发生显著降低。强光照试验中,黄芩苷镁盐的质量减少,10 d后含量下降明显,颜色也发生较大变化,表明黄芩苷镁盐对光照敏感,提示其宜避光保存。
本实验室在前期研究中,发现黄芩苷镁盐在纯水中的溶解度为129.1 mg/mL[8],而黄芩苷在纯水中的溶解度为0.058 mg/mL,两者水溶性差异明显。黄芩苷在水中的溶解度虽可随pH值有所增加,但与黄芩苷镁盐的溶解度比较差异明显,故黄芩苷镁盐更有利于制成水溶性注射剂或注射用无菌粉末。
综上所述,黄芩苷镁盐的水溶性和稳定性均良好。本研究对黄芩苷镁盐制剂的开发以及对含黄芩苷药物的制剂和储存具有一定意义。但本课题组尚未对黄芩苷镁盐进行体内药动学等方面的研究,其在体内的吸收、分布、代谢和排泄的规律尚未明确,成为本课题组后续研究工作的重点。
[1] 黄志军.黄芩苷药理作用研究进展[J].天津药学,2012,24(3):61-64.
[2] 张喜平,田华,程琪辉.黄芩苷的药理作用研究现状[J].中国药理学通报,2003,19(11):1212-1215.
[3] 狄斌,冯年平,刘文英,等.复方双黄连与黄芩单方中黄芩苷在大鼠肠道菌群中代谢的比较[J].中国新药杂志,2005,14(1):89-93.
[4] 曹岗,邵玉蓝,金奇.黄芩活性成分提取分离研究进展[J].抗感染药学,2009,6(2):87-91.
[5] 梁英,韩鲁佳.黄芩中黄芩苷和黄芩素提取、分离纯化的研究进展[J].农业工程学报,2003,19(z1):218-222.
[6] 张婷,朱婷婷.不同赋形剂对黄芩苷溶液稳定性的影响[J].中药新药与临床研究,2004,15(3):192-194.
[7] 张琪,陈忻.黄芩苷的药动学研究进展[J].中南药学,2011,9(3):209-212.
[8] 刘翠哲.一种黄芩苷镁化合物及其制备方法与它的用途:中国,201610068926.3[P].2014-02-11.
[9] 彭其胜,穆瑶,陈欢.HPLC法测定黄芩免煎颗粒和饮片中黄芩苷的含量[J].中国药房,2016,27(9):1259-1261.
[10] Qiu F,Tang X,He ZG,et al.Stability of baicalin aqueous solution by validated RP-HPLC[J].Journal of Chinese Pharmaceutical Sciences,2004,13(2):134-137.
[11] 冯蕾,刘旭,杨晖.黄芩苷锌稳定性影响因素实验研究[J].昆明医学院学报,2008,29(5):26-28.
[12] 王雷,王学艳,周雪琴,等.黄芩苷在不同溶媒中的稳定性研究[J].中国药师,2006,9(2):129-131.
[13] 于波涛,张志荣,刘文胜,等.黄芩苷稳定性研究[J].中草药,2002,33(3):218-220.
[14] 何琳,丁沐淦,卢秀霞,等.黄芩苷在不同pH值缓冲液中理化常数的测定[J].西北药学杂志,2012,27(3):208-211.
[15] 万春艳,林玉庆.黄芩苷药剂中pH稳定性的研究[J].黑龙江医药,2007,20(3):239-240.
Study on the Stability of Baicalin Magnesium Salt
XU Haijian1,LIU Yixin1,WANG Zhixuan1,SONG Hongru2,LIU Cuizhe1(1.Hebei Key Laboratory of Research and Development of TCM,Chengde Medical University,Hebei Chengde 067000,China;2.Hebei North University,Hebei Zhangjiakou 075061,China)
OBJECTIVE:To study the stability of baicalin magnesium salt.METHODS:The stability of baicalin magnesium salt at high temperature(60℃),high humidity(90%),strong illumination(4 000 lx),different temperatures(20,37,50,60℃)and pHs(6.80,5.70,4.60,4.30,3.90,3.60,3.20)was investigated,and HPLC was used to detect the drug contents.RESULTS:High humidity test indicated that the quality of baicalin magnesium salt was increased by(6.17±0.12)%in the 5th day and increased by(6.92±0.05)%in the 10th day.Drug contents in the 10th day were respectively(94.78±0.12)%,(94.79±0.20)%,(94.66±0.15)%in the high temperature,high humidity,strong illumination tests(n=3).In phosphate buffer solution(pH 6.80),baicalin magnesium salt was stable only when the temperature was below 20℃;and it was yet stable in pure water(pH 6.76)at 37℃.pH stability test showed that the most stable pH was 4.30.CONCLUSIONS:Baicalin magnesium salt has hygroscopicity to some extent.Strong illumination affects the stability more seriously than high temperature and high humidity.The stability of baicalin magnesium salt in pure water is superior to in phosphate buffer solution,and the salt is stable in weak acid solution.
Baicalin magnesium salt;High temperature;High humidity;Strong illumination;Temperature;pH;Stability;HPLC
R921.2
A
1001-0408(2017)22-3076-04
2016-09-05
2017-06-17)
(编辑:刘明伟)
河北省自然科学基金资助项目(No.H2014406036);河北省教育厅高等学校科学技术研究重点项目(No.ZH2012050)
*硕士研究生。研究方向:中药制剂现代化。电话:0314-2290359。E-mail:1556275925@qq.com
#通信作者:研究员,博士。研究方向:中药制剂现代化。电话:0314-2290359。E-mail:liucuizhexy@163.com
DOI10.6039/j.issn.1001-0408.2017.22.14
