牛病毒性腹泻病毒基因分型二重RT-PCR检测方法的建立
2017-08-28王建昌王金凤袁万哲
崔 元 , 王建昌 , 王金凤 , 袁万哲,3
(1.河北农业大学动物医学院, 河北保定071001;2.河北出入境检验检疫局检验检疫技术中心, 河北石家庄050051;3.河北省兽医生物技术工程技术研究中心, 河北保定071001)
牛病毒性腹泻病毒基因分型二重RT-PCR检测方法的建立
崔 元1, 王建昌2, 王金凤2, 袁万哲1,3
(1.河北农业大学动物医学院, 河北保定071001;2.河北出入境检验检疫局检验检疫技术中心, 河北石家庄050051;3.河北省兽医生物技术工程技术研究中心, 河北保定071001)
为了同步检测牛病毒性腹泻病毒(BVDV)基因1型和基因2型并能够加以区分,根据GenBank中已发表的BVDV基因1型和基因2型、牛蓝舌病病毒(BTV)、口蹄疫病毒(FMDV)、猪瘟病毒(CSFV)、牛传染性鼻气管炎病毒(IBRV)的全基因序列,采用Primer Premier 5.0软件,针对BVDV的高度保守的5′端非编码区的核苷酸序列,设计了两对特异性引物,二重RT-PCR方法扩增目的片段的大小分别为222 bp和119 bp,经过对反应体系和条件的优化,本研究建立了在同一反应体系中鉴别检测BVDV基因1型和2型的RT-PCR方法,扩增出了与预期大小相符的目的片段。该方法便捷,特异性高,敏感性强,重复性好,可作为BVDV分型鉴定和快速诊断的有效方法。
BVDV; 二重RT-PCR; 基因性
牛病毒性腹泻是由牛病毒性腹泻病毒(BVDV)引发的牛的一种传染病,临床上可引起牛发热、黏膜溃疡、白细胞减少、腹泻及怀孕母牛流产或产出畸胎等。成熟的BVDV病毒粒子呈直径为40~60 nm的球形或圆形,囊膜表面有10~12 nm的环形亚单位,病毒基因组为单分子线状正链单股RNA,大小约12.5 kb[1]。BVDV可在胎牛肾、睾丸、皮肤、肌肉、肺、脾、鼻甲、气管细胞、猪肾细胞中增殖传代[2]。
研究表明,BVDV在不同的毒株之间有着明显的遗传和抗原异质性特征,根据BVDV是否使细胞病变将其分为致细胞病变型和非致细胞病变型。BVDV基因组由5′-非翻译区(5′-UTR)和3′-非编码区(3′-NCR)组成,中间是一个大的开放阅读框(Open reading frame, ORF),5′-UTR区具有很高的保守性,常根据此区域设计引物来检测BVDV或进行基因型的区分[3]。二重RT-PCR的特点是能在同一PCR反应体系中同时检测并鉴别两种病原体,在临床上具有很高的应用价值。本研究旨在建立一套可以同时检测并区分BVDV两种基因型的二重RT-PCR方法,为BVDV的检疫、临床鉴别诊断提供有效的检测方法。
1 材料与方法
1.1 材料
OregonC24V株、890株均由新疆出入境检验检疫局检验检疫技术中心赠送;BTV、CSFV、FMDV、IBRV均由河北出入境检验检疫局检验检疫技术中心实验室保存;基因组提取试剂盒、SanPrep柱式质粒DNA小量抽提试剂盒、pMD®19-T Simple Vector、Prime ScriptTMⅡ1st strand cDNA Synthesis试剂盒等。
1.2 方法
1.2.1 引物的设计与合成 根据GenBank中已发表的BVDV OregonC24V、SD0803、ZM-95等6株BVDV1型毒株和890、JZ05-1、XJ-04等6株BVDV2型毒株的全基因序列,用DNAStar 6.0软件进行序列比对,使用Primer5.0软件设计两对分别针对BVDV1和BVDV2的特异性扩增引物F1/R1和F2/R2,引物序列见表1。

表1 试验中所用引物序列信息
1.2.2 病毒核酸的提取 采用病毒DNA/RNA提取试剂盒,提取BVDV1、BVDV2、BTV、FMDV、CSFV、IBRV的DNA或RNA。
1.2.3 病毒cDNA的合成 使用Primer ScriptTMⅡ1st strand cDNA Synthesis试剂盒,将RNA反转录。反转录体系如下:Random 6mers(50 μmol/L)1.5 μL,dNTP Mixture(10 mmol/L)1 μL,RNA 5 μL,DEPC水2.5 μL,65 ℃ 5 min,立即冰浴;5×primer ScriptⅡBuffer 4 μL,Primer ScriptⅡRTase 1 μL,RI 0.5 μL,DEPC水4.5 μL;30 ℃ 10 min;70 ℃ 15 min。。
1.2.4 BVDV1和BVDV2二重RT-PCR反应条件的优化
1.2.4.1 引物浓度的优化 分别对F1/R1和F2/R2的浓度进行优化。PCR体系为25 μL,包括TaqMixture 12.5 μL,引物F/R(20 μmol/L)分别设定浓度为0.2、0.4、0.6、0.8 μmol/L,cDNA 1.0 μL,ddH2O 补足至25 μL。反应条件为94 ℃ 5 min;94 ℃ 30 s,53 ℃ 30 s,72 ℃ 30 s,35个循环;72 ℃ 5 min。电泳检测,确定最佳引物浓度。
1.2.4.2 退火温度的优化 使用最佳引物浓度,对二重RT-PCR进行退火温度的优化。退火温度设定为51 ℃、53 ℃、55 ℃、57 ℃、59 ℃,电泳检测,选取最优退火温度。
1.2.5 特异性检测 以BVDV1、BVDV2、BTV、FMDV、CSFV、IBRV的基因组为模板,采用优化条件扩增,并用引物F1/R1扩增BVDV2阳性模板,用引物F2/R2扩增BVDV1阳性模板,以检测该方法的特异性。
1.2.6 质粒构建 将BVDV1和BVDV2特异性片段连接到pMD19-T载体,转化至DH5α感受态细胞,挑取阳性克隆,将菌液送至上海生工生物工程技术服务有限公司测序,测序结果进行BLAST比对分析。
采用SanPrep柱式质粒DNA小量抽提试剂盒提取BVDV1和BVDV2的质粒。
1.2.7 灵敏性检测 测定构建质粒的浓度,换算成相应的拷贝数,进行10倍梯度稀释,分别按最佳反应条件进行单重和二重PCR扩增。
1.2.8 重复性检测 用优化后的二重RT-PCR方法进行3次重复检测,以验证建立方法的稳定性。
2 结果
2.1 引物浓度的优化结果 BVDV1反应体系中最优引物浓度为0.4 μmol/L(图1),BVDV2反应体系中最优引物浓度为0.8 μmol/L(图2)。因此二重RT-PCR方法的最佳反应体系为2×TaqPCR Master Mix 12.5 μL,F1/R1(20 μmol/L)0.5 μL,F2/R2(20 μmol/L)1 μL,cDNA 1 μL,ddH2O补足至25 μL。

图1 BVDV1引物浓度优化结果
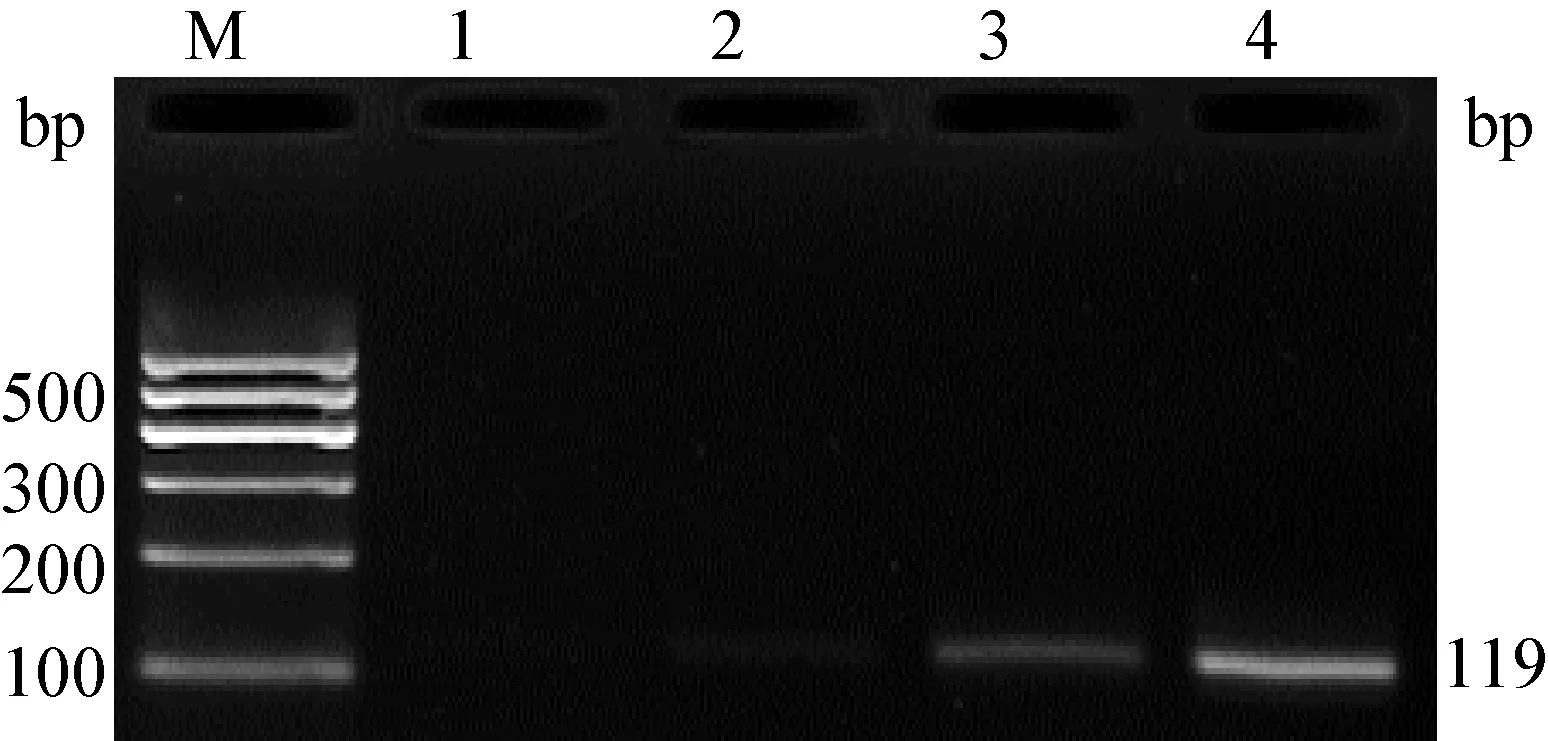
图2 BVDV2引物浓度优化结果
2.2 退火温度的优化结果 二重RT-PCR方法最佳退火温度为51 ℃(图3)。最佳反应条件为94 ℃ 5 min;94 ℃ 30 s,51 ℃ 30 s,72 ℃ 30 s,35个循环;72 ℃ 5 min。
2.3 特异性的检测 结果显示,BVDV1和BVDV2的目的片段大小分别为222 bp和119 bp,与预期大小相符,两对引物之间无非特异性扩增,且分别用两对引物扩增不同基因型的阳性模板均未出现条带。测序结果经BLAST分析证实与已发表序列一致。用此方法检测BTV、FMDV、CSFV、PRV均未出现条带,表明本方法具有良好的特异性(图4)。

图3 BVDV1和BVDV2二重RT-PCR方法退火温度优化结果
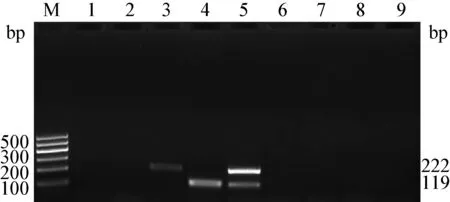
图4 BVDV二重PCR特异性扩增结果
2.4 灵敏性的检测 根据优化条件对10倍梯度稀释后的质粒进行扩增,结果显示,单重PCR(图5,图6)和二重PCR(图7)最低检测限均为103copies,二者的灵敏性结果一致,表明同一体系中两个基因型间未产生明显的相互抑制,灵敏性较高。

图5 BVDV1 RT-PCR灵敏性结果

图6 BVDV2 RT-PCR灵敏性结果

图7 二重RT-PCR灵敏性结果
2.5 重复性检测 应用建立的BVDV二重RT-PCR方法进行3次重复检测,均出现目的基因条带,表明重复性较好。
3 讨论
BVDV的5′-UTR区域高度保守、稳定[4],本试验对BVDV多株病毒基因组的5′-UTR区域的核苷酸序列进行比对和分析,设计出2对特异性引物,分别用于检测两种基因型,保证了建立方法的特异性。以OregonC24V株和890株的RNA反转录后获得的cDNA为模板进行RT-PCR,结果表明,应用上述引物可分别扩增出与预期大小相符的DNA片段,对其序列进行测定和分析,结果显示OregonC24V株和890株分别属于BVDV1和BVDV2,该结果与文献报道一致。表明该RT-PCR方法可特异性将BVDV分为两种基因型,其分类结果与文献报道相一致。
在本试验中,引物设计是重点和难点。由于BVDV基因组5′-UTR区域较短,且两种基因型的同源性较高,因此,在能够区分两种基因型的同时,又能够使两对引物的退火温度接近、引物长度18~25 bp、G+C的含量在50%左右、碱基分布均匀,并且扩增出的目的片段的长度有一定差距成了本研究的重点和难点。此外,引物浓度与模板量之间存在相互制约的关系,引物浓度不足可导致扩增效率降低,过高则易出现二聚体。在本研究最初建立的二重RT-PCR方法中,使用了同等物质的量的引物,但扩增结果不理想,即使在优化反应条件后仍存在单个基因扩增条带不明显的情况,为解决这一问题,分别对引物不同浓度的扩增效果进行了对比,并据此改变了PCR体系中两对引物的比例,最终达到平衡,得到了良好的扩增结果。
目前实验室常用的用来检测BVDV的方法有病毒的分离鉴定、琼脂扩散试验、酶联吸附试验、荧光定量RT-PCR等。其中ELISA能够检测组织器官或培养物中有无BVDV,并且能够监测牛群中BVDV的抗体水平及潜伏感染的比率[5],此方法已广泛应用,但在诸多检测方法中,血清学检测方法与RT-PCR方法相比敏感性较低,与猪瘟病毒存在抗体的交叉反应[6],多存在费力耗时、准确率低等缺点。随着分子生物学的发展和RT-PCR检测技术的日益成熟,在众多检测方法中其被认为是一种准确性高、重复性好、快速、特异、灵敏的检测方法,可广泛应用于病原体的检测、基因表达等诸多领域[7]。总之,本研究建立的BVDV二重RT-PCR检测方法具有操作简便快捷、检测结果特异性高、敏感性好、重复性好、检测应用范围广等优点,可作为BVDV分型鉴定和快速诊断的有效方法。
[1] 殷震,刘景华. 动物病毒学[M]. 2版.北京:科学出版社, 1997: 645-652.
[2] 李庆超.牛病毒性腹泻病毒JZ05-1株基因分型、全基因序列测定及分析[D].北京:中国农业科学院, 2010.
[3] 王璐.牛病毒性腹泻病毒E0基因的表达及间接ELISA检测方法的建立[D].乌鲁木齐:新疆农业大学, 2012.
[4] 李宁.牛病毒性腹泻病毒RT-PCR方法的建立与gP48基因克隆及原核表达[D].保定:河北农业大学, 2012.
[5] 张俭伟,赵宏坤,杨少华,等.RT-PCR快速检测牛病毒性腹泻病毒方法的建立与应用[J].中国兽医学报,2008, 28(4): 367-370.[6] 孙宏进.基因2型牛病毒性腹泻病毒的分离与鉴定[D].扬州:扬州大学, 2010.
[7] 孟雨.牛病毒性腹泻病毒RT-PCR检测方法的建立及5′-UTR基因遗传变异分析[D].杨凌:西北农林科技大学, 2010.
YUAN Wan-zhe
Establishment of a RT-PCR assay for simultaneous dutecion of BVDV
CUI Yuan1, WANG Jian-chang2, WANG Jin-feng2, YUAN Wan-zhe1,3
(1.College of Veterinary Medicine, Agricultural University of Hebei, Baoding 071001, China; 2.Inspection and Quarantine Technical Center of Hebei Entry-Exit Inspection and Quarantine Bureau, Shijiazhuang 050051, China; 3. Hebei Engineering and Technology Research Center of Veterinary Biotechnology, Baoding 071001, China)
In order to detect and distinguish the genome sequences of genotype 1 BVDV and genotype 2 BVDV simultaneously, two pairs of primers that the specific to the 5'-untranslated region of BVDV were designed by Primer Premier 5.0, according to the complete sequences of BVDV1, BVDV2, BTV, FMDV, CSFV and IBRV in GenBank. The 5'-untranslated region of BVDV was the highest conservative region in the BVDV complete genome. The target fragments’ sizes were 222 bp and 119 bp. After the optimization of the reaction conditions, we set up a method which can distinguish genotypes of BVDV using RT-PCR just in one reaction system. This established assay can detect BVDV1 and BVDV2 specifically, sensitively and reproducibly, which is an efficient assay for BVDV detection and genotyping.
BVDV; duplex RT-PCR; genotype
2016-09-23
国家质量监督检验检疫总局科技计划项目(2015IK093)
崔元(1993-),女,硕士生,研究方向为预防兽医学,E-mail:1277107388@qq.com
王建昌(1981-),男,助理研究员,博士,研究方向为预防兽医学,E-mail:jianchangwang1225@126.com
袁万哲,E-mail:yuanwanzhe@126.com
S855.3
A
0529-6005(2017)07-0020-04
注:王建昌与崔元对本文具有同等贡献
