RP—HPLC法同时测定舒胸颗粒中3种皂苷类成分的含量
2017-08-22符传山洪挺王笑琴
符传山+洪挺+王笑琴
[摘要] 目的 建立RP-HPLC法同时测定舒胸颗粒中三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1的含量测定方法。 方法 采用色谱柱Diamosil C18(4.6×250mm,5μm),柱温30℃,流动相乙腈-水,梯度洗脱,检测波长203nm。 结果 3个皂苷类成分色谱峰面积与对照品进样量均呈良好的线性关系,r≥0.9993;样品加样回收率在98.9%~99.7%之间,RSD均小于1.4%。 结论 该方法灵敏度高、专属性好、操作简便、重复性好,可为舒胸颗粒质量控制提供依据。
[关键词] RP-HPLC;舒胸颗粒;三七皂苷R1;人参皂苷Rg1;人参皂苷Rb1
[中图分类号] R286.0 [文献标识码] A [文章编号] 2095-0616(2017)13-33-03
[Abstract] Objective To establish a method for the simultaneous determining of notoginsenoside R1, ginsenoside Rg1 and ginsenoside Rb1 in Shuxiong Granules by RP-HPLC. Methods The RP-HPLC analysis was performed on a Diamosil C18 (4.6×250 mm,5μm), the mobile phase was acetonitrile and water with gradient elution. The detection wave length was 203nm and the coumn temperature was 30℃. Results There was a good linear relationship between the peak area and the sample quantity for the three saponins, r≥0.9993. The recovery was between 98.9%-99.7% with RSD<1.4%. Conclusion The method has the advantage of sensitivity, specificity, simple operation, and repeatability. It is suitable for the quality control of Shuxiong Granules.
[Key words] RP-HPLC; Shuxiong granules; Notoginsenoside R1; Ginsenoside Rg1; Ginsenoside Rb1
舒胸颗粒由三七、红花、川芎3味药制成,主要用于瘀血阻滞所致的胸痹,症见胸闷、心前区刺痛;冠心病心绞痛。本品种原标准[1-2]分别收载于国家药品标准新药转正标准第27册和第37册,均采用薄层扫描法测定君药三七中人参皂苷Rg1的含量。由于三七中含有皂苷类成分较多,仅控制人参皂苷Rg1的含量不够全面,而且薄层扫描法的重现性不好。为有效控制药品质量,保证临床用药安全有效,经查阅文献 [3-6],研究建立RP-HPLC法同时测定舒胸颗粒中三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1的含量测定方法。其质量标准被《中国药典》2015年版一部[7]收录。
1 仪器与试药
美国沃特斯2695 alliance高效液相色谱仪,配备四元泵、紫外检测器、柱温箱、高精度自动进样器、Empower数据采集处理工作站;德国Sartorius BP211D电子天平;Milli-Q超纯水机;昆山KQ-5200B型超声波仪(昆山市超声仪器有限公司)。
人参皂苷Rg1、人参皂苷Rb1、三七皂苷R1对照品,均由中国药品生物制品检定所提供,含量测定用,批号分别为110703-200424、110704-200318、110745-200414;乙腈为色谱纯,水为自制超纯水,其他试剂均为分析纯;舒胸颗粒样品7批分别由A公司(规格:每袋装3g,批号为 080603、080903、080802、080902)、B公司(规格:每袋装1g,批号为070501、070502、070503)提供。
2 方法与结果
2.1 溶液的配制
2.1.1 混合对照品溶液的配制 分别称取人参皂苷Rg1、人参皂苷Rb1、三七皂苷R1对照品适量,精密称定,分别加甲醇制成质量浓度为2.21、1.72、1.04 mg/mL的对照品储备液。分别精密量取一定体积的对照品储备液,加甲醇稀释成0.221、0.172、0.104 mg/mL混合对照品溶液,摇匀,备用。
2.1.2 样品溶液的配制 取舒胸颗粒适量,研细,取粉末约0.5g,精密称定,置具塞锥形瓶中,精密加入甲醇50mL,称定重量,静置12h,然后于80℃水浴上加热回流2h,放冷至室温,再称定重量,用甲醇补足减失的重量,摇匀,取上清液用微孔滤膜(0.22μm)滤过,续滤液备用。
2.1.3 阴性对照溶液的配制 按处方量称取红花、川芎2味药,照舒胸颗粒生产工艺制备阴性对照样品。取阴性对照样品适量,照“2.1.2”项下方法制备阴性对照溶液,备用。
2.2 色谱条件与系统适用性试验
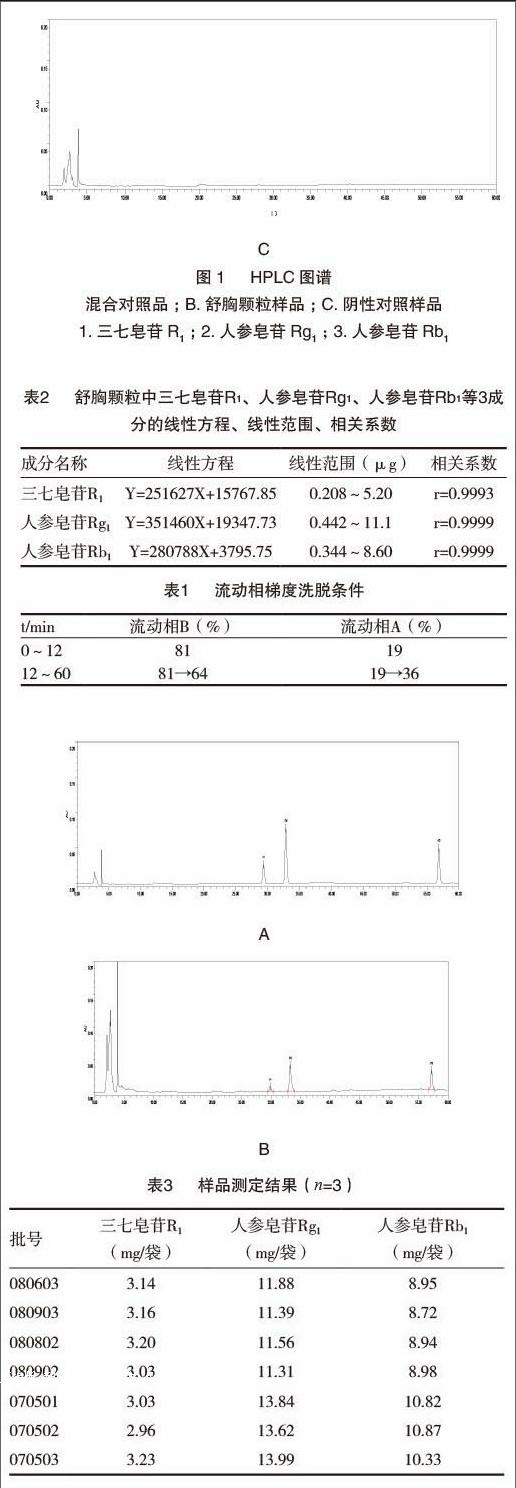
色谱柱为Diamosil C18柱(4.6×250mm,5μm),柱温为30℃,检测波长为203nm,流速为1.0mL/min,进样量为20μL。流动相A为乙腈,流动相B为水,按表1进行梯度洗脱;理论塔板数按三七皂苷R1峰计算,应不低于3000。结果显示三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1保留时间分别约为29.4、32.9、56.9min,与其他组分峰的分离度大于1.5,陰性对照样品在相应保留时间处无干扰。结果见图1。
2.3 方法學考察
2.3.1 线性关系 取“2.1.1”项下混合对照品溶液2、5、10、20、30、50μL,注入液相仪,照上述色谱条件进行分析测定。以每个对照品进样量(μg)为横坐标,以相应的峰面积为纵坐标,拟合标准曲线。结果表明均呈良好的线性关系,线性方程、线性范围、相关系数见表2。
2.3.2 精密度实验 精密吸取混合对照品溶液,按照上述色谱条件,进样20μL,连续进样6次,记录各色谱峰的峰面积。结果三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1峰面积的RSD分别为0.66%、0.54%和0.56%(n=6),均符合精密度实验要求。
2.3.3 重复性实验 取批号070501舒胸颗粒样品,研细,取粉末0.5g,共6份,精密称定,照“2.1.2”项下方法制成样品溶液,进样20μL。结果样品中三七皂苷R1 ,人参皂苷Rg1、人参皂苷Rb1的平均含量分别为3.19mg/g、14.0mg/g、10.9mg/g,RSD分别为1.2%、1.0%、1.5%,结果表明该方法重现性良好。
2.3.4 稳定性实验 取批号070501舒胸颗粒样品溶液,室温下放置,分别于0,4,8,12,16 h重复进样,记录色谱峰面积。结果三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1峰面积RSD分别为1.3%、0.39%、0.78%。数据说明该样品溶液在室温下放置16h所测成分稳定性良好。
2.3.5 回收率实验 取批号070501舒胸颗粒样品,研细,取粉末0.25g,共6份,精密称定,分别精密加入混合对照品溶液(三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1浓度分别为0.0400、0.0328、0.0268mg/mL)50mL,照“2.1.2”项下方法制备样品溶液并进行分析测定,计算加样回收率,结果三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1平均回收率为99.7%、98.9%、99.0%,RSD为1.3%、1.1%、1.0%。数据表明该方法回收率较好。
2.3.6 样品测定 取7批舒胸颗粒,照“2.1.2”项下方法制备样品溶液,按上述色谱条件进行分析测定,计算三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1的含量,结果见表3。
3 讨论
3.1 检测波长的选择
采用紫外分光光度计对混合对照品溶液进行光谱测定,结果三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1的紫外光谱均属末端吸收,且在203nm处有最大吸收,因此选择203nm为测定波长。
3.2 提取方式的优化
目前测定三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1含量的方法,文献报道主要有HPLC法[8-15]和TLC扫描法,但未见同时测定舒胸颗粒中三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1三个成分的文献报道。本研究对样品溶液的提取方法进行了热回流和超声提取的考察,结果表明:热回流法比超声处理法所测含量更大,说明其提取更完全,故选择热回流提取;本研究还对提取时间进行了考察,分别考察了热回流1、2、3h的提取情况,结果表明:热回流2h三种皂苷含量最高,3h与2h无差别,这说明2h已经提取较为完全,为节约时间,提高效率,故选择提取2h;另外,本研究还对提取溶剂进行了考察,分别采用甲醇、乙醇、50%甲醇三种溶剂进行实验,结果表明:甲醇提取三种皂苷含量最高,其提取最为完全,故最终确定甲醇为提取溶剂。
3.3 耐用性实验
取供试品溶液,分别采用A: DIKMA Diamonsil C18柱(4.6×250mm,5μm);B: Alltech Apollo C18柱(4.6×250mm,5μm);C: Agilent Zorbax SB-C18柱(4.6×150mm,5μm)三种不同品牌和填料的色谱柱进行测定,结果三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1峰在各种色谱柱上均分离良好,结果无明显差异,该方法耐用性良好。
本实验采用反相高效液相色谱法测定舒胸颗粒中3种皂苷的含量,方法学考察结果表明,该方法精密度、准确度、重复性均能满足定量分析要求,对评价舒胸颗粒质量标准提供了参考依据。
[参考文献]
[1]国家药品标准·新药转正标准[S]. 第27册,35.
[2]国家药品标准·新药转正标准[S]. 第37册,22.
[3] 国家药典委员会.中华人民共和国药典[S].北京:中国医药科技出版社,2010年版一部:11-12.
[4] 杨学芳,苏万福,唐晓霞,等.RP-HPLC测定药流净颗粒中三七皂苷R1与人参皂苷Rg1、Rb1的含量[J].中国民族民间医药,2013,9:17-18.
[5] 王银良,陈翠卿,陈向明,等.搜风通胶囊中三七皂苷R1、人参皂苷Rg1和Rb1的含量[J].中国医药科学,2013,3(11):100-104.
[6] 王建国,万慧杰,朱贺年.HPLC测定冠心丹参胶囊中人参皂苷Rb1、人参皂苷Rg1、三七皂苷R1[J].中国实验方剂学杂志,2011,17(3):98-100.
[7] 国家药典委员会.中华人民共和国药典[S].北京:中国医药科技出版社,2015年版一部:1166.
[8] 汪霞. RP-HPLC法测定舒胸胶囊中三七皂苷R1、人参皂苷Rg1的含量[J].中国药事,2011,25(3): 289-291.
[9] 李欣,陈晓辉,齐丹丹,等. HPLC法同时测定舒胸片中三七皂苷R1和人参皂苷Rg1的含量[J].药物分析杂志,2005,25(6): 648-650.
[10] 黎小伟,梁云飞,林伟国,等. HPLC测定舒胸片中4种皂苷的含量[J]. 中成药,2007,29(4): 522-524.
[11] 黄海欣. 舒胸片中三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1的含量测定[J]. 现代中药研究与实践,2010,24(1): 65-67.
[12] 付妍,付春旺,陈晓辉,等. HPLC法同时测定舒胸速释微丸中4种化学成分的含量[J]. 沈阳药科大学学报,26(8):629-632.
[13] 张武岗,张小娟,陈海芳,等.HPLC法同时测定舒胸滴丸中3种成分[J] .中成药,2014,36(4):773-775.
[14] 王德旺,马坤芳,季宏建. HPLC法测定红药片中三七皂苷R1、人参皂苷Rg1的含量[J]. 南京医科大学学报(自然科学版),2006,26(12):1292-1294.
[15] 曾学忠,卢炳旺. HPLC法测定舒筋通络胶囊中人参皂苷Rg1、Rb1及三七皂苷R1的含量[J].海峡药学2007,19(6):46-48.
(收稿日期:2017-01-07)
