NUDT15基因突变致巯唑嘌呤治疗克罗恩病并发严重骨髓抑制1例
2017-08-21潘柏申刘红春
周 琰 吴 炯 郭 玮 潘柏申 刘红春
(1复旦大学附属中山医院检验科, 2消化科 上海 200032)
NUDT15基因突变致巯唑嘌呤治疗克罗恩病并发严重骨髓抑制1例
周 琰1吴 炯1郭 玮1潘柏申1刘红春2△
(1复旦大学附属中山医院检验科,2消化科 上海 200032)
巯唑嘌呤(azathioprine,AZA)是临床常用的免疫抑制剂,主要用于急慢性淋巴细胞白血病的化疗,也可用于器官移植后预防排斥反应。AZA类药物在自身免疫性疾病的治疗中发挥着重要作用,常用于炎症性肠病(inflammatory bowel disease,IBD)缓解期的维持治疗。AZA的常见不良反应包括骨髓抑制、肝功能损伤、皮疹等。研究认为AZA诱发的严重骨髓抑制与患者的巯代嘌呤甲基转移酶(thiopurine S-methyltransferase,TPMT)的活性及基因单核苷酸多态性有关[1-3]。本文报告1例NUDT15基因突变致AZA治疗克罗恩病并发严重骨髓抑制的病例。
病例资料 患者,男性,40岁,因反复腹痛4个月入院:无明显诱因下反复出现左下腹腹痛,为阵发性绞痛,体位改变可少许缓解,伴恶心、呕吐胃内容物。至外院行胃镜检查示慢性糜烂性胃炎,结肠镜检查未见异常。遂至复旦大学附属中山医院进一步诊治。腹部平片示盆腔小肠异常扩张;腹部盆腔CT提示部分小肠肠壁增厚伴部分小肠扩张积液,空肠及盆腔回肠肠壁增厚、伴异常强化,邻近可见渗出和淋巴结增大;小肠镜检查示回肠多发溃疡伴疤痕形成,肠腔狭窄。病理检查示:慢性炎伴间质内个别中性粒细胞浸润。临床诊断:小肠克罗恩病。予以强的松30 mg/天,美沙拉嗪1.0 g/bid治疗;并加用AZA 50 mg/天,口服;每周随访血常规,白细胞正常,第7周查血常规示:红细胞计数4.87×1012/L,血红蛋白125 g/L,红细胞压积37.5%,血小板计数108×109/L,白细胞计数0.82×109/L,中性粒细胞计数0.1×109/L;凝血功能:凝血酶原时间14.2 s,凝血酶原时间比值1.25;国际标准化比值1.24;肝肾功能未见异常,C反应蛋白(C-reactive protein,CRP)>90 mg/L;伴有脱发全身乏力。停用AZA并予以禁食、抗感染、升白及对症支持治疗。第二天复查血常规示:白细胞计数1.23×109/L,中性粒细胞计数0.1×109/L。随访白细胞计数升至3.18×109/L出院,3周后复查白细胞计数7.04×109/L。
3个月后患者随访血常规示:血红蛋白117 g/L,血小板22×109/L,白细胞计数3.1×109/L;1周后再次复查血常规示:血红蛋白114 g/L,血小板18×109/L,白细胞计数2.23×109/L,三系进行性降低,再次入院。患者神清,四肢皮肤见少量瘀点,未见瘀斑,浅表淋巴结未及,胸骨无压痛,心肺听诊无殊,腹软,左下腹轻压痛,无反跳痛,肝脾肋下未及。骨髓穿刺结果示:骨髓增生低下,粒、巨二系增生低下,红系增生尚活跃伴轻度脱核延迟现象;淋巴细胞比例偏高;骨髓小粒减少,其内较空虚。Coombs试验阴性,胆红素水平正常,未见酱油色尿。免疫风湿系统检测结果示:自身抗体谱检测结果阴性,血清铁、铁蛋白、叶酸、维生素B12均正常。住院期间予以瑞白、维血宁、泼尼松对症治疗,停用AZA,好转后出院。患者出院后长期服用莎尔福1 g/bid,培菲康0.42 g/tid,因AZA导致骨髓抑制,改为甲氨蝶17.5 mg/qw维持治疗并定期随访。期间时有腹部隐痛症状,可自行缓解。定期随访血常规和CRP基本正常。出院后5个月复查血常规示:血小板计数123×109/L,白细胞计数4.26×109/L,中性粒细胞计数2.4×109/L。
AZA导致的骨髓抑制可能与TPMT基因多态性相关。常用的TPMT基因单核苷酸多态性检测(Sanger测序法)有TPMT*2 (rs1800462,238G>C)、TPMT*3C (rs1142345,A719G)、TPMT*3A/3B (rs1800460,G460A)和TPMT*4 (rs1800584)。该患者检测结果均为野生型,未见TPMT基因常见位点突变。为此我们检测了NUDT15基因单核苷酸多态性(Sanger测序法),结果显示:NUDT15 (rs116855232,R139C)纯合突变(图1)。临床立即停用AZA,辅助骨髓活检、Coombs和免疫学检测排除其他原因所致三系减低。最终诊断:回肠克罗恩病,AZA诱发三系减低(骨髓抑制、中性粒细胞缺乏、血小板减少)。
讨论 AZA的代谢途径较为复杂,一般认为其代谢产物物6-巯基嘌呤(6-mercaptopurine,6-MP)
通过3条相互抑制的代谢途径,转化为6-硫鸟嘌呤核苷酸(6-thioguanine nucleotide,6-TGN)发挥细胞毒效应,抑制T-淋巴细胞而影响免疫应答(图2)。
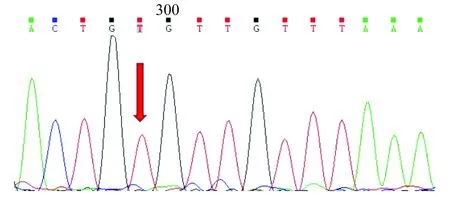
Arrow:Homozygous mutation,Genetype TT.
图1 NUDT15(rs116855232,R139C)测序图
Fig 1 Sanger sequencing of NUDT15 (rs116855232,R139C)
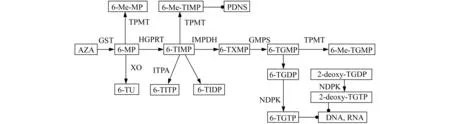
AZA:Azathioprine;GST:Glutathione S-transferase;6-MP:6-mercaptopurine;6-Me-MP:6-methyl-MP;TPMT:Thiopurine methyltransferase;XO:Xanthine oxidase;6-UT:6-thiouricacid;HGPRT:Hypoxanthine-guanine phosphoribosyltransferase;6-TIMP:6-thioinosine monophosphate;6-Me-TIMP:6-methyl-TIMP;ITPA:Inosine triphosphate pyrophosphatase;6-TITP:6-thioinosine triphosphate;6-TIDP:6-thioinosine diphosphate;PDNS:Purinedenovosynthesis;IMPDH:Inosine monophosphate dehydrogenase;6-TXMP:6-thioxan-thosine monophosphate;GMPS:Guanine monphosphate synthetase;6-TGMP:6-thioguanosine monophosphate;6-Me-TGMP:6-methyl-TGMP;6-TGDP:6-thioguanosinediphosphate;2-deoxy-TGDP:2′-deoxyguanosine-TGDP;6-TGTP:6-thioguanosine triphosphate;2-deoxy-TGTP:2′-deoxyguanosine-TGTP;NDPK:Nucleosi dediphos phate kinase.
图2 AZA体内代谢示意图
Fig 2 Metabolism of AZAinvivo
AZA用于IBD稳定期的诱导和维持治疗[4-5],其不良反应多为骨髓抑制、肝功能损伤、皮疹等。在AZA代谢过程中,黄嘌呤氧化酶、次黄嘌呤核苷酸转移酶等均无遗传多态性,因此认为具有基因多态性的TPMT和AZA引起的严重可逆性骨髓抑制相关。TPMT基因多态性引起TPMT酶活性减低,严重影响了活性代谢产物6-MP和6-TGNs药动学效应,增加骨髓抑制等不良反应的风险[5-7]。同时,TPMT甲基化ZAZ使之变成无活性的甲基巯嘌呤排出体外,从而阻碍6-TGN形成,这两条途径形成竞争[8]。TPMT酶活性的降低或缺失与其等位基因突变密切相关,11%的人携带TPMT酶中度活性等位基因的杂合子,TPMT缺陷的个体是低活性等位基因的纯合子。TPMT低活性会导致体内积聚高浓度TGNs,引起造血系统障碍,骨髓抑制,甚至死亡[9]。
研究表明TPMT的酶活性差异可以解释30%由AZA/6-MP引起的严重不良反应(尤其是骨髓抑制)[4]。本例患者在使用AZA (50 mg/天)时出现了严重的骨髓抑制、三系减低,排除自身免疫性溶血、血液系统恶性疾病和其他自身免疫性疾病,考虑因TPMT常见基因型突变引起酶活性异常所致。目前至少发现有29种TPMT基因多态性和酶活性改变相关。例如,TPMT*2~*6、*11~*16和TPMT酶活性降低显著相关,引发严重的骨髓抑制;其中发生频率较高的*2、*3、*4等位基因突变可以解释超过95%的TPMT酶活性降低[9]。我们检测了FDA推荐的TPMT 基因*1、*2、*3、*4多态性,均未见突变型。有报道,在东亚和拉美人群中NUDT15 (rs116855232,R139C)基因多态性是诱导AZA相关不良反应的突变位点[10-11]。该位点突变引起的AZA治疗后严重骨髓抑制,在急慢性淋巴细胞白血病的化疗多有报道[12]。其突变频率在东亚人群中较TPMT基因多态性(2%)更为常见,由此诱发的白细胞减少症在亚洲人群中约为13%,高于欧洲人群的5%。NUDT15参与编码嘌呤特异性核苷二磷酸酶,Moriyama等[13]发现NUDT15通过AZA活性代谢产物tGTP和tdGTP去磷酸化,阻止tGTP和tdGTP掺入到DNA,从而诱发严重的毒性作用。NUDT15改变AZA代谢的具体机制以及突变发生后对基因功能的影响尚不明确[14]。不排除存在其他尚未发现的基因位点影响AZA治疗效果。AZA治疗引起的骨髓抑制是可逆的,患者在停用药物6个月后血常规各项指标恢复正常,这也证实了由AZA治疗引发骨髓抑制、三系减低的临床诊断。
该病例提示应用AZA时TPMT基因型检测正常者并不能完全排除不良反应发生的可能性,应考虑其他基因单核苷酸多态性导致AZA对患者造成的不良反应,密切关注骨髓抑制的发生。同时,应定期随访血常规、肝肾功能,加强宣教和随访,以减少临床不良事件的发生。
NUDT15基因突变; 巯唑嘌呤; 骨髓抑制
[1] CHISICK L,OLESSCHUK C,BERNSTEIN CN.The utility of thiopurine methyltransferase enzyme testing in inflammatory bowel disease[J].CanJGastroenterol,2013,27(1):39-43.
[2] RELLING MV,Hancock ML,Boyett,etal.Prognostic importance of 6-mercaptopurine dose intensity in acute lymphoblastic leukemia[J].Blood,1999,93(9):2817-2823.
[3] RELLING MV,Hancock ML,Rivera GK,etal.Mercaptopurine therapy intolerance and heterozygosity at the thiopurine S-methyltransferase gene locus[J].JNatCancerInst,1999,91(23):2001-2008.
[4] SAHASRANAMAN S,HOWARD D,ROY S.Clinical pharmacologyand pharmacogenetics of thiopurines[J].EurJClinPharmacol,2008,64(8):753-767.
[5] RELLING MV,GARDNER EE,SANDBORN WJ,etal.Clinical pharmacogenetics implementation consortium guidelines for thiopurine methyltransferase genotype and thiopurinedosing:2013 update[J].ClinPharmacolTher,2013,93(4):324-325.
[6] LINDQVIST M,SKOGLUND K,KARLGREN A,etal.Explaining TPMT genotype /phenotype discrepancy by haplotyping of TPMT*3A and identification of a novel sequence variant,TPMT*23[J].PharmacogenetGenomics,2007,17(10):891-895.
[7] BOOTH RA,ANSARI MT,LOIT E,etal.Assessment of thiopurine Smethyltransferase activity in patients prescribed thiopurines:a systematic review[J].AnnInternMed,2011,154(12):814-823.
[8] KUBOTA T,CHIBA K.Frequencies of thiopurine S-methyltransferase mutant alleles (TPMT*2,*3A,*3B and *3C) in 151 healthy Japanese subjects and the inheritance of TPMT*3C in the family of a propositus[J].BrJClinPharmacol,2001,51(5):475-477.
[9] KUMAGAI K,HIYAMA K,ISHIOKA S,etal.Allelotype frequency of the thiopurine methyltransferase (TPMT) gene in Japanese[J].Pharmacogenetics,2001,11(3):275-278.
[10] TANAKA Y,KATO M,HASEGAWA D,etal.Susceptibility to 6-MP toxicity conferred by a NUDT15 variant in Japanese children with acute lymphoblastic leukaemia[J].BrJHaematol,2015;171(1):109-115.
[11] YANG JJ,LANDIER W,YANG W,etal.Inherited NUDT15 variant is a genetic determinant of mercaptopurine intolerance in children with acute lymphoblastic leukemia[J].JClinOncol,2015,33(11):1235-1242.
[12] LEE YJ,HWANG EH,PARK JH,etal.NUDT15 variant is the most common variant associated with thiopurine-induced early leukopenia and alopecia in Korean pediatric patients with Crohn′s disease[J].EurJGastroenterolHepatol,2016,28(4):475-478.
[13] MORIYAMA T,NISHII R,PEREZ-ANDREU V,etal.NUDT15 polymorphisms alter thiopurine metabolism and hematopoietic toxicity[J].NatGenet,2016,48(4):367-373.
[14] AILING Z,JING Y,JINGLI L,etal.Further evidence that a variant of the gene NUDT15 may be an important predictor of azathioprine-induced toxicity in Chinese subjects:a case report[J].JClinPharmTher,2016,41(5):572-574.
上海青年临床医技人才(临床检验专业)培养资助计划(沪医卫基[2016]04号);复旦大学附属中山医院青年基金(2016ZSQN-34);国家自然科学基金面上项目(81572064);上海市卫生计生系统重要薄弱学科建设项目(2015ZB0201)
R733.7,R979.5
B
10.3969/j.issn.1672-8467.2017.04.027
2016-11-03;编辑:段佳)
△Corresponding author E-mail:liu.hongchun@zs-hospital.sh.cn
*This work was supported by Shanghai Outstanding Youth Clinical Medical Talents (Medical Laboratory Scientists) Training Funding (HYWJ[2016]04),the Youth Fundation of Zhongshan Hospital,Fudan University (2016ZSQN-34),the General Program of National Natural Science Foundation of China (81572064) and the Key Developing Disciplines of Shanghai Municipal Commission of Health and Family Planning (2015ZB0201).
