噬菌体展示技术在食品安全分析中的应用
2017-08-09赵岩岩赵圣明刘贤金李红波河南科技学院食品学院河南新乡453003江苏省农业科学院食品质量安全与检测研究所江苏南京004南京农业大学江苏省肉类生产与加工质量安全控制协同创新中心江苏南京0095
赵岩岩,赵圣明,梁 颖,刘贤金,张 浩,李红波,屠 康(.河南科技学院食品学院,河南新乡 453003; .江苏省农业科学院食品质量安全与检测研究所,江苏南京 004; 3.南京农业大学,江苏省肉类生产与加工质量安全控制协同创新中心,江苏南京 0095)
噬菌体展示技术在食品安全分析中的应用
赵岩岩1,赵圣明1,梁 颖2,刘贤金2,张 浩1,李红波1,屠 康3,*
(1.河南科技学院食品学院,河南新乡 453003; 2.江苏省农业科学院食品质量安全与检测研究所,江苏南京 210014; 3.南京农业大学,江苏省肉类生产与加工质量安全控制协同创新中心,江苏南京 210095)
随着噬菌体展示技术的发展,其在食品安全领域的应用也越来越多,该技术可以作为一种高效的抗体制备技术应用于食品中常见的抗生素、生物毒素、有害小分子的检测及食源性致病菌控制,同时可以开发有毒待检物的替代品建立绿色检测技术。此外,噬菌体展示技术在新型食品防腐剂开发等方面也具有广阔的应用前景。本文在介绍噬菌体展示技术的基础上,对其在食品安全领域的应用进行了综述。
噬菌体展示技术,高通量筛选,食品安全,检测
噬菌体展示技术是上世纪80年代兴起的一种生物学技术,该技术以噬菌体或噬菌粒为载体,将外源多肽或蛋白基因整合到噬菌体基因组中,外源蛋白以融合形式表达并展示在噬菌体表面,可以实现表型和基因型的同步筛选[1-2]。随着噬菌体技术的不断发展和完善,噬菌体展示技术迅速成为诸多领域的研究热点,其在食品安全领域的应用也越来越广泛。本文在对噬菌体展示技术进行介绍的基础上,进一步对其在食品安全分析中的应用进行分类综述,并展望了该技术在食品领域的应用前景,以期为相关学者提供参考。
1 噬菌体展示技术
20世纪80年代,噬菌体展示技术逐步建立并发展起来,该技术系统由改造后的噬菌体、辅助噬菌体和宿主细菌等构成,可以对多基因进行体外克隆、体内克隆和重组表达[3]。噬菌体展示技术可以将抗体表达在重组噬菌体衣壳蛋白的表面,通过对抗原进行多轮亲和筛选,分离获得目的抗体,为抗体的制备提供了新的方法[4-5]。
噬菌体展示技术所展示的片段,可以是天然抗体、免疫抗体、人工合成抗体或多肽,对应的库分别为天然抗体库、免疫抗体库、人工合成抗体库和肽库[6]。以未经免疫动物的mRNA为模板,克隆抗体可变区基因,连接到载体上,构建获得的抗体库为天然抗体库。由于天然抗体库未经免疫,相对免疫库多样性更好,不仅局限于对某一种或几种抗原的识别,能够对多种抗原进行识别,其应用范围相对更加广泛。以免疫动物的杂交瘤细胞或B细胞的mRNA为模板,克隆抗体可变区基因,并将其与载体连接,构建的库为免疫抗体库。经抗原免疫后,机体会产生大量的特异性抗体,因此,免疫抗体库含有大量的特异性抗体基因,可以针对抗原筛选高亲和力的抗体。抗原与抗体的特异性结合主要取决于抗体重链、轻链可变区,通过基因工程手段对抗体可变区基因进行改造,利用这种方法获得的抗体库称为人工合成抗体库。展示的抗体片段包括Fab、scFv、sDAB和DAB等抗体分子[7],其结构示意图见图1。通过化学合成寡核苷酸片段,连接载体,构建的展示库称为肽库,肽库编码的肽段可以是从几肽到数十肽的随机肽段。
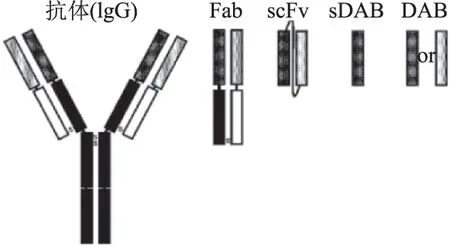
图1 抗体分子结构[7]Fig.1 Antibody molecule structures[7]
噬菌体展示技术为研究蛋白间的相互作用提供了有利工具,在医药、食品、农业检测等领域得到了广泛应用[8]。为了满足各种应用环境的要求和挑战,噬菌体展示技术也在不断地改良和更新,目前为止已经构建了M13[3]、λ[9]、T4[10]和T7[11]等噬菌体展示系统。噬菌体展示技术发展历程如图2所示。
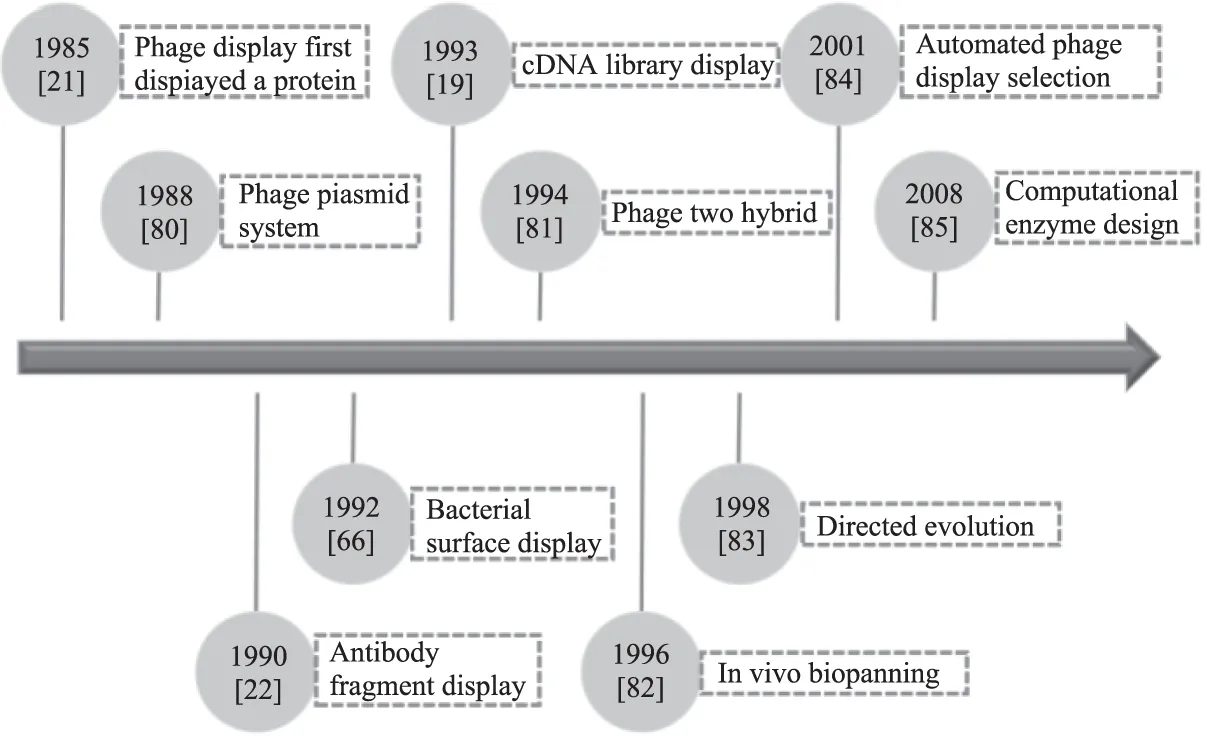
图2 噬菌体展示技术发展历程[12]Fig.2 The development history of the phage display[12]
在抗体筛选上,与传统的杂交瘤技术相比,噬菌体展示技术的优势主要表现在:减少或避免实验动物的使用、抗体生产周期短、成本低、操作相对简便[13]。此外,筛选的高效率性使得目标蛋白含量在非常低的情况下,通过感染得到富集,使获得高亲和力目标蛋白成为可能;利用噬菌体展示技术筛选获得的蛋白,可确定其基因型,因此更方便地对其进行基因改造,以期获得更为理想的蛋白。
噬菌体展示技术将不同DNA编码的蛋白片段作为噬菌体衣壳蛋白的一部分展示在噬菌体表面,可以实现在大肠杆菌中表达数百万大库容的文库,在对蛋白进行筛选的过程中,同时实现了对基因的筛选,即基因型与表型的统一[14]。展示特异结合位点的噬菌体可以通过多轮结合、洗涤、洗脱和扩增的筛选过程得到富集。筛选示意图如图3所示。利用某一靶标对展示库进行筛选,与该靶标相关的配基会被结合,未结合的噬菌体在洗涤过程中被洗去,结合的噬菌体通过洗脱进行回收,然后扩增富集回收的噬菌粒,经几轮筛选后,获得具有高结合活性的噬菌粒,再进一步对其生物学活性进行分析,即可获得目的配基[15]。
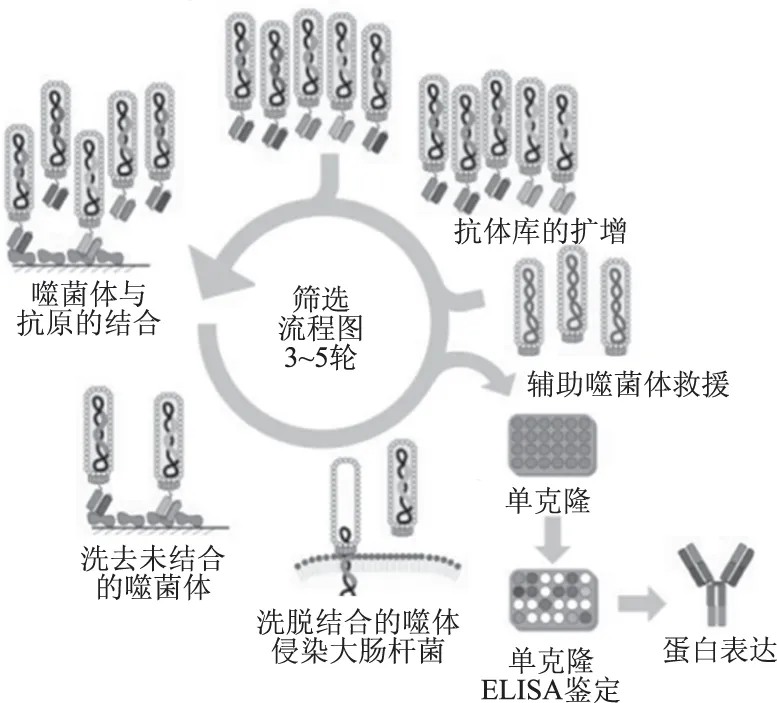
图3 抗体库筛选流程图[16]Fig.3 Selection of antibody by phage display protocol[16]
2 噬菌体展示技术在食品安全领域的应用
自从1985年Smith首次报道噬菌体展示技术以来,噬菌体展示技术迅速的成为诸多领域的研究热点,其中包括食品安全领域。食品安全长期以来一直是人们关注的焦点问题。随着噬菌体展示技术的发展,利用噬菌体展示技术筛选食品中有害物质抗体的研究也越来越多,包括在抗生素分析中的应用,生物毒素分析中的应用,农药小分子检测中的应用,及食源性致病菌防治中的应用。下面主要对噬菌体展示技术在食品安全这几个方面的应用展开详细的介绍。
2.1 在抗生素分析中的应用
由于抗生素的滥用导致食品中抗生素残留超标已经成为食品安全领域人们愈发关注的焦点。噬菌体展示技术为抗生素免疫检测中抗体的获得提供了新思路,近年来已通过噬菌体展示技术筛选获得了多种抗生素的抗体。Burmester等[17]利用免疫小鼠构建的单链抗体库,筛选获得与氨苄西林具有良好识别活性的单链抗体,并对其晶体结构、结合位点进行了分析研究。Xiao等[18]利用构建的免疫单链抗体库,筛选伊维菌素单链抗体,最终获得10个与伊维菌素具有良好结合活性的克隆。Nejad[19]利用莫能菌素作为半抗原免疫小鼠构建免疫单链抗体库,筛选获得能够识别莫能菌素的单链抗体,并建立了荧光偏振免疫分析方法。孟辉等[20]以免疫获得的杂交瘤细胞株为基因来源构建噬菌体展示单链抗体库,经筛选后获得9个与庆大霉素具有结合活性的单链抗体。上述噬菌体展示抗体的开发,使抗体的大量制备变得简单易行,所获得的抗体在今后的改造过程当中也更容易操作,为免疫检测技术在抗生素检测中的发展奠定了良好的基础。
2.2 在生物毒素分析中的应用
生物毒素包括细菌毒素、真菌毒素、植物毒素、动物毒素、海洋生物毒素等,常常污染食品和饲料,对人畜造成了极大的危害。因此对食品和饲料中生物毒素进行监测非常必要。基于噬菌体展示技术发展起来的检测方法已有很多,同时噬菌体展示技术的发展使毒素的无毒抗原制备成为可能。Nagumo等[21]利用磁珠筛选法对噬菌体抗体库进行筛选,获得识别鱼肉毒素的抗体。Zhao等[22]利用噬菌体展示技术筛选获得了能识别微囊藻毒素的多肽。Iain等[23]利用自己构建的软骨藻酸羊免疫抗体库,基于筛选获得的抗体建立了检测软骨藻酸的竞争ELISA方法。Doyle等[24]利用免疫羊驼构建的乙酰脱氧雪腐镰刀菌烯醇单域抗体库,筛选获得其单域抗体,并建立了竞争ELISA检测分析方法和荧光偏振免疫分析方法。Houwelingen等[25]利用噬菌体展示库筛选获得赭曲霉毒素的纳米抗体,建立了竞争ELISA检测方法。Wang等[26]利用噬菌体展示随机8肽库筛选获得能够模拟黄曲霉毒素表位的多肽,并建立了绿色ELISA检测方法。Xue等[27]制备黄曲霉细胞壁免疫鸡,构建鸡源单链抗体库,从中筛选出高亲和力的单链抗体,与碱性磷酸酶融合表达后建立高灵敏度的黄曲霉检测方法。Qiu等[28]利用纳米抗体库和呕吐毒素的单克隆抗体进行筛选,获得两个与呕吐毒素单克隆抗体具有结合活性的纳米抗体,可以替代呕吐毒素作为包被抗原应用到免疫检测中,同时对模拟抗原的分子机制进行了研究。Hu等[29]对亲和力成熟的单链抗体库进行筛选,获得识别伏马菌素的单链抗体,并用于伏马菌素的免疫检测。Xu等[30]利用噬菌体单域抗体库筛选获得桔霉素的抗独特型抗体,并应用于桔霉素的检测中。Wang等[31]筛选获得了玉米烯醇的抗独特型抗体,并建立了免疫PCR检测方法,用于谷物中玉米烯醇的检测。同时一些毒素的抑制剂也被发现,Gupta等[32]利用噬菌体展示技术筛选获得能够中和大肠杆菌内毒素的单域抗体。上述抗体的制备为生物毒素的检测提供了有效的检测方法;一些抗独特型抗体可以替代有毒抗原的使用,建立了绿色免疫检测新技术,降低了检测过程中有毒抗原给检测人员及环境造成的危害。
2.3 在食品中有害小分子检测中的应用
自噬菌体展示技术出现以来,已筛选获得多种农药小分子的抗体和抗独特型抗体[33],为小分子的免疫检测提供了新材料。与此同时,建立食品中多残留免疫检测方法,用于农药的快速筛查已经成为目前一个热门研究方向,噬菌体展示技术的发展为其提供了有力的工具。Tiejun等[34]通过免疫小鼠并构建甲胺磷免疫噬菌体展示抗体库,从中筛选获得与甲胺磷具有良好结合活性的抗体,并建立甲胺磷竞争ELISA检测方法。Brichta等[35]采用固相筛选法利用2,4-二氯苯氧乙酸除草剂对未经免疫的抗体库进行筛选,获得具有结合活性的抗体,并建立了间接竞争ELISA检测方法。Yi等[36]利用丙酸、阿特拉津、西玛津、异丙隆衍生物作为半抗原混合免疫家兔,构建噬菌体单链抗体库,筛选出与半抗原具有结合活性的单链抗体。González-Techera等[37]利用噬菌体展示的免疫复合物多肽,构建了检测草脱净电化学免疫传感器。Liu等[38]利用7肽库筛选获得识别吡虫啉的多肽,建立了竞争ELISA检测方法,并对水样和土样中吡虫啉进行了检测。Hua等[39]基于噬菌体展示肽库筛选获得的多肽,建立了有机磷农药多残留检测方法。小分子农药对人体和环境也存在着一定的毒性,其抗独特型抗体在免疫检测中可以替代抗原,开发无毒免疫检测技术。实践生产环节中需要此类快速筛查技术对果蔬中的农药残留进行初步检测,保证人们能够享受新鲜果蔬,同时也确保了食品的安全性。除了检测农药小分子外,噬菌体展示技术还被用于食品添加剂的检测。Lee等[40]研究对12肽库进行5轮筛选后,获得能够识别苯甲酸甲酯和对羟基苯甲酸丙酯的多肽,并有望应用于检测。
2.4 在食源性致病菌控制中的应用
目前利用噬菌体展示技术,筛选肽或蛋白用于食源性致病菌防治的研究已有报道。在实际应用中这些多肽或蛋白可能出现稳定性差、易降解等问题,利用其易于改造的特点,Pini等[41]利用十肽库对大肠杆菌进行筛选,获得具有抑菌活性的多肽,并将其改造成对肽酶和蛋白酶稳定、抑菌活性显著提高的抗菌肽。Bishop-Hurley等[42]利用噬菌体展示肽库筛选获得11个与空肠弯曲杆菌具有结合活性并能抑制其生长的多肽。Sainath等[43]利用噬菌体展示随机肽库筛选获得识别大肠杆菌表面的多肽,获得的多肽对革兰氏阴性菌具有抑菌活性,对大肠杆菌和绿脓杆菌具有良好的抑菌活性。鉴于上述新型抗菌物质的发现,通过噬菌体展示技术筛选获得抑菌蛋白替代传统的化学防腐剂在食品防腐保鲜领域将具有广阔的市场应用前景。Agrawal等[44]筛选肽库获得可以用于鼠伤寒沙门氏菌检测的多肽,可以用于检测食品中鼠伤寒沙门氏菌污染的程度。在食品安全备受人们关注的大环境下,相信该技术也将能够被更广泛地应用于食源性致病菌的预防和控制中。
3 前景与展望
我国是农业大国,抗生素、农药的使用,食品中微生物及其毒素的污染,给食品安全带来了潜在的威胁。食品中有害成分的检测及致病微生物的控制已经成为当前食品安全领域的研究热点,近年来基于噬菌体展示技术发展起来的高通量筛选技术在食品安全领域得到了广泛的应用。在筛选特异性的噬菌体、抗体、多肽等时,噬菌体展示筛选库容量大、周期短、操作简单成本低等优势[45]。在对食品中有毒有害物质进行检测时,可以利用噬菌体展示技术筛选其模拟抗原,进一步结合相关免疫学检测技术,建立绿色、安全的检测方法,以期减少对人体和环境所造成的危害。利用噬菌体展示技术筛选获得具有抑菌活性的多肽可以用于食品中微生物污染的控制。在食品安全领域快速发展的大背景下,噬菌体展示技术也会得到飞速发展,其优势也将得到更充分的应用。抗独特型抗体具有模拟抗原活性的潜能,今后对噬菌体展示技术的研究,可以从筛选获得农药的抗独特型抗体开展,筛选具有农药功效的绿色替代品,减少农药的使用,从根源上减少农药对食品造成的污染;还可以将噬菌体展示技术与其他先进技术如胶体金技术结合使用,两者的结合使其在应用中更加快速、便捷;也可以将食源性致病菌的蛋白质组以噬菌体展示的形式表达,可以用于药物靶标的筛选,用于分析药物与微生物的相互作用,为食源性致病菌的防治提供新思路。
[1]PANDE J,SZEWCZYK M M,GROVER A K. Phage display:Concept,innovations,applications and future[J]. Biotechnology Advances,2010,28(6):849-858.
[2]FREI J C,LAI J R. Protein and antibody engineering by phage display[J]. Methods in Enzymology,2016,580:45-87.
[3]CRUZ S D L,CUBILLOS-ZAPATA C,LóPEZ-CALLEJA I M,et al. Isolation of recombinant antibody fragments(scFv)by phage display technology for detection of almond allergens in food products[J]. Food Control,2015,54:322-330.
[4]CLEMENTI N,MANCINI N,SOLFOROSI L,et al. Phage display-based strategies for cloning and optimization of monoclonal antibodies directed against human pathogens[J]. International Journal of Molecular Sciences,2012,13(7):8273-8292.
[5]CRUZ S D L,CUBILLOS-ZAPATA C,LóPEZ-CALLEJA I M,et al. Isolation of recombinant antibody fragments(scFv)by phage display technology for detection of almond allergens in food products[J]. Food Control,2015,54:322-330.
[6]RAHBARNIA L,FARAJNIA S,BABAEI H,et al. Evolution of phage display technology:from discovery to application[J]. Journal of Drug Targeting,2017,25(3):216-224.
[7]GULIG P A,MARTIN J L,MESSER H G,et al. Phage display methods for detection of bacterial pathogens[M]. New York:Springer,2007:755-783.
[8]CHEN X,DRESKIN S C. Application of phage peptide display technology for the study of food allergen epitopes[J]. Molecular Nutrition and Food Research,2016:1600568.
[9]MARUYAMA I N,MARUYAMA H I,BRENNER S. Lambda foo:a lambda phage vector for the expression of foreign proteins[J]. Proceedings of the National Academy of Sciences,1994,91(17):8273-8277.
[10]REN Z J,BLACK L W,LEWIS G K,et al. Phage display of intact domains at high copy number:a system based on SOC,the small outer capsid protein of bacteriophage T4[J]. Protein Science,1996,5(9):1833-1843.
[11]ROSENBERG A,GRIFFIN K,STUDIER F W,et al. T7 select phage display system:a powerful new protein display system based on bacteriophage T7[J]. Innovations,1996,6:1-6.
[12]YUAN S L,LI X,CHEN H B,et al. Research progress in the phage display technology mapping epitope for major food allergens[J]. Science and Technology of Food Industry,2015,36(3):379-384.
[13]WINTER G,GRIFFITHS A D,HAWKINS R E,et al. Making antibodies by phage display technology[J]. Annual Review of Immunology,1994,12(1):433-455.
[14]TAN Y,TIAN T,LIU W,et al. Advance in phage display technology for bioanalysis[J]. Biotechnology Journal,2016,11(6):732-745.
[15]FUKUDA M N. Screening of peptide-displaying phage libraries to identify short peptides mimicking carbohydrates[J]. Methods Enzymol,2006,416:51-60.
[16]DüBEl S,REICHERT J M. Handbook of therapeutic antibodies[M]. Second edition,Wiley:Wiley-VCH Verlag GmbH and Co. KGaA:2014:43-76.
[17]BURMESTER J,PUGLIESE L K A,HONEGGER A,et al. Selection,characterization and X-ray structure of anti-ampicillin single-chain Fv fragments from phage-displayed murine antibody libraries[J]. Journal of Molecular Biology,2001,309(3):671-685.
[18]ZHANG X,Zhang C,LIU Y,et al. Construction of scFv phage display library with hapten-specific repertories and characterization of anti-ivermectin fragment isolated from the library[J]. European Food Research and Technology,2010,231(3):423-430.
[19]NEJAD S M,VELDHUIS S L,RICHARD G,et al. Selection of single chain variable fragment(scFv)antibodies from a hyperimmunized phage display library for the detection of the antibiotic monensin[J]. Journal of Immunological Methods,2010,360(1-2):103-118.
[20]孟辉,温凯,沈建忠,等. 抗庆大霉素噬菌体抗体库的构建和筛选[J]. 中国畜牧兽医,2011,38(1):76-80.
[21]NAGUMO Y,OGURI H,TSUMOTO K,et al. Phage-display selection of antibodies to the left end of CTX3C using synthetic fragments[J]. Journal of Immunological Methods,2004,289(1-2):137-146.
[22]ZHAO S W,SHEN P P,ZHOU Y,et al. Selecting peptide ligands of microcystin-LR from phage displayed random libraries[J]. Environment International,2005,31(4):535-541.
[23]SHAW I,O’REILLY A,MARGARET C,et al. Development of a high-affinity anti-domoic acid sheep scFv and its use in detection of the toxin in shellfish[J]. Analytical Chemistry,2008,80(9):3205-3212.
[24]DOYLE P J,GHAHROUDI M-A,GAUDETTE N,et al. Cloning,expression,and characterization of a single-domain antibody fragment with affinity for 15-acetyl-deoxynivalenol[J]. Molecular Immunology,2008,45(14):3703-3713.
[25]HOUWELINGEN A V,SAEGER S D,RUSANOVA T,et al. Generation of recombinant alpaca VHH antibody fragments for the detection of the mycotoxin ochratoxin A[J]. World Mycotoxin Journal,2008,1(4):407-417.
[26]WANG Y,WANG H,LI P,et al. Phage-displayed peptides that mimic aflatoxins and its application in immunoassay[J]. Journal of Agricultural and Food Chemistry,2013,61(10):2426-2433.
[27]XUE S,LI H P,ZHANG J B,et al. Chicken single-chain antibody fused to alkaline phosphatase detects Aspergillus pathogens and their presence in natural samples by direct sandwich enzyme-linked immunosorbent assay[J]. Analytical Chemistry,2013,85(22):10992-10999.
[28]QIU Y L,HE Q H,XU Y,et al. Deoxynivalenol-mimic nanobody isolated from a naïve phage display nanobody library and its application in immunoassay[J]. Analytica Chimica Acta,2015,887:201-208.
[29]HU Z Q,LI H P,WU P,et al. An affinity improved single-chain antibody from phage display of a library derived from monoclonal antibodies detects fumonisins by immunoassay[J]. Analytica Chimica Acta,2015,867:74-82.
[30]XU Y,XIONG L,LI Y,et al. Citrinin detection using phage-displayed anti-idiotypic single-domain antibody for antigen mimicry[J]. Food Chemistry,2015,177:97-101.
[31]WANG X,HE Q,YANG X,et al. Anti-idiotypic VHH phage display-mediated immuno-PCR for ultrasensitive determination of mycotoxin zearalenone in cereals[J]. Talanta,2016,147:410-415.
[32]GUPTA A K,SINGH A. Single-domain antibody selected from the phage display library neutralizes Escherichia coli endotoxin-induced effects on leukocytesinvitroand in Swiss albino mice[J]. International Journal of Infectious Diseases,2016,45:136-137.
[33]HUA X D,SHI H Y,WANG M H. Phage display peptide library technology and its research progress in immunoassay of pesticide residue[J]. Journal of Food Safety and Quality,2014(12):3955-3961.
[34]LI T,ZHANG Q,LIU Y,et al. Production of recombinant ScFv antibodies against methamidophos from a phage-display library of a hyperimmunized mouse[J]. Journal of Agricultural and Food Chemistry,2006,54(54):9085-9091.
[35]BRICHTA J,VESELA H,FRANEK M. Production of scFv recombinant fragments against 2,4-dichlorophenoxyacetic acid hapten using naïve phage library[J]. Veterinární Medicína,2003,48(9):237-247.
[36]LI Y,COCKBURN W,KILPATRICK J B,et al. High affinity ScFvs from a single rabbit immunized with multiple haptens[J]. Biochemical and Biophysical Research Communications,2000,268(2):398-404.
[37]GONZáLEZ-TECHERA A,ZON M A,MOLINA P G,et al. Development of a highly sensitive noncompetitive electrochemical immunosensor for the detection of atrazine by phage anti-immunocomplex assay[J]. Biosensors and Bioelectronics,2015,64(64):650-656.
[38]LIU Z,LIU J,WANG K,et al. Selection of phage-displayed peptides for the detection of imidacloprid in water and soil[J]. Analytical Biochemistry,2015,485(23):365-367.
[39]HUA X,LIU X,SHI H,et al. Development of a heterologous enzyme-linked immunosorbent assay for organophosphorus pesticides with phage-borne peptide[J]. RSC Advances,2014,4(80):42445-42453.
[40]LEE J,KIM Y H,MIN J. Screening of phage display-derived peptides to detect parabens[J]. New Biotechnology,2016,33:172-173.
[41]PINI A,GIULIANI A,FALCIANI C,et al. Antimicrobial activity of novel dendrimeric peptides obtained by phage display selection and rational modification[J]. Antimicrobial Agents and Chemotherapy,2005,49(7):2665-2672.
[42]BISHOP-HURLEY S L,REA P J,MCSWEENEY C S. Phage-displayed peptides selected for binding to Campylobacter jejuni are antimicrobial[J]. Protein Engineering Design and Selection,2010,23(10):751-757.
[43]RAO S S,MOHAN K V,ATREYA C D. A peptide derived from phage display library exhibits antibacterial activity against E. coli and Pseudomonas aeruginosa[J]. Plos One,2013,8(2):e56081.
[44]TAN Y,TIAN T,LIU W,et al. Advance in phage display technology for bioanalysis[J]. Biotechnology Journal,2016,11(6):732-745.
[45]AGRAWAL S,KULABHUSAN P K,JOSHI M,et al. A high affinity phage-displayed peptide as a recognition probe for the detection of Salmonella typhimurium[J]. Journal of Biotechnology,2016,231:40-45.
Application of phage display technology in food safety
ZHAO Yan-yan1,ZHAO Sheng-ming1,LIANG Ying2,LIU Xian-jin2,ZHANG Hao1,LI Hong-bo1,TU Kang3,*
(1.Department of Food Science,Henan Institute of Science and Technology,Xinxiang 453003,China; 2.Ministry of Agriculture Institute of Food Quality Safety and Detection, Jiangsu Academy of Agricultural Sciences,Nanjing 210014,China; 3.Jiangsu Collaborative Innovation Center of Meat Production and Processing, Quality and Safety Control,Nanjing Agricultural University,Nanjing 210095,China)
In this article,the phage display technology was described,and its application in food safety was summarized. With the development of the phage display technology,it is widely used in the food safety. It can be used as an efficient method of generation of antibody to detect antibiotic,bio-toxin and small molecule in food,used to screening mimic for developing green detection technology,and the control of foodborne pathogenic bacterial. In addition,this technology also showed broad application in the field of developing novel food preservatives.
phage display technology;high throughput screening;food safety;detection
2016-12-20
赵岩岩(1987-),女,博士,讲师,研究方向:微生物与生物技术,E-mail:zhaoyanyan@hist.edu.cn。
*通讯作者:屠康(1968-),男,博士,教授,研究方向:农产品无损检测、农产品贮藏与加工,E-mail:kangtu@njau.edu.cn。
河南省高校科技创新团队支持计划(16IRTSTHN007);河南省科技攻关项目(162102110065,172102310240);河南科技学院高层次人才科研项目(2016019)。
TS201
A
1002-0306(2017)14-0342-05
10.13386/j.issn1002-0306.2017.14.067
