四种蛋白酶酶解对桦褐孔菌多糖的α-葡萄糖苷酶抑制活性影响
2017-08-09佟世生胡锦荣张京声董文霞北京城市学院生物医药学部北京00094中国农业大学食品与营养工程学院北京00083
佟世生,胡锦荣,张京声,董文霞,王 丽,刘 萍,*(.北京城市学院生物医药学部,北京 00094;.中国农业大学食品与营养工程学院,北京 00083)
四种蛋白酶酶解对桦褐孔菌多糖的α-葡萄糖苷酶抑制活性影响
佟世生1,胡锦荣2,张京声2,董文霞2,王 丽2,刘 萍2,*
(1.北京城市学院生物医药学部,北京 100094;2.中国农业大学食品与营养工程学院,北京 100083)
为了探究桦褐孔菌高温水提粗多糖(High temperature water-extracted polysaccharides,HIOP)中结合蛋白质组成键型与其α-葡萄糖苷酶抑制活性的关系,用4种不同的蛋白酶对HIOP进行酶解,测定蛋白酶水解后对其分子量组成及α-葡萄糖苷酶抑制活性的影响。结果显示,与原HIOP在10 μg/mL时的α-葡萄糖苷酶抑制率83.72%相比,经中性蛋白酶、碱性蛋白酶、胃蛋白酶和胰蛋白酶酶解处理后的HIOP,α-葡萄糖苷酶抑制率最低分别为53%、65%、6.5%和7.1%,其中胃蛋白酶和胰蛋白酶酶解处理显著降低了HIOP的α-葡萄糖苷酶抑制活性,表明HIOP中结合蛋白在HIOP的α-葡萄糖苷酶抑制活性中有一定作用。结合四种蛋白酶的作用效果与作用键型推测,HIOP中结合蛋白的活性中心可能含有芳香族氨基酸、酸性氨基酸、赖氨酸或精氨酸,破坏此类肽键,α-葡萄糖苷酶抑制活性明显降低,而四种蛋白酶酶解均未使HIOP分子量发生较大改变,说明四种蛋白酶酶解仅影响了HIOP与α-葡萄糖苷酶活性中心结合的部位。
桦褐孔菌粗多糖,蛋白酶,α-葡萄糖苷酶抑制活性
α-葡萄糖苷酶抑制剂多被用于糖尿病的日常血糖控制,其通过抑制位于小肠的α-葡萄糖苷酶,使淀粉类分解为葡萄糖的速度减慢,从而减缓肠道内葡萄糖的吸收,降低餐后高血糖的升高[1-3]。目前常见的药物为阿卡波糖,已广泛应用于临床[4]。但阿卡波糖在抑制α-葡萄糖苷酶活性的同时,会引发肠道不适等副作用[5],有一定的局限性。因此开发高效低副作用的新型α-葡萄糖苷酶抑制剂是非常重要的。目前许多研究表明一些天然产物对α-葡萄糖苷酶具有明显抑制作用。李朝晖等[6]发现,从枸杞子中提取的多糖能够抑制消化道内α-葡萄糖苷酶的活性,有良好的降血糖作用。张钟等[7]研究发现,荔枝果肉水溶性多糖对α-葡萄糖苷酶具有明显抑制作用,且其抑制效果是阿卡波糖的1.25倍。

表1 α-葡萄糖苷酶活性抑制率反应体系Table 1 Reaction system of inhibition activity against α-glucosidase
桦褐孔菌(Inonotusobliquus),又称白桦茸(Chaga),是生长于白桦树上的真菌。它主要分布在北纬45~50°的地区,如北美北部、芬兰、俄罗斯、中国黑龙江、吉林省长白山地区等。目前国内外对于桦褐孔菌的研究发现桦褐孔菌多糖具有抗免疫、抗肿瘤、抗氧化等广泛的药理作用[8-13]。俄罗斯Komsomlshi制药公司还发现桦褐孔菌精粉对糖尿病的治愈率为93%[14],可以修复已损坏的β-细胞[15-17]。本实验前期研究发现,桦褐孔菌高温水提粗多糖(High temperature water-extracted polysaccharides,HIOP)对α-葡萄糖苷酶有明显的抑制作用,其中10 μg/mL的HIOP对α-葡萄糖苷酶抑制率高达83.72%,而阿卡波糖在1000 μg/mL时,α-葡萄糖苷酶抑制率也仅为27.03%。因此HIOP具有成为一种新型的α-葡萄糖苷酶抑制剂的潜力。而众所周知,多糖分子的结构进行适当修饰可以显著增强其生物活性[18-20]。因此对HIOP分子结构的研究非常必要。前期实验中发现HIOP中含有一定量的结合蛋白,而结合蛋白在桦褐孔菌多糖的α-葡萄糖苷酶抑制活性中是否有作用无法确定。因此本文分别使用中性蛋白酶、碱性蛋白酶、胃蛋白酶、胰蛋白酶四种不同的蛋白酶对HIOP进行酶解处理。以HIOP的α-葡萄糖苷酶抑制活性和大分子物质组成的变化为主要测定因素,对HIOP 中的结合蛋白对其α-葡萄糖苷酶抑制活性及分子组分变化进行了初步的研究,为药物的开发与利用提供一定的参考和借鉴。
1 材料与方法
1.1 材料与仪器
桦褐孔菌高温水提粗多糖(HIOP) 本实验室前期分离,北京蓝弋化工有限公司:中性蛋白酶(60000 U/g)、碱性蛋白酶(1000000 U/g) 美国Sigma公司:胃蛋白酶(800 U/g)、胰蛋白酶(250000 U/g)、α-葡萄糖苷酶(酿酒酵母)、对硝基苯基-α-D-吡喃葡萄糖苷(PNPG) 美国Corning公司;96孔酶标板。
TGL-16C离心机 上海安亭科学仪器厂;TU-1810紫外分光光度计 上海棱光科技有限公司;M200 pro多功能酶标仪 Tecan集团奥地利有限公司;1260 Infinity凝胶渗透色谱仪 美国Agilent公司。
1.2 实验方法
1.2.1 酶解处理 实验组:向浓度为10 mg/mL的50 mL HIOP溶液中分别添加中性蛋白酶溶液、碱性蛋白酶溶液、胃蛋白酶溶液、胰蛋白酶溶液(四种酶均配为酶活大小为1000 U/mL),按照总反应体系的1%、2%、3%、4%、5%的体积百分数,添加量为500、1000、1500、2000、2500 U/mL;对照组:在50 mL水溶液中(与10 mg/mL的HIOP溶液等体积),再添加与实验组相同量的酶溶液。在酶的最适条件下酶解3 h后,于100 ℃下水浴加热10 min,使其中的酶充分灭活。酶解多糖液8000 r/min离心10 min去除沉淀后,稀释酶解多糖溶液使其多糖浓度为10 μg/mL,测定实验组与对照组的α-葡萄糖苷酶抑制率。实验中以未经任何处理的10 μg/mL HIOP为空白组。
1.2.2 酶解后分子组成变化 使用凝胶渗透色谱(GPC)法测定酶添加量5%所得酶解糖液的分子量组成变化[21-23]。色谱条件:色谱柱,Waters UllrallydrogelTM Linear(规格为7.8 mm×300 mm);检测器,Waters 2410示差折光检测器;流动相,0.1 mol/L NaNO3溶液;流速,0.9 mL/min;柱温,45 ℃。
1.2.3α-葡萄糖苷酶抑制率测定 使用96孔酶标板进行α-葡萄糖苷酶抑制率的测定[24-25]。吸取pH6.8的磷酸盐缓冲液60 μL和待测样品溶液20 μL置于96孔板上,加入2 U/mL的α-葡萄糖苷酶溶液20 μL,混匀后于37 ℃反应10 min,再加入5 mmol/L的PNPG溶液20 μL,混匀,于37 ℃继续反应10 min,最后加入0.1 mol/L的Na2CO3溶液30 μL调节反应体系的pH至碱性,终止反应。具体反应体系如表1所示。使用酶标仪,测定405 nm波长处的吸光度值,根据以下公式,计算抑制率R。

式中:A1为样品溶液组的吸光度;A2为样品对照组的吸光度;A3为对照组溶液的吸光度;A4为空白对照组溶液的吸光度。
1.2.4 数据处理 实验中每个处理重复三次,采用Origin8.0作图分析。
2 结果与分析
2.1 中性蛋白酶酶解对HIOP的α-葡萄糖苷酶抑制活性及组分的影响
从图1可以看出,经中性蛋白酶酶解处理后的HIOP的α-葡萄糖苷酶抑制率下降,其中在中性蛋白酶酶浓度为500 U/mL时,经酶解后的HIOP的α-葡萄糖苷酶抑制率由原来83.72%降至52.58%,但酶浓度为500~1500 U/mL时,酶解处理后的HIOP的α-葡萄糖苷酶抑制率变化不明显。其中,在酶浓度较高(2000~2500 U/mL)时,经酶解后的HIOP的α-葡萄糖苷酶抑制率出现小幅度回升现象,但抑制率仍明显低于未经酶解处理的HIOP。推测可能是大量酶液的添加使得反应体系中产生了颜色叠加现象,从而影响了实验结果的测定,使得测定的HIOP的α-葡萄糖苷酶抑制率出现回升现象。

图1 中性蛋白酶酶解对HIOP的α-葡萄糖苷酶抑制活性的影响Fig.1 Effect of neutral protease hydrolysis on α-glucosidase inhibitory rate of HIOP
中性蛋白酶是由枯草芽孢杆菌经发酵提取而得的,属于一种内切酶。在50 ℃、pH6.0~7.5的条件下,能将大分子蛋白质水解为氨基酸等产物。从图1中可以看出,经中性蛋白酶酶解后,HIOP的α-葡萄糖苷酶抑制率出现下降现象,推测可能是中性蛋白酶水解了HIOP中的结合蛋白,从而使其α-葡萄糖苷酶抑制率降低。说明HIOP中的结合蛋白在HIOP的α-葡萄糖苷酶抑制活性中有一定的作用。进一步研究中性蛋白酶酶解对HIOP组分及分子量大小的影响,结果见图2,从图2中可以看出,实验组与未经酶解处理后的空白组相比,峰值的保留时间并没有发生改变。说明中性蛋白酶酶解处理对HIOP的分子量大小及组成并没有产生影响,因此推测中性蛋白酶处理可能只是对HIOP的生物活性中心的结构产生了影响。
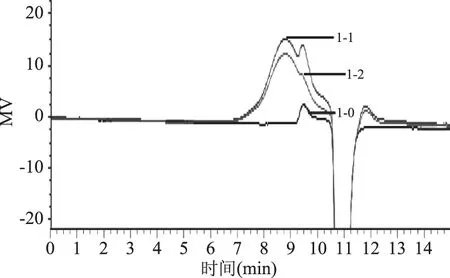
图2 中性蛋白酶酶解对HIOP物质的影响Fig.2 The effect of neutral protease on composition of HIOP 注:1-0为对照组;1-1为实验组; 1-2为空白组;图4、图6、图8同。
2.2 碱性蛋白酶酶解对HIOP的α-葡萄糖苷酶抑制活性及组分的影响
从图3可以看出,经碱性蛋白酶酶解处理后的HIOP的α-葡萄糖苷酶抑制活性出现了少量下降,碱性蛋白酶酶浓度为500~1000 U/mL时,酶解后的HIOP的α-葡萄糖苷酶抑制率从未经酶解前的83.72%降至65%左右。而在酶浓度为(1500~2500 U/mL)时,发现经酶解后的HIOP的α-葡萄糖苷酶抑制率出现小幅度回升现象,但抑制率仍明显低于未经酶解处理的HIOP。推测可能是大量酶液的添加使得反应体系中产生了颜色叠加现象,从而影响了实验结果的测定,使得测定的HIOP的α-葡萄糖苷酶抑制率出现回升现象。

图3 碱性蛋白酶酶解对HIOP的 α-葡萄糖苷酶抑制活性的影响Fig.3 Effect of alkaline protease hydrolysis on α-glucosidase inhibitory rate of HIOP
碱性蛋白酶是经细菌原生质体诱变方法培育的2709枯草杆微生物通过深层发酵、提取及精制而成的一种蛋白水解酶,是一种内切酶。在40~55 ℃、pH9~11碱性条件下能水解蛋白质分子肽链生成多肽或氨基酸,具有较强的分解蛋白质的能力[26]。从图3中可以看出,碱性蛋白酶酶解处理后,HIOP的α-葡萄糖苷酶抑制率下降,推测可能是碱性蛋白酶水解了HIOP中的结合蛋白,从而使其α-葡萄糖苷酶抑制率降低,说明HIOP中的结合蛋白在HIOP的α-葡萄糖苷酶抑制活性中有一定的作用。进一步研究碱性蛋白酶酶解对HIOP组分及分子量大小的影响,结果见图4,从图4中可以看出,实验组与未经酶解处理的HIOP相比,峰值的保留时间没有发生改变。说明蛋白酶酶解处理对HIOP的分子量大小及组成并没有产生影响,碱性蛋白酶处理可能只是对HIOP的生物活性中心结构产生了影响。

图4 碱性蛋白酶酶解对HIOP物质的影响Fig.4 The effect of alkaline protease on composition of HIOP
2.3 胃蛋白酶酶解对HIOP的α-葡萄糖苷酶抑制活性及组分的影响
由图5可以看出,与未经酶解前的抑制率83.72%的 HIOP相比,胃蛋白酶酶解所得HIOP的α-葡萄糖苷酶抑制率显著降低。在蛋白酶酶浓度为500 U/mL时,α-葡萄糖苷酶抑制率仅为6.59%。酶浓度为1000 U/mL时,酶解处理后的HIOP的α-葡萄糖苷酶抑制率为6.30%。说明小剂量酶的添加显著降低了HIOP的α-葡萄糖苷酶抑制率,而随着酶添加量的增加,α-葡萄糖苷酶抑制率略微回升,可能是由于酶添加量的增加改变了α-葡萄糖苷酶酶解体系的环境,因此低剂量胃蛋白酶(500~1000 U/mL)的酶解结果更显著代表酶解效果。

图5 胃蛋白酶酶解对HIOP的α-葡萄糖苷酶抑制活性的影响Fig.5 Effect of pepsin hydrolysis on α-glucosidase inhibitory rate of HIOP
胃蛋白酶是一种消化性蛋白酶,由胃部中的胃粘膜主细胞所分泌,功能是将食物中的蛋白质分解为小的肽片段,它作用的主要部位是芳香族氨基酸或酸性氨基酸的氨基所组成的肽键[27]。从图5可以看出,蛋白酶酶解使HIOP的α-葡萄糖苷酶抑制率显著降低。推测可能是,蛋白酶水解了HIOP中结合蛋白里的芳香族氨基酸或酸性氨基酸的氨基所组成的肽键,从而使其α-葡萄糖苷酶抑制活性出现大幅度的下降,说明HIOP中的结合蛋白在HIOP的α-葡萄糖苷酶抑制活性中有一定的作用,且结合蛋白中有芳香族氨基酸或酸性氨基酸。进一步研究胃蛋白酶酶解对HIOP组分及分子量大小的影响,结果如图6所示,从图6中可以看出,实验组与未经酶解处理的HIOP相比,峰值的保留时间没有发生改变。说明蛋白酶酶解处理对HIOP的分子量大小及组成并没有产生影响,胃蛋白酶处理可能只是对HIOP的活性结构产生了影响。

图6 胃蛋白酶酶解对HIOP物质的影响Fig.6 The effect of pepsin on composition of HIOP
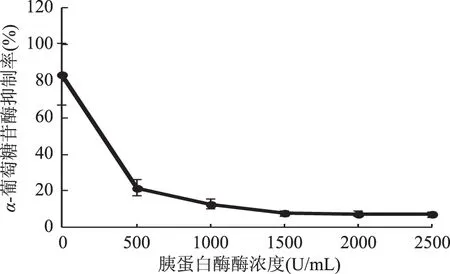
图7 胰蛋白酶酶解对HIOP的α-葡萄糖苷酶抑制活性的影响Fig.7 Effect of trypsin hydrolysis on α-glucosidase inhibitory rate of HIOP
2.4 胰蛋白酶酶解对HIOP的α-葡萄糖苷酶抑制活性及组分的影响
由图7可以看出,胰蛋白酶酶解处理后,HIOP的α-葡萄糖苷酶抑制率显著降低。其中在胰蛋白酶酶浓度仅为500 U/mL时,HIOP的α-葡萄糖苷酶抑制率降从未经酶解前的83.72%降至21.68%。并且,随着酶活的增加,HIOP的α-葡萄糖苷酶抑制率仍然不断降低,并在1500 U/mL及以上时,HIOP的α-葡萄糖苷酶抑制率变化不明显。
胰蛋白酶是特异性最强的蛋白酶,能选择性地水解蛋白质中由赖氨酸或精氨酸的羧基所构成的肽链,属于是肽链内切酶[28]。如图7所示,胰蛋白酶酶解处理后,HIOP的α-葡萄糖苷酶抑制率显著降低。推测可能是,胰蛋白酶水解了HIOP中结合蛋白里由赖氨酸或精氨酸的羧基所构成的肽链,从而使其α-葡萄糖苷酶抑制活性出现大幅度的下降,说明HIOP中的结合蛋白在HIOP的α-葡萄糖苷酶抑制活性中有一定的作用,且结合蛋白中有赖氨酸或精氨酸。进一步研究胰蛋白酶酶解对HIOP组分及分子量大小的影响,结果如图8所示,从图8中可以看出,实验组与未经酶解处理的HIOP相比,峰值的保留时间没有发生改变。说明蛋白酶酶解处理对HIOP的分子量大小及组成并没有产生影响,胰蛋白酶处理可能只是对HIOP的活性结构产生了影响。

图8 胰蛋白酶酶解对HIOP物质的影响Fig.8 The effect of trypsin on composition of HIOP
3 结论
HIOP中结合蛋白在HIOP的α-葡萄糖苷酶抑制活性中是有一定的作用。结合四种蛋白酶的作用效果与作用键型推测,HIOP中的结合蛋白可能含有芳香族氨基酸、酸性氨基酸、赖氨酸或精氨酸,破坏此类肽键,α-葡萄糖苷酶抑制活性明显降低。四种蛋白酶酶解均未使HIOP分子量发生较大改变,说明四种蛋白酶仅影响了HIOP与α-葡萄糖苷酶活性中心结合的部位。本文通过对多糖HIOP的结构的初步研究,为后期研究多糖分子的结构、结构修饰等提供了一定理论基础。
[1]殷建华,李晋川,曹康,等. 天然产物降血糖活性成分研究进展[J]. 成都医学院学报,2007,2(2):154-155.
[2]Ribnicky D M,Poulev A,Watford M,et al. Antihyperglycemic activity of TarralinTM,an ethanolic extract ofArtemisiadracunculusL.[J]. Phytomedicine International Journal of Phytotherapy & Phytopharmacology,2006,13(8):550-557.
[3]Ademiluyi A O,Oboh G. Soybean phenolic-rich extracts inhibit key-enzymes linked to type 2 diabetes(α-amylase andα-glucosidase)and hypertension(angiotensin I converting enzyme)invitro[J]. Experimental & Toxicologic Pathology Official Journal of the Gesellschaft Fur Toxikologische Pathologie,2011,65(3):305-309.
[4]于彩云,高兆兰,陈天姿,等. 天然产物中α-葡萄糖苷酶抑制剂的研究进展[J]. 食品工业科技,2015,36(22):42-43.
[5]王桂霞. 米格列醇与阿卡波糖治疗2型糖尿病的临床疗效及不良反应比较[J]. 中国医药指南,2014(27):41-42.
[6]李朝晖,马晓鹂,吴万征. 枸杞多糖降血糖作用的细胞实验研究[J]. 中药材,2012,35(1):124-127.
[7]张钟,吴文婷,王萍,等. 荔枝水溶性多糖作为α-葡萄糖苷酶抑制剂的活性测定[J]. 食品科学,2013,34(13):175-179.
[8]陈义勇,黄友如,刘晶晶,等. 桦褐孔菌多糖IOP3a体内抗肿瘤活性及其机制[J]. 食品与生物技术学报,2013,32(9):983-988.
[9]Zhao F,Mai Q,Ma J,et al. Triterpenoids from Inonotus obliquus,and their antitumor activities[J]. Fitoterapia,2014(101):34-40.
[10]Chen Y,Gu X,Huang S Q,et al. Optimization of ultrasonic/microwave assisted extraction(UMAE)of polysaccharides from Inonotus obliquus,and evaluation of its anti-tumor activities[J]. International Journal of Biological Macromolecules,2010,46(4):429-435.
[11]Huang S Q,Ding S,Fan L. Antioxidant activities of five polysaccharides from Inonotus obliquus[J]. International Journal of Biological Macromolecules,2012,50(5):1183-1187.
[12]Du X J,Mu H M,Zhou S,et al. Chemical analysis and
antioxidant activity of polysaccharides extracted from Inonotus obliquus sclerotia[J]. International Journal of Biological Macromolecules,2013,62(11):691-696.
[13]高愿军,张家泉,王娟娟,等. 桦褐孔菌多糖口服液降血糖作用研究[J]. 食品科技,2010(7):93-95.
[14]黄年来. 俄罗斯神秘的民间药用真菌--桦褐孔菌[J]. 中国食用菌,2002,21(4):7-8.
[15]Byung-keun Yang,Kai-Yip Cho,Michael A Wilson,et al. Effect of Inonotus obliquus mcelia on the level of plasma glucose and lipides in streptozotocin-indused diabetic rats[J]. The Korean Journal of Mycology,2005,33(2):64-68.
[16]Jae-Young Cha,Bang-Sil Jun,Chi-Hyeoung Lee,et al. Hypoglycemic and antioxidative effect of fermented chaga mushroom(Inonotusobliquus)on streptozotocin-induced diabetic rats[J].Journal of Life Science,2005,15(5):809-818.
[17]Yoo Kyoung Park,Jung Shin Kim,Eun Jae Jeon,et al. The improvement of Chaga mushroom(Inonotusobliquus)extract supplementation on the blood glucose and cellular DNA damage in streptozotocin-induced diabetic rats[J]. Korean Journal of Nutrition,2009,42(1):5-13
[18]孟思彤,徐艳芝,王振月. 多糖的化学修饰对其生物活性影响研究进展[J]. 天然产物研究与开发,2014(11):1901-1905.
[19]陈小红,马芳,严云斌,等. 茯苓多糖的结构改性及抗氧化活性研究[J]. 湖北农业科学,2015,54(18):4563-4566.
[20]卢可可,张月巧,袁娅,等. 硫酸化修饰多糖抗肿瘤活性构效关系及分子机制研究进展[J]. 食品科学,2014,35(23):297-302.
[21]何华. 生物药物分析[M]. 北京:化学工业出版社,2014.
[22]陈义勇. 桦褐孔菌多糖纯化、结构及其抗肿瘤机制研究[D].无锡:江南大学,2010.
[23]金鑫,赖凤英,JinXin,等. 仙人掌多糖的提取、分离纯化及GPC法测定其分子量[J]. 现代食品科技,2006,22(2):138-140.
[24]Kim J S,Hyun T K,Kim M J. The inhibitory effects of ethanol extracts from sorghum,foxtail millet and proso millet onα-glucosidase andα-amylase activities[J]. Food Chemistry,2011,124(4):1647-1651.
[25]Cremonesi F,Torti E,Pecile A,et al. Evaluation ofα-Glucosidase Activity in Dog Semen and its Use in Fertility Diagnosis[J]. Veterinary Research Communications,2003,27 Suppl 1(1):587-589.
[26]姚刚,程建军,孙鹏,等. 枯草芽孢杆菌发酵产碱性蛋白酶的研究[J]. 食品科学,2009,30(23):347-351.
[27]王萍,吴燕燕,李来好,等. 虾类胰蛋白酶的研究进展[J].生物技术通报,2011(2):42-47.
[28]刘宇,董平,梁兴国. 胃蛋白酶的分离现状及其活性研究进展[J]. 生物学杂志,2016,33(3):75-79.
Effects of four kinds of proteases onα-glucosidase inhibitory activity of polysaccharide fromInonotusobliquus
TONG Shi-sheng1,HU Jin-rong2,ZHANG Jing-sheng2,DONG Wen-xia2,WANG Li2,LIU Ping2,*
(1.Bio-pharmaceutical College,Beijing City University,Beijing 100094,China; 2.College of Food Science and Nutritional Engineering,China Agricultural University,Beijing 100083,China)
The relationship betweenα-glucosidase inhibitory activity and the composition bond type of binding protein of high temperature water-extracted polysaccharides(HIOP)that extracted fromInonotusobliquuswas studied. HIOP was enzymatically digested with four different proteases,and the effect of protease hydrolysis on its molecular weight composition andα-glucosidase inhibitory activity was determined. The inhibitory rate ofα-glucosidase by original HIOP was 83.72% at 10 μg/mL,while the lowestα-glucosidase inhibition rate of HIOP that hydrolyzed by neutral protease,alkaline protease,pepsin,and trypsin were 53%,65%,6.5% and 7.1%,respectively. The binding protein in HIOP had a role in theα-glucosidase inhibitory activity of HIOP. In addition,in consideration of the effects of these four kinds of enzymes,it could be speculated that the active sites of the binding proteins in HIOP contain aromatic amino acids,acidic amino acids,lysine or arginine. If we destroy such peptide bonds,theα-glucosidase inhibitory activity of HIOP could be significantly reduced. But,the four proteases did not change the molecular weight of HIOP,indicating that the four proteases only affected the binding site of HIOP toα-glucosidase activity center.
the polysaccharide ofInonotusobliquus;proteases;α-glucosidase activity
2016-11-28
佟世生(1970-),男,博士,研究方向:天然产物的开发与利用,E-mail:shishengt@163.com。
*通讯作者:刘萍(1970-),女,博士,研究方向:多糖结构与功能,E-mail:liuping@cau.edu.cn。
国家自然基金项目(21576282)。
TS201.2
A
1002-0306(2017)14-0162-05
10.13386/j.issn1002-0306.2017.14.032
