双膦酸盐的今昔与思考
2017-08-06张萌萌
张萌萌
《中国骨质疏松杂志》社,北京 100102
双膦酸盐(bisphosphonates,BPs)又称偕二膦酸盐,是近30年来发展起来的抗代谢性骨病的一类新药,能特异地与骨质中的羟基磷灰石结合,浓集于骨骼,并在骨表面保留长达数月至数年,在破骨细胞进行骨吸收活动时被其摄取,抑制破骨细胞活性[1],从而抑制骨吸收,增加骨密度。
双膦酸盐类药物是临床应用较多、最有发展前景的骨吸收抑制剂,用于治疗各类骨疾患及钙代谢性疾病,如原发性骨质疏松、继发性骨质疏松、变形性骨炎、恶性肿瘤骨转移引起的高钙血症和骨痛症等。由于双膦酸盐高效的抑制骨吸收作用,目前已成为国际上各国指南认可的治疗骨质疏松症的一线药物。
1 双膦酸盐的发展历史
20世纪60年代初,Fleisch等发现血浆及尿液中存在抑制异位钙化作用的焦磷酸盐,它可能是钙化生理调节因子,但焦磷酸盐口服无效,注射给药又迅速被焦磷酸酯酶水解失活,达不到治疗效果。后来研究发现,以P-C-P基团取代焦磷酸盐结构中的P-O-P基团可改变焦磷酸盐的理化性质,有效抵制体内水解酶的生物降解作用,改变其生物学性质及毒理作用,保持一定的稳定性,随后合成了一系列双膦酸盐类化合物。
1968年人类报道了第一个双膦酸盐,1977年,第一代的依替膦酸钠(Etidronate),由美国宝洁(Proter & Gamble,P&G)公司开发上市,作为骨代谢调节剂用于治疗骨质疏松症、恶性肿瘤、高钙血症和Paget’s病等,依替膦酸钠对体内磷酸钙有较强的亲和力,能抑制人体异常钙化和过量骨吸收,减轻骨痛;降低血清碱性磷酸酶和尿羟脯氨酸的浓度。但依替膦酸钠抑制骨吸收作用较弱,使用时要求剂量较高,接近其抑制骨正常矿化的剂量,长期使用可导致骨软化。1986年,氯屈膦酸钠(Clodronate)上市,其抗骨质吸收作用强度是依替膦酸钠的10倍,而抑制骨矿化作用减小,克服了依替膦酸钠的缺点,成为使用最广泛的第一代双膦酸盐类药物。
1998年,瑞士诺华、中国深圳海王公司分别研发了第二代双膦酸盐——帕米膦酸钠(Pamidronate),在碳原子1号位上加上羟基(R),并在侧链(R′)上引入氨基,即含氮双膦酸盐,这样的结构增加了双膦酸盐的活性,其抗骨质吸收的作用明显优于第一代双膦酸盐,比依替膦酸钠抗骨质吸收作用强100倍,适用于恶性肿瘤并发的高钙血症和溶骨性癌转移引起的骨痛。
随后美国的研究发现,双膦酸盐的抗骨质吸收能力随其侧链的延长而增加,进一步延长帕米膦酸钠的侧链,形成一个以4个碳原子为骨架的侧链结构,成为活性最强的第二代双膦酸盐——阿仑膦酸钠(Alendronate)[2],其抗骨质吸收能力是依替膦酸的1000倍,适用于成人骨质疏松的治疗,以预防髋部和椎体骨折。
阿根廷Gador公司的研究者将帕米膦酸氨基上的氮二甲基化后,形成了奥帕膦酸钠(Olpadronate),活性得到进一步提高,抗骨质吸收能力是帕米膦酸的7倍,用于防治骨质疏松,治疗Paget’s病和恶性肿瘤引起的高钙血症。
德国Boehringer Mannheim公司在奥帕膦酸钠的氮原子上引入一个饱和羟链,形成了活性更强的第三代双膦酸盐——伊班膦酸钠(Ibandronate),并于1996年在德国首次上市,用于治疗恶性肿瘤所致的高钙血症及多发性骨髓瘤和实体瘤的骨转移等,并可预防和治疗骨质疏松症,是目前适应证最广的双膦酸盐药物[3],其特点是高效、作用时间长、低毒、使用方便、可以长间歇给药等。
由美国宝洁(Procter & Gamble,P&G)公司与Hoechst Marion Roussrl公司研发,在双膦酸盐的侧链上引入环状结构,合成吡啶双膦酸盐——利塞膦酸钠(Risedronate),并于1998年首次在美国上市,其抗骨吸收作用更强,毒副作用小,具有很好的临床应用前景,临床上用于治疗不同程度的Paget’s骨病(变形性骨炎),2004年又获美国食品药品监督管理局(Food and Drug Administration,FDA)认可,用于预防和治疗绝经后骨质疏松症与糖皮质类固醇性骨质疏松的防治[4-5]。
随后,瑞士诺华(Novatris)公司研制开发了抗骨质吸收作用更强、抑制骨矿化作用更小的药物——唑来膦酸钠(Zoledronate),属于含有咪唑环的第三代双膦酸盐,并于2000年首次在加拿大上市,目前已在欧盟、美国等80多个国家和地区广泛使用。可用于控制恶性肿瘤骨转移[6]、治疗绝经后骨质疏松症、恶性高钙血症等。
2 第一代、第二代、第三代双膦酸盐的化学结构
双膦酸盐类药物抗骨吸收作用的主要机制为:(1)直接改变破骨细胞的形态学特征,阻止成熟破骨细胞在骨表面形成一个浓度梯度,从而抑制破骨细胞功能;(2)与骨质中的羟磷灰石结合,直接干扰骨吸收;(3)抑制破骨细胞前体向骨骼表面游走和聚集,抑制其向多核细胞分化;(4)直接抑制成骨细胞介导的细胞因子,如白介素6(IL-6)、肿瘤坏死因子(TNF)的产生,间接抑制细胞因子对破骨细胞的激活;(5)诱导破骨细胞凋亡,缩短破骨细胞生存期。
其中,双膦酸盐分子中P-C-P基本结构是其产生抑制骨吸收活性的必要条件。双膦酸盐分子中磷酸根上的氧原子能与钙离子螯合,形成二配位体而发挥抑制骨吸收活性[7],并有助于药物向细胞内转运。双膦酸盐类药物化学结构式见图1。
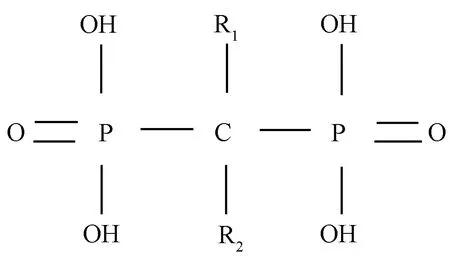
图1 双膦酸盐类药物化学结构式Fig.1 The chemical structural formula of bisphosphonates
双膦酸盐类药物的药效强度取决于各药的碳原子上取代侧链的类型,即C原子上的R1和R2侧链取代基。R1侧链取代基主要参与双膦酸盐与骨基质中的羟基磷灰石的结合[8],决定了双膦酸盐分子在体内能否迅速而选择性地结合到骨基质表面。R2侧链取代基对双膦酸盐类药物抗骨质吸收的强度起着重要作用[9]。R2取代基侧链的长短对双膦酸盐的活性起决定性作用,适宜的碳链长度可提高药物的稳定性和生物利用度,但也不能无限地延长,当延长至一定程度,反而会减弱双膦酸盐的强度;侧链中若含有氮原子,可显著增加双膦酸盐药物活性。
目前根据双膦酸盐类药物结构特点,可以将其划分为三代产品。
2.1 第一代:不含氮双膦酸盐
2.1.1依替膦酸钠(Etidronate):化学名:(1-羟基亚乙基)二膦酸二钠盐;分子式:C2H6Na2O7P2。
2.1.2氯屈膦酸钠(Clodronate):化学名:二氯亚甲基二磷酸二钠;分子式:CH2Cl2Na2O6P2。
2.1.3替鲁膦酸钠(Tiludronate):化学名:(4-氯苯硫基)甲叉二膦酸;分子式:C7H9ClO6P2S。
2.2 第二代:含氮双膦酸盐
第二代双膦酸盐以侧链含氨基为主要特点,抗骨质吸收的作用明显优于第一代双膦酸盐。如帕米膦酸钠和阿仑膦酸钠分别比第一代的依替膦酸钠强100倍和1000倍。
2.2.1帕米膦酸钠(Pamidronate):化学名称:3-氨基-1-羟基亚丙基-1,1-二膦酸二钠五水合物;分子式:C3H9NNa2O7P2·5H2O。
2.2.2阿仑膦酸钠(Alendronate):化学名称:(4-氨基-1-羟基亚丁基)二膦酸单钠盐三水合物;分子式:C4H12NNaO7P2·3H2O。其化学结构式见图2。
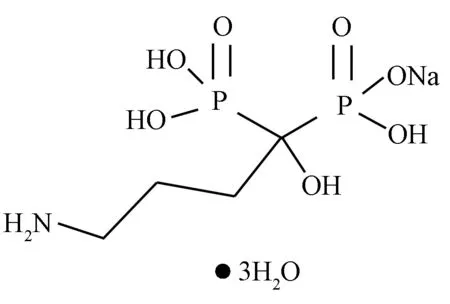
图2 阿仑膦酸钠(第二代双膦酸盐)化学结构式Fig.2 The chemical structural formula of Alendronate (The second generation bisphosphonate)
2.3 第三代:具有杂环结构的含氮双膦酸盐
第三代双膦酸盐药物的结构特点为在保留氨基中氮原子的基础上,进一步延长侧链长度或引入环状结构,其抗骨吸收作用更强。如R1上的H原子被吡啶甲基取代使抗骨吸收作用提高,利塞膦酸钠的强度为依替膦酸钠的5000倍;如R1侧链的N原子上加入甲基和戊基得到的伊班膦酸钠,其活性比依替膦酸钠强10000倍。含有双氮杂环的唑来膦酸其抑制骨吸收作用是阿仑膦酸钠的25~114倍、帕米膦酸的100~850倍,具有更强的抗骨质疏松治疗作用。
2.3.1伊班膦酸钠(Ibandronate):化学名称:1-羟基-3-(甲基戊基胺)-丙烷-1,1-双膦酸钠;分子式:C9H22NO7P2NaH2O。
2.3.2利塞膦酸钠(Risedronate):化学名称:2-(3-吡啶基)-1-羟基乙烷-1,1-双膦酸单钠盐;分子式:C7H10NNaO7P2·2.5H2O。
2.3.3唑来膦酸钠(Zoledronate):化学名称:1-羟基-2-(1-咪唑基)-亚乙基-1,1-二磷酸一水化物;分子式:C5H10N2O7P2·H2O。其化学结构式见图3。

图3 唑来膦酸(第三代双膦酸盐)化学结构式Fig.3 The chemical structural formula of Zoledronate (The third generation bisphosphonate)
第三代双膦酸盐抗骨吸收作用强、临床应用安全方便、副作用小,具有广阔的发展前景。唑来膦酸钠是第三代双膦酸盐的代表。
3 第三代双膦酸盐抗骨吸收研究作用
在骨质疏松规范治疗中,第三代双膦酸盐类药物因其具有强大的抗骨质吸收作用,临床应用越来越广泛。目前,其代表药物唑来膦酸(Zoledronate)是抗骨质疏松药理活性最强的药物,已在包括美国和欧盟在内的80多个国家和地区获准治疗绝经后骨质疏松。2009年,唑来膦酸获得中国国家食品药品监督管理总局的新药批准,用于治疗绝经后骨质疏松症[10]。2012年法国国家卫生管理局制定的药物治疗骨质疏松症指南中将唑来膦酸盐作为治疗骨质疏松的首选药物[11]。
唑来膦酸对骨表面某些结构有高亲和力,吸收后可以在骨小梁表面聚集,通过甲羟戊酸通路与骨矿盐的羟基磷灰石结合,抑制甲羟戊酸代谢的关键酶——法尼基焦磷酸合成酶(Farnesylpyrophosphate,FPP),使甲羟戊酸途径不能合成FPP和双香叶基焦磷酸(Pyrophosphate,GGPP),抑制破骨细胞结构蛋白的合成,使破骨细胞丧失骨吸收能力,并加速破骨细胞凋亡,从而抑制破骨细胞介导的骨吸收过程;同时可激活被抑制的成骨细胞,促进骨重建,增加骨密度。
国内外许多医学机构对其药理作用、药代动力学特征、临床疗效等进行了大量的动物实验及临床试验研究。
Shane等[12]对72只大鼠模拟失重的实验显示,唑来膦酸钠能维持骨小梁的微结构、抑制破骨细胞功能、增加骨密度(bone mineral density,BMD)。
柳维等[13]探索唑来膦酸对骨质疏松性大鼠股骨干骺端骨缺损修复的影响,结果显示,唑来膦酸注射组大鼠模型股骨骨密度增加较快,缺损区新骨生成明显,破骨细胞活性降低、数量减少,说明唑来膦酸可较好地促进骨质疏松性大鼠股骨干骺端骨缺损的修复。
Rogers等[14]研究显示,唑来膦酸抑制破骨细胞内作用于甲羟戊酸通路的关键酶,使小G蛋白异戊二烯化过程受到抑制,小G蛋白对维持破骨细胞的功能至关重要,从而抑制破骨细胞的增殖、分化。
王雪鹏等[15]观察唑来膦酸对骨质疏松性骨折大鼠模型局部骨痂力学强度的影响,发现唑来膦酸可增强骨质疏松性骨折断端的骨痂结构力学强度,这与唑来膦酸抑制骨吸收、提高骨痂内部骨小梁数量、维持大量编织骨有关。而延迟注射唑来膦酸抑制骨折后期骨痂重建,虽然不会损害编织骨数量,但可能会损害骨痂内部骨小梁力学强度和连接数目。
Wedemeyer等[16]的动物实验研究显示,唑来膦酸能有效抑制骨吸收并刺激骨痂形成,保留骨小梁数量,增加骨骼生物力学强度。
陈越等[17]研究唑来膦酸对去势大鼠骨质疏松性骨折愈合过程中转化生长因子(TGF-β)表达的影响,结果显示,唑来膦酸能加快骨痂形成,促进成骨细胞转化生长因子β的表达,促进骨质疏松性骨折的愈合。
Black等[18]对唑来膦酸治疗绝经后骨质疏松及骨折愈合的临床研究显示,唑来膦酸是治疗绝经后骨质疏松的有效手段。
Reid等[19]对美国、澳大利亚、中国香港、以色列和 12个欧洲国家的833例糖皮质激素继发骨质疏松患者的临床试验表明,唑来膦酸治疗组患者腰椎骨密度、股骨颈骨密度、全髋骨密度均高于利塞膦酸治疗组,唑来膦酸治疗组患者血清骨代谢标记物(Ⅰ型胶原羧基末端肽CTX,Ⅰ型前胶原氨基末端肽PINP)水平于用药9~11 d后即显著下降。唑来膦酸在预防和治疗糖皮质激素继发骨质疏松方面效果明显。
陈根强等[20]对120例糖皮质激素继发的骨质疏松患者随机双盲试验的研究显示,唑来膦酸静脉滴注能够显著增加患者腰椎、股骨颈骨密度,降低血清骨吸收标志物I型胶原羧基末端肽(β-CTX)及骨形成标志物I型前胶原氨基末端肽(PINP)水平,疗效优于利塞膦酸治疗组。
Eastell等[21]的一项对唑来膦酸一年一次治疗骨质疏松的回顾性研究认为,唑来膦酸能降低约40%的髋部骨折风险。
高雷等[22]研究双膦酸盐对绝经后骨质疏松患者骨量的影响,结果显示,唑来膦酸联合钙剂治疗绝经后骨质疏松,能显著改善患者的疼痛症状,提高患者全髋骨密度,增加骨量,降低骨质疏松性骨折的发生率,是治疗绝经后骨质疏松安全有效的方法。
Jacques等[23]研究表明,对绝经后骨质疏松患者每年给予5 mg唑来膦酸1次,患者髋部骨密度、椎体骨密度均有明显提高,骨折发生率降低。
美国骨与骨矿研究协会的一项研究报告显示,唑来膦酸每年给药1次,连续给药3年,能降低70%的脊柱骨折、40%的髋部骨折,骨折总发生率减少24%。
4 正确使用双膦酸盐
国内外的众多临床研究及临床实践都显示,第三代双膦酸盐能够明显提高骨密度、降低椎体和髋部骨折发生的危险性。
美国加利福尼亚大学Black教授等[24]对3889例绝经后骨质疏松患者给予唑来膦酸治疗3年后发现,唑来膦酸治疗组较安慰剂组椎体骨折风险减少70%,髋部骨折的风险减少41%,可显著降低骨质疏松性骨折的发生率。
南京大学医学院附属鼓楼医院林华教授等[25]对收治的89例绝经后骨质疏松患者,给予唑来膦酸治疗后1年发现,原发性骨质疏松组腰椎骨密度增加5.8%,股骨颈骨密度增加2.9%,而继发性骨质疏松组腰椎骨密度增加3.4%,股骨颈骨密度增加2.1%。
美国克瑞顿大学医学院Recker教授等[26]对7736名绝经后骨质疏松患者给予唑来膦酸治疗,结果显示,第1年患者椎体骨折风险降低60%,第2年与第3年分别降低71%和70%,三年内疗效逐渐增加,骨密度增加6%左右。
吉林大学第四医院骨质疏松诊疗中心对长春地区257例绝经后骨质疏松症患者,给予静脉滴注唑来膦酸5 mg注射液,患者腰椎1-4、股骨颈骨密度在滴注唑来膦酸1、2、3年后均较治疗前有明显提高,并且无严重不良反应发生,唑来膦酸治疗绝经后骨质疏松症安全有效[27]。
美国杜克大学医学中心对2127例患者多中心随机双盲安慰剂对照研究显示,唑来膦酸 5 mg治疗组骨折发生率为8.6%,较安慰剂组(13.9%)显著下降,骨折风险明显下降。唑来膦酸治疗组全髋骨密度、股骨颈骨密度较对照组显著提高[28]。
翟明玉等[29]对临床收治的120例老年严重骨质疏松症患者的临床研究显示,治疗组(给予钙尔奇+阿法骨化醇+唑来膦酸钠治疗)骨密度改善程度及骨痛缓解程度明显优于对照组(给予钙尔奇+阿法骨化醇治疗),治疗组血清碱性磷酸酶(ALP)水平较治疗前明显下降。提示唑来膦酸能显著缓解严重老年性骨质疏松症患者的骨痛症状,提高患者的BMD水平。
樊勤学等[30]对新疆53例原发性骨质疏松症患者的临床观察显示,5 mg唑来膦酸治疗组患者腰椎、股骨颈骨密度均显著提高。
Black等一项关于唑来膦酸的长达9年的研究显示[31],5 mg唑来膦酸每年使用一次,连续使用6年,可提高骨质疏松患者髋部骨密度,骨密度值随着用药时间的延长而增加,峰值则出现在第4~5年内;改善血清骨转换指标水平;降低骨质疏松性骨折发生率。部分患者持续使用3年,在第9年检测髋部骨密度、血清骨转换指标水平及骨折发生率,结果与第6年之后停药的患者并无显著差异。表明几乎所有接受6年连续唑来膦酸注射的患者可以停药长达3年,患者骨密度仍维持较好水平。
第三代双膦酸盐治疗骨质疏松效果显著,具有良好的安全性和耐受性,但有时仍有不良反应发生。最常出现的是流感样症状(约9%),包括发热(7.2%)、疲乏(4.1%)、寒战(2.8%)、骨痛(9.1%)、关节痛和肌痛(约3%)等。其发生不良反应的主要机制[32]是:唑来膦酸抑制甲醛戊酸(HMG-CoA)途径,导致香叶焦磷酸(isopentenyl pyrophosphate,IPP)增多。IPP与γδT 细胞表面受体结合,促进γδT细胞活化增殖,释放γ干扰素(INF-γ)、肿瘤坏死因子-α(TNF-α),促进白细胞介素-6(IL-6)的释放,从而导致患者发热。
为加强临床用药的安全性,减少不良反应的发生,临床应注意正确合理使用第三代双膦酸盐——唑来膦酸。
首先,在注射前需要给患者检测以下项目:血常规、尿常规、生化二、肝功一、血脂、感染性标志物、骨钙素、降钙素、甲状旁腺素、1,25-二羟基维生素D3、风湿三项、肿瘤8项、常规心电图检查、骨密度测定、DR-胸腹:胸部、DR-下肢:膝关节、彩超:肝胆胰脾。
计算肌酐清除率,肌酐清除率大于35 ml/min,方可用药。
其次,用药情况。(1)如果血钙低于2.5 mmol/L,可静点0.9%氯化钠注射液100 ml,葡萄糖酸钙注射液2 g(根据情况1~2 d);如果血钙高于2.5 mmol/L,无需静点。(2)应用唑来前一天晚上开始服用布洛芬缓释胶囊,每日两次,每次300 mg(连续口服3 d)。(3)应用唑来膦酸当天,分三步静点:①葡萄糖氯化钠注射液500 ml,静点;②唑来膦酸注射液5 mg(100 ml),30 min点完(绝对不能少于15min),最好用输液泵控制;③葡萄糖氯化钠注射液500 ml,静点。
第三,入院日起常规口服罗盖全、钙尔奇D。罗盖全,0.25 ug,每日一次,饭后口服;钙尔奇D,0.6 g/d,每晚睡前口服。
第四,静点唑来膦酸之后可能会引起发热、骨痛的处置。(1)大量饮水;(2)解热镇痛药:注射用赖氨匹林,每次0.9 g(100 ml)。
第三代双膦酸盐给药方便、提高了患者对治疗的依从性,在临床应用实践中应规范用药,减少副作用的发生,提高患者对治疗的依从性,达到增加骨密度、降低骨折风险的目的,才有更好的前景。
双膦酸盐从发现到应用于临床,经历了漫长的时间,对其结构、活性、作用机制的研究引领骨质疏松领域治疗理念的不断更新,为不同种类双膦酸盐作用于破骨细胞、成骨细胞、骨重建局部调节因子的分子机制和临床特征,提供了有力的循证医学证据。
