基于指纹图谱评价麻黄汤中药物的成分分析研究
2017-07-31余新华邵永生韩春生胡永固姚连清
余新华 周 虹 邵永生 韩春生 胡永固 姚连清 王 俊 杨 杰
(1 河南省信阳市第三人民医院,信阳,464000; 2 中国人民解放军第154医院,信阳,464000; 3 河南省信阳市中心医院,信阳,464000)
中药研究
基于指纹图谱评价麻黄汤中药物的成分分析研究
余新华1周 虹2邵永生3韩春生1胡永固1姚连清1王 俊1杨 杰1
(1 河南省信阳市第三人民医院,信阳,464000; 2 中国人民解放军第154医院,信阳,464000; 3 河南省信阳市中心医院,信阳,464000)
目的:基于指纹图谱评价麻黄汤中药物的成分分析,阐释中药复方合理配伍的科学内涵。方法:制备混合对照品溶液和麻黄汤水煎液供试品溶液,以流动相为0.1%甲酸-水溶液(A)-0.1%甲酸-乙腈溶液(B);梯度洗脱0~30 min,3%~5% B,30~35 min,55%~95% B,35~40 min,95% B;柱温40 ℃;流速0.5 mL/min;进样量5 μL作为色谱条件进行研究,并根据国家药典委员会提出的中药指纹图谱相似度评价系统2004A进行相似度分析,采用MATLAB软件进行数据处理和统计。结果:1)各色谱峰的相对保留时间和相对峰面积的RSD值均小于5%,表明实验方法学重复性良好。2)8种对照品组成的混合对照品所得指纹图谱无干扰峰,基线稳定;所得实际质荷比和计算质荷比误差小。3)麻黄汤水煎液指纹图谱分离出31个化合物。4)麻黄汤水煎液药物成分分析获得的31种化合物中以第28种2,3,7-三甲基吲哚和第29种乙酸麻黄碱属于麻黄汤水煎液特殊成分,其余29种均可归属于明确药物来源,所有药物的化合物实际质荷比和计算质荷比的误差均在正负100以内,结果为真。结论:麻黄汤水煎液药物成分分析获得的31种化合物中以第28种2,3,7-三甲基吲哚和第29种乙酸麻黄碱属于麻黄汤水煎液特殊成分,其中主要为来源于麻黄的生物碱类成分,来源于桂枝和苦杏仁的有机酸类成分,以及来源于甘草的黄酮类成分。
指纹图谱;麻黄汤;成分分析;研究
中药复方是中医药理论和中医方剂学的精髓,目前中药复方的研究主要集中在“是否有效”以及“疗效机制”方面[1-4],近年来随着研究的深入研究员逐渐向“药效物质基础”方面进行探究,中药复方通过水浸泡、煎煮、熬制,使多种药物成分共同作用,进而综合发挥药理作用治疗疾病,与此同时单一味中药化学成分又是复方发挥药效作用的重要物质基础,为复方中药物的相互作用、相辅相成提供物质基础[5-8]。麻黄汤是《伤寒论》中太阳症发汗解表的经典代表方剂,深受古今中医药学临床医师的推崇,临床主要用于太阳表症,帮助机体发汗解表、兼宣肺平喘[9]。然而目前关于麻黄汤中药物的成分分析较少,由此,本实验借助指纹图谱技术,对麻黄汤全方药物组成成分展开定性研究,初步研究麻黄汤药效物质组成。现将结果报道如下。
1 仪器与试药
1.1 仪器 快速液相(美国Agilent公司提供,型号:1200);电子天平(德国Sartorius公司提供,型号:BP121S);离心机(上海安亭科学仪器厂提供,型号:A316);恒温水浴锅(北京国华医疗器械厂,型号:HW159)。
1.2 试剂 甲醇和乙腈均为色谱纯,均购自Fisher scientific公司,批号分别是LOT:111280和LOT:096328;盐酸麻黄碱、盐酸伪麻黄碱、甘草次酸、桂皮酸对照品均购自于中国食品药品检定研究院,超纯水、甘草酸、苦杏仁苷、毛蕊异黄酮、甘草苷对照品均购自于成都瑞芬思生物科技有限公司。
1.3 分析样品 麻黄汤:麻黄、桂枝、杏仁、甘草药材,以上药材均有河南省信阳市第三人民医院中药房提供。
2 方法与结果
2.1 色谱质谱条件 色谱条件:Agilent SB-C18RRHD(3.0 mm×100 mm,1.8 μm)色谱柱展开研究,流动相为0.1%甲酸-水溶液(A)-0.1%甲酸-乙腈溶液(B);精密量取5 μL进样量,柱温控制在40 ℃,以0.5 mL/min的流速进行梯度洗脱,梯度洗脱条件如下:0~30 min,3%~5% B,30~35 min,55%~95% B,35~40 min,95% B。质谱条件:电喷雾离子源(ESI),干燥气(氮气)流速为6.0 L/min;干燥气温度为250 ℃;正离子模式;毛细管电压、锥孔电压、RF透镜电压分别为4 000 V、-500 V、80.0 V;雾化器压力100 kPa;扫描范围为m/z=50~1 200。
2.2 对照品溶液的制备 取已购的盐酸麻黄碱、盐酸伪麻黄碱、桂皮酸、苦杏仁苷、甘草酸、甘草苷、甘草次酸、毛蕊异黄酮,分别精密称取0.0072 g、0.0145 g、0.0291 g、0.0324 g、0.0366 g、0.0374 g、0.0441 g、0.0491 g于10 mL容量瓶中,并用甲醇定容获得混合对照品母液;再精密移取50 μL混合对照品母液于1 mL容量瓶中,并用甲醇定容获得混合对照品溶液:其中盐酸麻黄碱浓度、盐酸伪麻黄碱浓度、桂皮酸浓度、苦杏仁苷浓度、甘草酸浓度、甘草苷浓度、甘草次酸浓度、毛蕊异黄酮浓度分别的终浓度为36 ng/mL、72.5 ng/mL、145.5 ng/mL,为162 ng/mL、183 ng/mL、187 ng/mL、220.5 ng/mL、245.5 ng/mL。
2.3 供试品溶液的制备 根据《伤寒论》麻黄汤剂量将麻黄、桂枝、苦杏仁和甘草分别浸泡30 min,麻黄先煎20 min,余药尽入同煎30 min,获得第1次水煎液;药渣再加水煎煮30 min,获得第2次水煎液;合并2次麻黄汤水煎液滤液并定容至500 mL。精密量24 mL麻黄汤水煎液,加入120 mL乙酸乙酯(分析纯),将麻黄汤中药物成分脂溶性部位提取出来获得下层麻黄汤水煎液;精密量取0.5 mL下层麻黄汤水煎液,选择甲醇-乙腈(1∶1)混合溶剂2 mL作为提取剂,离心10 min过滤上清液,供试品溶液制备完成,储存待用。
2.4 专属性试验 取同一供试品溶液根据2.3制备的供试品溶液,采用薄层层析的方法对麻黄汤进行专属性试验,结果显示供试品溶液选择水煎剂,以水为溶剂提取麻黄汤水煎液,鉴别结果显示麻黄汤中麻黄、桂枝、杏仁、甘草均水溶性成分为主。
2.5 线性关系考察 精密取2.2制备混合对照品溶液0.1 μL、0.5 μL、1 μL、2 μL、5 μL、10 μL、20 μL,分别编号1~7并连续进样,以峰面积为Y轴,5 μL进样浓度为X轴,绘制标准曲线,并根据对照品的回归方程计算各有效成分在各自浓度范围内的线性关系;结果显示线性关系良好。
2.6 中间精密度试验 取同一供试品溶液根据2.3制备的供试品溶液,依照1.1的色谱条件,连续5次进样,测试HPLC仪器的精密度;结果显示精密度良好。
2.7 供试品溶液稳定性试验 取同一供试品溶液根据2.3制备的供试品溶液,依照1.1的色谱条件,连续5次进样,测试样品的稳定性;结果显示稳定性良好。
2.8 重复性试验 取同一对照品溶液根据2.2制备的混合对照品溶液,依照2.1的色谱质谱条件,连续5次进样,测试指纹图谱方法的重复性。结果表明,各色谱峰的相对保留时间和相对峰面积的RSD值均小于5%,表明实验方法学重复性良好。

表1 大于总峰面积5%的色谱峰相对峰面积精密度结果
2.9 回收率试验 取6份同一供试品溶液根据1.1制备的供试品溶液,编号A-F并分别加入盐酸麻黄碱对照品、桂皮醛对照品、苦杏仁苷对照品、甘草酸对照品,计算各有效成分在HPLC中的加样回收率;结果显示加样回收率试验结果中平均回收率为99.60%,RSD为2.0%,显示加样回收率试验良好。
2.10 样品测定结果
2.10.1 混合对照品溶液药物成分分析 8种对照品组成的混合对照品指纹图谱如图1所示,所得指纹图谱无干扰峰,基线稳定;所得实际质荷比和计算质荷比误差小。见表2。
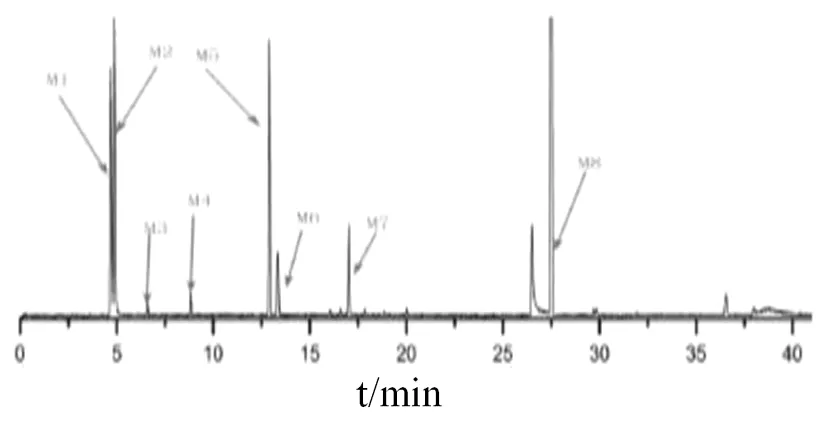
图1 麻黄汤混合对照品溶液指纹图谱
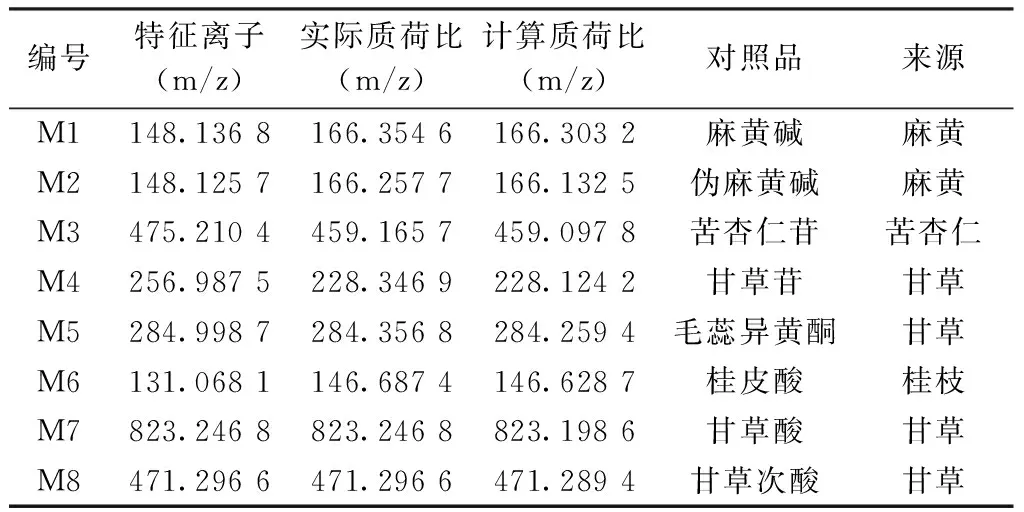
编号特征离子(m/z)实际质荷比(m/z)计算质荷比(m/z)对照品来源M1148.1368166.3546166.3032麻黄碱麻黄M2148.1257166.2577166.1325伪麻黄碱麻黄M3475.2104459.1657459.0978苦杏仁苷苦杏仁M4256.9875228.3469228.1242甘草苷甘草M5284.9987284.3568284.2594毛蕊异黄酮甘草M6131.0681146.6874146.6287桂皮酸桂枝M7823.2468823.2468823.1986甘草酸甘草M8471.2966471.2966471.2894甘草次酸甘草
2.10.2 麻黄汤水煎液色谱图 如图2所示,麻黄汤水煎液指纹图谱分离出31个化合物。
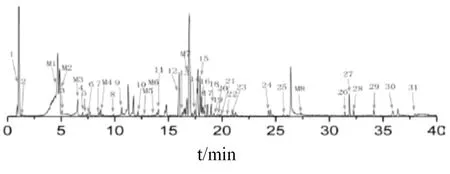
图2 麻黄汤水煎液指纹图谱
2.10.3 麻黄汤水煎液药物成分分析 麻黄汤水煎液药物成分分析获得的31种化合物中以第28种2,3,7-三甲基吲哚和第29种乙酸麻黄碱属于麻黄汤水煎液特殊成分,其余29种均可归属于明确药物来源,所有药物的化合物实际质荷比和计算质荷比的误差均在正负100以内,结果为真。
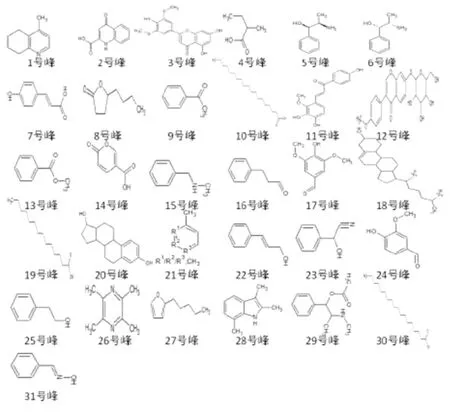
图3 麻黄汤水煎液药物成分化合物结构式
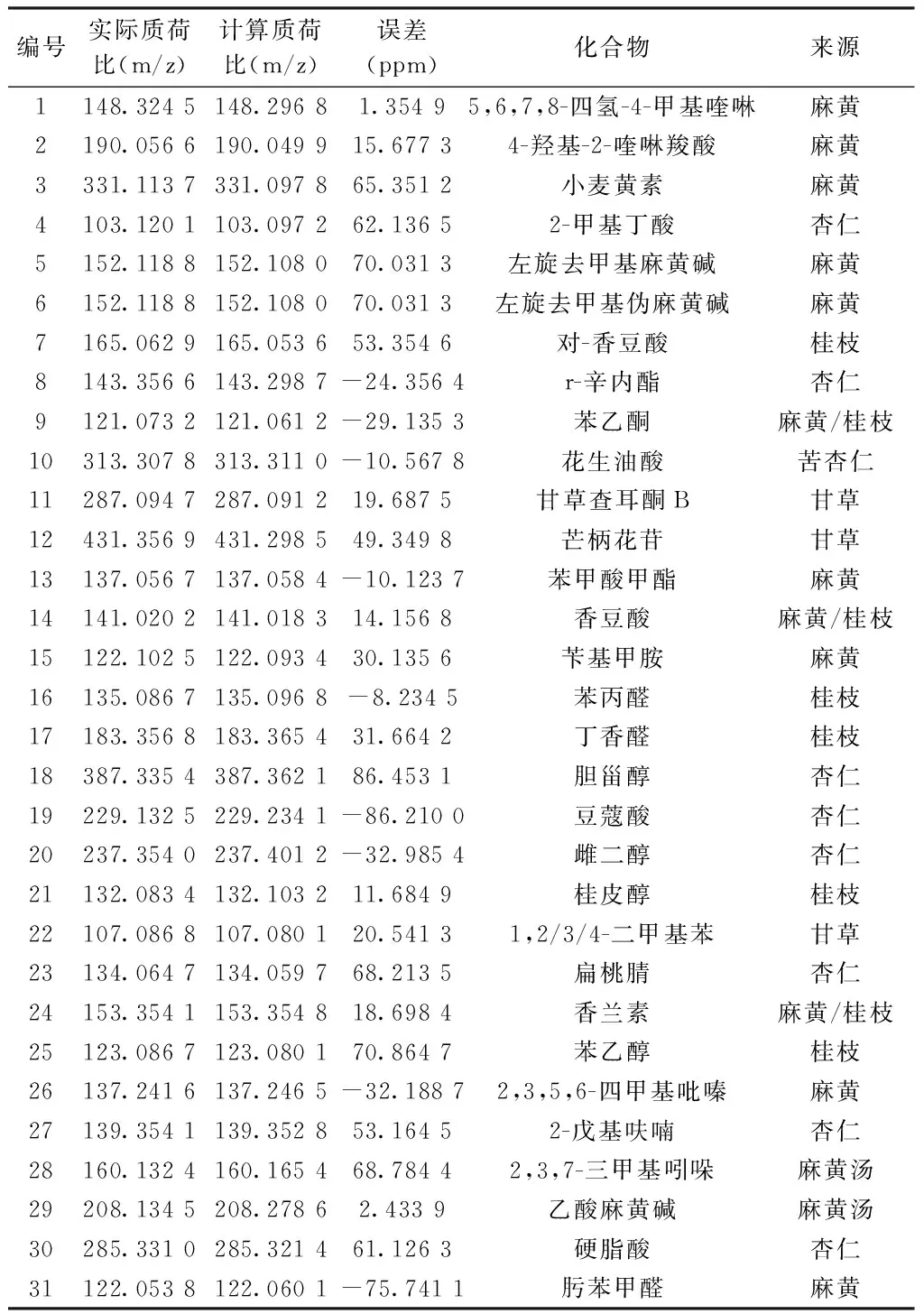
编号实际质荷比(m/z)计算质荷比(m/z)误差(ppm)化合物来源1148.3245148.29681.35495,6,7,8-四氢-4-甲基喹啉麻黄2190.0566190.049915.67734-羟基-2-喹啉羧酸麻黄3331.1137331.097865.3512小麦黄素麻黄4103.1201103.097262.13652-甲基丁酸杏仁5152.1188152.108070.0313左旋去甲基麻黄碱麻黄6152.1188152.108070.0313左旋去甲基伪麻黄碱麻黄7165.0629165.053653.3546对-香豆酸桂枝8143.3566143.2987-24.3564r-辛内酯杏仁9121.0732121.0612-29.1353苯乙酮麻黄/桂枝10313.3078313.3110-10.5678花生油酸苦杏仁11287.0947287.091219.6875甘草查耳酮B甘草12431.3569431.298549.3498芒柄花苷甘草13137.0567137.0584-10.1237苯甲酸甲酯麻黄14141.0202141.018314.1568香豆酸麻黄/桂枝15122.1025122.093430.1356苄基甲胺麻黄16135.0867135.0968-8.2345苯丙醛桂枝17183.3568183.365431.6642丁香醛桂枝18387.3354387.362186.4531胆甾醇杏仁19229.1325229.2341-86.2100豆蔻酸杏仁20237.3540237.4012-32.9854雌二醇杏仁21132.0834132.103211.6849桂皮醇桂枝22107.0868107.080120.54131,2/3/4-二甲基苯甘草23134.0647134.059768.2135扁桃腈杏仁24153.3541153.354818.6984香兰素麻黄/桂枝25123.0867123.080170.8647苯乙醇桂枝26137.2416137.2465-32.18872,3,5,6-四甲基吡嗪麻黄27139.3541139.352853.16452-戊基呋喃杏仁28160.1324160.165468.78442,3,7-三甲基吲哚麻黄汤29208.1345208.27862.4339乙酸麻黄碱麻黄汤30285.3310285.321461.1263硬脂酸杏仁31122.0538122.0601-75.7411肟苯甲醛麻黄
3 讨论
在麻黄汤药物提取溶剂的选择中,考虑到ESI(Electrospray Ionization,电喷雾电离技术)属于软电离质谱离子化技术,受试样品最常用的溶剂是甲醇、水和乙腈[10],本课题组前期研究中在以甲醇、水和乙腈作为提取剂对麻黄汤水煎液进行药物提取之前,尝试直接将麻黄汤水煎液高速离心去掉药渣过滤上清液进样分析,结果显示这一方法残留较多杂质离子等,鉴于UPLC-Q-TOF/MS的高度灵敏性,残留杂质离子形成了干扰峰影响色谱峰的定性分析。本课题组前期研究中发现在甲醇、水和乙腈中以甲醇-乙腈(1∶1)的提取率最高,分离度最好,杂质离子最少,这一结果与相关研究以甲醇-乙腈(1∶1)作为萃取剂结果相吻合[11-12],由此本实验以甲醇-乙腈(1∶1)作为麻黄汤水煎液的萃取剂。在指纹图谱研究中流动相条件至关重要,一般在ESI的研究中其接口多采用同轴夹套液流,接口中的液体常常为甲醇、甲酸-水溶液、乙腈加入不同量的甲酸、或其他铵盐类缓冲溶液[13-15],本研究结果发现当流动相条件为0.1%甲酸-水溶液(A)-0.1%甲酸-乙腈溶液(B),在混合对照品指纹图谱中,各对照品的峰形对称且基线分离度最高最清晰,获得了独立清晰的各个药物色谱峰,即使是对同分异构体化合物如麻黄碱与伪麻黄碱、去甲基麻黄碱与去甲基伪麻黄碱也能够分离清楚。
在稳定的麻黄汤萃取方法和流动相条件下,本研究进行了多次重复性实验对方法学的严谨性进一步考察,结果表明UPLC-Q-TOF/MS对麻黄汤水煎液药物成分分离分析方法稳定,由此我们进一步将麻黄汤水煎液供试品溶液进行指纹图谱分析,结果从麻黄汤水煎液中分离鉴定出31个主要药物的化学成分,其中23.08%生物碱类成分来源于麻黄,如苯丙胺类生物碱麻黄碱、伪麻黄碱、去甲基麻黄碱、去甲基伪麻黄碱,以及喹啉类生物碱5,6,7,8-四氢-4-甲基喹啉、4-羟基-2-喹啉羧酸等;10.27%黄酮类成分来源于甘草;20.52%有机酸类成分来源于桂枝和杏仁,仅有3.2%是来源于苦杏仁的其主要成分为脂肪酸类。此外,在本次实验研究中也分离鉴定出第29种乙酸麻黄碱和第28种2,3,7-三甲基吲哚2个麻黄汤配伍后新产生的化合物,这2个化合物可能是麻黄汤复方中特有的成分[16-17]。
[1]陈荣荣,郭浩,徐砚通,等.中药复方和有效成分对血管新生促进或抑制作用的研究进展[J].中草药,2013,44(23):3413-3421.
[2]戴莹,姜艳艳,刘洋,等.基于类药有效组分特征图谱的中药复方质量表征模式研究[J].北京中医药大学学报,2011,34(5):326-332.
[3]景姗,王新月,杨雪,等.溃疡性结肠炎大鼠肺、肠组织先天与后天免疫应答的改变及中药复方的干预作用[J].中国中西医结合杂志,2015,35(1):63-70.
[4]刘亮.中药复方益糖康对大鼠胰岛细胞凋亡的影响[D].沈阳:辽宁中医药大学,2010.
[5]陈修平,寻克丽,王一涛.中药复方药效物质基础的系统药理学评价[J].中草药,2010,41(1):1-5.
[6]程红,姚志红,戴毅,等.中药复方制剂仙灵骨葆胶囊HPLC指纹图谱研究[J].中国药学杂志,2013,48(10):772-776.
[7]杨胜,张定堃,苏柘僮,等.中药复方制剂质量控制的研究[J].中国医药生物技术,2010,5(5):387-391.
[8]周刚,何燕萍.中药复方新药研发中质量标准研究需关注的问题[J].中国中药杂志,2014,39(17):3389-3391.
[9]张保国,刘庆芳.麻黄汤现代药效学研究与临床运用[J].中成药,2007,29(3):415-422.
[10]李睿,曾岑,王平,等.基于GC-MS和UPLC-Q-TOF-MS的麻黄汤化学成分识别[J].中国中药杂志,2014,39(4):704-709.
[11]刘春海,罗杰英.麻黄汤麻黄先煎的试验研究[J].中医药学报,2002,30(6):16-17.
[12]魏凤环,罗佳波,陈飞龙,等.配伍及煎煮方法对麻黄汤中桂皮醛含量的影响[J].中药材,2003,26(9):664-666.
[13]魏凤环,罗佳波,陈飞龙,等.GC-MS法测定麻黄汤不同配伍对桂皮醛含量的影响[J].中草药,2004,35(6):635-638.
[14]贺丰,罗佳波,陈飞龙,等.GC-MS法研究麻黄汤中麻黄碱、伪麻黄碱的人体内过程[J].中药新药与临床药理,2004,15(5):336-338,347.
[15]朱全红,陈飞龙,白霜,等.GC-MS法测定尿液中麻黄汤代谢产物麻黄类生物碱的浓度[J].药物分析杂志,2005,22(9):1030-1034.
[16]钱燕娟,梁静,蒋小丰,等.高效毛细管电泳法测定麻黄汤中3种有效成分的含量[J].中国临床药学杂志,2008,17(6):371-373.
[17]吴昭晖,罗佳波,谭晓梅.配伍对麻黄汤中甘草HPLC指纹图谱的影响[J].中国中药杂志,2006,31(3):209-212.
(2016-10-25收稿 责任编辑:王明)
Study on Components of Mahuang Decoction Based on Fingerprint
Yu Xinhua1, Zhou Hong2, Shao Yongsheng3, Han Chunsheng1, Hu Yonggu1, Yao Lianqing1, Wang Jun1, Yang Jie1
(1XinyangThirdPeople′sHospital,Xinyang464000,China; 2The154thHospitalofPLA,Xinyang464000,China; 3XinyangCentralHospital,Xinyang464000,China)
Objective:To analyze the components of Mahuang Decoction based on fingerprint analysis and to explain the scientific connotation of favourable compatibility of Chinese herbal medicine. Methods:The mixed standard solution and Mahuang Decoction sample solution were prepared with the mobile phase of 0.1% formic acid aqueous solution (A)-acetonitrile-0.1% formic acid (B). Gradient elution was 0~30 min, 3%~5% B, 30~35 min, 55%~95% B, 35~40 min, 95% B. Column temperature was set at 40 C and the flow rate was 0.5 mL/min. Sample volume 5 L was set as chromatographic condition and similarity analysis was conducted based on fingerprint similarity evaluation system 2004A proposed by the Chinese Pharmacopoeia Commission. Data processing and statistics were analyzed by MATLAB software. Results:1) The relative retention time and relative peak areaRSDof all spectral peaks were less than 5%, which indicated that the reproducibility of the experimental method was good. 2) Fingerprints of mixed control solution including eight hybrid compositions showed no interference peaks, the baseline was stable and the actual Z and Z error calculation were less. 3) Fingerprint of Mahuang Decoction isolated 31 compounds. 4) In 31 compounds obtained from Mahuang Decoction, 2, 3, 7-3-methylindole and acetic acid ephedrine were special components of Mahuang Decoction and the rest 29 kinds were attributed to specific drug sources. Actual error Z and Z calculated of all drug compounds were±100 and the result was true. Conclusion:In 31 compounds obtained from Mahuang Decoction, 2, 3, 7-3-methylindole and acetic acid ephedrine are special components, which are mainly alkaloids from ephedra, organic acids from bitter almond and cassia twig and flavonoids from licorice.
Fingerprint; Mahuang Decoction; Component analysis; Study
国家高技术研究发展计划(863计划)项目(2014AA22304)
王俊(1974.12—),女,大学本科,副主任中药师,信阳市临床药学质量控制中心副主任,研究方向:临床药物合理应用,E-mail:wjun777@126.com
R284.1
A
10.3969/j.issn.1673-7202.2017.07.045
