顶空气相色谱法测定利奥西呱原料药中9种残留溶剂的含量
2017-07-31杨昭毅
杨昭毅,刘 斌
(安徽医科大学附属省立医院药剂科,安徽 合肥 230001)
顶空气相色谱法测定利奥西呱原料药中9种残留溶剂的含量
杨昭毅,刘 斌
(安徽医科大学附属省立医院药剂科,安徽 合肥 230001)
建立同时测定利奥西呱原料药中残留溶剂甲醇、异丙醇、二氯甲烷、正己烷、乙酸乙酯、六甲基二硅醚、三乙胺、甲苯与N,N-二甲基甲酰胺残留量的方法。采用顶空进样气相色谱法,以二甲基亚砜为溶剂,外标法计算残留溶剂量。9种残留溶剂色谱峰的理论板数均>10 000,相邻峰的分离度均>1.5,在考察的浓度范围内各溶剂线性关系良好(r=0.9982~0.9997);RSD<10%;平均加标回收率为90.86%~105.01%。各残留溶剂的检测限和定量限分别为0.000025%~0.0026%,0.000051%~0.0088%,均低于《中国药典》规定。利奥西呱原料中检出甲醇、正己烷、乙酸乙酯与DMF残留,但均未超过限度,其余溶剂未检出。该方法操作简单、方法灵敏、结果准确,可用于利奥西呱原料药中残留溶剂检测。
利奥西呱;顶空进样气相色谱法;残留溶剂;外标法
0 引 言
利奥西呱(Riociguat)是一种口服的可溶性鸟苷酸环化酶受体激动剂。2013年9月获美国FDA批准,是第一个获得批准的治疗肺动脉高压(PAH)和慢性血栓栓塞性PAH(CTEPH)的孤儿药[1]。2014年初,日本及欧洲也相继批准利奥西呱用于治疗CTEPH和PAH。我国食品药品监督管理总局(CFDA)于2014年3月也受理了利奥西呱口服片剂进口的申请。临床试验表明,利奥西呱在治疗PAH和CTEPH上疗效确切,具有良好的安全性及耐受性;且该药为口服制剂,服用方便,具有良好的市场前景[2-3]。
在该药的合成过程[4]中,需要使用人用药品注册技术要求国际协调会(ICH)限制使用的第2类溶剂(甲醇、二氯甲烷、正己烷、N,N-二甲基甲酰胺与甲苯)和限制使用的第3类溶剂(异丙醇、乙酸乙酯)[5]。这些溶剂会对人体健康和环境造成危害,控制其残留量对保证药品质量和用药安全具有重要的意义。目前国内尚未见有关利奥西呱原料药残留溶剂的检测方法报道。为更好地控制产品质量,本文建立了顶空气相色谱法测定利奥西呱原料药中9种有机溶剂残留量的方法。
1 仪器与材料
7890气相色谱仪(FID检测器)、7697A顶空进样器、毛细管色谱柱DB-624(30m×0.530mm×1.80μm),美国Agilent公司;AL-104电子分析天平,瑞士梅特勒-托利多公司。
甲醇、异丙醇、二氯甲烷、六甲基二硅醚、N,N-二甲基甲酰胺(DMF)、二甲基亚砜(DMSO)均为色谱纯。甲苯、三乙胺、乙酸乙酯、正己烷均为分析纯。
盐酸利奥西呱原料,批号分别为141110,141112,141114(某制药有限公司)。
2 方法与结果
2.1 色谱条件
色谱柱为 DB-624(30 m×0.530 mm×1.80 μm)毛细管柱。检测器:氢火焰离子检测器,进样口温度230℃。柱温采取程序升温,起始温度为40℃,维持3min,按15℃/min的速率升温至200℃,保持1min。顶空进样,检测器温度250℃;顶空平衡温度为75℃,平衡时间为20min,进样体积为5mL。
2.2 溶液配制
空白溶剂:取DMSO 5 mL,置顶空瓶中,密封,即得。
对照品溶液:精密称定甲醇1 500 mg、异丙醇2500mg、二氯甲烷 300mg、正己烷145mg、乙酸乙酯2 500 mg、六甲基二硅醚40mg、甲苯450mg、三乙胺160mg、DMF 440mg,分别用 DMSO 稀释至 50mL,即为储备液。精密量取上述储备液1mL置同一100mL容量瓶中加DMSO至刻度,摇匀得对照品溶液。取5mL置顶空瓶中,密封备用。
供试品溶液:取盐酸利奥西呱原料约1 g,精密称定,置10mL容量瓶中,加DMSO溶解并稀释至刻度,摇匀,精密量取5mL,置顶空瓶中,密封即得。
2.3 专属性试验
分别精密量取2.2项对照品溶液5.0mL,在2.1条件下进样测定,对各溶剂在色谱图中的位置进行定位。另精密量取供试品溶液,同法测定。空白溶剂、对照品溶液及供试品色谱图见图1。
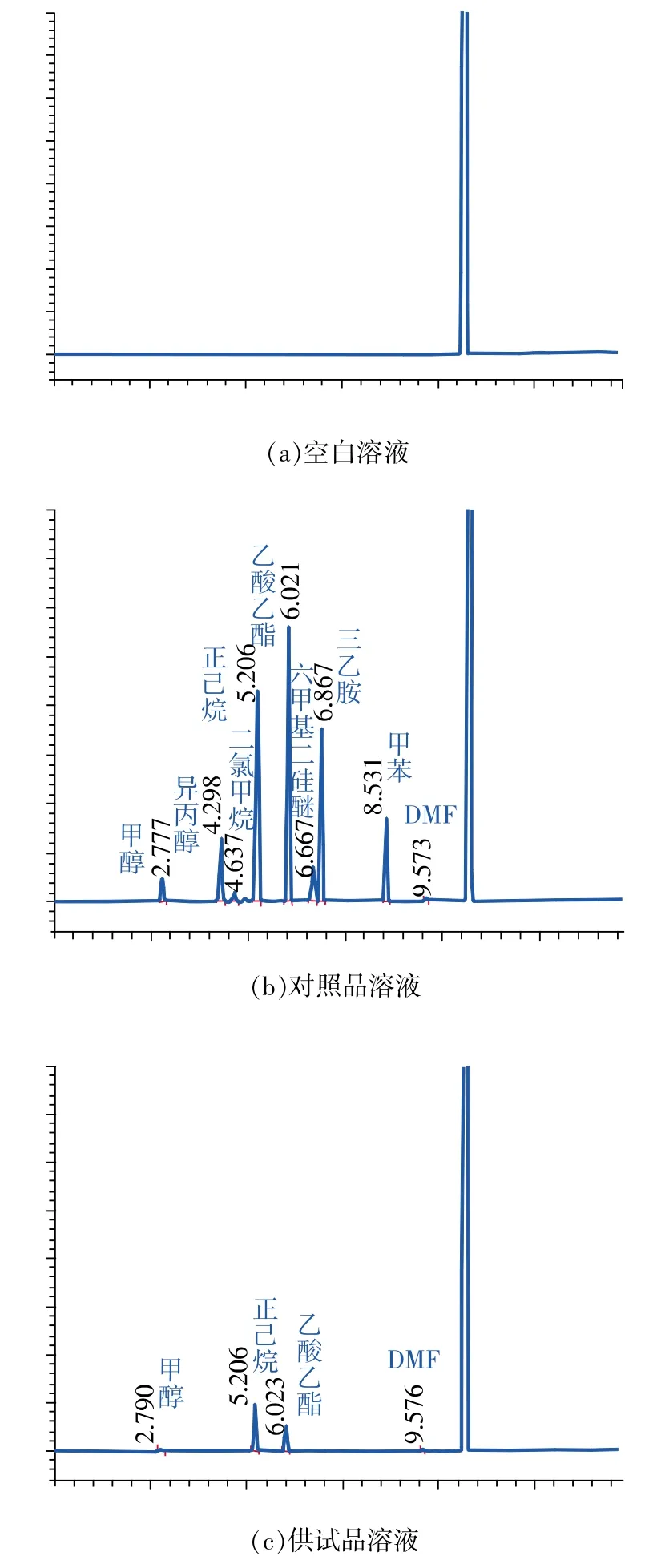
图1 气相色谱图
结果表明,甲醇、异丙醇、二氯甲烷、正己烷、乙酸乙酯、六甲基二硅醚、三乙胺、甲苯与DMF的保留时间分别为 2.777,4.298,4.637,5.206,6.021,6.667,6.867,8.531,9.573min。空白溶剂不干扰各残留溶剂的检测,对照品溶液中各溶剂峰的分离度均大于1.5,理论塔板数均大于10 000,供试品中在甲醇、正己烷、乙酸乙酯与DMF处检出残留峰,本法专属性良好。
2.4 线性关系
分别精密量取2.2项下各对照品储备液0.2,0.4,0.8,1.0,1.2mL置100 mL容量瓶中,加DMSO至刻度,摇匀,制成各对照品的标准曲线储备液。
取上述标准曲线储备液中甲醇10 μL、二氯甲烷20μL、DMF 100μL置10mL容量瓶A中;再分别取其他各标曲储备液0.1 mL置不同10 mL容量瓶中,加DMSO至刻度,摇匀后依次精密量取异丙醇400 μL、正己烷 100 μL、乙酸乙酯 300 μL、六甲基二硅醚800 μL、三乙胺 140μL、甲苯 300 μL 置于容量瓶A中,加DMSO稀释至刻度,摇匀,制成混合标准曲线溶液。
精密量取上述标准曲线溶液各5mL,置顶空瓶中,密封;按2.1项下色谱条件测定,记录色谱图,以质量浓度为横坐标,峰面积为纵坐标进行线性回归,甲醇、异丙醇、二氯甲烷、正己烷、乙酸乙酯、六甲基二硅醚、三乙胺、甲苯与DMF的回归方程及线性范围见表1。结果表明:各溶剂在质量浓度范围内与其峰面积均呈良好线性关系(r=0.9982~0.9997)。

表1 线性关系考察试验结果
2.5 精密度试验
精密量取2.2项下对照品溶液各5mL(共6份),分别置顶空瓶中,密封。按2.1项下色谱条件测定峰面积,计算得甲醇、异丙醇、二氯甲烷、正己烷、乙酸乙酯、六甲基二硅醚、三乙胺、甲苯与DMF峰面积的RSD 分别为 0.53%,0.36%,1.12%,4.82%,0.44%,3.22%,1.36%,0.31%,0.35%(n=6)。结果表明各溶剂峰面积的RSD均小于10.0%,本法精密度良好,满足溶剂残留测定要求。
2.6 回收率
精密称取盐酸利奥西呱原料1g,置10mL容量瓶中,分别精密加混合对照品溶液0.08,0.1,0.12mL,轻轻振摇使其溶解,加DMSO稀释至刻度,摇匀,分别作为低浓度(80%)、中浓度(100%)和高浓度(120%)加标溶液。每种浓度溶液平行制备3份,考察本方法的回收率,结果见表2。
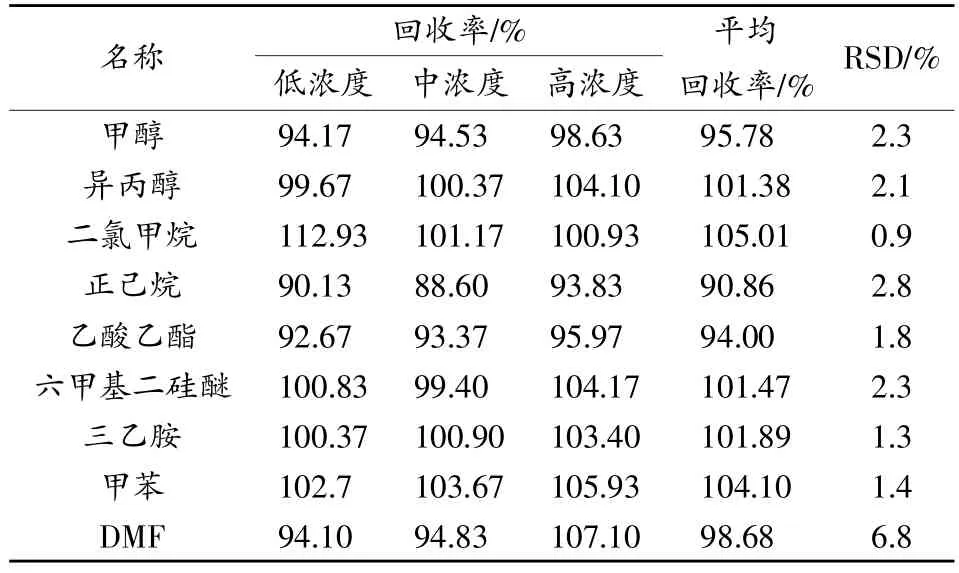
表2 9种溶剂的回收率试验结果
结果表明9种溶剂在高、中、低各加标量下回收率均在80%~120%之间,满足残留溶剂测定要求。
2.7 检测限、定量限
精密量取2.2项下对照品储备液,用DMSO逐级稀释,精密量取各稀释溶液5 mL,分别置顶空瓶中,密封。 以信噪比 S∶N=3∶1,10∶1 的浓度作为各溶剂的检测限与定量限,按2.1项下色谱条件测定峰面积,结果见表3。
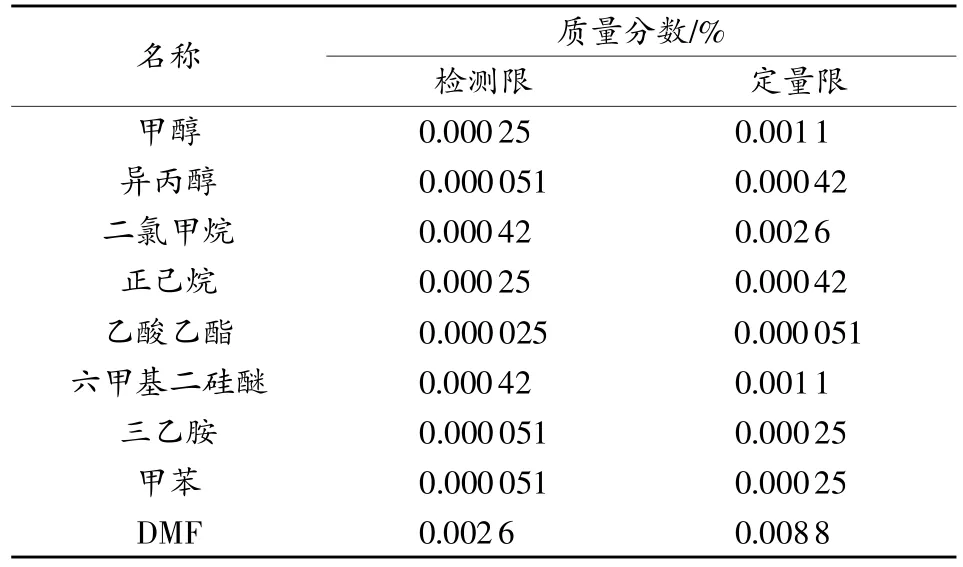
表3 9种残留溶剂的检测限、定量限
结果表明在上述色谱条件下,各残留溶剂的检测限和定量限均低于《中国药典》[5](Ch.P)规定限度,本法的灵敏度较高。
2.8 样品溶剂残留量测定
取盐酸利奥西呱原料3批,按上述方法进行残留溶剂检查,结果见表4。检测结果表明3批样品中均检出甲醇、正己烷、乙酸乙酯与DMF残留,各残留均未超过限度,其余溶剂未检出。
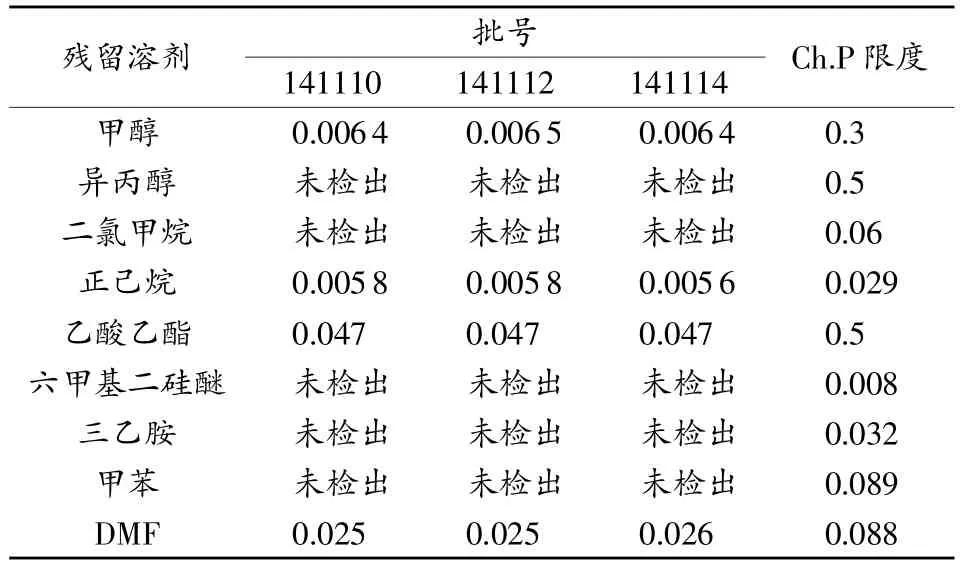
表4 利奥西呱样品残留溶剂检查(n=3) %
3 讨 论
3.1 进样方式的选择
目前各国药典测定有机溶剂残留的方法主要为直接进样法和顶空进样法。通常情况下,沸点低的溶剂建议采用顶空进样法,沸点高的溶剂采用溶液直接进样法[6-7],同时考虑到有机溶剂残留检测通常要同时检测多种溶剂,为了提高检测的可行性和简便性,有学者建议尽量在同样的检测条件下检测尽量多种的残留溶剂[8]。本品有机溶剂残留量检查中对低沸点的二氯甲烷、异丙醇、乙酸乙酯的测定首选为顶空进样法,据文献[9-10]报道高沸点的DMF测定选择顶空进样法亦可以满足测定要求,故笔者选择顶空进样法测定利奥西呱原料中9种有机溶剂的残留量。
3.2 顶空平衡温度及平衡时间的选择
在顶空平衡时间为20min时,笔者分别考察了平衡温度为65,75,85,95℃时的色谱峰峰面积。结果显示,随着平衡温度的升高,色谱峰峰面积增大,但85℃以上后,各成分峰面积均无显著增加;当平衡温度升高至95℃时,色谱图中出现多个未知杂质峰干扰测定结果,可能为DMSO受热的分解产物[11]。在平衡温度为75℃时,色谱图中无未知杂质峰,各成分均能满足测定要求,因此选择75℃作为平衡温度。
顶空平衡有一定的时间要求,以保证样品溶液的气液两相达到平衡,但也不宜过长,否则会引起顶空瓶气密性变差,导致定量准确性降低[12]。在顶空平衡温度75℃时,笔者分别考察了平衡时间为20,30,40min时的色谱峰峰面积。结果显示,不同平衡时间的峰面积基本一致,说明20min已经能达到气液平衡,因此选择20min为顶空平衡时间。
3.3 测定结果分析
根据对人体健康可能造成的危害,目前将残留溶剂共分为4类69种。第2类残留溶剂共28种,毒性比第1类溶剂小,属于限制使用。第3类残留溶剂共26种,是药品生产质量管理规范(GMP)或其他质量要求限制使用的溶剂。此次测得的4种溶剂残留中,甲醇、正己烷和DMF属于第2类,乙酸乙酯属于第3类,因此有必要对这4种溶剂残留进行控制,以确保该药物的质量和安全性,同时减少有机溶剂对环境的影响。
4 结束语
本实验首次采用顶空气相色谱法对利奥西呱原料药中的9种残留溶剂进行检测。方法学验证结果表明该方法色谱条件分离度良好,灵敏度高,在考察的浓度范围内线性关系良好,回收率符合规定,检测方法简便、准确,可以作为生产企业和有关检测机构对利奥西呱原料药中的残留溶剂进行质量控制方法,同时也可为从事相关残留溶剂检测的分析工作者提供参考。
[1]潘雄,程应樟,程晓曙.治疗肺动脉高压新药-利奥西呱[J].中国药学杂志,2016,51(2):159-162.
[2]肖桂芝,刘永贵,汤立达.治疗栓塞性肺动脉高压和成人肺动脉高压新药利奥西呱[J].中国新药杂志,2015,24(1):1-4.
[3] 孟晓冬,单福祥,王燕慧.肺动脉高压治疗进展[J].心血管病学进展,2016,37(3):319-322.
[4] 王宏博,邓乾亚,袁博.利奥西呱的合成[J].中国医药工业杂志,2016,47(6):675-678.
[5] 国家药典委员会.中华人民共和国药典:四部[M].2015年版.北京:中国医药科技出版社,2015:105-107.
[6]European Pharmacopoeia[M].8.0 edition.2013:141-145.
[7] 谭必琴,刘雁鸣.提高气相色谱法测定药物残留溶剂灵敏度的方法[J].中南药学,2016,14(8):846-850.
[8]国家食品药品监督管理总局.化学药物残留溶剂研究的技术指导原则[EB/OL].[2016-03-29].http://www.cda.gov.cn/WS01/CL1616/83419.html.
[9]秦立,胡昌勤,刘文英.顶空气相色谱法测定药品中残留溶剂的影响因素考察[J].药物分析杂志,2005,25(7):823-826.
[10]崇小萌,胡昌勤.利用中等极性气相色谱系统分析药物残留溶剂[J].药物分析杂志,2014,34(11):2048-2053.
[11]张玲,杨华良,王家明.GC测定安立生坦原料药中6种有机溶剂残留[J].中国现代应用药学,2014,31(10):1238-1241.
[12]杨晨,任凤英,杨红,等.顶空气相色谱法测定盐酸头孢替安酯原料药中残留溶剂含量[J].医药导报,2016,35(2):177-180.
(编辑:莫婕)
Determination of 9 residual solvents in Riociguat by headspace gas chromatography
YANG Zhaoyi,LIU Bin
(Department of Pharmacy,Provincial Hospital Affiliated to Anhui Medical University,Hefei 230001,China)
To establish a method for simultaneous determination of the nine residual solvents (methanol,isopropanol, dichloromethane, normal hexane, ethyl acetate, hexamethyl disiloxane, triethylamine,methylbenzene and N,N-dimethylformamide) in Riociguat.Headspace gaschromatographywas applied and dimethyl sulfoxide solvent was used.External standard method was adopted to calculate residual solvent content.The good linear relation of 9 kind of organic solvents were achieved(r=0.998 2 ~0.999 7) with theoretical plate number at chromatographic peak being >10 000 and resolution of adjacentpeak being >1.5 within investigated concentration range.The RSDs of precision was<10%.The average recoveries ranged from 90.86%to 105.01%.Detection limit and quantitation limit(percentage in sample for test)were 0.000025%~0.0026%,0.000051%~0.0088%,which is lower than the regulations in Chinese Pharmacopoeia.The methanol, normal hexane, ethyl acetate and DMF were detected in Riociguat, and they are within limit.No othersolvents detected.The analyticalmethod issimple, accurate and sensitive, and is suitable forthe determination of residual solvents in Riociguat.
Riociguat; headspace gas chromatography; residual solvents; external standard method
A
1674-5124(2017)06-0042-04
10.11857/j.issn.1674-5124.2017.06.009
2016-10-19;
2016-12-13
杨昭毅(1982-),男,安徽合肥市人,主管药师,博士,研究方向为临床药学、药物分析。
刘 斌(1975-),男,安徽合肥市人,副主任药师,硕士,研究方向为药物制剂、临床药学。
