复方斑蝥胶囊联合化疗对三阴性乳腺癌患者肿瘤标志物、免疫指标、生命质量的影响及疗效评价
2017-07-24孔秋梅张文芳
孔秋梅 张文芳
·论著·
复方斑蝥胶囊联合化疗对三阴性乳腺癌患者肿瘤标志物、免疫指标、生命质量的影响及疗效评价
孔秋梅 张文芳
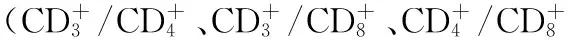
三阴性乳腺癌;复方斑蝥胶囊;化疗;肿瘤标志物;免疫;生命质量;治疗结果;不良反应
三阴性乳腺癌是指雌激素受体、孕激素受体和人表皮生长因子受体2消极表达或低表达的一种特殊亚型的乳腺癌,其具有较高的侵袭能力,机体远处转移、内脏转移风险大,术后复发率高,治疗手段有限的特点[1]。目前临床对三阴性乳腺癌治疗多采用化疗、放疗等措施,但临床缺乏有效的循证学证据[2]。中成药在我国临床治疗中占有重要地位,研究表明,益气方联合厄洛替尼治疗三阴性乳腺癌可以增强后者的抗肿瘤作用[3],人参皂苷Rg3可以有效增强紫杉醇对三阴性乳腺癌的细胞毒性和细胞凋亡作用[4]。复方斑蝥胶囊是一种中药复合制剂,主要成分为斑蝥、人参、黄芪、刺五加、三棱、半枝莲、莪术、女贞子、熊胆粉和甘草。临床研究表明,复方斑蝥胶囊具有提高免疫力、激活抑癌基因、杀死癌细胞的作用,常用于消化道肿瘤、恶性淋巴瘤和妇科肿瘤的治疗[5-7]。本研究采用复方斑蝥胶囊联合化疗治疗三阴性乳腺癌,观察其对患者肿瘤标志物、免疫指标、生化指标的影响,并进行疗效评价和安全性分析。
1 资料与方法
1.1 一般资料 选取2015年1月至2016年11月在我院住院治疗的三阴性乳腺癌患者86例作为研究对象,年龄31~65岁,平均年龄(51.2±7.2)岁;肿瘤直径1.4~7.1 cm,平均(4.4±2.2)cm;病程4~6个月,平均(4.63±0.73)个月;分期:Ⅰ期20例;Ⅱ期44例;Ⅲ期18例;Ⅳ期4例;淋巴结转移:0个23例,1~3个38例;≥4个25例;绝经前33例,绝经后53例。患者根据随机数字表分为常规化疗组和复方斑蝥组,每组43例。常规化疗组年龄32~64岁,平均年龄(50.9±7.0)岁;肿瘤直径1.5~7.1 cm,平均(4.5±2.1)cm;病程4~6个月,平均(4.73±0.75)个月;分期:Ⅰ期9例;Ⅱ期23例;Ⅲ期10例;Ⅳ期1例;淋巴结转移:0个11例,1~3个20例;≥4个12例;绝经前17例,绝经后26例。复方斑蝥组年龄31~65岁,平均年龄(51.6±7.7)岁;肿瘤直径1.4~7.1 cm,平均(4.3±2.0)cm;病程4~6个月,平均(4.59±0.81)个月;分期:Ⅰ期11例;Ⅱ期21例;Ⅲ期8例;Ⅳ期3例;淋巴结转移:0个12例,1~3个18例;≥4个13例;绝经前16例,绝经后27例。2组患者平均年龄、病程、分期、淋巴结转移、是否绝经等相关资料比较,差异无统计学意义(P>0.05)。
1.2 纳入与排除标准
1.2.1 纳入标准:①患者均符合“中国抗癌协会乳腺癌诊治指南与规范(2013版)”[8]的相关诊断标准,且雌激素受体、孕激素受体和人表皮生长因子受体2均为阴性表达;②患者预计生存时间>6个月;③既往未接受放化疗等治疗措施;④治疗前患者心、肝、肾、骨髓、血液系统功能正常;⑤患者意识清楚,能积极配合临床诊疗;⑥患者和(或)家属知情同意,并签署知情同意书。
1.2.2 排除标准:①重要脏器功能受损者;②出现脑转移者;③对治疗药物成分过敏者;④依从性差、有精神疾患不能配合诊疗者;⑤出现重要脏器转移者;⑥伴有严重感染、免疫系统疾病者;⑦患者和(或)家属不同意参加试验者;⑧非医疗原因退出试验者。
1.3 治疗方法
1.3.1 常规化疗组:采用环磷酰胺注射液(江苏恒瑞医药股份有限公司,国药准字H32026196),600 mg/m2联合紫杉醇注射液(太极集团四川太极制药有限公司,国药准字H19994040)165 mg/m2加入0.9%氯化钠溶液进行静脉滴注,1次/周,连用2周,休息1周,再进行用药,3周为1个疗程,连用3个疗程。
1.3.2 复方斑蝥组:在常规化疗组治疗基础上加用复方斑蝥胶囊(陕西华西制药股份有限公司,国药准字Z20003270),3粒/次,2次/d,3周为1个疗程,连用3个疗程。
1.4 观察指标 2组患者均于治疗前和治疗结束后分别采集空腹肘静脉血5 ml,2 500 r/min离心5 min取上清液,备检。
1.4.1 肿瘤标志物:采用免疫荧光法全自动免疫分析仪检测CA125、CA153水平,试剂盒购自上海酶联生物技术有限公司。
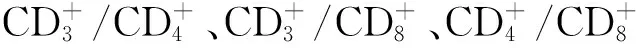
1.4.3 生命质量评价:采用EORTC生命质量测定量表QLQ-C30对患者治疗前后躯体、角色、情绪、认知、社会和总体生活质量进行评价。
1.4.4 不良反应:参照美国卫生及公共服务部“常见不良反应事件评价标准(CTCAE)4.0”[9]进行评价。主要观察消化道不良反应和骨髓抑制情况。
1.5 疗效判定 参照实体肿瘤疗效评价标准-RECIST 1.1[10]进行评价:完全缓解:肿瘤消失,患者乳房、腋窝下未触及肿瘤和(或)淋巴结;部分缓解:肿瘤基本消失,肿瘤最大直径之和减少≥30%;稳定:肿瘤减小,25%≤肿瘤最大径之和减少<50%;进展:患者出现新病灶,且肿瘤最大径之和增加≥25%。总有效率=(完全缓解+部分缓解)/总例数×100%。
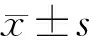
2 结果
2.1 2组治疗前后肿瘤标志物水平比较 2组治疗前CA125、CA153水平比较,差异无统计学意义(P>0.05)。常规化疗组治疗后CA125水平低于治疗前,差异有统计学意义(P<0.05),CA153低于治疗前,但差异无统计学意义(P>0.05)。复方斑蝥组治疗后CA125、CA153水平均低于治疗前,且低于常规化疗组,差异均有统计学意义(P<0.05)。见表1。
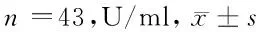
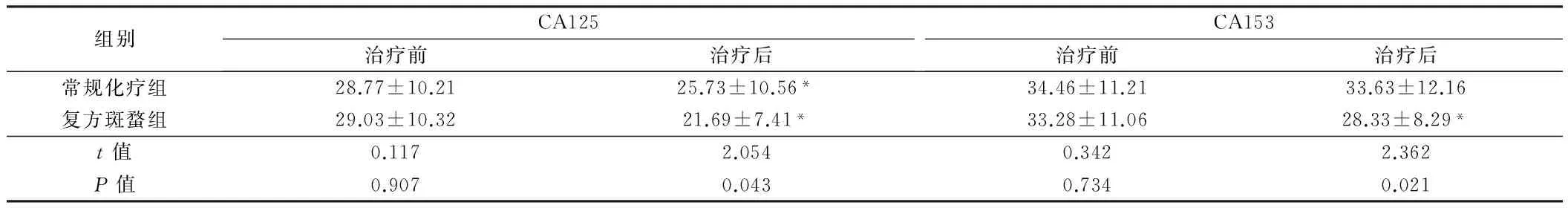
组别CA125治疗前治疗后CA153治疗前治疗后常规化疗组28.77±10.2125.73±10.56*34.46±11.2133.63±12.16复方斑蝥组29.03±10.3221.69±7.41*33.28±11.0628.33±8.29*t值0.1172.0540.3422.362P值0.9070.0430.7340.021
注:与治疗前比较,*P<0.05
2.3 2组治疗前后生命质量评价 2组治疗前躯体、角色、情绪、认知、社会、总体生活质量评分比较,差异无统计学意义(P>0.05)。常规化疗组治疗后躯体、角色、情绪、社会、总体生活质量评分均高于治疗前,差异有统计学意义(P<0.05),而社会评分比较,差异无统计学意义(P>0.05)。复方斑蝥组治疗后躯体、角色、情绪、认知、社会、总体生活质量评分显著高于治疗前,且高于常规化疗组,差异均有统计学意义(P<0.05)。见表3。
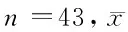
表2 2组治疗前后免疫学指标比较 ±s
注:与治疗前比较,*P<0.05
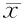
表3 2组治疗前后生命质量评价 n=43,分,±s
注:与治疗前比较,*P<0.05;与常规化疗组比较,#P<0.05
2.4 2组不良反应比较 2组骨髓抑制比较,差异无统计学意义(U=0.687,P=0.492),复方斑蝥组消化道不良发生情况较常规化疗组轻,差异有统计学意义(u=1.994,P=0.046)。见表4。

表4 2组不良反应比较 n=43,例(%)
2.5 2组疗效比较 复方斑蝥组疗效优于常规化疗组,差异有统计学意义(u=2.611,P=0.009),且复方斑蝥组总有效率优于常规化疗组,差异有统计学意义(P<0.05)。见表5。
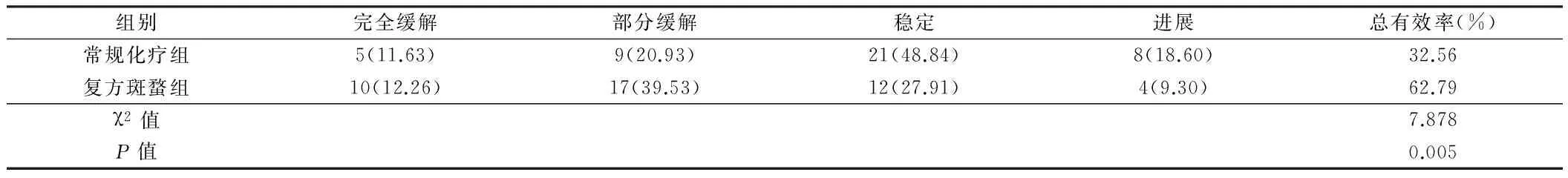
表5 2组疗效比较 n=43,例(%)
3 讨论
三阴性乳腺癌绝大部分病例是低分化癌,其临床特点是更具侵略性,频繁的局部复发率和器官转移,治疗选择有限[11]。Kumar等[12]研究发现,三阴性乳腺癌由于缺乏药物靶向受体,化疗是惟一推荐的可以改善疾病预后的治疗措施,对化疗敏感的患者可以达到完全缓解,而这种方法也可以使患者保留乳房。本研究采用复方斑蝥胶囊联合化疗治疗三阴性乳腺癌取得了较好的临床效果。
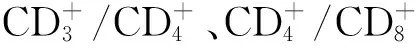
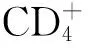
综上所述,复方斑蝥胶囊联合化疗治疗三阴性乳腺癌,可以有效降低患者血清肿瘤标志物水平,提高患者免疫力,有效改善患者生命质量,消化道不良反应小,临床效果显著。
1 Der EM,Gyasi RK,Tettey Y,et al. Triple-Negative Breast Cancerin Ghanaian Women:The Korle Bu Teaching Hospital Experience. Breast J,2015,21:627-633.
2 Jamdade VS,Sethi N,Mundhe NA,et al. Therapeutictargets of triple-negative breast cancer:a review. Br J Pharmacol,2015,172:4228-4237.
3 Liao MJ,Ye MN,Zhou RJ,et al. Yiqi formula enhances the antitumor effects of erlotinib for treatment of triple-negative breast cancer xenografts. Evid Based Complement Alternat Med,2014,2014:628-712.
4 Yuan Z,Jiang H,Zhu X,et al. Ginsenoside Rg3 promotes cytotoxicity of Paclitaxel through inhibiting NF-κB signaling and regulating Bax/Bcl-2 expression on triple-negative breast cancer. Biomed Pharmacother,2017,89:227-232.
5 殷飞,李进军,曹凤,等.复方斑蝥胶囊对肝癌患者TACE治疗前后细胞免疫功能的影响.世界华人消化杂志,2011,19:1843-1846.
6 曹永艳,王猛,黄开顺,等.复方斑蝥胶囊血清诱导人肝癌SMMC-7721细胞蛋白质组差异表达分析.中国中药杂志,2007,32:831-834.
7 夏恪迪,张赢予,张馨木,等.复方斑蝥胶囊体内抗肿瘤作用的实验研究.中国药业,2007,16:13-14.
8 中国抗癌协会乳腺癌专业委员会.中国抗癌协会乳腺癌诊治指南与规范(2013版).中国癌症杂志,2013,23:637-684.
9 U.S.Department Of Health And Human Services,National Institutes of Health,National Cancer Institute.Common Terminology Criteria for Adverse Events (CTCAE)Version 4.0.NIH Publication,2009.117.
10 Eisenhauer EA,Therasse P,Bogaerts J,et al. New response evaluation criteria in solid tumours:revised RECIST guideline(version 1.1). Eur J Cancer,2009,45:228-247.
11 Navrátil J,Fabian P,Palácová M,et al.Triple Negative Breast Cancer. Klin Onkol,2015,28:405-415.
12 Kumar P,Aggarwal R. Anoverview of triple-negative breast cancer. Arch Gynecol Obstet,2016,293:247-269.
13 Mirzaei HR,Nasrollahi F,Mohammadi Yeganeh L,et al. Dose-dense epirubicin and cyclophosphamide followed by weekly Paclitaxelin node-positive breast cancer.Chemother Res Pract,2014,2014:259312.
14 Robert N,Krekow L,Stokoe C,et al. Adjuvant dose-dense doxorubicin pluscyclophosphamidefollowed by dose-dense nab-paclitaxelis safe in women with early-stage breast cancer:a pilot study. Breast Cancer Res Treat,2011,125:115-120.
15 谢泽新,王金烁,刘延冰.观察斑蝥钠维生素B6注射液联合化疗治疗晚期胃癌的近期疗效和不良反应.河北医药,2016,38:1554-1556.
16 张若燕.中药斑蝥及复方斑蝥制剂在治疗恶性肿瘤中的作用.内科,2006,1:73-74.
17 段秋立.复方斑蝥胶囊治疗非小细胞肺癌的疗效观察.中药药理与临床,2016,32:191-192.
10.3969/j.issn.1002-7386.2017.14.012
065000 河北省廊坊市人民医院肿瘤科
张文芳,065000 河北省廊坊市人民医院肿瘤科;
E-mail:zwf7873@126.com
R 737.9
A
1002-7386(2017)14-2128-04
2017-01-18)
