贻贝壳合成碳羟基磷灰石及其在含Cd2+废水处理中的应用
2017-07-12孙彩霞
王 瑜,许 丹,孙彩霞,贾 润
(沧州师范学院化学与化工学院,河北沧州061001)
贻贝壳合成碳羟基磷灰石及其在含Cd2+废水处理中的应用
王 瑜,许 丹,孙彩霞,贾 润
(沧州师范学院化学与化工学院,河北沧州061001)
以贻贝壳为原料合成碳羟基磷灰石(CHAP)吸附废水中的Cd2+离子,通过正交试验,考察了CHAP的用量、镉离子初始浓度、吸附时间以及pH值等因素对废水中镉的去除率及吸附性能的影响.通过扫描电镜(SEM)和红外光谱(FTIR)分析,对CHAP的形貌和结构进行表征.结果表明:在常温常压下,当废水中镉离子初始浓度为50mg·L-1、吸附时间为30min、pH值为6.0,CHAP的加入量为2g/L时,CHAP对废水中镉离子的去除率可达98.36%.
碳羟基磷灰石;吸附;Cd2+离子;正交试验;扫描电镜;红外光谱
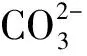
贻贝是一种可人工养殖的贝类,世界许多国家和地区都有养殖,北欧、北美、澳大利亚等地贻贝养殖盛行,我国的浙江、福建、山东、辽宁等省沿海盛产贻贝,每年的产量巨大,多达几十万吨.贻贝加工生产淡菜后,差不多十几万吨的贻贝壳被废弃堆积于附近的海滩上,造成资源的浪费,扩展废弃贻贝壳的资源化利用途径成为亟待解决的问题.
人工合成CHAP大多采用废弃鸡蛋壳为原料来制备[9],本文在前人工作的基础上,采用掺杂技术,以废弃的贻贝壳为原料,尿素为添加剂,合成新型的碳羟基磷灰石,用其处理含Cd2+离子废水,方法简便、高效、成本低,吸附剂可以重复使用,是一种有广阔应用前景的绿色洁净环境功能材料,具有极大的研究开发和利用价值.
1 试验部分
1.1 主要试剂和材料
试验采用的主要试剂有:H3PO4、Ca(OH)2、尿素、KOH、NH4Cl、Cd粒(99.99%)、Cd(NO3)2·4H2O.以上试剂均为分析纯,所用水为蒸馏水和二次亚沸蒸馏水.
原子吸收分光光度法测定镉所使用的标准储备液和标准工作液均由一定质量的Cd粒(99.99%)溶于少量硝酸中并加二次亚沸蒸馏水稀释到一定体积配制.含镉离子的模拟废水用Cd(NO3)2·4H2O配制.贻贝壳采购自海鲜市场.
1.2 主要仪器
85-2A双向恒温磁力搅拌器、DK-8D数显恒温水浴锅(江苏省金坛市医疗仪器厂);PHSJ-3F实验室pH计、FA2004N电子天平、722N可见分光光度计(上海精密科学仪器有限公司);202-2型干燥箱(上海市实验仪器总厂);Nicolet iS5傅里叶变换红外光谱仪(赛默飞世尔科技(中国)有限公司),TM3030台式扫描电镜(日本株式会社日立高新技术那珂事业所);4510型原子吸收分光光度计(上海嘉鹏科技有限公司).
1.3 碳羟基磷灰石的制备
将在海鲜市场购买的贻贝外壳清洗干净,除去苔藓、贝肉、足丝,在105℃下烘干,研磨,过100目筛.取一定量干燥过筛的贻贝壳粉末,边搅拌边加入过量的磷酸,使其生成磷酸二氢钙.反应方程式为:
CaCO3+2H3PO4=Ca(H2PO4)2+H2O+CO2↑
缓慢加入蒸馏水,待冷却后过滤除去不溶物.向滤液中加入氢氧化钾溶液,调pH为弱碱性,反应方程式为:Ca(H2PO4)2+2KOH=CaHPO4↓+Na2HPO4+2H2O,再按物质的量比1:1加入尿素固体和用蒸馏水调成糊状的氢氧化钙乳浊液,再将混合物用10%KOH溶液调节pH值为10,在80℃的水浴锅中热处理24h,生成目标产品碳羟基磷灰石,该反应方程式为:CaHPO4+(NH2)2CO+Ca(OH)2→Ca10[(PO4)6-x,(CO3·OH)x](OH)2.过滤,用5%的氯化铵洗涤至中性,抽滤后于60℃干燥箱中干燥6h得到CHAP.
1、加强城市的基础设施建设和国际化的城市设计。在城市中的各类双语标识、各语种口译专业人员配备、服务业从业人员的外语沟通水平等各个方面提高国际游客的便利度。
1.4 吸附试验设计
用Cd(NO3)2·4H2O配制浓度为1000mg·L-1的含镉离子的模拟废水.取一定体积的含镉离子的模拟废水,将其调节到适当的pH值,用蒸馏水稀释至100mL,再加入一定质量的CHAP,在常温常压下搅拌一定时间进行吸附,静置1h后,采用原子吸收分光光度法分析上层清液中残余的镉离子浓度,按下列公式计算其吸附去除率.
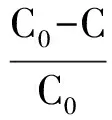
式中:η——去除率;C0——镉离子初始浓度mg/L;C——吸附后的镉离子浓度mg/L.
用正交试验的方法设计不同的反应条件,根据其去除率来确定吸附的最佳条件组合.
2 试验结果与讨论
2.1 CHAP的表征
图1为CHAP的FT-IR图谱.
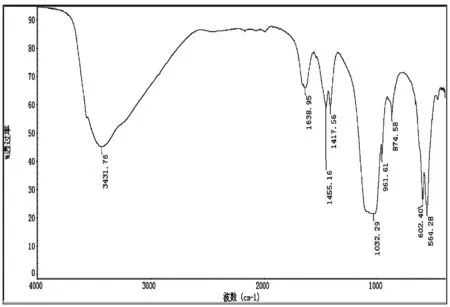
图1 碳羟基磷灰石的红外光谱图
由图1可见:在3431.76cm-1处有一个很强的吸收峰是结构羟基的伸缩振动特征峰,961.61cm-1处的吸收峰为结构磷酸根的ν1振动吸收峰,472.07cm-1处为结构磷酸根的ν2振动吸收峰,602.40cm-1和564.28cm-1处为结构磷酸根的ν3、ν4弯曲振动吸收峰,1638.95cm-1、1455.16cm-1和1417.56cm-1、874.58cm-1处是碳酸根的吸收峰,1455.16cm-1以及1417.56cm-1这两个分裂峰能够区别于碳酸盐中碳酸根的单峰,是碳羟基磷灰石中含有碳酸根的重要标志.

图2 碳羟基磷灰石扫描电镜图
由图2可以看出:碳羟基磷灰石是无定型沉淀,颗粒的粒径特别细小,微粒之间能够团聚成孔状,具有很高的通透性,其表面较为粗糙且具有很多的微小空隙,作为吸附剂而言具有较强的吸附性,有利于提高物理吸附和离子交换吸附能力.
2.2 Ca/P物质的量比的测定
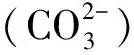
2.3 CHAP对镉离子的吸附条件选择
2.3.1 正交试验设计
CHAP在对镉离子的吸附过程中,影响因素很多,如温度、吸附时间、CHAP加入量、镉离子初始浓度等等.单一变量法的实验次数多,步骤繁琐,而且实验结果容易发生偏离.采用数理统计的方法进行试验设计,正交表将各因素和水平之间的组合合理安排,实现了各因素和水平之间的整齐可比性和均匀分散性,能减少试验次数,给出试验误差的估计,达到因素间的均衡搭配[10].
根据初步试验,选择镉离子初始浓度(A)、CHAP加入量(B)、pH值(C)、反应时间(D)四个因素为考察因素,CHAP对废水中镉离子的去除率(η)为考察指标,采用L9(34)正交表来进行四因素三水平的实验设计,因素水平表见表1,正交试验结果分析见表2,实验在常温常压下按照正交表顺序及吸附试验设计依次进行.

表1 正交设计因素水平表

表2 正交试验结果分析
注:K1、K2、K3分别为各因素不同水平的算数和,k1、k2、k3分别为各因素不同水平的算数平均值,R为极差.
由k1、k2、k3和η判断试验结果随各因素用量变化的趋势,正交组合A2B3C2D2是去除效果最好的实验条件,即镉离子初始浓度为50mg·L-1、CHAP加入量为0.2g、pH值为6.0、吸附时间为30min时去除率应该是最高的.因为分析出的最优组合A2B3C2D2并未包含在上述做过的九组实验中,所以应该按照该最优组合做一次验证实验,验证实验所得到的CHAP对废水中的去除率为98.36%,大于正交试验的结果中的最大值96.65%,说明A2B3C2D2确是该实验的最优组合.从表2中算出各列的极差,极差R从大到小对应的影响因素的排序为:D>A>B>C,这一结果表明吸附时间对去除率的影响最大,其次是镉离子初始浓度、CHAP用量和pH值.
2.3.2 CHAP的重复利用
考虑到吸附剂的循环利用和吸附后的重金属离子的回收,对按照最优组合的实验条件吸附镉离子后的CHAP进行蒸馏水洗涤处理,烘箱加热干燥后待用.利用再生后的CHAP进行镉离子的再生吸附试验,结果如表3.试验结果表明,经过蒸馏水洗涤后,CHAP的吸附性能仍然很好,保持在97%以上,所以在实际工作中,本着绿色可循环的原则可多次重复使用.
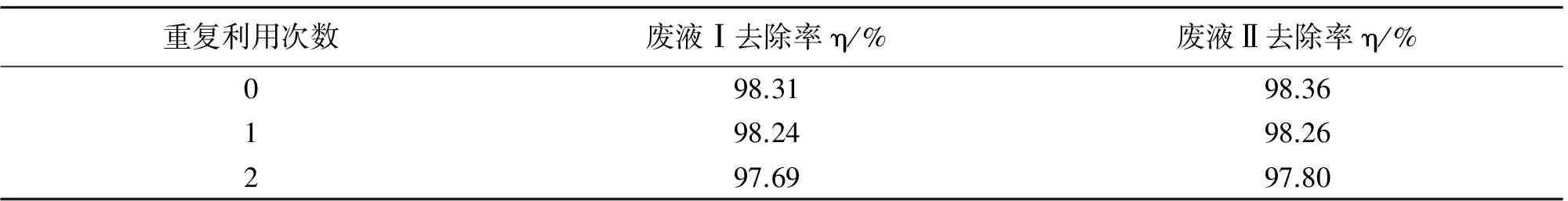
表3 CHAP的重复利用(n=3)
3 结论
碳羟基磷灰石是一种新型的环境矿物材料,可利用废弃的贻贝壳为原料制备,具有制备工艺简单,制作成本低廉的特点,对重金属离子有良好的离子交换和吸附性能,在常温常压下,2g·L-1的CHAP去除100mL 50mg·L-1含镉离子废水,在pH值为6.0、吸附时间为30min时去除率可高达98.36%.用蒸馏水对吸附镉离子后的CHAP进行洗涤处理,CHAP的吸附性能仍然很好,保持在97%以上,说明CHAP具有较好的再生性.贻贝壳的资源化利用不仅能带来经济效益,更重要的是实现了“废物”利用.
[1] Myroslav Sprynskyy. Study of the selection mechanism of heavy metal(Pb2+,Cu2+,Ni2+and Cd2+)adsorption on clinoptilolite[J]. Journal of Colloid and Interface Science, 2006,304(1):21-28.
[2] 刘培,陈晨.螯合沉淀法处理含铬电镀废水[J].电镀与涂饰,2013,32(5):45-48.
[3] 尔丽珠,秦晓丹,张惠源.离子交换法移动处理重金属废水[J].电镀与精饰,2007,29(2):48-51.
[4] 王继斌.趋磁细菌在重金属废水处理中的应用[J].中国环境管理干部学院学报,2011,21(5):54-56.
[5] 邓娟利,胡小玲,管萍,等.膜分离技术及其在重金属废水处理中的应用[J].材料导报,2005,19(2):23-26.
[6] 邵刚.膜法水处理技术[M].北京:冶金工业出版社,2000.
[7] KIM S,MOON S H,KIM K W,et al. Pilot scale study on the exsitu electrokinetic removal of heavy from municipal wastewater sludges[J]. Water Research,2002,36:4765-4774.
[8] 唐文清.碳羟基磷灰石的合成及吸附性能的研究[D].长沙:湖南大学,2006.
[9] 唐文清,曾荣英,李小明,等.合成碳羟基磷灰石对废水中苯胺的吸附机理[J].硅酸盐学报,2010,38(11):2167-2171.
[10] 郑用熙.分析化学中的数理统计方法[M].北京:科学出版社,1991.
[责任编辑:尤书才]
Carbon Hydroxylapatite Synthesized with Mussel Shells and Its Application in Cd2+Ionic Wastewater Treatment
WANG Yu, XU Dan, SUN Cai-xia, JIA Run
(College of Chemistry and Chemical Engineering, Cangzhou Normal University, Cangzhou, Hebei 061001, China)
Crbon hydroxylapatite (CHAP) synthesized with mussel shells as raw material can adsorb Cd2+ions in wastewater. The influence of such factors as dosage of CHAP, initial concentration of Cd2+ions, adsorption timespan and pH on the removal rate of cadmium and adsorptive property is examined in orthogonal test. And the morphology and structure of CHAP are represented with scanning electron microscope (SEM) and infrared spectroscopy (FTIR) analysis. The result shows that, with normal temperature and pressure, when the initial concentration of Cd2+ions in wastewater is 50 mg·L-1, adsorption time is 30 min, pH is 6.0, and additive amount of CHAP is 0.2g, the removal rate of Cd2+ions in wastewater can reach 98.36%.
carbon hydroxylapatite; adsorb; Cd2+ions; orthogonal test; scanning electron microscope; infrared spectroscopy
2016-10-02
王 瑜(1962-),女,山东潍坊人,沧州师范学院化学与化工学院教授,研究方向:微量元素分子光谱分析.
X307
A
2095-2910(2017)02-0024-05
