水合盐相变储能材料的研究进展
2017-07-12孟令然郭立江李晓禹陈胜利李建强
孟令然,郭立江,李晓禹,王 会,陈胜利,周 园,李建强
水合盐相变储能材料的研究进展
孟令然1,2,郭立江1,李晓禹1,王 会1,陈胜利2,周 园3,李建强1
(1中国科学院过程工程研究所湿法冶金清洁生产技术国家工程实验室,中国科学院绿色过程与工程重点实验室,北京100190;2中国石油大学(北京)化学工程学院,重质油国家重点实验室,北京102249;3中国科学院青海盐湖研究所青海省盐湖资源化学重点实验室,青海西宁 810008)
水合盐相变储能材料具有储热密度大、导热系数大、相变温度适中、低价易得等优点,具有较好的应用前景,成为近年来的研究热点。本文分析了水合盐相变储能材料的研究态势;详述了国内外对水合盐相变材料的热物性及应用探索方面的研究工作及进展;针对水合盐相变储能材料在应用过程中存在的过冷、相分离及对容器腐蚀性问题的特点,详述了解决这些问题的方法及进展;对水合盐相变材料的应用及发展前景进行了展望,认为对水合盐相变材料过冷、相分离及循环稳定性问题的研究和解决方法还需要加强。
水合盐;储能;相变材料;稳定性;腐蚀性
我国能源资源总量比较丰富,但人均能源资源拥有量较低。然而,与此相对的是,我国能源效率总体仍然偏低,单位GDP能耗是世界平均水平的2.5倍,美国的3.3倍,也高于巴西、墨西哥等发展中国家。同时,占总能源消费60 %以上[1]的煤炭消费,也造成了大范围、区域性的重度雾霾频发。能源的紧缺和低利用率问题,正在成为制约社会经济可持续发展的重要因素。《中华人民共和国国民经济和社会发展第十三个五年规划纲要》提出:“大力开发、推广节能技术和产品,开展重大技术示范。实施建筑能效提升和绿色建筑全产业链发展计划,推进能源综合梯级利用。”因此,能源的节约与综合梯度利用,是我国经济社会可持续发展的重要保证,已经成为国家战略需求。
相变储能技术利用相变储能材料(phase change materials,PCMs)在相变过程中产生的潜热进行能量的储存和释放,进而调和热能供给与需求在时间和空间上不相匹配的矛盾,是实现能源节约与综合梯度利用的有效技术手段之一。相变材料的性能直接影响储能的效果。相变材料按化学成分分类主要包括有机相变材料(石蜡、脂肪酸等),无机相变材料(水合盐类、金属类)和复合相变材料。水合盐是典型的相变储能材料,与其它相变材料相比,具有价格便宜、体积蓄热密度大(约350 MJ/m3)、相变潜热大(86~328 J/g)、熔点固定、热导率大[约0.7 W/(m·℃)]等优点[2]。因此,水合盐作为相变储能技术的材料,具有经济和技术可行性,在太阳能利用、建筑节能、冷藏物流链、电力系统调峰、余热回收、采暖空调及家用电器等许多领域都有广泛的应用前景,成为研究的热点。
1 水合盐相变储能材料的研究态势
本文对最近40年(1976—2016年4月)报道的水合盐相变材料研究论文进行了全面的调研,以Web of Science数据库为数据源统计了自1976年以来每年发表的相关论文数量,如图1所示。从图1很清楚的看出,研究水合盐相变材料的论文数量呈逐年上升的态势,这种趋势表明水合盐相变储能材料研究工作引起了国内外学者越来越多的关注。从研究内容来分析,对水合盐相变储能材料的特性表征、性能研究及过冷、稳定性等方面的研究成为主要方向,占66%,如图2所示。此外,水合盐相变储能系统的数值模拟计算及共熔混合物的研究也备受关注,相关论文分别占9%和6%,如图2所示。
对各国关于水合盐相变材料的研究力量进行分析,结果表明,关于水合盐相变材料论文发表数量前3的国家分别是中国、日本和美国,如图3所示。对各国关于水合盐相变材料主要研究方向进行统计,如图4所示。可以看出,国家主要研究方向主要集中于能源与燃料、工程、热力学、化学、材料科学等。
2 水合盐相变储能材料的基础热物性研究
为了使水合盐相变材料更有效地应用到储能系统中,研究者们一直努力发展高性能的水合盐相变储能材料。文献报道的对单组分水合盐相变储能材料的研究工作,主要集中在相变潜热、相变温度等热物特性的测定,部分研究工作还报道了水合盐的密度、热导率等参数。张寅平等[3]、TELKS[4-6]、LANE[7-9]、BELTON等[10]、GUION等[11]、ABHAT等[12]、KENISARIN等[13]和ZAIBA等[14]都对前人报道的常用单组分水合盐相变储能材料的热物性研究工作进行了详细的总结。表1列出了文献报道的部分单组分水合盐相变储能材料热物性数据,包括相变温度、相变潜热、密度、比热容、热导率等。
相变储能技术的经济和技术性要求相变储能材料具有较大的相变潜热,并且有适宜的相变温度,因此单一组分水合盐已无法满足不断发展的相变储能技术的需求。随着研究的深入,人们发现另外一 种无机盐的加入会降低体系的相变温度。根据这 个规律,DONG等[15]、LI等[16]、VOGIT等[17]、RAI等[18]研究了二元及多元体系水合盐相变储能材料, 并获得了一系列的混合盐相变储能材料体系,如表2所示。

表1 单组分水合盐相变储能材料热物性

续表1

表2 混合水合盐相变储能材料及其相变温度和相变潜热
3 水合盐相变储能材料的应用研究
早在20世纪60年代,美国国家航天局就开展了相变材料在航天领域的应用研究工作。TELKES[4-6]和LANE[7-8]在水合盐相变储能材料热物性研究的基础上,对应用过程的传热、系统设计等方面做了大量工作。TELKS对Na2SO4·10H2O的储放热循环进行了千余次实验,并建立了以Na2SO4·10H2O为相变储能材料的世界上第一座被动式太阳房[4-6]。LANE[7]开展了将CaCl2·6H2O封装在塑料管中收集太阳能来改变室温的应用研究工作。日本对相变储能材料的研究也起步较早。三菱公司和东京电力公司合作开展了将水合硝酸盐、磷酸盐、氟化物和氯化钙[22]应用于制冷和空调系统的研究工作。
1990年美国加州发明了两种空调用蓄冷用相变材料,它们分别被称为“41”和“47”型,对应的相变温度为5 ℃和8 ℃[23];1982年Calor Group 公司发表的相变温度为7.5 ℃凝胶化的Na2SO4·10H2O/NH4Cl/KCl的相变材料体系,称该种相变材料是Calotherm 7,并在美国已商品化[24];瑞典Climator公司研制生产了一种名为C7的相变材料,其相变温度为7 ℃,非常适合在空调蓄冷中使用[25]。
2022年世界杯将在多哈举行,多哈气温白天高达50 ℃,晚上仍在30 ℃以上,因此多哈足球场馆实施制冷项目来克服严酷的环境。该项目制冷系统配置有太阳能集热器、吸收式溴冷机组和相变储能系统,相变储能系统以相变温度为6 ℃的水合盐为介质。系统运行时,由太阳集热器在高温环境中收集太阳能为溴冷机提供热源驱动产生冷量,冷量由相变系统储存起来,待需要时通过出风口将冷风引入场馆,可以使场馆温度控制在27 ℃[26]。FRAID等[27]采用微胶囊技术封装CaCl2·6H2O做相变材料制备相变储热地板,与普通地板相比,相变储热地板表面温度波动较小,热舒适性较好。
在我国,华中师范大学和西藏太阳能研究示范中心合作,以盐碱湖泊里的芒硝等材料掺入添加剂,研发出太阳能高密度储热相变材料。清华大学的张寅平等[3]开展了将水合盐相变材料应用于墙体的一系列理论研究工作。阮德水教授课题组[28-30]对Na2SO4·10H2O等经典无机水合盐相变材料的相图、成核因素、过冷度、能量存储等应用过程中存在的问题进行了全面探索。
刘应江、罗飙[31]申请专利,发明了一种常规空调工况分布式相变储能空调系统,相变材料可采用CaCl2·6H2O加入氯化钙基其它添加剂的体系,这种常规空调工况分布式相变储能空调系统比常规空调系统综合节电费用50%左右。
近年来,国内市场有种热袋,水合盐作为其相变材料,相变温度20 ℃左右,利用一块金属片作为成核晶种材料,当用手挤压金属片时,使它的表面成为晶体生长中心,从而结晶放热,再配备某些具有活血作用中药袋,从而达到理疗的作用,对于治疗类风湿等疾病有一定的疗效[32]。人们还利用水合盐相变材料制备了坐垫,可以使人体在夏天获得舒适的温度,并且可以循环使用。
4 水合盐相变储能材料存在问题的研究
研究者们发现,以水合盐作为相变储能材料的应用过程中存在共性关键问题,即过冷、相分离和对金属容器的腐蚀性。针对这些共性问题,研究者们也开展了研究工作,提出了一些解决方法。
4.1 过 冷
过冷是指水合盐相变储能材料在从液相转化成固相过程中,温度降低至其相变温度以下仍不发生相变,使其释热温度发生变化,影响使用效果。目前,文献报道的解决过冷的主要方法是添加成核剂和冷指法。
(1)添加成核剂 产生过冷现象的原因是大多数结晶水合盐结晶时成核性能差所致,一般采用添加成核剂的方法来避免过冷,但寻找适合某种特定水合盐的成核剂比较困难,有研究表明可选择与该种水合盐晶格参数相差15%以内的物质作为成核剂。
LANE[33]通过分析水合盐的晶体结构和计算晶格参数,确定几种晶格参数较近的成核剂,通过实验比较成核剂对过冷度的改善情况,推测出高效的成核剂,表3为其实验结果。

表3 几种水合盐相变材料较好成核剂

续表3
TELKES对Na2SO4·10H2O进行了长期实验研究,提出用硼砂作为Na2SO4·10H2O相变材料的成核剂,发现在封闭系统内可使其过冷度降低到2 ℃以下。PILAR等[34]对MgCl2·6H2O的过冷现象进行了研究,得出在MgCl2·6H2O中添加Mg(OH)2可以抑制该材料的过冷现象,而且也发现分别添加质量分数为1%和0.5%的SrCO3和Sr(OH)2几乎可以完全抑制该材料的过冷现象。WADA等[35]研究表明Na4P2O7·10H2O有助于NaCH3COO·3H2O结晶。阮德水等[36]、文越华等[37]也开展了用硼砂作为NaSO4·10H2O的成核剂的研究工作。刘栋等[38]通过实验发现在室温和冰水浴两种冷却环境下,锶盐都能有效降低CaCl2·6H2O体系的过冷度,还指出工业级中的杂质会影响成核剂的成核作用,使材料的过冷度增加。FELLECHENFELD等[39]用SrCl2·6H2O做CaCl2·6H2O的成核剂。刘欣等[40]给3组Na2SO4·10H2O加入相同的成核剂硼砂和晶型改变剂六偏磷酸钠,发现过冷度都较小。
(2)冷指法 冷指法是指预留一部分固态结晶水合物作为相变凝结核,用于引发相变[3]。这种方法能有效地解决过冷问题,但其缺点是使用不方便、相变过程不能自发进行、每次都需要人工操作[41]。
4.2 相分离
相分离是指水合盐相变材料在熔化过程中形成一些无水盐或低水合物,在被加热到熔点以上,有些无水盐(或低水合物)仍不能溶于其结晶水中,且会与水形成密度差而沉积到底部从而降低了水合盐储热密度。目前解决相分离的方法有:①加入增稠剂或悬浮剂;②加入晶体结构改变剂;③盛装相变材料的容器采用薄层结构;④摇晃或搅动。
国外,BISWAS[42]对相分离问题进行了研究,在Na2SO4·10H2O中加入质量分数为3%的硼砂后,经几次熔化-凝固循环后的储热量就降为原先的 25%,若在加入硼砂的Na2SO4·10H2O中再加入适量的增稠剂活性白土,则在经历了许多次加热冷却循环后,储热容量仍能保持原先值的50%。RYU等[43]在水合盐相变储能材料中加入增稠剂(如活性白土、SAP、CMC),减小了水合盐相变储能材料的相分离问题,在加入增稠剂的水合盐相变材料中加入不同种类成核剂,寻找最佳成核剂,其研究结果如表4所示。MARKS[44]用增稠剂(凹凸棒石黏土)来减小相分离的效应。
国内,文越华等[37]用羧甲基纤维素钠作为增稠剂减小相分离现象;徐建霞等[45]、陈爱英等[46]也研究了增稠剂对相变储能材料的相分离现象的抑制作用。表5列出了常用几种水合盐相变储能材料的成核剂和增稠剂[46]。
4.3 对金属容器的腐蚀性
为了加强在使用过程中的传热效果,一般选择金属材质的容器对相变储能材料进行封装。然而,水合盐对金属材料具有一定的腐蚀性,这也成为水合盐相变储能材料应用过程中的一个共性问题,LANE[7]、CABEZA等[47]、FARRELL等[48]、GARCÍA- ROMERO等[49]、MORENO等[50]、SCHRÖDER[51]、HEINE[52]、ZALBA等[53]、NAGANO等[54]和PORISINI[55]开展了大量的研究工作,分别研究了特定的水合盐相变储能材料对不同型号的铝、铝合金、铜、不锈钢、碳钢等金属材料的腐蚀性。本文将其部分研究结果列于表6。从表6中可以看出,大量水合盐对金属容器有腐蚀性,但不锈钢对水合盐相变材料的耐腐蚀性最优;其次,铝纯度和碳钢含碳量的不同材质都会影响材料的耐腐蚀性。

表4 不同成核剂对水合盐相变材料过冷度的影响
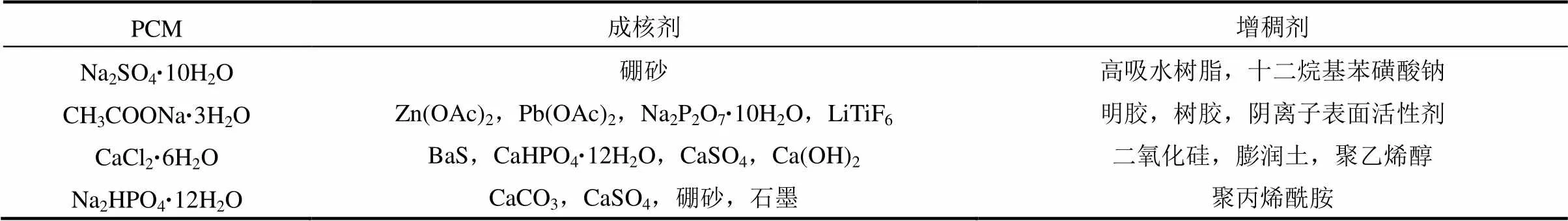
表5 常用几种水合盐相变材料的成核剂和增稠剂
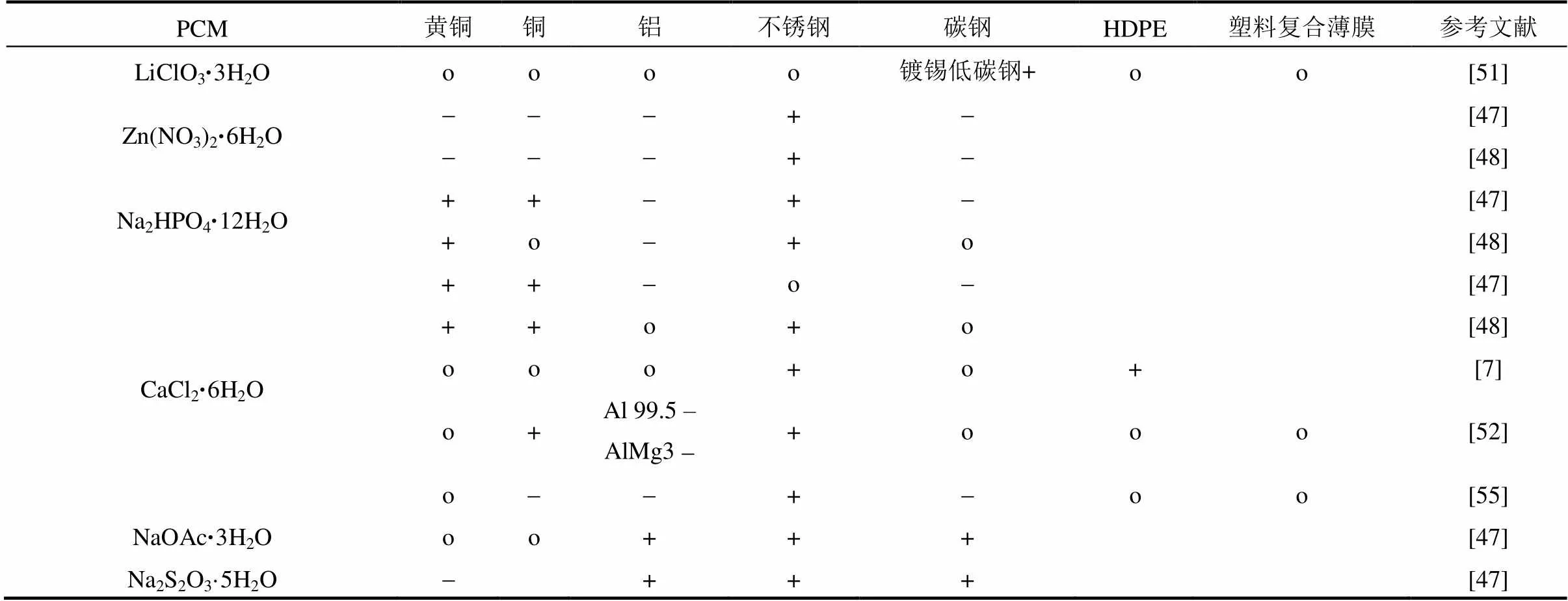
表6 不同水合盐相变材料对容器的腐蚀性
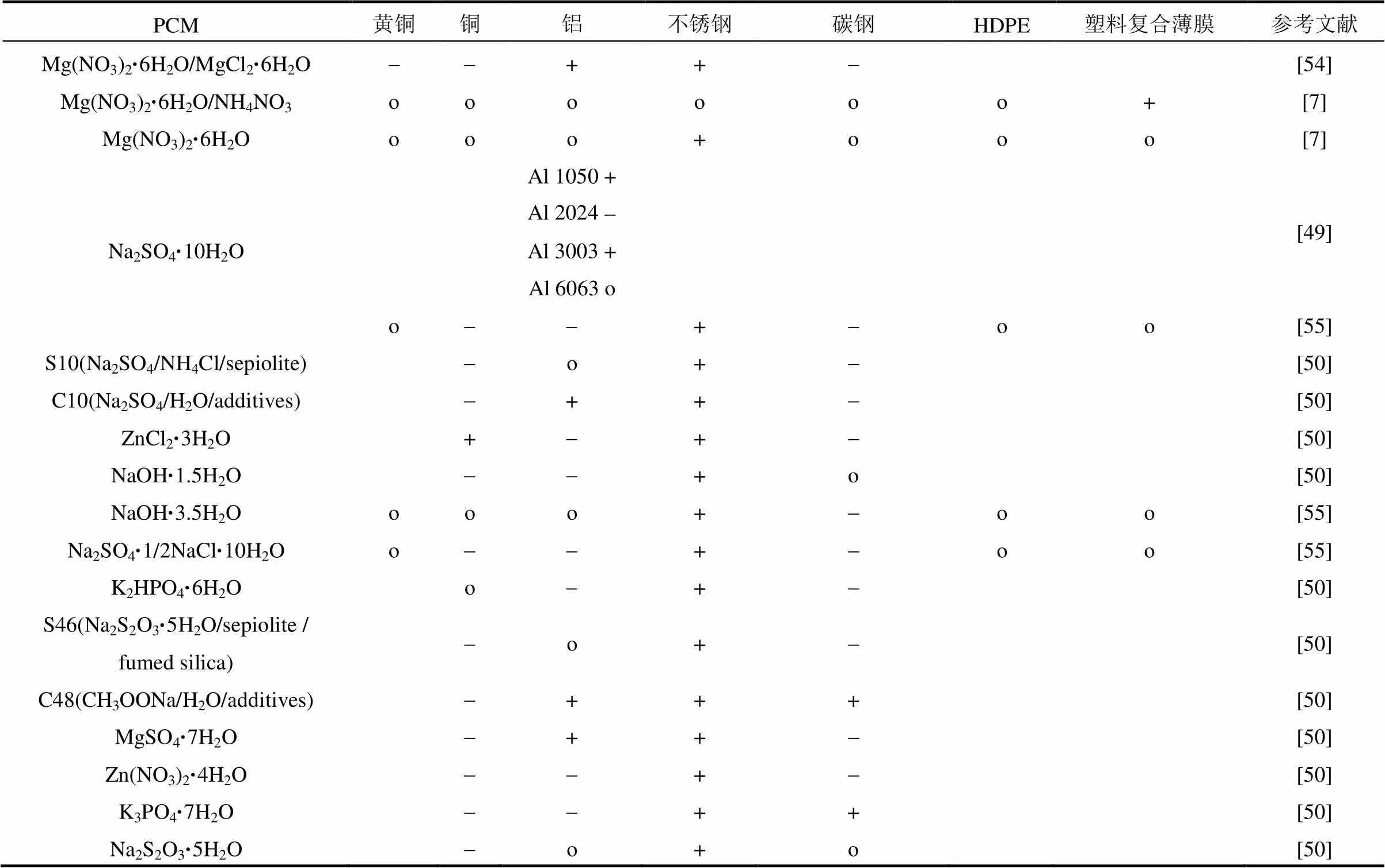
续表6
+耐腐蚀;-有腐蚀性;o无说明
4.4 循环稳定性
由于水合盐相变储能材料存在着过冷、相分离和对容器的腐蚀性等问题,这些问题造成了使用过程中稳定性差,经过一段时间的循环储放热后,相变储能材料会出现逐渐失效的现象。
国外开展水合盐相变储能材料循环稳定性研究工作较早。ZALBA等[53]、RATHOD等[56]、FARID等[57]对水合盐相变材料的长期使用稳定性进行了研究;KENISARIN等[58]提出相变材料应至少能够循环1000次来检验其应用稳定性;TELKS发现Na2SO4·10H2O相变材料的实验寿命最多达1000多次,并预测该相变材料可相变2000次;美国学者MARKS[59]发现随着循环次数的增多,Na2SO4·10H2O的储热能力下降,且在Na2SO4·10H2O中加入成核剂硼砂和增稠剂活性白土经多次循环后其相变潜热还是下降将近50%;KIMURA等[60]对CaCl2·6H2O进行了冷热循环实验,发现含微过量水的CaCl2·6.11H2O( LANE等[62]和PORISIM[55]发现CaCl2·6H2O冷热循环次数能达到5000多次。PORISIM[55]对4种商业水合盐PCM(CaCl2·6H2O、Na2SO4·10H2O、Na2SO4·1/2NaCl·10H2O、NaOH·3.5H2O)进行了循环稳定性的研究。NaOH·3.5H2O、Na2SO4·1/2 NaCl·10H2O分别在循环10次、300次后吸热、放热峰消失了;Na2SO4·10H2O在循环100次性能有所下降且能继续循环2000次;CaCl2·6H2O的循环稳定性最好,循环5650次仍具有吸热、放热峰。 国内,方玉堂等[63]和胡季平[64]分别研究了NaCH3COO·3H2O、Na2SO4·10H2O在成核剂和增稠剂存在情况下的循环稳定性较好,并分析了储放热失效的原因。 水合盐相变储能材料具有储热密度高、导热系数大、相变温度适中、低价易得等优点,具有较好的应用前景。国内外对水合盐相变储能材料开展了大量的研究工作,为其应用提供了科学依据。然而,水合盐作为相变储能材料,仍存在过冷、相分离和对金属容器的腐蚀性问题。虽然许多学者对这些问题进行了大量的研究工作,也提出了不同的解决方法,却没有完全成功解决这些问题。 在水合盐相变材料的实际应用中,除了考虑相变温度和相变焓两个主要问题,其过冷、相分离及循环稳定性问题的研究和解决还需要突破,固-液相变过程有液体产生必须要有容器或其它封装形式封装,并考虑其腐蚀性和对环境的污染问题等。此外,在机理研究方面,水合盐相变材料的过冷、相分离问题及复合相变材料与相图的结合研究仍需要完善与加强。 [1] 赵浩博. 论我国能源结构战略性调整策略[J]. 财经界, 2016(21): 367-368. [2] FARID M M, KHUDHAIR A M, RAZACK S A K, et al. A review on phase change energy storage: Materials and applications[J]. Energy Conversion & Management, 2004, 45(9/10): 1597-1615. [3] 张寅平, 胡汉平, 孔祥冬. 相变贮能-理论和应用[M]. 合肥: 中国科学技术大学出版社, 1996. [4] TELKES M. Thermal storage in salt-hydrates[J]. Solar Materials Science, 1980, 1: 377-404. [5] TELKES M. Thermal storage for solar heating and cooling[C]// Proceedings of the Workshop on Solar Energy Storage Subsystems for the Heating and Cooling of Buildings, USA: Charlottesville, Virginia, 1975. [6] TELKES M. Nucleation of supersaturated inorganic salt solutions[J]. Industrial & Engineering Chemistry, 1952, 44(6): 1308-1310. [7] LANE G A. Low temperature heat storage with phase change materials[J]. International Journal of Ambient Energy, 2011, 1(3): 155-168. [8] LANE G A. Solar heat storage: Latent heat materials. Volume 2. Technology[M]. Florida: CRC Press, 1983. [9] LANE G A. Solar heat storage: Latent heat materials. Volume 1. Background and scientific principles[M]. Florida: CRC Press, 1983. [10] BELTON G, AJAMI F. Thermochemistry of salt hydrates[R]. USA: Pennsylvania University, 1973. [11] GUION J, SAUZADE J D, LAÜGT M. Critical examination and experimental determination of melting enthalpies and entropies of salt hydrates[J]. Thermochimica Acta, 1983, 67(2/3): 167-179. [12] ABHAT A. Low temperature latent heat thermal energy storage: Heat storage materials[J]. Solar Energy, 1983, 30(4): 313-332. [13] KENISARIN M, MAHKAMOV K. Salt hydrates as latent heat storage materials: Thermophysical properties and costs[J]. Solar Energy Materials & Solar Cells, 2015, 145: 255-286. [14] ZALBA B, JOSÉ M A MARÍN, CABEZA L F, et al. Review on thermal energy storage with phase change: Materials, heat transfer analysis and applications[J]. Applied Thermal Engineering, 2003, 23(3): 251-283. [15] DONG O, ZENG D, ZHOU H, et al. Phase change materials in the ternary system NH4Cl+CaCl2+H2O[J]. Calphad, 2011, 35(3): 269-275. [16] LI G, ZHANG B, LI X, et al. The preparation, characterization and modification of a new phase change material: CaCl2·6H2O- MgCl2·6H2O eutectic hydrate salt[J]. Solar Energy Materials and Solar Cells, 2014, 126: 51-55. [17] VOIGT W, ZENG D. Solid-liquid equilibria in mixtures of molten salt hydrates for the design of heat storage materials[J]. Pure and Applied Chemistry, 2002, 74(10): 1909-1920. [18] RAI A K, KUMAR A. A review on phase change materials & their applications[J]. International Journal of Advanced Research in Engineering & Technology (IJARET), 2012, 3(2): 214-225. [19] BAUMANN H, HECKENKAMP J. Latent heat storage materials[J]. Nachrichten Aus Chemie Technik Und Laboratorium, 1997, 45(11): 1075-1081. [20] NAGANO K, MOCHIDA T, IWATA K, et al. Thermal performance of Mn(NO3)2·6H2O as a new PCM for cooling system[C]//5th Workshop of the IEA ECES IA Annex, 2000. [21] DINCER I, ROSEN M. Thermal energy storage: Systems and applications[M]. USA: John Wiley & Sons, 2002. [22] 刘雨时. 严寒地区村镇建筑用无机相变材料的制备与封装[D]. 哈尔滨: 哈尔滨工业大学, 2014. [23] LANE G A. PCM science and technology: The essential connection[J]. ASHRAE Transactions, 1985, 91(2B): 1897-1910. [24] AMES D A. Thermal storage forum: Eutectic cool storage current developments[M]. ASHRAE Journal, 1990: 46-53. [25] 刘剑虹, 刘瑞虹, 王超会, 等. Na2SO4·10H2O 复合相变储能体系的热力学测试[J]. 节能, 2007, 26(9): 13-14. LIU Jianhong, LIU Ruihong, WANG Chaohui, et al. Thermodynamics test of Na2SO4·10H2O phase change compound system[J]. Energy Conservation, 2007, 26(9): 13-14. [26] PEARSON A. Interest growing in heat-eating materials[J]. Construction Research and Innovation, 2011, 2(3): 14-17. [27] FARID M, KONG W J. Underfloor heating with latent heat storage[J]. Proceedings of the Institution of Mechanical Engineers, Part A: Journal of Power and Energy, 2001, 215(5): 601-609. [28] 阮德水, 张太平. 相变贮热材料的DSC研究[J]. 太阳能学报, 1994(1): 19-24. RUAN Deshui, ZHANG Taiping. DSC investigation of phase change materials[J]. Acta Energy Solaris Sinica, 1994(1): 19-24. [29] 阮德水, 张太平. 水合盐相变热长期贮存的研究[J]. 太阳能学报, 1993(1): 16-22. RUAN Deshui, ZHANG Taiping. Study on long-term heat storage using molten salt hydrates[J]. Acta Energy Solaris Sinica, 1993(1): 16-22. [30] 黎厚斌, 胡起柱, 阮德水. NaNO2-NaOAc-HCOONa三元体系相图研究[J]. 华中师范大学学报 (自然科学版), 1995(4): 469-472. LI Houbin, HU Qizhu, RUAN Deshui. Studies on the phase diagram of the ternary system NaNO2-NaOAc-HCOONa[J]. Journal of Central China Normal University (Natural Sicence), 1995(4): 469-472. [31] 刘应江, 罗飙. 常规空调工况分布式相变储能空调系统: CN 103912948A[P]. 2014-07-09. [32] 王志强, 曹明礼, 龚安华. 相变储热材料的种类、应用及展望[J]. 安徽化工, 2005, 31(2): 8-11. WANG Zhiqiang, CAO Mingli, GONG Anhua. Variety application and future of the phased-change material to store the heat[J]. Anhui Chemical Industry, 2005, 31(2): 8-11. [33] LANE G A. Phase change materials for energy storage nucleation to prevent subcooling[J]. Solar Energy Mater. Solar Cells, 1991, 27: 135-60. [34] PILAR R, SVOBODA L, HONCOVA P, et al. Study of magnesium chloride hexahydrate as heat storage material[J]. Thermochimica Acta, 2012, 546(20): 81-86. [35] WADA T, YAMAMOTO R. Studies on salt hydrate for latent heat storage. I. Crystal nucleation of sodium acetate trihydrate catalyzed by tetrasodium pyrophosphate decahydrate[J]. Bulletin of the Chemical Society of Japan, 1982, 55(11): 3603-3606. [36] 阮德水, 李元哲. 相变贮热材料在太阳房中的应用研究[J]. 华中师范大学学报 (自然科学版), 1992(4): 456-460. RUAN Deshui, LI Yuanzhe. Research on the application of phase change materiai in the passive solar house[J]. Journal of Central China Normal University (Natural Sicence), 1992(4): 456-460. [37] 文越华, 张公正, 王正刚, 等. Na2SO4·10H2O复合相变储冷体系的热力学性质[J]. 北京理工大学学报, 1999, 19(6): 778-781. WEN Yuehua, ZHANG Gongzheng, WANG Zhenggang, et al. Thermodynamic properties of sodium sulfate-based complex phase-change cool storage system[J]. Transactions of Beijing Institute of Technology, 1999, 19(6): 778-781. [38] 刘栋, 徐云龙. 成核剂对CaCl2·6H2O相变材料储热性能的影响[J]. 太阳能学报, 2007, 28(7): 732-738. LIU Dong, XU Yunlong. Effect of nucleating agent on thermal properties of CaCl2·6H2O phase change material[J]. Acta Energy Solaris Sinica, 2007, 28(7): 732-738. [39] FEILCHENFELD H, SARIG S. Calcium chloride hexahydrate: A phase-changing material for energy storage[J]. Industrial & Engineering Chemistry Product Research & Development, 1985, 24(1): 130-133. [40] 刘欣, 徐涛, 高学农, 等. 十水硫酸钠的过冷和相分离探究[J]. 化工进展, 2011, 30(s1): 755-758. LIU Xin, XU Tao, GAO Xuenong, et al. Study on supercooling and phase separation of Na2SO4·10H2O[J]. Chemical Industrial and Engineering Prograss, 2011, 30(s1): 755-758. [41] 万福新, 王金波, 杜守琴, 等. 一种六水氯化钙相变蓄能材料组合物: CN 102134473A[P]. 2011-6-18. [42] BISWAS D R. Thermal energy storage using sodium sulfate decahydrate and water[J]. Solar Energy, 1977, 19(1): 99-100. [43] RYU H W, WOO S W, SHIN B C, et al. Prevention of supercooling and stabilization of inorganic salt hydrates as latent heat storage materials[J]. Solar Energy Materials & Solar Cells, 1992, 27(2): 161-172. [44] MARKS S. An investigation of the thermal energy storage capacity of Glauber's salt with respect to thermal cycling[J]. Solar Energy, 1980, 25(3): 255-258. [45] 徐建霞, 柯秀芳. CH3COONa·3H2O相变储能性能研究[J]. 材料开发与应用, 2007, 22(6): 24-27. XU Jianxia, KE Xiufang. An investigation on phase change property of CH3COONa·3H2O as energy storage material[J]. Development and Application of Materials, 2007, 22(6): 24-27. [46] 陈爱英, 汪学英, 曹学增. 相变储能材料的研究进展与应用[J]. 材料导报, 2003, 17(5): 42-44. CHEN Aiying, WANG Xueying, CAO Xuezeng. Research and application of phase change material (PCM) used as energy storing material[J]. Materials Review, 2003, 17(5): 42-44. [47] CABEZA L F, ROCA J, NOGUÉS M, et al. Immersion corrosion tests on metal-salt hydrate pairs used for latent heat storage in the 48 ℃to 58 ℃ temperature range[J]. Materials and Corrosion, 2002, 53(12): 902-907. [48] FARRELL A J, NORTON B, KENNEDY D M. Corrosive effects of salt hydrate phase change materials used with aluminium and copper[J]. Journal of Materials Processing Technology, 2006, 175(s1/2/3): 198-205. [49] GARCÍA-ROMERO A, DELGADO A, URRESTI A, et al. Corrosion behaviour of several aluminium alloys in contact with a thermal storage phase change material based on Glauber's salt[J]. Corrosion Science, 2009, 51(6): 1263-1272. [50] MORENO P, MIRÓ L, SOLÉ A, et al. Corrosion of metal and metal alloy containers in contact with phase change materials (PCM) for potential heating and cooling applications[J]. Applied Energy, 2014, 125: 238-245. [51] SCHRÖDER J. R and D of systems for thermal energy storage in the temperature range from-25 ℃ to 150 ℃[M]. Germany: Springer Netherlands, 1980: 197-200. [52] HEINE D. The chemical compatibility of construction materials with latent heat storage materials[C]//Proceedings of the International Conference on Energy Storage, UK: Brighton, 1981. [53] ZALBA B, JOSÉ M A MARÍN, CABEZA L F, et al. Review on thermal energy storage with phase change: Materials, heat transfer analysis and applications[J]. Applied Thermal Engineering, 2003, 23(3): 251-283. [54] NAGANO K, OGAWA K, MOCHIDA T, et al. Performance of heat charge/discharge of magnesium nitrate hexahydrate and magnesium chloride hexahydrate mixture to a single vertical tube for a latent heat storage system[J]. Appl. Therm. Eng., 2004, 24: 209-220. [55] PORISINI F C. Salt hydrates used for latent heat storage: Corrosion of metals and reliability of thermal performance[J]. Solar Energy, 1988, 41(2): 193-197. [56] RATHOD M K, BANERJEE J. Thermal stability of phase change materials used in latent heat energy storage systems: A review[J]. Renewable and Sustainable Energy Reviews, 2013, 18: 246-258. [57] FARID M M, KHUDHAIR A M, RAZACK S A K, et al. A review on phase change energy storage: Materials and applications[J]. Energy Conversion & Management, 2004, 45(9/10): 1597-1615. [58] KENISARIN M, MAHKAMOV K. Solar energy storage using phase change materials[J]. Renewable & Sustainable Energy Reviews, 2007, 11(9): 1913-1965. [59] MARKS S. An investigation of the thermal energy storage capacity of Glauber's salt with respect to thermal cycling[J]. Solar Energy, 1980, 25(3): 255-258. [60] KIMURA H, KAI J. Phase change stability of CaCl2·6H2O[J]. Solar Energy, 1984, 33(6): 557-563. [61] TYAGI V V, BUDDHI D. Thermal cycle testing of calcium chloride hexahydrate as a possible PCM for latent heat storage[J]. Solar Energy Materials&Solar Cells, 2008, 92(8): 891-899. [62] LANE G A, ROSSOW H E. Reversible phase change compositions of calcium chloride hexahydrate with potassium chloride: US 4613444[P]. 1986-9-23. [63] 方玉堂, 金策, 梁向晖, 等. 三水醋酸钠/甲酰胺复合相变材料的制备及性能[J]. 化工学报, 2015, 66(12): 5142-5148. FANG Yutang, JIN Ce, LIANG Xianghui, et al. Preparation and performance of sodium acetate trihydrate/formamide composite phase change material[J]. CIESC Journal, 2015, 66(12): 5142-5148. [64] 胡季平, 封银平, 郝新民. 十水硫酸钠相变储热材料的使用寿命及失效原因[J]. 新能源, 1990(10): 13-15. Salt hydrate based phase change materials for thermal energy storage—A review 1,2,1,1,1,2,3,1 (1National Engineering Laboratory for Hydrometallurgical Cleaner Production Technology, Key Laboratory of Green Process and Engineering, Institute of Process Engineering, Chinese Academy of Sciences, Beijing 100190, China;2State Key Laboratory of Heavy Oil Processing, College of Chemical Engineering, China University of Petroleum, Beijing 102249, China;3Key Laboratory of Salt Lake Resources Chemistry of Qinghai Province, Qinghai Institute of Salt Lakes, Chinese Academy of Sciences, Xi'ning 810008, Qinghai, China) Salt hydrates based phase change materials (PCMs) have a number of advantages such as high energy density, high thermal conductivity, moderate phase transition temperature and low price, making the materials promising candidates for numerous potential applications and hence a hot research topic over the past decade. This paper reviews and analyses the state-of-the-art development of the salt hydrate based PCMs and summarizes the progress in the thermophysical properties and applications of the materials. Main challenges in the industrial uptake of the salt hydrates based PCMs are supercooling, phase separation and corrosion. The progress and methods in resolving these challenges are discussed. Finally, recommendations are given for further research and applications of the salt hydrates based PCM. salt hydrate; heat storage; phase change materials; stability; corrosion 10.12028/j.issn.2095-4239.2017.0003 TB 34 A 2095-4239(2017)04-623-10 2017-01-11; 2017-04-18。 国家重点研发计划“绿色建筑及建筑工业化”重点专项子课题(2016YFC0700905),江苏省生态建材与环保装备协同创新中心/盐城工学院“用于建筑节能的高效相变保温隔热材料”项目(YCXT201609),柴达木盐湖化工科学研究联合基金项目(U1407105)。 孟令然(1990—),女,硕士研究生,主要研究方向为水合盐相变储能材料,E-mail:lrmeng@ipe.ac.cn; 李建强,研究员,主要研究方向为相变储能材料与储能过程,E-mail:jqli@ipe.ac.cn。5 展 望
