N-取代马来酰亚胺光敏感纳米粒子的制备及其药物可控释放性能研究
2017-07-10余丽丽罗晓民
吴 弟, 余丽丽, 罗晓民
(1.陕西科技大学 轻工科学与工程学院, 陕西 西安 710021; 2.西安医学院 药学院, 陕西 西安 710021)
N-取代马来酰亚胺光敏感纳米粒子的制备及其药物可控释放性能研究
吴 弟1, 余丽丽2, 罗晓民1
(1.陕西科技大学 轻工科学与工程学院, 陕西 西安 710021; 2.西安医学院 药学院, 陕西 西安 710021)
以甲基丙烯酸甲酯(MMA)和呋喃保护的N-羟乙基马来酰亚胺的甲基丙烯酸酯(D)为单体,偶氮二异丁腈(AIBN)为引发剂,含有邻硝基苄基的邻硝基苯乙二醇二甲基丙烯酸甲酯(CL)为光敏感交联剂,通过微乳聚合的方法制备了一种新型光敏感纳米粒子.并以尼罗红(NR)作为模型分子,研究了纳米粒子对脂溶性药物的包载和释放性能.
邻硝基苄基; N-取代马来酰亚胺; 光敏感; 微乳聚合
0 引言
环境敏感型纳米粒子是目前药物载体材料的研究热点之一.根据环境刺激的类别差异,可分为温敏感型[1]、pH敏感型[2]、光敏感型[3]、氧化还原敏感型[4]等各类敏感型纳米粒子.与pH和氧化还原等化学刺激相比,光刺激是一种洁净的外部物理刺激,可控性较强,无需体内化学环境的变化,毒副作用更小[5].光敏感纳米药物载体通常是通过在结构中引入光敏感的化学基团(如偶氮苯、螺吡喃、香豆素等[6]),用波长≤360 nm的高强度的紫外光(6~20 mW/cm-2)[7]刺激来实现其光响应,但存在生物体不能耐受的问题,限制了其实际应用.因此,亟需开发低毒、高效、高响应波长的光敏感药物载体.
据文献报道,邻硝基苄酯(ONB)及其衍生物类光敏感性基团对低强度的光(365 nm、490 nm、719 nm)刺激具有一定的响应性能力[8],并且此类光敏感性基团种类较多,合成简便,光解效果更佳,因而在光敏感药物载体方面具有更高的研究价值[9].同时,临床研究表明,在载体表面引入主动靶向性基团将更有利于药物的定位输送.由于马来酰亚胺在水相环境中可与巯基发生迈克尔加成反应[10,11],可作为药物载体中含巯基的主动靶向性基团的连接点[12],为后续光敏感药物载体的进一步功能化改性提供反应点位.但是由于马来酰亚胺本身可参与自由基聚合[10],因此关于自由基聚合构建的含有马来酰亚胺结构的纳米粒子报道较少.
为此,本实验合成了呋喃保护的马来酰亚胺单体,并将其与ONB类光敏交联剂进行微乳聚合,首次获得了含有马来酰亚胺单体的光敏感纳米粒子,并以尼罗红(NR)为模型分子分析该粒子对于脂溶性分子的低强度紫外光(5 000μW/cm2)的刺激响应性能.为光敏感靶向性药物载体的设计开发提供理论依据和基础实验数据.
1 实验部分
1.1 主要试剂
邻硝基苯乙酮,化学纯,广东翁江化学试剂;甲基丙烯酰氯,97%,萨恩化学技术(上海);氧杂酸酐,生化级,上海阿拉丁生化科技;乙醇胺,分析纯,上海阿拉丁生化科技;甲基丙烯酸甲酯(MMA),分析纯,上海晶纯生化科技.
1.2 制备方法
1.2.1 光敏感交联剂邻硝基苯乙二醇二甲基丙烯酸甲酯(CL)的合成
邻硝基苯乙二醇二甲基丙烯酸甲酯(CL)的合成路线如图1所示.具体的制备方法、表征及性能检测详见参考文献[13].

图1 CL的合成路线
1.2.2 单体D的合成
呋喃保护的N-羟乙基马来酰亚胺(单体B)和呋喃保护的N-羟乙基马来酰亚胺的甲基丙烯酸酯(单体D)的合成路线如图2所示.取氧杂酸酐(单体A)1.0 g(6.0 mmoL)溶于30 mL甲醇中,制成溶液1;另取乙醇胺0.36 mL(6.0 mmoL)加入甲醇2 mL、三乙胺(TEA)0.8 mL(6.0 mmoL),制成溶液2;然后将溶液2滴加到溶液1中,60 ℃搅拌回流3.5 h;冷却至室温,TLC检测(展开剂二氯甲烷(DCM)∶甲醇∶冰乙酸=20∶1∶1),无水Na2SO4干燥,浓缩后用适量的95%乙醇洗涤,干燥得到白色固体状的单体B 0.889 g,产率为71 %.
取单体B 0.515 g(2.464 mmoL)于50 mL圆底烧瓶中,加入适量的四氢呋喃(THF)使其完全溶解,共沸除水,加入15 mL DCM使其完全溶解,冰浴(0 ℃)搅拌,再加入0.58 mL甲基丙烯酰氯和0.54 mL TEA,反应2.5 h,TLC检验(展开剂乙酸乙酯(EA)∶石油醚(PE)=3∶4),用40 mL饱和NaHCO3洗涤三次,无水Na2SO4干燥,浓缩,再以EA∶PE=3∶4为洗脱剂柱层析纯化,得到目标产物白色固体状的单体D 0.533 g,产率为77 %.
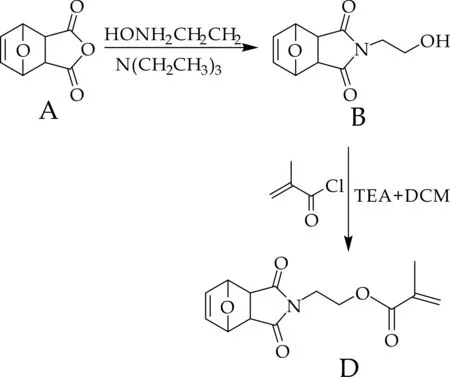
图2 单体B和单体D的合成路线
1.2.3 光敏感纳米粒子的合成
光敏感纳米粒子的合成路线如图3所示.量取40μL甲基丙烯酸甲酯(MMA)于10 mL茄型瓶中,称取10 mg单体D溶于0.5 mL DCM中加入上述反应瓶中,再依次加入质量分数w=5%的AIBN的DCM溶液10 uL、CL 2.5 mg、蒸馏水5 mL、十二烷基硫酸钠(SDS)0.5 mg,超声处理(1 200 W,2 s超声,2 s间歇)3 min,转移至厚壁耐压瓶中通N25 min后升温至80 ℃搅拌6 h.冷却至室温,敞口搅拌过夜,使DCM自然挥发,用水透析24 h(每2 h换一次透析液)后,最终将产物冷冻干燥,制得白色光敏感纳米粒子.
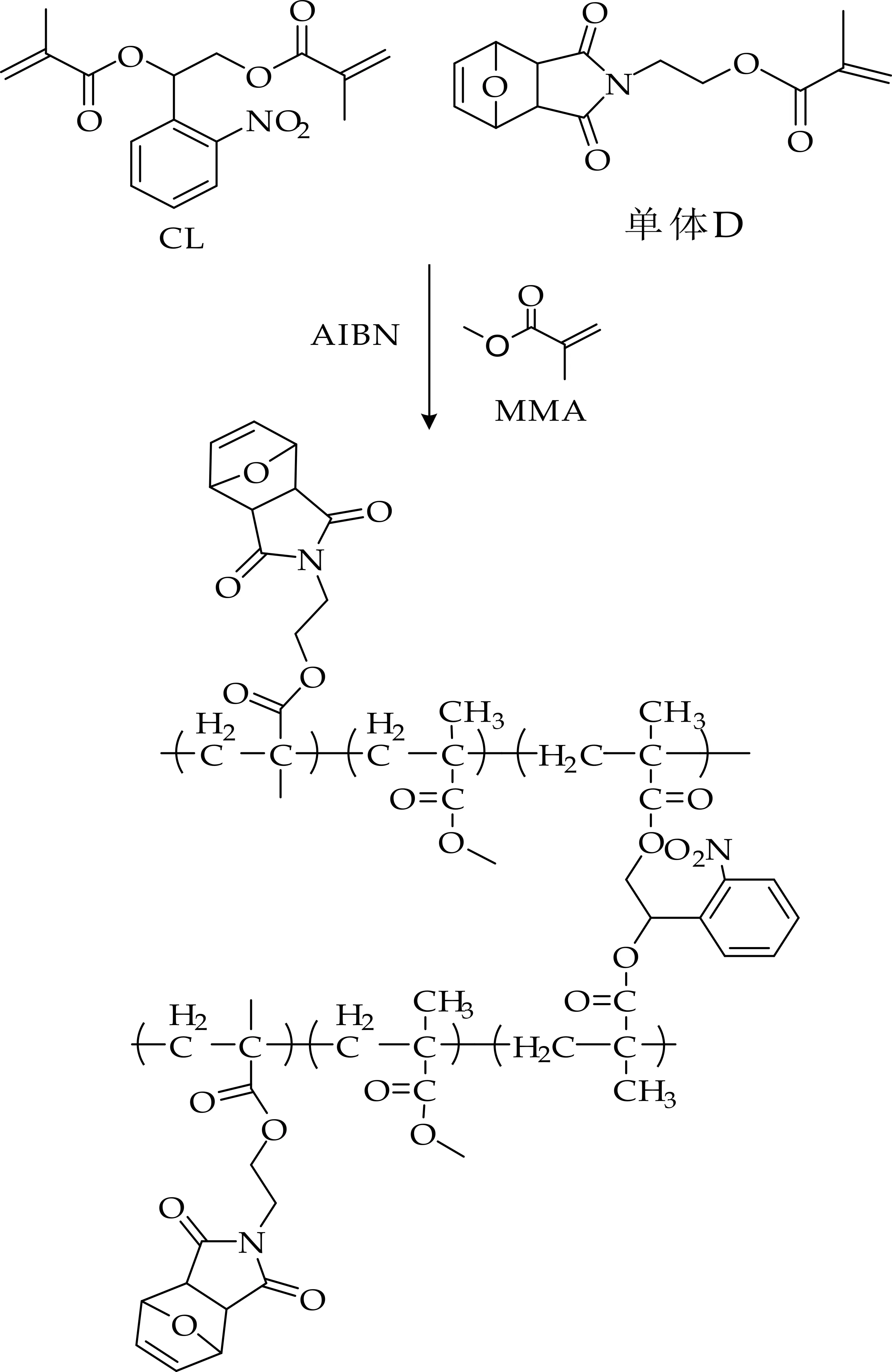
图3 光敏感纳米粒子的合成路线
1.2.4 载NR光敏感纳米粒子的合成
精确称取NR 4 mg于10 mL容量瓶中,用THF溶解并定容至10 mL配制NR母液备用.量取50μL MMA于10 mL称量瓶中,量取120μL NR母液溶于0.5 mL DCM中加入上述称量瓶中,再依次加入w=5%的偶氮二异丁腈(AIBN)的DCM溶液10μL、CL 2.5 mg、蒸馏水5 mL、SDS 0.5 mg,超声处理(1 200 W,2 s超声,2 s间歇)3 min,转移至厚壁耐压瓶中通N25 min后升温至80 ℃搅拌6 h,冷却至室温,打开瓶盖,过夜,待DCM挥发完,透析冷冻干燥,制得包载NR的光敏感纳米粒子.
1.3 检测及表征
1.3.1 结构表征
核磁共振氢谱(1H-NMR):AVANCEⅢ 400MHz核磁共振仪,德国Bruker公司,溶剂为氘代氯仿(CDCl3);红外光谱(FT-IR):TENSOR27,德国Bruker公司;场发射扫描电镜(SEM):S4800型,日本理学公司;紫外光源:B-100AP紫外灯(365 nm),美国UVP公司.
1.3.2 载NR纳米粒子的光敏感性能测试
用美国Perkin Elmer公司LS55荧光分光光度计测试样品的荧光光谱.将制备好的载NR纳米粒子取1 mL超声10 min充分分散,先用紫外灯(365 nm)照射0 min、0.5 min 、1 min、 2 min、 4 min、 8 min、15 min后分别扫描三个样品的荧光发射,其中激发波长为557 nm,狭缝值Ex=10、Em=6,波长范围为580~700 nm.
2 结果与讨论
2.1 单体D的结构表征
单体D的1H-NMR谱见图4所示.由图4可知,δ=6.50处为2、3双键上的2个H信号(为单峰);δ=6.05、δ=5.54两处单峰为10位置双键上的氢信号,由于存在双键的立体异构,因此该处的峰出现在两个不同的化学位移上;δ=5.24处为醚键连接的1,4两个位置上的H信号;δ=4.26附近为8处H的信号,与反应物相比该处的信号向低场移动明显,证明了酯键的生成;δ=3.80附近为酰胺键连接的7处的H信号,该处与反应物相比没有显著的变化;δ=2.85处为5、6两个对称位置的H信号;δ=1.88处出现了9位置的甲基信号.因此1H-NMR表征结果显示得到的单体结构符合预期.

图4 单体D的1H-NMR谱图
2.2 光敏感纳米粒子的结构表征
2.2.1 FT-IR分析
图5为纳米粒子的红外谱图.由图5可知,3 446.2 cm-1处为D基团的-NH的吸收峰,2 935.6 cm-1处为CL基团和D基团的-CH3吸收峰,1 728.1 cm-1为CL基团和D基团中羰基C=O键的吸收峰,1 576.1 cm-1处的吸收峰为NO2中N=O双键的振动吸收区域,1 447.4 cm-1处是甲基的变形振动吸收峰,1 134.9 cm-1处是醚键C-O-C的吸收峰.

图5 纳米粒子的红外光谱图
图6为不同光照时间下纳米粒子的红外图谱.由图6可知,在1 730.9 cm-1处为缔合的羧基C=O双键的吸收峰,随光照时间的增加强度增大C=O双键的强度增加,而且在983.1 cm-1处出现的新峰为羧基的-OH峰吸收佐证了羧基的存在,所以光照裂解形成了羧酸,在1 576.1 cm-1处的吸收峰为NO2中N=O双键的振动吸收区域,吸收峰随光照时间的增长而逐渐消失,可能是由于苯环上的NO2的裂解发生变化而引起的,1 454.1 cm-1为NO的红外吸收区域,1 272.4 cm-1和1 339.2 cm-1两个位置处出现新峰可以归属为芳香胺的C-N特征吸收峰,从而证明了苯环上的NO2在光照后生成NO.

图6 纳米粒子在紫外光照射下的红外光谱图
2.2.2 SEM形貌观察
图7为纳米粒子光照前后的SEM图.由图7可知,该实验获得的纳米粒子粒径分布较为均匀,球形较为完整,但是存在着一些黏连的现象需要改善.光照后,纳米粒子有部分结构的坍塌,粒子之间的黏连现象更加显著.

(a)光敏感纳米粒子的光照前SEM图

(b)光敏感纳米粒子的光照后SEM图图7 光敏感纳米粒子的SEM图
2.3 光敏感纳米粒子NR包载与释放
图8(a)、(b)和(c)分别为含CL 5%、15%和25%的载NR纳米粒子随光照时间的荧光图谱.NR是一种脂溶性荧光分子,当其被包载于粒子的核心时,体系显示较强的荧光,而当其被释放进出水相后,NR沉降出来,荧光强度快速下降.从图8可以直观地看出,光照可加快NR的释放,相同光照时间对不同浓度CL的纳米粒子影响不同.由此可见,该粒子可用于脂溶性药物的包载与光控释放.

(a)CL比例为5%的载NR纳米粒子光照后荧光图谱

(b)CL比例为15%的载NR纳米粒子光照后荧光图谱

(c)CL比例为25%的载NR纳米粒子光照后荧光图谱

(d)不同比例CL的纳米粒子对应的NR释放比率图8 不同比例CL的载NR纳米粒子光照后荧光图谱以及NR释放比率
图8(d)为不同交联度的载NR纳米粒子在光照过程中的NR释放动力学曲线.由图8(d)可知,在低强度UV(365 nm,5 000μW/cm2)照射下,NR被持续快速的释放;照射后大约30 s内,有大约30%~50%的NR被释放,照射15 min后大约70%~90%的NR被释放,表明这种纳米粒子具有较高的光敏感性和释放效率.
交联剂是粒子药物光控释放能力的一个重要影响因素.当交联剂含量小于15%时,15 min的光照可引起80 %以上的药物释放,当其交联剂含量达到25%时,其15 min光控释放效率达到90%以上.但是由于本实验前期只对比了交联剂为15%以下的样品,因此选择了交联剂含量较少的样品(5%)为主要研究对象,建议后期的实验可重点考察高浓度交联剂情况下粒子的各项性能.
3 结论
(1)实验合成了呋喃保护的含马来酰亚胺的单体D.
(2)通过微乳聚合的方法,首次合成了含有马来酰亚胺基团的光敏感型纳米粒子药物载体,为后期含巯基的功能性基团的引入奠定了基础,可实现光敏感纳米粒子的功能多样化.
(3)这种纳米粒子对NR光控释放性能的研究有效地证明了该纳米粒子具有较高的光敏感性和释放效率,并且可控性良好,对生物体伤害较低,可以实现药物快速、高效、安全、按需释放的目的,从而有效提高药物的利用率.
[1] Kohori F,Sakai K,Aoyagi T,et al.Preparation and characterization of thermally responsive block copolymer micelles comprising poly (N-isopropylacrylamide-b-DL-lactide)[J].Journal of Controlled Release,1998,55(1):87-98.
[2] 邢 洋.低分子肝素pH敏感巯基壳聚糖纳米粒的研究[D].太原:山西医科大学,2014.
[3] Chen L,Wang W,Su B,et al.A light-responsive release platform by controlling the wetting behavior of hydrophobic surface[J].Acs Nano,2014,8(1):744-751.
[4] Li Y L,Zhu L,Liu Z,et al.Reversibly stabilized multifunctional dextran nanoparticles efficiently deliver doxorubicin into the nuclei of cancer cells[J].Angew Chem Int Ed Engl,2009,48(52):9 914-9 918.
[5] Wang H C,Zhang Y,Possanza C M,et al.Trigger chemistries for better industrial formulations[J].ACS Applied Materials & Interfaces,2015,12(7):6 369-6 382.
[6] Jiang Z,Li H,You Y,et al.Controlled protein delivery from photosensitive nanoparticles[J].Journal of Biomedical Materials Research Part A,2015,103(1):65-70.
[7] Chung Sung Lee,Kun Na.Photochemically triggered cytosolic drug delivery using pH-responsive hyaluronic acid nanoparticles for light-induced cancer therapy[J].Biomacromolecules,2014,15(11):4 228-4 238.
[8] Bagheri A,Yeow J,Arandiyan H,et al.Polymerization of a photocleavable monomer using visible light[J].Macromolecular Rapid Communications,2016,37(11):905-910.
[9] 莫 斌.光断裂型支化和嵌段接枝共聚物的合成及性能研究[D].苏州:苏州大学,2015.
[10] 卢彦兵,孙荣欣,孙丽丽,等.基于RAFT过程的N-(4-羧基苯基)马来酰亚胺和苯乙烯可控自由基共聚合[J].高分子材料科学与工程,2009,25(3):39-41,45.
[11] Hermanson G T.Bioconjugation techniques[M].New York:Academic Press,2008:183.
[12] 周 杰.马来酰亚胺聚谷氨酸天冬氨酸靶向肽聚合物药物载体系统的建立与应用[D].上海:华东师范大学,2013.
[13] 余丽丽.光敏纳米药物载体制备及其性能研究[D].西安:陕西科技大学,2011.
【责任编辑:蒋亚儒】
Study on synthesis and control release of N-substituted maleimide photosensitive nanoparticle
WU Di1, YU Li-li2, LUO Xiao-min1
(1.College of Bioresources Chemical and Materials Engineering, Shaanxi University of Science & Technology, Xi′an 710021, China; 2.Department of Pharmacy, Xi′an Medical University, Xi′an 710021, China)
A novel type of photosensitive nanoparticles were prepared by a microemulsion polymerization process,using methyl methacrylate (MMA) and furan protected methacrylate N-hydroxyethyl maleimide (D) as monomers,2,2-azobisisobutyronitrile (AIBN) as initiator,O-nitrophenyl ethylene glycol dimethacrylate (CL) containing O-nitrobenzyl as photosensitive cross-linker.Package load capacity and the light controlled release ability of this nanoparticles for liposoluble drugs were studied using Nile red (NR) as the model molecules.
O-nitrobenzyl; N-substituted maleimide; photo sensitive; microemulsion polymerization
2017-01-21
陕西省教育厅产业化培育计划项目(16JF003)
吴 弟(1988-),男,安徽滁州人,在读硕士研究生,研究方向:光敏感纳米药物载体
2096-398X(2017)04-0016-05
O625.61
A
