基于科学取向教学论的概念课型教学实践
2017-07-07郑丽瑜
郑丽瑜

科学取向教学论对教学实践的重要贡献,就是它认识了不同类型的学习与教学策略、教学评价之间的必然联系。根据该教学论可将现有中学化学课堂教学分为如下几类课型:元素化合物课、概念课、原理课、基本技能课、高级技能课、复习课等。
其中,概念课的教学具有三个显性的教学任务:
1.知道概念是什么(名称、定义、属性和例证分析);
2.运用概念去办事(分类、属性的运用);
3.辨明新概念与有关概念的关系,形成概念系统。
因此,根据概念课的显性教学任务,我们在设计教学环节时一般按照以下的顺序。
1.获得概念:提供尽可能充足的实验事实或数据或经验,加以归纳、概括形成概念。或通过复习原有概念,并分析与新概念的关系,用演绎的方法形成概念。
2.明确概念的适用范围和条件:初步建立概念后,通过解释、判断正或反例、主动举例等变式训练,理解概念的本质属性,明确其适用范围和条件等。
3.运用概念对外办事:通过在新的情景中运用概念进行分类或解释、比较新旧概念、运用概念的属性作出推论等变式训练,巩固、内化新概念,形成概念系统。
本文是基于科学取向教学论的理论指导,对人教版必修2《原电池》的教材内容与学生学习能力起点、教学目标(终点)等进行分析,通过创设情境,激发学生兴趣;提供验证实验,习得原电池概念,理解原电池的工作原理;通过科学探究,总结构成原电池形成的条件,力图帮助学生在学习原电池相关知识的过程中,培养运用原电池相关知识解决问题的能力。
一、教学背景分析
1.教材分析
原电池原理是中学化学重要基本理论之一,从反应物之间电子转移的角度看,原电池概念的形成是氧化还原反应本质的拓展和应用;从思维角度看,“将化学能直接转化为电能”的思想,是对火力发电的原理“化学能一热能一机械能一电能”思维方式的反思和突破。
2.学生分析
经过一年半化学的学习,学生已经掌握了金属的活动性顺序,氧化还原反应等相关知识,学生也已经具备了一定的基础知识和分析问题、解决问题的能力。
同时由于原电池学生第一次接触学习,学习上力求激发兴趣,不宜马上拓展。
二、教学目标分析
课标要求:《化学课程标准》对于原电池的要求描述是:举例说明化学能与电能的转化关系及其应用。
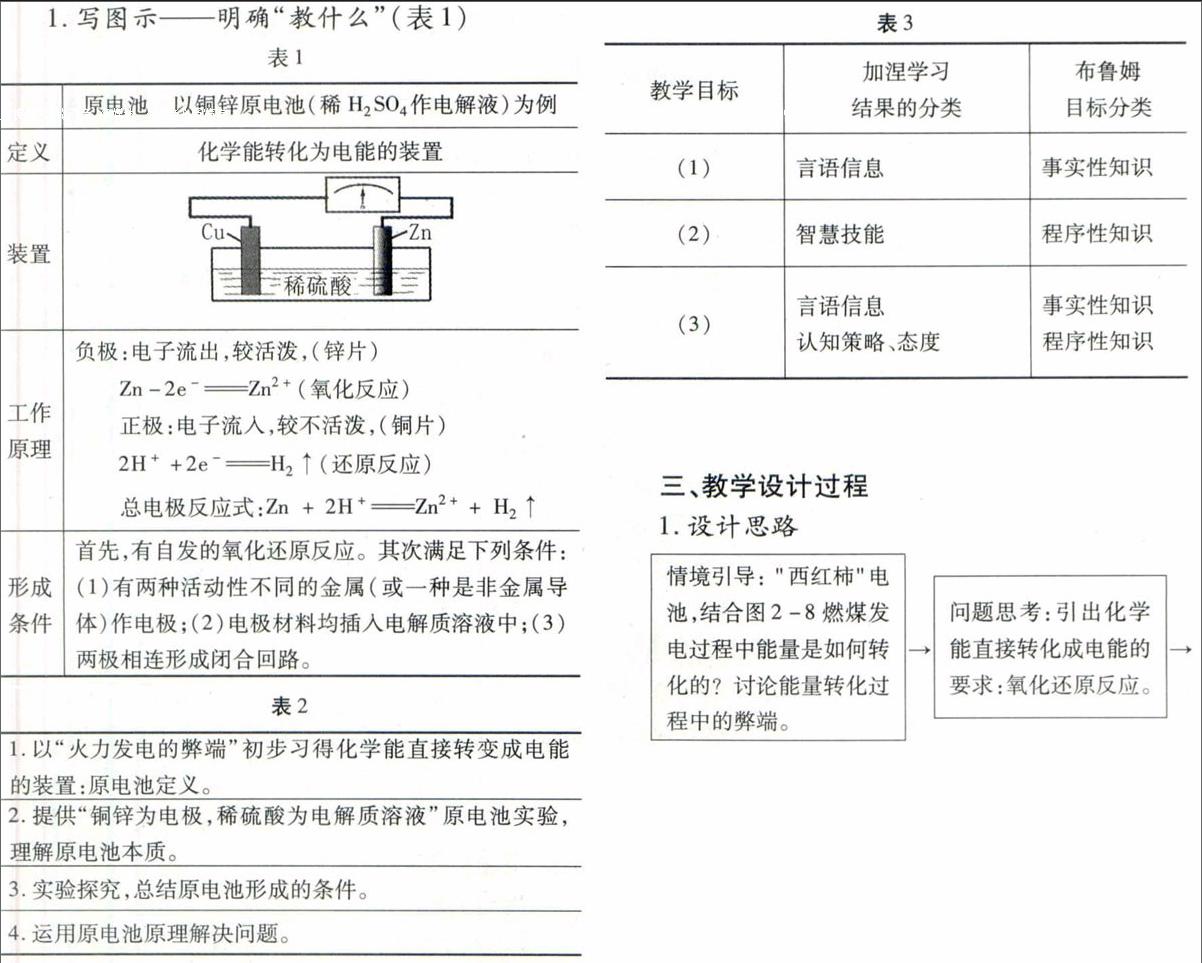
1.写图示——明确“教什么”(表1)
2.定内容,析途径——确定教学方法和学习途径
根据图式,本节课主要学习原电池定义(命题学习)、原电池原理(宏观一微观一符号三重表征学习)、原电池形成条件(实验归纳途径学习)。
3.清序列——确定教学顺序
(1)写出主要结论和建立的逻辑过程(见表2)
(2)获得结论的途径
学生学习经历遵循实验归纳途径:提出问题、假设猜测、规划研究方案、设计实验、执行实验、处理数据、获得结论等环节。
4.教学目标的设置
科学取向教学论强调目标的导学、导教和指导测量和评价的作用。为此,教学目标设置要简明、精要,可以观察和测量。教学目标应陈述预期学生学习的结果,用学生通过学习后会做什么(技能)和会说什么(知识)来陈述目标。本节课的教学目标设置如下:
.
(1)了解原电池的定义:知道火力发电的原理是将化石燃料燃烧放出的能量(即化学能)先转变为机械能再转变为电能,知道原电池是化学能转化为电能的装置。
(2)理解原电池的工作原理:能以铜锌原电池(稀H:SO4作电解液)为例,从宏观(实验现象)——微观(线路中电子、溶液中离子流动的方向分析)——符号(电极反应式)三重表征,判断正负极,正确规范书写电极反应方程式。
(3)通过探究实验,能说出原电池形成的条件,会判断原电池装置图,了解对比实验在科学探究中的运用,学会控制实验条件的研究方法。
5.知识类型分析(见表3)
综上,本节课属于概念课的范畴。以下是教学实践过程。
2.教学流程
环节一:获得概念
通过火力发电初步习得化学能可以转化为电能。
[引入]展示“西红柿”电池(激发兴趣和探究欲望),沒有电,为何灯泡会亮呢?
[讨论]物质中的化学能有无可能转化为电能呢?又是如何转化的?今天我们一起来学习原电池。首先我们看课本第40页,通过图2—7,我们可以了解到我国目前发电总量构成中,火电仍居榜首。结合图2-8燃煤发电过程中能量是如何转化的?
[提问]上述能量转化过程有何弊端?
[小结]环境污染,转化步骤多、损失大,有无化学能直接转化为电能的装置?
[师生小结]原电池的定义:我们把化学能转化为电能的装置叫做原电池
设计意图:以一个水果电池进行课堂引入,马上抓住了学生的注意力,激起学生的兴趣,唤起其好奇心。后续提供了火力发电的弊端,引导学生选择一种能将化学能直接转化为电能的化学反应,然后提出原电池概念,水到渠成。
环节二:明确概念的适用范围和条件
提供实验事实,理解原电池的工作原理(宏观一微观一符号三重表征学习)
[提问]要将化学能直接转化成电能,必须要选择合适类型的化学反应。电流是电子的定向移动引起的,在前面学过的哪种反应类型有电子的转移?
[学生回答]氧化还原反应。
[过渡]要想使氧化还原反应释放的能量不通过热能直接转变为电能,就要设计一种装置,使氧化反应和还原反应分别在两个不同的区域进行,并使其间的电子转移,在一定条件下形成电流。
宏观:
[演示实验]实验2-4:将锌片和铜片用导线连接(导线中间接入一个电流表),平行插入盛有稀硫酸的烧杯中,观察现象并准确记录。
微观:
[提问]第41页《学与问》:根据你所了解的电学知识,你知道电子是怎样流动的吗?你如何判断装置的正、负极?
[学生回答]电子从负极流向正极,电流表指针偏向的是正极。
[教师设疑]1.铜不与稀硫酸反应,铜片上的气体是哪里来的?
2.氢离子转变为氢气所需的电子从何而来?
讨论结果预设:锌失去的电子通过导线转移到铜片上,氢离子在铜片上得电子转变为氢气;
电流计指针偏转说明导线中有电子流过,证明氢离子得到的电子确实是锌片失去,通过导线传递到铜片上的。
设计意图:我们发现电流表的指针发生偏转,说明产生了电流,通过实验,引导学生从三重表征学习原电池的工作原理,过程中从实验现象中设计疑问,让学生更深刻理解原电池工作原理。
环节三:明确概念的适用范围和条件
通过实验探究,总结原电池形成的条件(实验归纳途径学习)
提出问题:
[过渡]原电池的发明实现了化学能和电能的直接转化,怎么判断一个类似的装置能否组成原电池?(能否有电流产生)
猜想、设计方案并实验:
[学生活动]第41页“科学探究”,学生自行从给定的实验用品中选择组成原电池,画出电池装置示意图。根据小组画出的示意图进行实验,讨论哪些装置可以形成原电池。(使学生学会控制实验条件的方法,探究原电池的组成条件)
实验用品:锌片、铜片、铁片、石墨电极各两套,导线、金属夹、灵敏电流表、稀硫酸、酒精溶液、烧杯。
[講解]根据学生可能的实验结果cu-zn、Cu-Fe、Cu-C、Cu-Cu、Zn-Fe、Zn-C、Zn-Zn、Fe-c、Fe-Fe、C-C等可能组合进行分析,得出可形成原电池的装置。
思考讨论与处理数据:
[思考与交流]通过以上实验,原电池应由哪几部分构成,各起什么作用?构成一个原电池需要哪些条件?(教师还可以根据学生提出的实际情况进行更深的探讨,在探究中点燃学生思维的火花。)
得出结论:[小结]组成原电池的条件:应由有两种活动性不同的金属(或一种是非金属导体)作电极;电解质溶液提供离子移动;导线,使两极相连形成闭合电路。相对活泼的金属做负极。
[教师强调]构成原电池的条件:两极一液成回路。
设计意图:这是课本的科学探究,按照实验归纳学习的途径,通过让学生自主设计原电池装置,分析归纳总结出原电池形成的条件,培养学生思考和探究的思维能力。此环节可以按照学生的水平层次,教师可进行改进。
环节四:运用概念对外办事
运用原电池原理解决问题
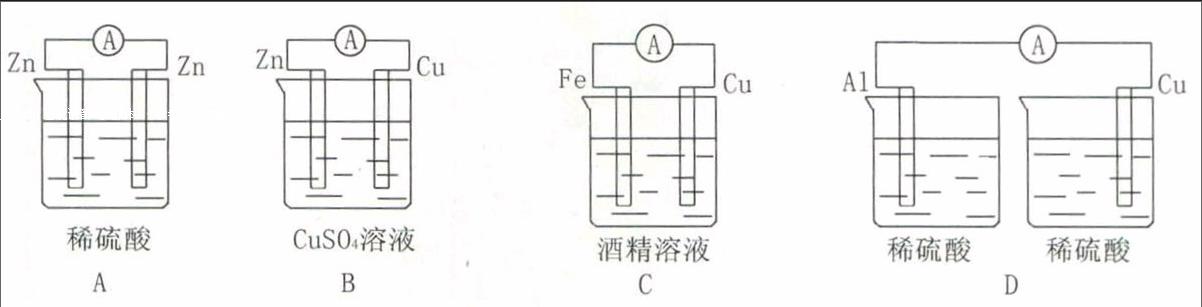
1.下列各装置中能组成原电池的是( )
2.“西红柿”电池中灯泡为何亮了?
3.故事:在伦敦的上流社会,有一位贵族夫人格林太太,她有一口整齐洁白的牙齿。但其中镶有两颗假牙:一颗是黄金的一这是格林太太富有的象征;另一颗是不锈钢的(这是一次车祸留下的痕迹)。
令人百思不解的是:打从车祸以后,格林太太经常头疼,夜间失眠,心情烦躁……尽管一些国际上知名的专家教授绞尽脑汁但格林太太的病症未能有丝毫的减轻,而且日趋严重……她的病真的就没治了吗?
后来是一位化学家解除了她的痛苦。通过这节课的学习,你能知道是怎么一回事吗?
设计意图:通过对原电池的学习,运用所学知识解决生活中的问题,学以致用,培养学生解决问题的能力,体现化学学科的价值,生活处处是化学。
[课堂小结]
四、教学实践反思
本教学实践研究,在科学取向教学论的指导下,通过理论与实践结合,以“原电池”的教学实践为例,总结出中学化学概念课型的一般教学规范。同时,课堂教学有差异性,科学取向教学论是个“理念”,它必将要求教师在根据实际的学情和教学内容上进行调整,吃透教材和课标,确定好教学目标,进行符合学生认知水平的教学设计,实施有效教学。
笔者向部分学生了解了上课后的感受与收获,大部分学生都提到一点,就是这些原来感觉复杂的概念,现在变得简单且易懂。科学取向教学论指导下的概念课课型通过获得概念、明确概念和运用概念这三步,帮助学生更好地去掌握概念。在教学设计中,既要能够有效解决问题,也要能够让学生容易掌握,关键在于如何去设计解决问题的操作步骤。
