磨玻璃结节肺腺癌CT征象与病理分类及EGFR、ALK基因突变相关性的研究进展
2017-07-07肖旻徐秋贞
肖旻,徐秋贞
(1.东南大学 医学院,江苏 南京 210009; 2.东南大学附属中大医院 放射科,江苏 南京 210009)
·综 述·
磨玻璃结节肺腺癌CT征象与病理分类及EGFR、ALK基因突变相关性的研究进展
肖旻1,徐秋贞2
(1.东南大学 医学院,江苏 南京 210009; 2.东南大学附属中大医院 放射科,江苏 南京 210009)
肺癌是最常见的恶性肿瘤之一,其中以肺腺癌最为高发,其不同组织亚型的临床特点、影像表现、病理学和基因学特征各不相同。2011年2月,国际肺癌研究学会(IASLC)、美国胸科学会(ATS)和欧洲呼吸学会(ERS)公布了肺腺癌的国际多学科分类。根据此分类法,我们将从磨玻璃结节肺腺癌的病理分类与CT征象的相关性,以及肺腺癌EGFR、ALK基因突变与CT征象相关性两方面入手,作一综述。
肺腺癌; 磨玻璃结节; 表皮生长因子受体; 间变性淋巴瘤激酶; 文献综述
肺腺癌是最常见的肺癌组织亚型,无论吸烟与否,患者诊断肺癌后的平均5年生存率是17%[1],肺腺癌患者预后与切除肺叶的组织病理学侵袭性直接相关[2]。肺腺癌的CT征象与其病理学及生物学特性有十分密切的关系,对临床诊断、治疗及预测肺腺癌的转归有重要价值。
肺腺癌表皮生长因子受体(epidermal growth factor receptor,EGFR)和间变性淋巴瘤激酶(anaplasticlymphoma kinase,ALK)是目前已知的肺腺癌的主要突变基因。基因与影像检测相结合的手段不仅可以客观解释肿瘤影像学表现的多样性和复杂性,并且可预测某些特征影像表现与基因的相关性。作者就近年来肺腺癌CT征象与病理学分类及EGFR、ALK基因突变相关方面的研究进展作一综述。
1 肺腺癌的分类
肺腺癌的病理分类不断被更新,同时其他如影像学、基因学、肿瘤学等相关学科的发展使人们对肺腺癌的认识逐步加深。2011年,国际肺癌研究学会(IASLC)、美国胸科学会(ATS)和欧洲呼吸学会(ERS)公布了多学科肺腺癌分类,该分类建议完全废止细支气管肺泡癌,将其划入新增的亚型里[3]。新分类将肺腺癌分为4类,分别为浸润前病变、微浸润性腺癌(minimally invasive adenocarcinoma,MIA)、浸润性腺癌(invasive carcinoma,IPA)以及变型。不典型腺瘤样增生(atypical adenomatous hyperplasia,AAH)及原位癌(adenocarcinoma in situ,AIS)归于浸润前病变。
2 磨玻璃结节(GGN)肺腺癌的病理学分类与CT征象
2.1 AAH
1999年,WHO首次提出了AAH的概念,它提出,AAH是一个局限于肺泡和呼吸细支气管的立方或柱状上皮细胞层的不典型增生,是一种浸润前的病变[4]。Yokose等[5]研究发现,554名肺癌患者中有12%的病人被发现AAH。AAH在CT上的典型表现是无实性成分的微弱GGN,即一个典型的边界清楚的椭圆形或圆形病灶[6]。它可以是孤立病灶,也可以是多病灶,通常小于5 mm,也有病例报道有2 cm大小的AAH[7]。磨玻璃密度提示肺泡隔内肺泡壁细胞不典型增生。有文献表明,纯GGN不一定是AAH,因为AIS和腺癌可具有相同的外观[8]。
2.2 AIS
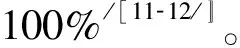
2.3 MIA
2011年新分类定义MIA为浸润深度5 mm,但大小≤3 cm的肺腺癌。虽然其生长方式仍以贴壁为主,但在CT中,这些基质浸润的部分表现为实性结节中的小实性成分。Yim等[13]对21名组织病理学诊断为BAC(微小浸润0~5 mm混合亚型,基本上相当于MIA)的患者进行随访发现其5年生存率为100%。2009年,Maeshima等[14]报道了122名诊断为BAC(0~5 mm浸润)的病人术后5年生存率为100%。近期,Kadota等报道了2名AIS患者和34名MIA患者术后未复发[15]。综上,大量研究表明MIA患者的术后生存率较高。
2.4 IPA
Yoshizawa等[2]研究发现,切除的肺腺癌组织中,绝大多数是IPA。对IPA进行分类的困难之处在于其组织学生长的广泛异质性。新分类根据IPA的主要生长模式,将其分为贴壁生长为主、腺泡为主、乳头状为主、微乳头状为主或具有黏液产生的实性为主4个类型。以前归类为黏液性BAC在新分类中定义为浸润性黏液腺癌。有学者认为,浸润性黏液腺癌和其他亚型的肺腺癌在遗传学上是截然不同的,这与KRAS突变及HNF4α表达水平上调有关[16]。
IPA的CT表现取决于优势亚型,但由于其浸润性,多数结节中有实性成分,这与组织病理学中看到的>5 mm明显浸润相对应[3]。与此类似,贴壁生长为主腺癌中的磨玻璃成分与肿瘤的非浸润成分相对应。除此以外,尚未有研究提出IPA亚型间CT表现的不同之处。
近年来,使用成像技术来预测肺腺癌的浸润性成为新的研究热点。一些研究发现,在CT上,结节实性部分的大小比结节的总大小更能预测肺癌患者的预后[17]。空气支气管征的存在显著提示病灶为IPA而非MIA[18]。尽管如此,MIA与IPA之间的差异并不总是很显著。尽管结节内部存在大的实性成分提示IPA可能大,有人发现当病灶>16.4 mm时,纯GGN更有可能是IPA[18]。
2.5 CT征象与病理分类的相关性
吴芳等[19]研究发现,将肺腺癌患者胸部CT中病灶的流行病学与影像学特征如位置、大小、形状、密度、空泡征等与其病理亚型AAH、AIS、MIA及IPA作对照,得出病灶大小、密度、空泡征的有无以及边缘情况差异有统计学意义(P<0.05),而其他如性别分布、年龄大小、空气支气管征等则差异无统计学意义。随着AAH到IPA的恶性程度的增加,病变体积增大、密度增加,空泡征、分叶征、毛刺征出现的概率也显著增加。
3 EGFR基因突变的相关研究
有研究[20]发现,女性腺癌患者中,非吸烟者EGFR基因突变发生率较高。就分化程度而言,Liu等[21]报道原发性肺腺癌中中、低分化者突变率低于高分化者。一般情况下,肿瘤分化程度越高,预后越好,这表明利用EGFR突变检测阳性率判定肺癌的预后与组织学上根据肺癌细胞分化程度判定肺癌的预后具有一致性。Hong等[22]对肺癌患者的CT分析发现,EGFR突变组与未突变组的CT征象(包括大小、形状、边界、增强程度、空气支气管征、毛刺征)没有显著差异,而EGFR突变腺癌患者CT中的GGN所占比例明显高于EGFR未突变腺癌患者。Rizzo等[23]对突变组和未突变组的肺腺癌患者进行对比,内容包括病灶所在的肺叶、直径、形状、边缘、磨玻璃成分、密度、空洞、空气支气管征、胸膜增厚、肿瘤内坏死、病灶所在的肺叶内结节、非病灶所在的肺叶内结节、胸膜凹陷征、病灶部位、钙化、气肿、纤维化、胸膜渗出的CT征象,结论为两组患者空气支气管征和胸膜凹陷征差异有统计学意义(P<0.05),即这两种征象在EGFR基因突变组出现的可能性大于未突变组,其余CT征象在两组间差异无统计学意义。另有研究表明,有EGFR基因突变的患者肺内GGN生长更快[24]。
4 ALK基因突变的相关研究
ALK是一种酪氨酸激酶受体,其突变很罕见,但在临床晚期肺腺癌的年轻患者中较常见,这些患者通常无吸烟史[25]。Rizzo等[23]对ALK突变组和未突变组的肺腺癌患者进行对比研究,内容包括病灶所在的肺叶、直径、形状、边缘、磨玻璃成分、密度、空洞、空气支气管征、胸膜增厚、肿瘤内坏死、病灶所在的肺叶内结节、非病灶所在的肺叶内结节、胸膜凹陷征、病灶部位、钙化、气肿、纤维化、胸膜渗出的CT征象,得出两组中胸腔积液差异有统计学意义(P<0.05),即ALK基因突变组出现胸腔积液的可能性大于未突变组。这与Yamamoto等[26]研究的结论相似,认为大量胸腔积液与ALK基因突变存在相关性。
5 结 语
综上所述,肺腺癌的CT征像与其病理分类之间有密不可分的关系,不同病理亚型的肺腺癌影像表现的差异性对临床治疗及预测肺腺癌患者的转归有提示意义。同时,肺腺癌CT征象与EGFR、ALK基因突变的相关性研究尚未得出定论,仍需继续深入。因此,掌握肺腺癌的CT征象与病理分类以及EGFR、ALK基因突变的相关性对放射科医生准确诊断GGN肺腺癌患者有重要意义,对临床医生制定合适的治疗方案及判断患者的预后也有重要的指导价值。











R734.2; R814.42
A


