种子生长法聚合金纳米棒的优化条件研究
2017-07-03李家萌曹颖孔玉芳廉晓丽杨毅梅
李家萌,曹颖,孔玉芳,廉晓丽,杨毅梅
(大理大学基础医学院,云南大理671000)
种子生长法聚合金纳米棒的优化条件研究
李家萌,曹颖,孔玉芳,廉晓丽,杨毅梅*
(大理大学基础医学院,云南大理671000)
目的:利用种子生长法制备金纳米棒,探索最佳制备条件。方法:通过对种子生长法中增长媒质的不同成分浓度比例及生长温度的控制聚合成形貌特征不同的金纳米棒,并利用紫外分光光度计进行测定。结果:通过对GNRs在制备过程中还原剂、活性剂、温度等条件的优化,发现在增长媒质中CTAB的最佳浓度为0.095 mol∕L,AA的最佳浓度为0.640 mmol∕L,AgNO3的最佳浓度为72 mmol∕L,种子的最佳生长温度为28°C。结论:本实验系统研究了金纳米棒聚合过程中的生长机理和最佳实验条件,合成了具有所需的光学性质的金纳米棒。
金纳米棒;生长机理;优化
纳米技术(Nanotechnology)是指利用单个原子或分子制造物质,并研究物质结构在0.1至100纳米范围内的性质和应用,已经成为21世纪的关键技术之一〔1-2〕。金纳米棒(Gold Nanoparticles,GNRs)以其优良性质以及合成简单、成本低等优点使其在生物标记、医学检验、生物医学等领域的研究已经成为学者们的研究热点〔3-4〕。
贵金属纳米结构的光学生物传感器是基于局部表面等离子共振(surface plasmon resonance,SPR)的现象〔5〕,即纳米SPR。纳米金作为一种研究最早的贵金属纳米材料,是指有一定的金原子数的八面体构造的结构,只有几纳米大小的颗粒,纳米金颗粒直径小、比表面积大,因此单位面积可以连接数量很多的生物分子,利用表面增强拉曼散射(surface-enhanced Ramanscattering,SERS)效应起到信号放大的作用〔6〕,且标记了纳米金的生物活性分子的结合性质也得到了很大的提高,在生物学应用中表现出特殊的吸引力。金纳米棒有两个等离子共振(SPR)吸收带:横向SPR和纵向SPR吸收峰,其中纵向等离子体吸收峰的位置可以随其长径比的增大而逐渐红移,金纳米棒SPR的这种可调性使其能作为很好的SERS基底,因为按照SERS的电磁场增强机制,当激发光和SPR共振时,可以最大程度提高单个纳米颗粒的增强功能。
金纳米棒合成的有效调控直接决定着其后续应用研究的效果,种子介导的生长法合成金纳米棒主要包括两步〔7〕:(1)利用NaBH4还原HAuCl4溶液,制备小粒径3.5 nm左右的球形金纳米颗粒种子。(2)将种子制剂加入增长媒质,让小粒径的金纳米颗粒在棒胶束溶液生长成棒状。种子生长法将金纳米颗粒成核过程与金棒生长过程分步进行,从而使产物的产率及金粒子转化率都优于成核与生长同步进行的模板法所制备的产物。金纳米棒球状较球状其长度有明显优势,纵向金纳米粒子吸收峰调谐是由其大小和异质的形状决定,种子生长法可以通过优化还原剂、溶剂等不同成分的比例控制以及温度、生长时间等条件是生长后的纳米金颗粒的粒径通过各种条件的改变得以控制,提高金纳米棒反应体系的反应速率和生长速率,合成具有所需性质的金纳米棒,最大程度提高单个纳米颗粒的生物功能。本研究通过GNRs的纵向SPR吸收峰的长径与红移成正比的特点优化反应条件,最大程度提高单个金纳米颗粒生物功能,着重于高通量的探索。
1 实验部分
1.1 材料与仪器氯金酸(HAuCl4)、溴化十六烷基三甲基铵(CTAB)、硝酸银(AgNO3)、硼氢化钠(NaBH4)和抗坏血酸(AA)来自生工生物工程(上海)股份有限公司,均为国产分析纯试剂;试验用水均为Millipore公司(18.25 MΩ.cm@25℃,TOC:1~3 ppb)的超纯水仪制备的超纯水。
TU-1901型紫外可见分光光度计(上海MAPADA公司)测定GNRs反应溶液的UV-vis光谱,A值设置在0~2,波长范围设置在400~900 nm;JJ-BC电子分子天平、隔水式恒温培养箱(生工生物工程(上海)股份有限公司)。
1.2 试验步骤
1.2.1 配置种子制剂混合HAuCl4(0.1 mol∕L,140 μL)和6.86 mL纯水制备2 mmol∕L的HAuCl4溶液,新鲜制备NaBH4(0.01 mol∕L)低温保存5~10 min。混合的HAuCl4(2 mmol∕L,625μL)、CTAB(0.2 mol∕L,1.88 mL)、1.37 mL纯水,搅拌1 min,将450μL低温的NaBH4加入步骤3混合液,快速搅拌2 min,溶液颜色变为棕黄色,存放入28°C下2 h。
1.2.2 GNRs的制备以CTAB为变量的增长媒质:分别将含0.00、0.06、0.10、0.14、0.18、0.20、0.22、0.24 mol∕L的CTAB(11.875 mL)的8个玻璃瓶加入纯水(7.71 mL),再加入HAuCl4(2 mmol∕L,5 mL)溶液变为深黄色,最后每个玻璃瓶依次加入AgNO3(0.01 mol∕L,150μL)、AA(0.1 mol∕L,160μL)得到无色透明的增长媒质。以AgNO3为变量的增长媒质配置:在8个玻璃瓶中分别混合CTAB(0.2 mol∕L,11.875 mL)、纯水(7.71 mL)、HAuCl4(2 mmol∕L、5 mL)溶液变为深黄色,分别加入0.000、0.002、0.004、0.006、0.008、0.010、0.012、0.014 mol∕L的AgNO3(150μL)于8个玻璃瓶中,最后将AA(0.1 mol∕L,160μL)分别加入玻璃瓶中得到无色透明的增长媒质。以AA为变量的增长媒质配置:在8个玻璃瓶中分别混合CTAB(0.2 mol∕L,11.875 mL)、纯水(7.71 mL)、HAuCl4(2 mmol∕L、5 mL)溶液变为深黄色,依次加入AgNO3(0.01 mol∕L,150μL),最后分别将0.00、0.02、0.04、0.06、0.08、0.1、0.12、0.14 mol∕L的AA(160μL)加入8个玻璃瓶中得到无色透明的增长媒质。
1.2.3 金棒合成加108μL种子溶液于25 mL增长媒质中,混合均匀,在28℃中孵育12 h,最终得到深紫色GNRs溶液。
1.2.4 容器清洗所有定量容器及反应容器用清水冲洗后,放入王水中浸泡过夜取出,用纯水反复冲洗5遍以上。
2 实验结果与讨论
2.1 单因素控制对GNRs合成的影响
2.1.1 CTAB用量在GNRs合成中的影响在含有CTAB的种子溶液中,HAuCl4包裹在CTAB中,还原剂通过还原反应将离子还原成紧密的结合在CTAB胶束上。在富含电子的金种子表面AuⅠ通过电子转移发生还原反应形成单质金Au0。见图1。
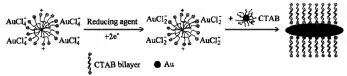
图1 金纳米棒形成示意图
在含有CTAB的增长媒质中,CTAB双份子层表面吸附着金纳米棒,第一层中的CTAB首基面向金表面,与金纳米棒顶端的晶面相比,CTAB首基优先结合在侧面上〔8〕。同时,由于金纳米棒顶端曲率较大,因此相对于侧面而言,金纳米棒更倾向于沿着两端方向生长,从而形成长度更长、纵横径比更大的金纳米棒〔9〕。
封三图1为在不同CTAB浓度情况下合成GNRs的颜色变化图。在加入浓度为0.00 mol∕L的CTAB时,光谱扫描曲线为一个接近平直的曲线,没有GNRs的横向或纵向表面等离子共振吸收峰(TSPR或LSPR)。当将增长媒质中加入浓度为0.06 mol∕L的CTAB的时候,GNRs的TSPR波长在531 nm,LSPR波长在687 nm。此时GNRs的纵横径比较小,且在反应体系中会存在球形、梭形等不规则的杂质。但随着CTAB浓度的增加,GNRs的LSPR峰逐渐红移,由此可知GNRs的纵横径比也在不断增加。TSPR峰未发生变化始终保持在531 nm。当加入的CTAB的浓度达到0.2 mol∕L(在增长媒质中浓度为0.095 mol∕L)的时候,其LSPR的波长为778 nm,达到最大值。但GNRs的LSPR峰波长并不是一直呈增加趋势的,此后将CTAB的浓度增加到0.22 mol∕L和0.24 mol∕L的时候,其LSPR的波长并没有呈增长趋势,LSPR的波长降到为772 nm。见图2。同时由图3可以看出,随着CTAB浓度的升高,GNRs的纵横吸光度值比也在不断增加,说明体系中GNRs的产率也在不断升高。当CTAB的浓度到达一定量,吸光度值比不再增加,这是由于生长溶液的粘稠度过大,对Ag+的吸附产生不利影响,也不利于Au的沉积,从而使GNRs的产率不再升高。

图2 GNRs的Vis-NIR吸收光谱图
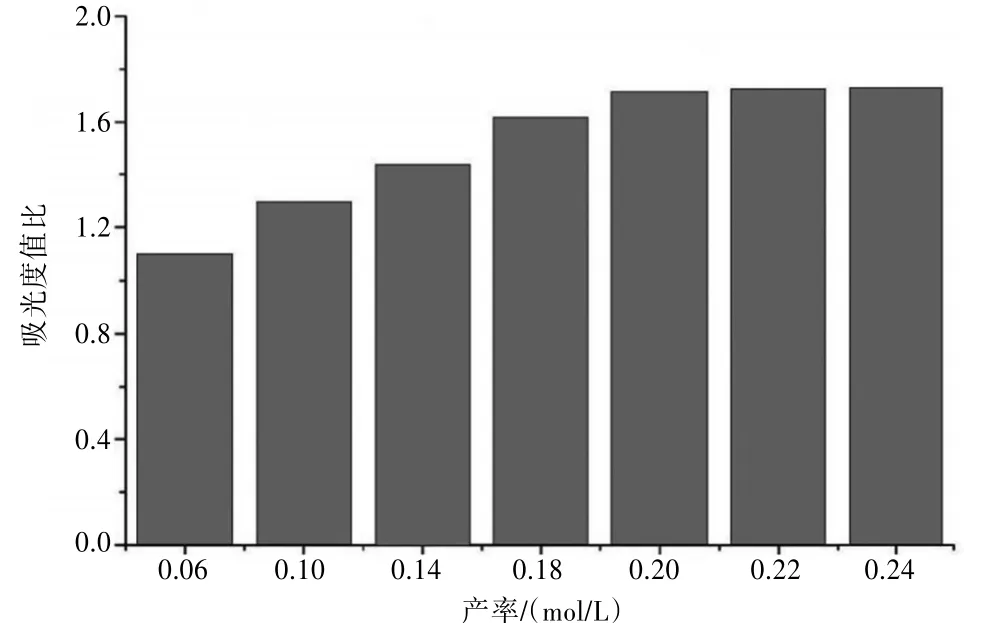
图3 不同CTAB浓度条件下制备的GNRs的纵横吸光度值比
2.1.2 AA的用量在GNRs合成中的影响在纳米金的制备过程中还原剂占有重要的因素,硼氢化钠、柠檬酸钠、抗坏血酸等都是比较常见的还原剂〔10-12〕,但因其各自的特点不同在金纳米棒制备的过程中,我们选择的还原剂又有所不同。在增长媒质中通常选用弱的还原剂,柠檬酸钠、抗坏血酸都为较弱的还原剂,但柠檬酸钠在还原过程中由于其弱还原性和稳定剂的作用,聚合纵横径比较大的GNRs在常温下很难进行反应,给实验条件的创造带来很大的障碍。抗坏血酸(AA)也是较弱的还原剂,不能将Au3+直接还原Au以合成GNRs,因此在实验中,AA不被用于种子溶液中对金离子的还原反应,而用于增长媒质中在金棒生长过程中,并制备径粒可控和形貌可控的金纳米棒。见图4。

图4 硼氢化钠、抗坏血酸、柠檬酸钠的分子结构式
封三图2是在不同AA浓度情况下合成的GNRs颜色变化图。在加入浓度为0.00 mol∕L的AA时,光谱扫描曲线为一个接近平直的曲线,没有GNRs的TSPR或LSPR。当将增长媒质中加入浓度是0.06 mol∕L的AA的时候,GNRs的TSPR波长在531 nm,LSPR波长在706 nm随着AA浓度的增加,GNRs的LSPR峰逐渐红移,由此可知GNRs的纵横径比也在不断增加。TSPR峰未发生变化始终保持在531 nm。当加入的AA的浓度达到0.10 mol∕L(在增长媒质中浓度为0.640 mmol∕L)的时候,其LSPR的波长为782 nm,达到最大值。但GNRs的LSPR峰波长并不是一直呈增加趋势的,将AA的浓度增加到0.12 mol∕L后,其LSPR的波长并没有呈增长趋势,LSPR的波长降到为761 nm。此后再增加增长媒质中AA浓度时,其LSPR峰有继续减小趋势。LSPR的这种大幅度蓝移是由于随着生长溶液中AA的浓度不断升高,同时在同样时间也加快了HAuCl4中金离子被还原的速率,被还原出的Au+在体系中快速的沉积,其沉积速率明显高于了CTAB在晶种表面对Au+吸附的速率,从而导致了大量的金离子的沉积,生长出来的GNRs较短,从而出现LSPR出现大幅度蓝移。见图5。
由图6可以看出,随着AA浓度的升高,GNRs的纵横吸光度值比也出现了一个升高的过程,说明体系中GNRs的产率也在不断升高。当AA的浓度到达0.10 mol∕L的时候,吸光度值比达到最大。之后再增加AA的浓度,吸光度值比反而呈现一个下降趋势。由于AA的升高生长液中Au+的沉降速度与吸附速度不成正比,GNRs生长的短而粗,呈短哑铃状,从而也导致GNRs的产率也下降。
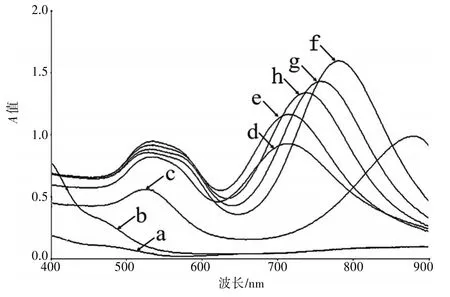
图5 GNRs的Vis-NIR吸收光谱图
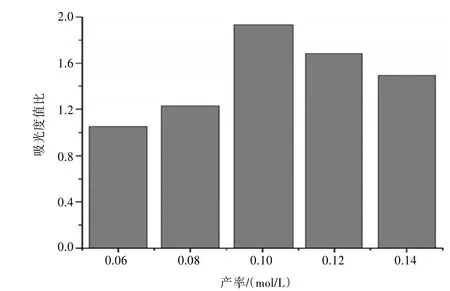
图6 不同AA浓度条件下制备的GNRs的纵横吸光度值比
2.1.3 AgNO3的用量在GNRs合成中的影响AgNO3
在GNRs的制备的反应过程中对提高金棒的产出率和纵横径比的控制起着重要的作用。在有AgNO3存在的种子介导的生长法合成金纳米棒的过程中,种子在加入增长媒质的生长过程中,抗坏血酸对Ag+的还原反应首先进行,将Ag+还原成五边形Ag孪晶纳米结构。Ag把Au+还原成Au0,辅助Au进行单向性生长,其还原反应过程为:,CTAB活性剂双层将金纳米棒侧面包裹,从而使金纳米棒在增长媒质中获得稳定的单向性生长。如果增长媒质中没有AgNO3加入则不能得到纵横径比较大的GNRs,因此Ag+在GNRs的聚合过程中起着至关重要的作用。见图7。

图7 有AgNO3存在的金纳米棒制备机理
在最优的CTAB与AA浓度的条件下,对比了AgNO3加入的浓度对GNRs制备的影响,并探讨制备GNRs的最佳AgNO3浓度。封三图3是在不同AgNO3浓度情况下合成的GNRs的颜色变化图。在加入浓度为0.000 mol∕L的AgNO3时,光谱扫描曲线发现只有GNRs的横向表面等离子共振吸收峰,说明种子溶液在增长媒质中并没有得到生长。当将增长媒质中加入浓度是0.002 mol∕L的AA的时候,GNRs的TSPR波长在531 nm,LSPR波长在737 nm随着AgNO3浓度的增加,GNRs的LSPR峰逐渐红移,由此可知GNRs的纵横径比也在不断增加。TSPR峰未发生变化始终保持在531 nm。当加入的的AgNO3浓度达到0.012 mol∕L(在增长媒质中浓度为72 mmol∕L)的时候,其LSPR的波长为785 nm,达到最大值。但GNRs的LSPR峰波长并不是一直呈增加趋势的,将AgNO3的浓度增加到0.014 mol∕L后,其LSPR的波长并没有呈增长趋势,LSPR的波长降到为774 nm。见图8。由图9可以看出,随着AgNO3浓度的升高,GNRs的纵横吸光度值比也在不断增加,说明体系中GNRs的产率也在不断升高。当AgNO3的浓度到达一定量,吸光度值比不再增加,并有略微的下降。
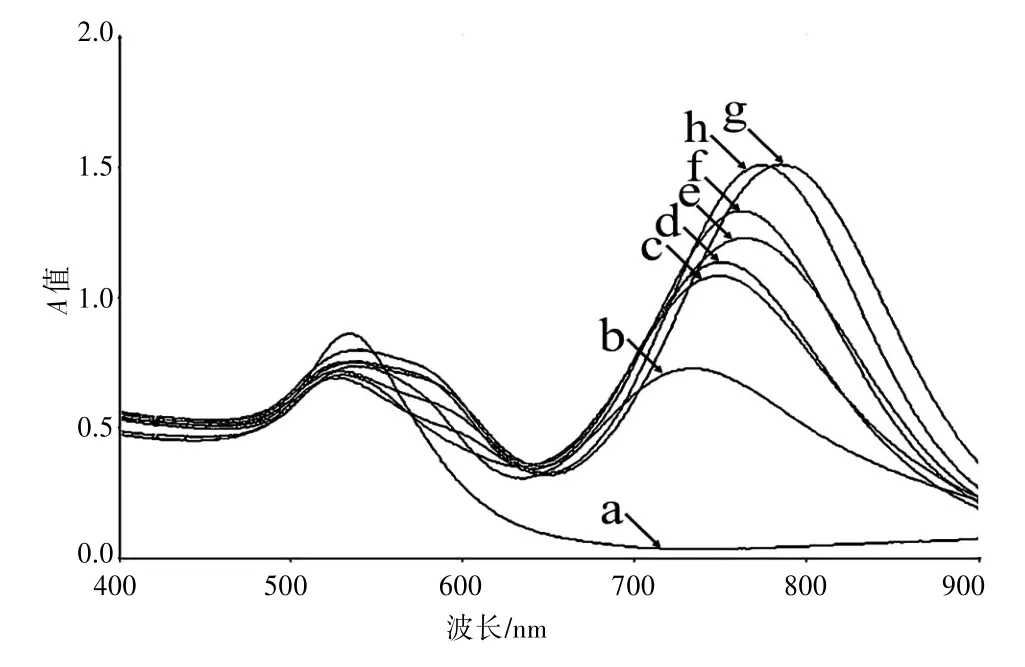
图8 GNRs的Vis-NIR吸收光谱图

图9 不同AgNO3浓度条件下制备的GNRs的纵横吸光度值比
2.2 温度对GNRs聚合的影响金纳米棒的聚合是还原剂对金离子的还原反应和种子溶液在增长媒质中生长的一系列化学反应协同进行的结果,但GNRs的聚合也受体系的热力学性质和环境的动力学过程的影响,而制备高产出率和高纵横径比的GNRs也必须兼顾在制备过程中的化学反应因素和物理因素〔15〕。温度作为GNRs聚合的物理因素,也对GNRs聚合起着至关重要的作用。通过上述实验结果,选取最佳反应条件CTAB(0.2 mol∕L,11.875 mL)、AgNO3(0.012 mol∕L,150μL)、AA(0.1 mol∕L,160μL)制备4瓶相同的增长媒质,分别加入108μL种子液,将4个反应体系分别放入25、28、38、48°C将种子进行生长。
图10是在不同温度情况下合成的GNRs的Vis-NIR吸收光谱图。当种子生长温度在25°C的时候,GNRs的TSPR波长为507 nm,LSPR波长为775 nm,其A值为1.402。当温度增加到28°C时,GNRs的LSPR峰红移明显为783 nm,GNRs的纵横径比也在不断增加,相比于25°C是A值也有所升高为1.531,A的升高说明金纳米棒的产出率也相对升高。当升种子的生长温度达到38°C的时候,其LSPR的波长还是相对也28°C时有所减少为777 nm,但A达到最大值为1.501。最后将种子升高温度达到48°C的时候,GNRs的LSPR峰波长继续呈减小趋势的,A值也有所减少。

图10 GNRs的Vis-NIR吸收光谱图
3 结论
本实验采用种子介导的生长法成功聚合了不同长径比、不同产出率形貌不同的GNRs。探讨了生长溶液中活性剂CTAB、还原剂AA、AgNO3用量以及种子生长温度、生长时间对制备不同长径比GNRs的影响,同时利用多种方法对所制备的GNRs进行分析,优化了制备高长径比金纳米棒的最佳实验条件。但在金纳米棒制备的过程中,仍存在整体产率,纯度不高,金棒生长受温度、湿度等环境条件影响较大等问题,值得进一步去探究。我们已经对金纳米棒的制备生长机理和反应条件有了初步的掌握,可最大程度的制备所需光学性质的金纳米棒,为纳米金在生物标记、医学检验、生物医学等领域的研究和应用奠定了更好的基础。
〔1〕VIGDERMAN L,KHANAL B P,ZUBAREV E R.Functionalgold nanorods:synthesis,self-assembly,and sensing applications〔J〕.Adv Mater Weinheim,2012,24(36):4811-4841.
〔2〕WANG J,CHEN G,JIANG H,et al.Advances in nanoscaled biosensors for biomedical applications〔J〕.Analyst,2013,138(16):4427-4435.
〔3〕HIRSCH L R,STAFFORD R J,BANKSON J A,et al. Nanoshell-mediated near-infrared thermal therapy of tumors under magnetic resonance guidance〔J〕.Proc Natl Acad SciUSA,2003,100(23):13549-13554.
〔4〕CHEN J,WANG D,XI J,et al.Immuno Gold Nanocages with Tailored Optical Properties for Targeted Photothermal Destruction of Cancer Cells〔J〕.Nano Letters,2007,7(5):1318-1322.
〔5〕LIZ-MARZÁN L M.Tailoring surface plasmons through the morphology and assembly of metal nanoparticles〔J〕. Langmuir,2006,22(1):32-41.
〔6〕NIKOOBAKHT B,EL-SAYED M A.Surface-Enhanced Raman Scattering Studies on Aggregated Gold Nanorods〔J〕.The Journal of Physical Chemistry A,2003,107(18):3372-3378.
〔7〕NIKOOBAKHT B,EL-SAYED M A.Preparation and Growth Mechanism of Gold Nanorods(NRs)Using Seed-Mediated Growth Method〔J〕.Chemistry of Materials,2003,15(10):1957-1962.
〔8〕GOLE A,MURPHY C J.Seed-Mediated Synthesis of Gold Nanorods:Role of the Size and Nature of the Seed〔J〕. Chemistry ofMaterials,2004,16(19):3633-3640.
〔9〕NIIDOMEA Y,NIIDOMEA T.Gold Nanorods:Application to Bioscience and Medicine〔J〕.Nano Biophoton,2007,18(8):3297-3299.
〔10〕SUN X P,ZHANG Z L,ZHANG B L,etal.Preparation of Gold Nanoparticles With Polyelectrolyte〔J〕.Chin Chem Lett,2003,14,477-481.
〔11〕YONEZAWA T,KUNITAKE T.Practical preparation of anionic mercapto ligand-stabilized gold nanoparticles and their immobilization〔J〕.Colloids and Surfaces A:Physicochemicaland Engineering Aspects,1999,149(1):193-199.
〔12〕JANA N R,GEARHEART L,MURPHY C J.Wet ChemicalSynthesis ofHigh Aspect Ratio CylindricalGold Nanorods〔J〕.The Journal of Physical Chemistry B,2001,105(19):4065-4067.
〔13〕GAO J,BENDER C M,MURPHY C J.Dependence of the Gold Nanorod Aspect Ratio on the Nature ofthe Directing Surfactant in Aqueous Solution〔J〕.Langmuir,2003,19(21):9065-9070.
〔14〕GOLE A,MURPHY C J.Seed-Mediated Synthesis of Gold Nanorods:Role of the Size and Nature of the Seed〔J〕.Chemistry of Materials,2004,16(19):3633-3640.
〔15〕OKITSU K,YUE A,TANABE S,et al.Formation of Colloidal Gold Nanoparticles in an Ultrasonic Field:Control of Rate of Gold(III)Reduction and Size of Formed Gold Particles〔J〕.Langmuir,2001,17(25):7717-7720.
Optimum Conditions of Gold Nanorods Preparation by Seed-Mediated Growth Method
Li Jiameng,Cao Ying,Kong Yufang,Lian Xiaoli,Yang Yimei*
(Pre-clinical College,Dali Universily,Dali,Yunnan 671000,China)
Objective:To explore gold Nanorods preparation with best conditions by seed-mediated growth method.Methods:To synthesize different morphological characteristics of gold Nanoparticles by controlling the concentration ratio of different compositions and the growth temperature,and the synthesized gold Nanoparticles were characterized by UV-vis spectroscopy.Results:By optimizing the reducing agent,surfactant,and temperature,etc,the best concentration of CTAB was 0.095 mol∕L,of AA was 0.640 mmol∕L,and of AgNO3was 72 mmol∕L.The besttemperature was 28°C.Conclusion:The gold Nanoparticles growth mechanism in the process of polymerization and the best experimental conditions were studied,and the optical properties of GNRs were successfully prepared.
gold Nanoparticles;growth mechanism;optimize
O6
A
2096-2266(2017)06-0049-06
10.3969∕j.issn.2096-2266.2017.06.012
(责任编辑李杨)
国家自然科学基金资助项目(81460316)
2017-01-04
2017-04-20
李家萌,硕士研究生,主要从事分子生物学研究.
*通信作者:杨毅梅,教授.
