阿德福韦酯纳米脂质载体的制备及处方优化Δ
2017-07-03孙珊珊王慧云王飞飞济宁医学院药学院山东日照276826
孙珊珊,王慧云,王飞飞,丁 林(济宁医学院药学院,山东日照 276826)
阿德福韦酯纳米脂质载体的制备及处方优化Δ
孙珊珊*,王慧云#,王飞飞,丁 林(济宁医学院药学院,山东日照 276826)
目的:制备阿德福韦酯纳米脂质载体(ADV-NLC),并优化其处方。方法:以硬脂酸和单硬脂酸甘油酯为固体脂质,油酸为液体脂质,双子(Gem ini)表面活性剂、聚山梨酯80为乳化剂,十二烷基硫酸钠(SDS)为稳定剂,采用溶剂分散-超声法制备ADVNLC。以粒径、多分散指数、Zeta电位和包封率为指标,单因素试验筛选Gem ini表面活性剂-聚山梨酯80比例、乳化剂用量(乳化剂与水相之比)、药脂比、固-液脂质比。结果:处方为乳化剂(双子表面活性剂-聚山梨酯80比例1∶2)用量3%、药脂比4.5%,固-液脂质比6∶5。所制ADV-NLC的平均粒径为(48.83±2.65)nm,多分散指数<0.3,Zeta电位为(-28.7±1.8)mV,包封率为(77.65±0.03)%(n=3)。结论:成功制得ADV-NLC,且处方合理、可行。
阿德福韦酯;纳米脂质载体;双子表面活性剂;处方优化
阿德福韦酯(Adefovir dipivoxil,ADV)是目前临床上用于治疗乙肝的常见药物,但由其引发的胃肠系统损害、低磷血症、骨软化症等不良反应屡见报道[1-4]。纳米脂质载体(Nanostructured lipid carrier,NLC)是在固体脂质纳米粒的基础上发展起来的新一代药物载体,通过在固态脂质中加入液态脂质,破坏其完整晶格结构,从而显著提高载药能力,且可控制药物释放[5-10]。本试验拟采用溶剂分散-超声法制备ADV-NLC,并优化其处方工艺,旨在开发一种高效、低毒、缓释的ADV新剂型及新型药物载体材料。
1 材料
1.1 仪器与透析袋
UV-2450紫外-可见分光光度计和LC-10AT高效液相色谱仪(日本岛津公司);ZEN3690粒度分析仪(英国Malvern公司);JY92-Ⅱ超声波细胞粉碎机(宁波新芝生物科技股份有限公司);冷冻干燥机(北京博医康实验仪器有限公司);透析袋(美国Union Carbide公司,截留分子量:8 000)。
1.2 药品与试剂
ADV标准品(大连美仑生物技术有限公司,批号:20130710,纯度:>98%);ADV原料药(郑州华文化工有限公司,批号:20140923,纯度:≥97%);单硬脂酸甘油酯(化学纯)、聚山梨酯80(化学纯)、硬脂酸(分析纯)、油酸(分析纯)均购自天津市博迪化工有限公司;双子(Gem ini)表面活性剂(2,4,7,9-四甲基-5-癸炔-4,7-二醇异氧化物,美国MSDS公司);丙酮、无水乙醇、甘露醇均为分析纯,正丙醇、十二烷基磺酸钠(SDS)、聚乙二醇(PEG)1000均为化学纯,乙腈、甲醇为色谱纯。
2 方法与结果
2.1 ADV-NLC的制备
采用溶剂分散-超声法制备ADV-NLC。精密称取处方量的单硬脂酸甘油酯、硬脂酸和油酸以及ADV,分散于丙酮-乙醇的混合溶剂(1∶1,V/V)中,于60水浴中熔融作为油相;另精密称取处方量的Gemini表面活性剂-聚山梨酯80和稳定剂正丙醇、PEG1000、SDS分散于20m L水中加热至相同温度作为水相;然后在搅拌的条件下将油相缓慢注入水相中,将得到的混悬液于恒温磁力搅拌器上60继续搅拌30m in,除去有机溶剂,形成初乳。将得到的初乳超声处理(功率:600W,间隔时间:3 s,工作时间:5 s,次数:50次)后,得到淡蓝色澄清透明的ADV-NLC水分散体系。
2.2 ADV-NLC的性质表征
将ADV-NLC水分散体系稀释一定倍数后,取适量于ZEN3690粒度分析仪样品池中,于25条件下以光散射法检测粒径和多分散指数;另取适量于U型样品池中检测Zeta电位,测试角度为90°。
2.3 ADV的含量测定
2.3.1 ADV标准液的制备 精密称取ADV标准品0.010 73 g,置于50m L量瓶中,用流动相[乙腈-磷酸盐缓冲液(PBS)(40∶60)]溶解定容至50m L,得到0.214 6 mg/m L的ADV标准贮备液。分别精密量取0.2、0.4、0.8、1.2、1.6 m L的ADV标准贮备液,置于10 m L量瓶中,并用流动相定容至刻度,得到4.292、8.584、17.168、25.752、34.336μg/m L的ADV标准液。
2.3.2 ADV检测波长的选择 采用UV-2450紫外-可见分光光度计在200~800 nm波长范围内对8.584μg/m L的ADV标准液进行扫描。结果显示,ADV在258 nm波长处有最大吸收,故选择258 nm为ADV的检测波长。
2.3.3 色谱条件 色谱柱:VP-ODS(250mm×4.6mm,5 µm);流动相:乙腈-PBS(40∶60);流速:1m L/min;检测波长:258 nm;进样量:20μL;柱温:25。
2.3.4 方法学考察 按相关方法进行考察。结果显示,ADV峰面积(y)与质量浓度(x)的回归方程为y= 17 468.002x+14 616.947(r=0.999 71),ADV线性范围为4.292~34.336μg/m L;平均回收率为96.13%(RSD=1.2%,n=6);精密度试验中峰面积的RSD为1.8%(n=6);稳定性试验中含量的RSD为2.1%(n=6)。
2.4 包封率的测定
取ADV-NLC水分散体系1m L于透析袋内,加超纯水补液至3m L,将其浸入47m L同种超纯水中,烧杯中加入搅拌子快速搅拌,平行9次。分别于0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0、4.5 h取出透析液,用紫外-可见分光光度计检测各透析液中ADV的吸光度,绘制吸光度-时间曲线,计算含量和包封率[包封率(%)=(W总-W游离)/ W总×100%]。ADV-NLC的吸光度-时间曲线见图1。
由图1可知,ADV-NLC释放2 h后曲线趋于平缓,表明此时游离ADV的扩散基本达到平衡,由此确定2 h为透析平衡时间。
2.5 处方筛选
2.5.1 Gem ini表面活性剂-聚山梨酯80比例对ADVNLC理化性质的影响 固定乳化剂的用量为3%(乳化剂与水相之比,m/V)、药脂比为4.5%(m/m)、固-液脂质比为6∶5(m/m),考察Gemini表面活性剂-聚山梨酯80比例(0∶1、1∶3、1∶2、1∶1、2∶1)对ADV-NLC理化性质的影响,结果见表1。

图1 ADV-NLC的吸光度-时间曲线Fig 1 Absorbance-time curvesof ADV-NLC
表1 Gem ini表面活性剂-聚山梨酯80比例对ADVNLC理化性质的影响(±s,n=3)Tab 1 Effectsof Gem inisurfactant-polysorbate 80 ratio on ADV-NLC physico-chem ical property(±s,n=3)
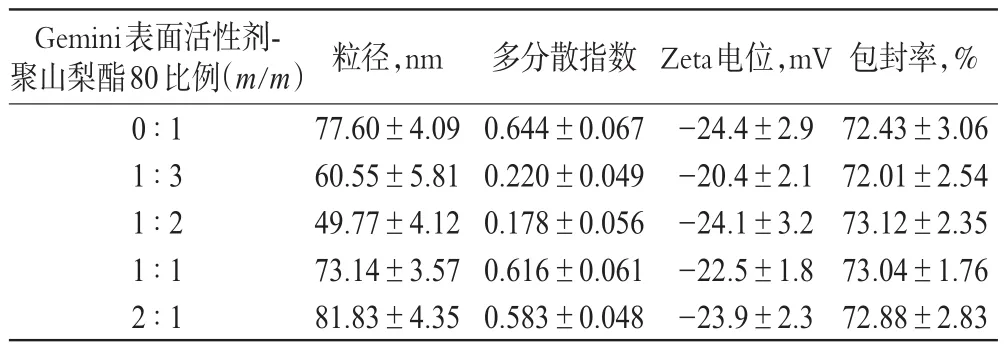
表1 Gem ini表面活性剂-聚山梨酯80比例对ADVNLC理化性质的影响(±s,n=3)Tab 1 Effectsof Gem inisurfactant-polysorbate 80 ratio on ADV-NLC physico-chem ical property(±s,n=3)
Gemini表面活性剂-聚山梨酯80比例(m/m)0∶1 1∶3 1∶2 1∶1 2∶1粒径,nm 77.60±4.09 60.55±5.81 49.77±4.12 73.14±3.57 81.83±4.35多分散指数0.644±0.067 0.220±0.049 0.178±0.056 0.616±0.061 0.583±0.048 Zeta电位,mV -24.4±2.9 -20.4±2.1 -24.1±3.2 -22.5±1.8 -23.9±2.3包封率,% 72.43±3.06 72.01±2.54 73.12±2.35 73.04±1.76 72.88±2.83
由表1可知,不同比例Gem ini表面活性剂-聚山梨酯80对ADV-NLC的包封率影响不明显,但对粒径和多分散指数影响较大。当Gemini表面活性剂-聚山梨酯80比例为1∶2时,所制备的ADV-NLC粒径和多分散指数最小,且粒度分布均匀,故选择Gemini表面活性剂-聚山梨酯80(1∶2)为乳化剂。
2.5.2 乳化剂用量对ADV-NLC理化性质的影响 固定Gemini表面活性剂-聚山梨酯80比例为1∶2、药脂比为4.5%、固-液脂质比为6∶5,考察乳化剂用量[2%、3%、4%、5%、6%、7%(乳化剂与水相之比,m/V)]对ADVNLC理化性质的影响,结果见表2。
表2 乳化剂用量对ADV-NLC理化性质的影响(±s,n=3)Tab 2 Effects of em ulsifier dosage on ADV-NLC physico-chem icalproperty(±s,n=3)
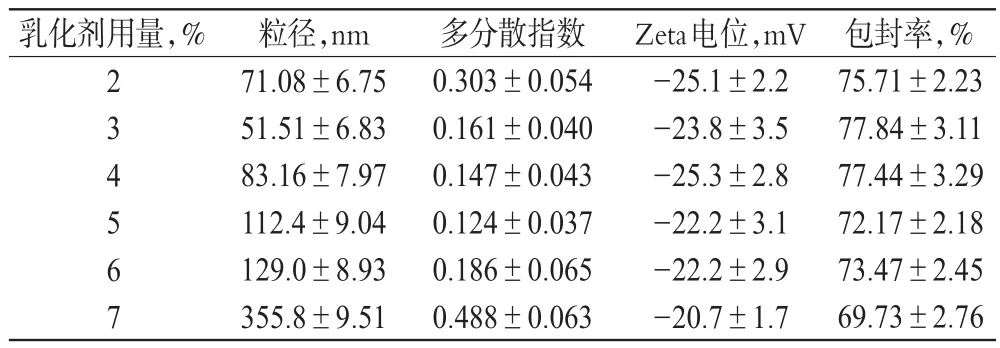
表2 乳化剂用量对ADV-NLC理化性质的影响(±s,n=3)Tab 2 Effects of em ulsifier dosage on ADV-NLC physico-chem icalproperty(±s,n=3)
乳化剂用量,% 234567粒径,nm 71.08±6.75 51.51±6.83 83.16±7.97 112.4±9.04 129.0±8.93 355.8±9.51多分散指数0.303±0.054 0.161±0.040 0.147±0.043 0.124±0.037 0.186±0.065 0.488±0.063 Zeta电位,mV -25.1±2.2 -23.8±3.5 -25.3±2.8 -22.2±3.1 -22.2±2.9 -20.7±1.7包封率,% 75.71±2.23 77.84±3.11 77.44±3.29 72.17±2.18 73.47±2.45 69.73±2.76
由表2可知,随着乳化剂用量增加,ADV-NLC粒径增大、包封率减小。当乳化剂用量为3%时,所制备的ADV-NLC粒径最小、包封率最高,故选择乳化剂用量为3%。
2.5.3 药脂比对ADV-NLC理化性质的影响 固定Gem ini表面活性剂-聚山梨酯80比例为1∶2、乳化剂用量为3%、固-液脂质比为6∶5,考察药脂比(1.8%、3.2%、4.5%、6.8%、9.1%,m/m)对ADV-NLC理化性质的影响,结果见表3。
表3 药脂比对ADV-NLC理化性质的影响(±s,n=3)Tab 3 Effects of drug-lipid ratio on ADV-NLC physico-chem icalproperty(±s,n=3)
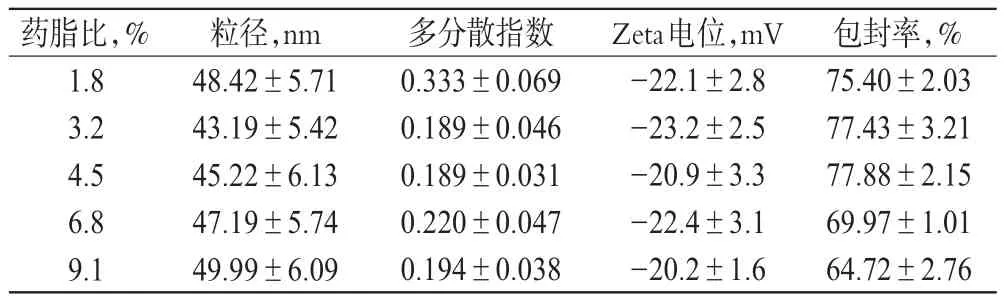
表3 药脂比对ADV-NLC理化性质的影响(±s,n=3)Tab 3 Effects of drug-lipid ratio on ADV-NLC physico-chem icalproperty(±s,n=3)
药脂比,% 1.8 3.2 4.5 6.8 9.1粒径,nm 48.42±5.71 43.19±5.42 45.22±6.13 47.19±5.74 49.99±6.09多分散指数0.333±0.069 0.189±0.046 0.189±0.031 0.220±0.047 0.194±0.038 Zeta电位,mV -22.1±2.8 -23.2±2.5 -20.9±3.3 -22.4±3.1 -20.2±1.6包封率,% 75.40±2.03 77.43±3.21 77.88±2.15 69.97±1.01 64.72±2.76
由表3可知,药脂比对ADV-NLC的粒径影响不显著,但对包封率影响较明显。当药脂比为4.5%时,ADVNLC的包封率最高;药脂比继续增加,包封率反而减小,故选择药脂比为4.5%。
2.5.4 固-液脂质比对ADV-NLC理化性质的影响 液态脂质的类型或含量不同,均会使NLC的粒径、多分散指数和释放行为发生改变[9]。固定Gemini表面活性剂-聚山梨酯80比例为1∶2、乳化剂用量为3%、药脂比为4.5%,考察固-液脂质比(3∶1、2∶1、6∶5、6∶7、2∶3、3∶5、1∶2、3∶7,m/m)对ADV-NLC理化性质的影响,结果见表4。
表4 固-液脂质比对ADV-NLC理化性质的影响(±s,n=3)Tab 4 Effects of solid-liquid lipid ratio on ADV-NLC physico-chem icalproperty(±s,n=3)
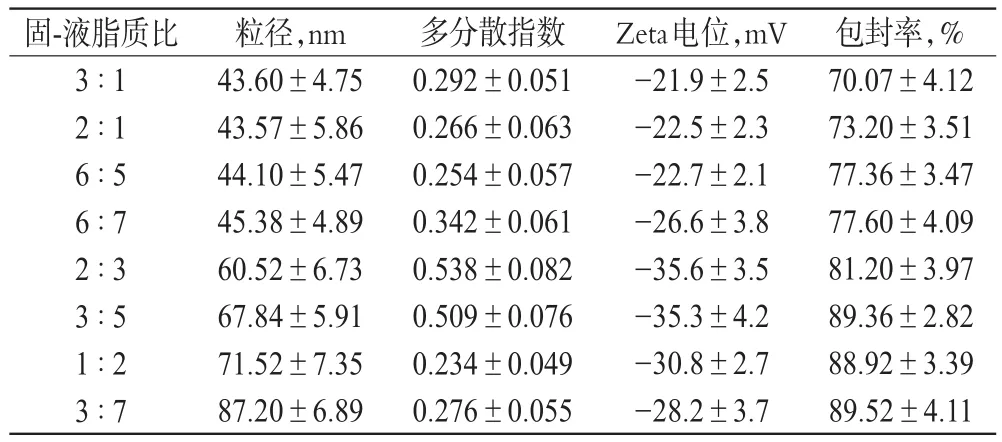
表4 固-液脂质比对ADV-NLC理化性质的影响(±s,n=3)Tab 4 Effects of solid-liquid lipid ratio on ADV-NLC physico-chem icalproperty(±s,n=3)
固-液脂质比3∶1 2∶1 6∶5 6∶7 2∶3 3∶5 1∶2 3∶7粒径,nm 43.60±4.75 43.57±5.86 44.10±5.47 45.38±4.89 60.52±6.73 67.84±5.91 71.52±7.35 87.20±6.89多分散指数0.292±0.051 0.266±0.063 0.254±0.057 0.342±0.061 0.538±0.082 0.509±0.076 0.234±0.049 0.276±0.055 Zeta电位,mV -21.9±2.5 -22.5±2.3 -22.7±2.1 -26.6±3.8 -35.6±3.5 -35.3±4.2 -30.8±2.7 -28.2±3.7包封率,% 70.07±4.12 73.20±3.51 77.36±3.47 77.60±4.09 81.20±3.97 89.36±2.82 88.92±3.39 89.52±4.11
由表4可知,随着油酸量的增加,ADV-NLC的粒径增大,包封率增加;当固-液脂质比达到3∶5时,继续增加油酸量,ADV-NLC的包封率无明显增加。考虑到油酸的用量太大可能会导致药物的突释效应,综合考虑,选择固-液脂质比为6∶5为最佳,此时ADV-NLC的粒径较小、包封率较高。
2.6 验证试验
筛选得到ADV-NLC的处方为乳化剂(Gem ini表面活性剂-聚山梨酯80比例1∶2)用量3%,药脂比4.5%,固-液脂质比6∶5。按此处方制得3批次的ADV-NLC,测得其平均粒径为(48.83±2.65)nm,多分散指数<0.3, Zeta电位为(-28.7±1.8)mV,包封率为(77.65± 0.03)%(n=3)。
3 讨论
在乳化剂的筛选中发现,与单独使用聚山梨酯80作为乳化剂比较,Gem ini表面活性剂-聚山梨酯80比例为1∶2时可产生良好的协同作用,可显著改善ADV-NLC的粒径及粒度分布。
综上所述,本试验成功制得了ADV-NLC,且处方合理、可行。
[1]Wang BF,Wang Y,Wang BY,etal.Osteomalacia and Fanconi’s syndrome caused by long-term low-dose adefovir dipivoxil[J].J Clin Pharm Ther,2015,40(3):345-348.
[2]Shimizu Y,HiraokaA,Yamago H,etal.Hypophosphatemiain patientsw ith hepatitis B virus infection undergoing long-term adefovir dipivoxil therapy[J].Hepatol Res,2014,44(11):1081-1087.
[3] Jeong HJ,Lee JM,Lee TH,etal.Two cases of hypophosphatemic osteomalacia after long-term low dose adefovir therapy in chronic hepatitis b and literature review[J]. JBone Metab,2014,21(1):76-83.
[4] 张帅,房舒舒,曹国颖.阿德福韦酯治疗乙肝致低磷血症及骨软化症文献汇总及数据分析[J].中国新药杂志,2015,24(15):1795-1800.
[5] Sang GL,Jeong JH,Kim SR,etal.Topical formulation of retinyl retinoate employing nanostructured lipid carriers [J].JPharmac Invest,2012,42(5):243-250.
[6] Vitorino C,A lves L,Antunes FE,et al.Design of a dual nanostructured lipid carrier formulation based on physicochem ical,rheological,and mechanical properties[J].J Nanoparticle Res,2013,doi:10.1007/s11051-013-1993-7. [7]Yuan H,Wang LL,Du YZ,etal.Preparation and characteristics of nanostructured lipid carriers for control-releasing progesterone by melt-emulsification[J].Colloids Surf BBiointerfaces,2007,60(2):174-179.
[8] 于莲,杨金儒,刘洋,等.槲皮素纳米结构脂质载体的制备及理化性质研究[J].中国中药杂志,2013,38(8):1151-1155.
[9] 袁菱,周蕾,陈彦,等.雷公藤红素纳米结构脂质载体的制备及其理化性质考察[J].中成药,2013,35(9):2023-2027.
[10] Mahrous GM.Proniosomes as a drug carrier for transdermal delivery of meloxicam[J].Bull Pharm Sci,2010,33(2):131-140.
[11] 肖超.紫杉醇磁性纳米脂质体的制备及其动物体内组织分布的研究[D].广州:华南理工大学,2010.
Preparation and Formulation Optim ization of Nanostructured Lipid Carriers of Adefovir Dipivoxil
SUN Shanshan,WANG Huiyun,WANG Feifei,DING Lin(School of Pharmacy,Jining Medical University,Shandong Rizhao 276826,China)
OBJECTIVE:To prepare nanostructured lipid carrier of adefovir dipivoxil(ADV-NLC),and optimize the formulation.METHODS:Using stearic acid and glycerin monostearate as solid lipid,oleic acid as liquid lipid,Gem ini surfactant and polysorbate 80 as emulsifier,sodium dodecyl sulfate(SDS)as stabilizer,solvent dispersion ultrasonic method was used to prepare ADV-NLC.And using particle size,polydispersity index,Zeta potential,encapsulation efficiency as indexes,single factor testwas conducted to screen Gem ini surfactant-polysorbate 80 ratio,emulsifier dosage(ratio of emulsifier to water phase),drug-lipid ratio,solid-liquid lipid ratio.RESULTS:The formula was as follow as 3%emulsifier(Gem ini surfactant-polysorbate 80 ratio of 1∶2),4.5%drug-lipid ratio,solid-liquid lipid ratio of 6∶5.The average particle size of the prepared ADV-NLC was(48.83±2.65)nm,polydispersity index<0.3,Zeta potentialwas(-28.7±1.8)m V,encapsulation efficiency was(77.65±0.03)%(n=3).CONCLUSIONS:ADV-NLC is successfully prepared,and the formulation is reasonable and feasible.
Adefovir dipivoxil;Nanostructured lipid carrier;Gemini surfactant;Formulation optimization
R943
A
1001-0408(2017)16-2259-03
2016-08-26
2016-10-20)
济宁医学院科研计划项目(No.JY2013KJ010)
*讲师,硕士。研究方向:药物新剂型与新技术。电话:0633-2983689。E-mail:sunshanshan815@163.com
#通信作者:教授,博士。研究方向:胶体药物传递系统。电话:0633-2983687。E-mail:wang_huiyun@126.com
DOI10.6039/j.issn.1001-0408.2017.16.27
