吉西他滨与培美曲塞联合顺铂治疗非小细胞肺癌的疗效比较及对血清肿瘤标志物的影响
2017-07-01吴红科姚菲菲张翠翠
卢 滨 吴红科 姚菲菲 张翠翠
吉西他滨与培美曲塞联合顺铂治疗非小细胞肺癌的疗效比较及对血清肿瘤标志物的影响
卢 滨 吴红科 姚菲菲 张翠翠
目的 探讨吉西他滨与培美曲塞联合顺铂治疗非小细胞肺癌(NSCLC)的疗效及其对血清肿瘤标志物的影响。方法 选取晚期NSCLC患者95例,随机分为对照组48例和观察组47例。在常规治疗基础上,对照组采用吉西他滨联合顺铂的治疗方案,观察组则采用培美曲塞联合顺铂的治疗方案。观察比较两组患者的治疗总有效率,治疗前后的血清肿瘤标志物水平,包括血清癌抗原125(CA125)、癌胚抗原(CEA)、神经元特异性烯醇化酶(NSE)以及细胞角质素片段抗原(Cyfra21-1),以及不良反应的发生情况。结果 治疗后,观察组临床治疗有效率为46.8%,对照组临床治疗有效率为43.8%,两组比较差异无统计学意义(P>0.05)。两组患者血清肿瘤标志物CA125、CEA、NSE及Cyfra21-1水平均有明显下降,且观察组的该4个指标水平显著低于对照组,差异具有统计学意义(P<0.05)。此外,观察组中性粒细胞减少、贫血以及血小板减少发生率显著低于对照组(P<0.05),而其他不良反应的发生情况比较无明显差异(P>0.05)。结论 培美曲塞联合顺铂与吉西他滨联合顺铂的治疗方案在NSCLC治疗中均效果良好,但培美曲塞联合顺铂治疗可明显改善血清肿瘤标志物水平,且不良反应发生率低,安全性好。
非小细胞肺癌;吉西他滨;培美曲塞;顺铂;血清肿瘤标志物
(ThePracticalJournalofCancer,2017,32:975~977)
肺癌是最为常见的1种肺部恶性肿瘤,近年来在全球范围内的发病率及死亡率逐年攀升,目前已居世界癌症患病率的首位,严重影响人们的生活质量及生命安全[1]。非小细胞癌症(NSCLC)是肺癌中的一大类,可占比全部肺癌的85%,已成为我国恶性肿瘤死亡率的首位[2]。而晚期NSCLC的手术治愈率较低,已逐渐不适于该种治疗方案,化疗则成为了主要治疗手段[3]。肿瘤标志物作为监测癌症患者化疗效果的主要指标,对于患者的预后以及后续治疗方案的制定极为重要[4]。然而,目前针对于全面化分析药物联用化疗对于癌症患者疗效以及对肿瘤细胞影响的研究鲜有报道。因此,本文拟比较分析吉西他滨与培美曲塞联合顺铂治疗NSCLC的疗效及其对血清肿瘤标志物的影响,现报告如下。
1 资料与方法
1.1 一般资料
选取2012年6月至2015年9月在郑州人民医院接受治疗的晚期非小细胞肺癌患者95例,随机分为对照组和观察组。对照组48例,男性28例,女性20例,年龄43~75岁,平均(51.7±5.4)岁。病理类型:腺癌39例,鳞癌9例;TNM分期标准:Ⅲa期10例,Ⅲb其11例,Ⅳ期27例;观察组47例,男性27例,女性20例,年龄44~75岁,平均(50.7±5.8)岁。病理类型:腺癌40例,鳞癌7例;TNM分期标准:Ⅲa期11例,Ⅲb其10例,Ⅳ期26例。两组性别、年龄、病理分类以及肿瘤分期等一般资料比较差异无统计学意义,具有可比性(P>0.05)。
1.2 纳入、排除标准
纳入标准:①经CT扫描、X线检查确诊为非小细胞肺癌;②肿瘤分期均为Ⅲ~Ⅳ期;③心电图、血常规以及血生化检验均正常;④本次治疗前未进行任何化、放疗,且所检测的血清肿瘤标志物至少有一项高于正常值。
排除标准:①易发生脑转移者;②血糖无法得到有效控制的糖尿病患者;③合并严重冠心病、肝肾功能不全者;④有本次研究涉及药物禁忌症者。
1.3 治疗方法
两组患者在化疗前1天、当天均给予地塞米松:4 mg/次,3次/d;维生素B12:1 mg/次,1次/d;叶酸:0.5 mg/次,1次/d。对照组患者在上述基础上,分别于第1天、第8天给予吉西他滨(江苏豪森药业股份有限公司,国药准字H20030105)1000 mg/m2,顺铂(江苏豪森药业股份有限公司,批准文国药准字H20010743)75 mg/m2,静脉注射;观察组患者在常规治疗上,第1天给予培美曲塞(江苏豪森药业股份有限公司,国药准字H20093996)500 mg/m2,顺铂75 mg/m2,静脉注射。治疗周期均为3周。
1.4 观察指标
观察记录治疗前后,两组患者的血清肿瘤标志物水平,包括血清癌抗原125(CA125)、癌胚抗原(CEA)、神经元特异性烯醇化酶(NSE)以及细胞角质素片段抗原(Cyfra21-1)的变化情况;观察比较两组患者的治疗有效率。
1.5 疗效评价标准
参照RECIST标准:完全缓解(CR):可见病灶均全部消失,肿瘤标志物水平正常,持续4周以上;部分缓解(PR):肿瘤病灶的直径总和低于基线≥30%,未出现新病灶;病变稳定(SD):病灶两径最大垂直径乘积增大或减小<25%,未出现新病灶;疾病进展(PD):病灶两径乘积的增大量≥25%,或有新病灶出现。治疗有效率=[(CR+PR)/总例数]100%。不良反应的评价参照WHO制定的抗癌药物反应分级标准:0~Ⅳ级。
1.6 统计学分析
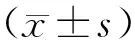
2 结果
2.1 两组患者的治疗效果比较
治疗后,观察组临床治疗有效率为46.8%,对照组临床治疗有效率为43.8%,两组比较差异无统计学意义(P>0.05),见表1。
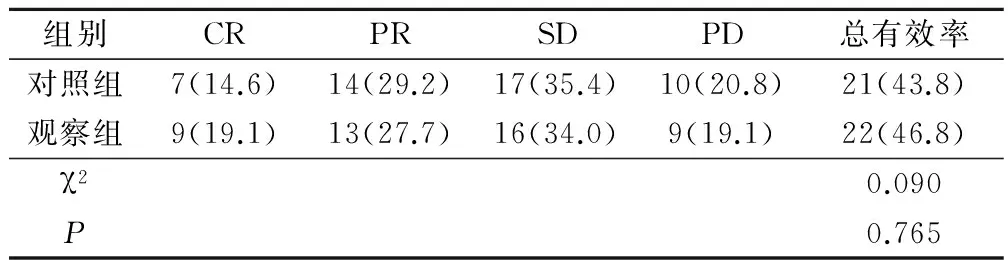
表1 两组患者的临床治疗效果情况比较(例,%)
2.2 治疗前后两组的血清肿瘤标志物水平比较
治疗前两组的血清肿瘤标志物水平比较无明显差异(P>0.05)。治疗后两组患者的血清肿瘤标志物水平均有明显下降,且观察组的4个指标水平显著低于对照组,差异具有统计学意义(P<0.05),见表2。
2.3 两组不良反应发生情况比较
治疗期间,两组均出现肝肾功能损伤、胃肠道反应、血液学毒性、皮疹、恶心等不良反应。其中,观察组中性粒细胞减少、贫血以及血小板减少的发生率显著低于对照组,差异具有统计学差异(P<0.05),而其他不良反应的发生情况比较无明显差异(P>0.05)。随着针对性的治疗后,所有患者的不良反应全部转好,见表3。
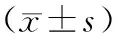
表2 治疗前后两组血清肿瘤标志物水平变化情况
注:与本组治疗前比较,▲为P<0.05。
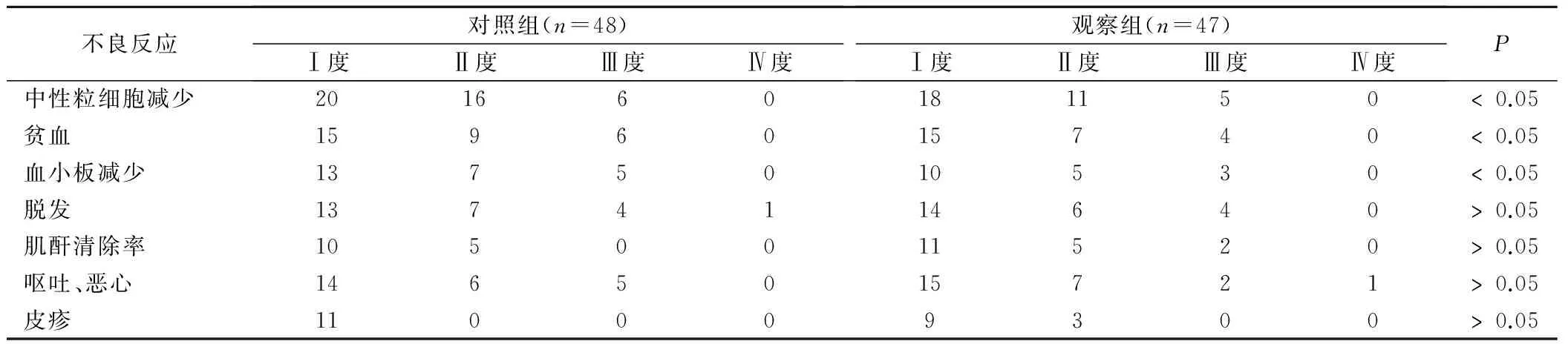
表3 治疗期间不良反应发生情况/例
3 讨论
近年来,针对于NSCLC的临床治疗仍以手术切除或放化疗为主,然而晚期的患者往往已失去手术治疗的最佳时机,放化疗就成为其唯一治疗的方法[5]。根据患者的病情结合药物治疗均可一定程度上延长NSCLC患者的生存时间及改善生活治疗[6],而晚期患者的生存率相对较低,早发现早治疗才是治疗的关键。培美曲塞是1类抗代谢癌药物,可同时有效抑制包括二氢叶酸还原酶、胸苷酸合成酶以及苷氨酰胺核苷甲酰基转移酶在内的多个叶酸依赖性代谢途径参与酶[7]。其可通过运载叶酸的载体以及叶酸结合蛋白的运输系统进入细胞,造成嘧啶和嘌呤的合成障碍,使细胞停滞于分裂间期(S期),而加快肿瘤细胞的凋亡,最终达到抗肿瘤作用[8]。另外,顺铂作用同于卡铂,是1类细胞周期的非特异性药物,可与DNA发生链间、链内的交联反应,引起DNA损伤,最终破坏DNA的复制和转录过程[9]。徐经芳等[10]研究表明,培美曲塞联合顺铂的治疗方案在治疗效果、控制率以及中位生存期等方面相近于吉西他滨联合顺铂的方案,但其在抑制血液毒性、脱发等方面效果明显。
血清肿瘤标志物是由肿瘤组织产生,多存在于肿瘤组织、血液及其他液体中,而在宿主细胞内其含量往往较正常参考值有明显升高[11]。由于检测的简单、快捷等优势,在对患者的疗效评价、病情发展状况评估中,血清肿瘤标志物具有明显的指示作用[12]。在针对于晚期NSCLC患者的化疗效果、改善预后以及后续治疗方案的制定中,血清肿瘤标志物的检测均能表现出优秀的指导作用[13]。本研究探究分析了吉西他滨与培美曲塞联合顺铂治疗非小细胞肺癌(NSCLC)的疗效及其对血清肿瘤标志物的影响,发现治疗后观察组的临床治疗有效率为46.8%,对照组的临床治疗有效率为43.8%,表明该2种治疗方案的疗效相当,均可达到治疗的目的。两组患者的血清肿瘤标志物CA125、CEA、NSE及Cyfra21-1均有明显下降,且观察组的该4个指标显著低于对照组,进一步证明血清肿瘤标志物在晚期NSCLC的药物结合化疗治疗中独特的疗效指示作用。此外,观察组的中性粒细胞减少、贫血以及血小板减少的发生率显著低于对照组,而其他不良反应的发生情况比较无明显差异。
综上所述,相较于吉西他滨联合顺铂的治疗方案,培美曲塞联合顺铂在晚期NSCLC的治疗中效果同样明显,并且可明显改善血清肿瘤标志物水平,且毒副作用发生率低,安全性好。
[1] Ryerson AB,Eheman CR,Altekruse SF,et al.Annual report to the nation on the status of cancer,1975-2012,featuring the increasing incidence of liver cancer〔J〕.Cancer,2016,122(9):1312-1337.
[2] Brahmer J,Reckamp KL,Baas P,et al.Nivolumab versus docetaxel in advanced squamous-cell non-small-cell lung cancer〔J〕.N Engl J Med,2015,373(2):123-135.
[3] Dimitroulis J,Stathopoulos GP.Evolution of non-small cell lung cancer chemotherapy (Review)〔J〕.Oncol Rep,2005,13(5):923-930.
[4] Jiang AG,Chen HL,Lu HY.The relationship between glasgow prognostic score and serum tumor markers in patients with advanced non-small cell lung cancer〔J〕.Bmc Cancer,2015,15(1):1-6.
[5] Arriagada R,Auperin A,Burdett S,et al.Adjuvant chemotherapy,with or without postoperative radiotherapy,in operable non-small-cell lung cancer:two meta-analyses of individual patient data〔J〕.Lancet,2010,375(9722):1267-1277.
[6] 田 伟,豆亚伟,戴 云,等.不同化疗方案治疗晚期非小细胞肺癌的临床疗效及肿瘤标志物与疗效的相关性研究〔J〕.河北医学,2016,22(8):1305-1307.
[7] Bover I,Begbie S,Tzekova V,et al.Maintenance pemetrexed plus best supportive care versus placebo plus best supportive care for non-small-cell lung cancer:a randomised,double-blind,phase 3 study〔J〕.Lancet,2009,374(9699):1432-1440.
[8] Lee JH,Yu CK,Shih JY,et al.Pemetrexed for heavily pretreated patients with advanced non-small cell lung cancer〔J〕.J Formos Med Assoc,2010,109(5):338-344.
[9] 彭东旭,方晓娟,杜均详,等.培美曲塞联合顺铂化疗对晚期非小细胞肺癌患者血清肿瘤标志物的影响〔J〕.临床肺科杂志,2016,21(7):1306-1309.
[10] 徐经芳.培美曲塞联合顺铂与吉西他滨联合顺铂治疗晚期非小细胞肺癌的临床研究〔J〕.现代肿瘤医学,2014,22(7):1572-1574.
[11] Cedrés S,Nuez I,Longo M,et al.Serum tumor markers CEA,CYFRA21-1,and CA-125 are associated with worse prognosis in advanced non-small-cell lung cancer (NSCLC)〔J〕.Clin Lung Cancer,2011,12(3):172-179.
[12] 姚 璧,乔晓媛.肿瘤标志物检测对晚期非小细胞肺癌长春瑞滨加顺铂方案化疗疗效的评价〔J〕.山西医药杂志,2014,43(18):2129-2131.
[13] Jiang AG,Chen HL,Lu HY.The relationship between glasgow prognostic score and serum tumor markers in patients with advanced non-small cell lung cancer〔J〕.Bmc Cancer,2015,15(1):1-6.
(编辑:吴小红)
Comparison of Clinical Efficacy of Pemetrexed or Gemcitabine Combined with Cisplatin for Patients with Non-small Cell Lung Cancer and Its Influence on Serum Tumor Markers
LUBin,WUHongke,YAOFeifei,etal.
People’sHospitalofZhengzhou,Zhengzhou,450003
Objective To investigate the clinical efficacy of pemetrexed or gemcitabine combined with cisplatin for patients with non-small cell lung cancer (NSCLC) and its influence on serum tumor markers.Methods 95 patients with NSCLC were randomly divided into the control group and the observation group.Based on conventional treatments,48 patients in the control group were treated with gemcitabine combined with cisplatin,and 47 patients in the observation group were treated with pemetrexed combined with cisplatin.The clinical efficacy,serum tumor markers including carcinoembryonic antigen (CEA),carbohydrate antigen 125 (CA125),neuronspecific anolase (NSE),and cytokeratin fragment antigen 21-1 (Cyfra21-1),and adverse reaction were investigated and compared.Results After treatment,total effective rate of the observation group was 46.8%,and that of the control group was 43.8% (P>0.05).And serum tumor markers including CA125,CEA,NSE,and Cyfra21-1 in both groups markedly decreased (P<0.05),and the 4 markers in the observation group were much lower than those of the control group (P<0.05).In addition,the incidence rate of neutropenia,anemia,and thrombocytopenia in the observation were significantly lower than those of the control group (P<0.05),while the changes in other adverse reactions between the 2 groups had no significant difference(P>0.05).Conclusion Gemcitabine combined with carboplatin and pemetrexed combined with cisplatin are effective for NSCLC,but pemetrexed combined with cisplatin can improve the levels of serum tumor markers with lower incidence of adverse reactions.
Non-small cell lung cancer (NSCLC);Gemcitabine;Pemetrexed;cisplatin;Serum tumor markers
450003 郑州人民医院
10.3969/j.issn.1001-5930.2017.06.031
R734.2
A
1001-5930(2017)06-0975-03
2016-11-09
2017-03-17)
