惠州市无偿献血者血液HBV,HCV,HIV(1+2型)核酸筛查汇集检测和单人份检测两种检测模式结果分析
2017-06-27万小春钟展华严凤好曾演强曾少丽湛玉武
万小春,钟展华,严凤好,曾演强,曾少丽,湛玉武
(惠州市中心血站,广东惠州516000)
惠州市无偿献血者血液HBV,HCV,HIV(1+2型)核酸筛查汇集检测和单人份检测两种检测模式结果分析
万小春,钟展华,严凤好,曾演强,曾少丽,湛玉武
(惠州市中心血站,广东惠州516000)
目的探索单人份检测模式与汇集检测模式两种血液核酸筛查方式对于血液核酸筛查结果的影响。方法先采用苏州华益美生物科技有限公司生产的乙型肝炎病毒、丙型肝炎病毒、人类免疫缺陷病毒(1+2型)核酸检测试剂盒(PCR-荧光法),对ELISA筛查合格的标本进行HBV、HCV、HIV(1+2型)核酸筛查(汇集检测模式),再用该试剂盒按照单人份检测模式对汇集检测过的样本进行复检。结果本研究采用单人份检测模式共检测5385例经过汇集检测模式筛查的样本,筛查出HBV DNA核酸阳性标本10例(阳性率1.86‰)。10例核酸阳性标本与汇集检测模式的结果一致,本研究的两种检测模式均未检测到HCV RNA核酸阳性和HIV(1+2型)RNA阳性的标本。结论在酶免检测的基础上应用核酸检测能有效避免HBV、HCV、HIV(1+2型)的漏检,降低输血传播相关病毒的风险。汇集检测和单人份检测两种检测模式对于检测结果无明显差异。
核酸检测;血液安全;单人份检测;汇集检测
病毒核酸检测技术(NAT)是直接检测病原体核酸的一系列技术的总称,相比血清学抗原抗体检测方法(EIA),血液病毒核酸检测技术可以有效缩短抗原抗体免疫检测的“窗口期”,从而大大降低经输血传播病毒的风险[1-3]。尽管NAT从理论上并不能完全消除病毒感染的“窗口期”,但可以有效地预防经输血传播病毒性疾病。单人份检测模式的标本处理相对直接,耗时较短,且即使出现检测阳性的样本也可以直接出具核酸检测结果而不必经过汇集检测的拆分检测,能有效缩短血液放行时间,实现快速检测,同时降低检测成本,血液核酸的单人份检测模式尤其适用于采样量相对较少的血小板样本的核酸检测以及日均采血量较少的血站开展核酸检测,因此,在原有核酸筛查试剂的技术基础上,以保证核酸检测结果准确性、稳定性为原则,开展了血液核酸单人份检测模式的探索,现将初步的研究结果报告如下。
1 材料与方法
1.1 标本2016年惠州市中心血站的无偿献血者标本5385例,献血者年龄为18~55周岁,经过HB-sAg、丙氨酸氨基转移酶筛查合格才允许捐献。
1.2 试剂与仪器
1.2.1 试剂NAT汇集检测采用苏州华益美生物科技有限公司产品,NAT单人份检测采用苏州华益美生物科技有限公司产品。
1.2.2 仪器华益美全自动核酸检测系统包括BACME全自动核酸提取系统(瑞士Hamilton)、ABI7500荧光PCR仪(美国ABI)。SLA-DI4800核酸提取仪(台湾)、ABI7500荧光PCR仪(美国ABI)。以上仪器均在校验合格期使用。
1.3 检测方法判定规则
1.3.1 常规检测所有血液标本均按照我国《献血者健康检查要求》(GB18467-2011)进行常规的HBsAg、抗-HCV、抗-HIV、抗-TP项目的2次ELISA检测和ALT项目的2次速率法检测,由不同人员用不同厂家的试剂严格按试剂说明书的要求进行检测。
任一种试剂检测为阳性的,重取血样双孔复试,复试任一孔为阳性的判定为不合格,其中2例抗HIV阳性标本送疾病预防控制中心确认实验确认。所有试验结果均按试剂盒说明书在实验室管理软自动判读。
1.3.2 核酸汇集检测对常规检测合格的标本进行核酸(NAT)检测,首先由全自动核酸提取仪自动混样,最多每8份标本(150μl/份)混合成1份(1.2ml)汇集池(pool)标本,由全自动核酸提取仪和荧光核酸扩增检测仪采用核酸定性筛查试剂进行HBV、HCV、HIV(1+2型)核酸检测。每批检测均设置1个阴性质控和1个阳性质控,1个外部阳性质控,每个汇集池均含DNA内对照(DNA IC)和RNA内对照(RNA IC)。
汇集检测为核酸阴性,汇集池中的标本合格;汇集检测为核酸阳性,对该汇集池子中的标本进行拆分检测,拆分检测无核酸反应性判定为NAT检测阴性,拆分检测为核酸阳性判定为NAT检测阳性。所有试验结果均按试剂盒说明书的要求用华益美实验室管理件自动判读。
1.3.3 核酸单人份检测每份标本分别取样400μl,按照操作说明书进行标本的处理、核酸扩增、分析,得出标本阴阳性结论。每批检测均设置1个阴性质控和1个阳性质控,每个样本和质控品均含DNA内对照(DNA IC)和RNA内对照(RNA IC)。该检测结果与汇集检测与拆分检测的结果进行分析。
2 结果
本实验严格按照考核试剂说明书要求操作,共对5385例临床用血标本进行了核酸检测。5385例EIA合格标本中,混合检测模式筛查出HBV DNA核酸阳性标本10例,在5385例标本中未检测到HCV RNA和HIV(1+2型)RNA阳性标本;5385例EIA合格标本中,单人份检测模式筛查出HBV DNA核酸阳性标本10例,在5385例标本中未检测到HCV RNA和HIV(1+2型)RNA阳性标本。
考核试剂检测单人份模式检测EIA合格的临床用血标本5385例。经考核试剂检测,其中10个样本检测为HBV DNA阳性,未检测到HCV RNA和HIV(1+2型)RNA阳性的样本。汇集模式检测EIA合格的临床用血标本5385例。汇集池数量为698个,其中检出阳性14个,拆分率2.0%,其中8个汇集池拆分检测出10例HBV DNA阳性样本,拆分收益率57.14%;汇集模式未检测到HCV RNA和HIV(1+2型)RNA阳性样本。
单人份模式结果和混合模式结果比对见表1~3。
3 讨论
我们采用单人份三联HBV DNA、HCV RNA和HIV(1+2型)RNA核酸鉴别检测试剂检测血液标本,实验结果显示惠州地区无偿献血人群中核酸初次反应率较低(1.86‰),这与汪德海等报道的结果基本一致,提示惠州地区的献血人群处于低感染状态,这有利于保障血液安全[4]。
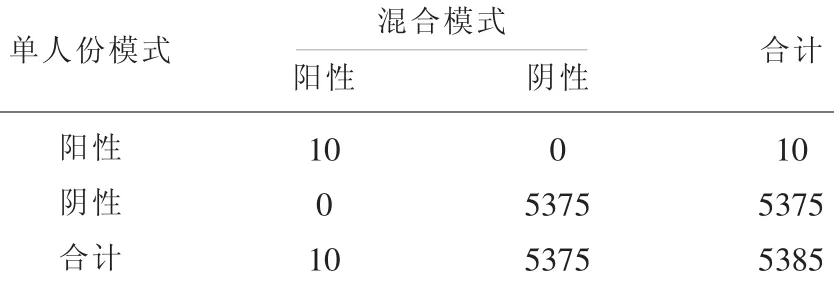
表1 单人份模式与混合模式HBV检测结果

表2 单人份模式与混合模式HCV检测结果

表3 单人份模式与混合模式HIV(1+2)检测结果
在本考核的5385例EIA合格标本中,混合检测模式筛查出HBV DNA核酸阳性标本10例,在5385例标本中未检测到HCV RNA和HIV(1+2型)RNA阳性标本;5385例EIA合格标本中,单人份检测模式筛查出HBV DNA核酸阳性标本10例,在5385例标本中未检测到HCV RNA和HIV(1+2型)RNA阳性标本,这可能与本次样本量较少有关,同时也显示HBV输血传播的残余风险高于HIV-1或HCV,本实验结果中NAT收益标本全部为HBV DNA反应性,这与已有的报道是相似的[5-10],也证实HBV输血传播的残余风险相对较高,这可能与我国HBV高感染率有关。
综上所述,在酶免检测的基础上进行核酸检测可以大大降低输血的残余风险,特别是HBV输血传播的残余风险;而核酸检测的两种模式汇集检测和单人份检测两种检测模式的结果一致,说明检测模式对于检测结果几乎没有影响。
[1]张妍,朱海峰,孙波,等.核酸检测技术在血液筛查中的应用及分析[J].中国输血杂志,2012,25(12):1298-1300.
[2]Yang MH,Li L,Hung YS,et al.The eficacy of individual-donation and minipool testing to detect low-level hepatitis B virus DNA in Taiwan.Transfusion,2010,50(1):65-74.
[3]颜秀娟.核酸血液筛查技术的应用进展[J].中国医药指南,2012,10(19):95.
[4]汪德海,王瑞,葛红卫.血站核酸检测实验室质量监控指标应用[J].中国输血杂志,2012,25(6):524-527.
[5]赵欣,王欢,李茂胜,李莹,等.实时荧光聚合酶链反应技术在献血者血液筛查中的应用[J].中国输血杂志,2014,27(1):65-68.
[6]Caodotti D,Allain JP.Transfusion-transmitted hepatitis B virus ifection[J].J Hepatol,2009,51(4):798-809.
[7]吕蒙恩,董杰,吴亚玲,祝宏,等.2011年杭州地区无偿献血者血液核酸筛查结果分析[J].中国输血杂志,2014,27(1):63-65.
[8]Shan H,Ren FR,Zhao HY,et al.A multi-Chinese blood centerstudy testing serologic negative donor samples for hepatitis C virus and human immunodefieiency virus with nucleic acid testing[J]. Transfusion,2007,47(11):2011-2016.
[9]梁浩坚,汪传喜,许结仪,等.2011~2014广州地区无偿献血者核酸检则结果分析[J].中国医药科学,2016,6(10):138-141.
[10]陈红,刘春兰,王亚彬,等.献血者HBV、HCV、HIV检测模式探讨[J].实验与检验医学,2014,32(6):778-779.
R193.3,R512.6,R512.91,R446.62
A
1674-1129(2017)03-0447-03
2016-12-19;
2017-04-04)
10.3969/j.issn.1674-1129.2017.03.054
