安宁滇红和紫枝玫瑰精油的出油率和香气成分分析
2017-06-23朱艳玲陈宣钦
朱艳玲,赵 雷,陈宣钦,杨 雁,*
(1.昆明医科大学海源学院,云南昆明 650106; 2.昆明医科大学第三附属医院云南省肿瘤医院,云南昆明 650118; 3.昆明理工大学,云南昆明 650504)
安宁滇红和紫枝玫瑰精油的出油率和香气成分分析
朱艳玲1,赵 雷2,陈宣钦3,杨 雁1,*
(1.昆明医科大学海源学院,云南昆明 650106; 2.昆明医科大学第三附属医院云南省肿瘤医院,云南昆明 650118; 3.昆明理工大学,云南昆明 650504)
采用水蒸汽蒸馏法从安宁八街滇红玫瑰和紫枝玫瑰中提取得到玫瑰精油,滇红玫瑰精油产率为0.125‰;紫枝玫瑰精油产率为0.185‰。两种玫瑰精油的物理性状基本一致。利用气相色谱-质谱联用(GC-MS)从滇红和紫枝玫瑰精油中分别鉴定出93个和65个组分。滇红玫瑰中各组分含量从高到低顺序为:烷烃>酚>酯>烯烃>醇>酮>醛酸。紫枝玫瑰中各成分含量从高到低为:烷烃>醇>醛>烯烃>酯>酮>酸。滇红和紫枝玫瑰精油的主要成分均为烷烃类,分别占总精油成分的47.600%和80.083%。滇红中甲基丁香酚的含量较高(18.584%),其作为食品添加香料具有较好的应用价值和潜力。
滇红,紫枝玫瑰,精油,气相色谱-质谱
云南是著名的“花卉王国”,花卉资源为全国之冠,具有适合各种花卉生长的气候条件,可食用花超过700种。云南食用玫瑰原引进品种为法国蔷薇,云南昆明近两千米的海拔,常年温暖的气候及酸性土壤环境十分适合它的生长,其在昆明及周边的种植历史已近20年[1]。现规模化种植的食用玫瑰多为法国蔷薇的变异种,其花朵香气浓,色泽鲜亮,品质好。天然的玫瑰精油是最重要的天然香料来源之一,也是生产现代工业玫瑰精油和各种护肤品的重要原料。天然玫瑰的精油组成十分复杂,主要成分是单萜类化合物,如玫瑰醚、香茅醇、香叶醇、芳樟醇、倍半萜烯和倍半萜等,其它的化合物烷烃系列(C17~C27)占量很大,其中香叶醇、香茅醇、橙花醇与它们的酯类构成了玫瑰花香的基本成分,也是玫瑰的主体香气成分[2]。这些化学成分种类及含量的差异,造成了玫瑰油香气的微妙差异。
不同产地的玫瑰出油量和香气成分具有很大不同。彭艳丽[3]等从产于平阴的丰花一号玫瑰精油中发现了28个化合物,确认了 22 种,从产于甘肃枯水的丰花一号发现了69种化合物,确认了25种;从产于吴江的丰花一号发现70种化合物,确认了26种。不同产地的玫瑰花出油率和化学成分不同主要可能与气候、土壤等因子有关。云南昆明市安宁八街镇是食用玫瑰的重要种植基地,种植的品种包括有滇红玫瑰、紫枝玫瑰、金边玫瑰,其中以滇红玫瑰和紫枝玫瑰最为盛产[4]。云南是滇红玫瑰的主要产地,目前安宁八街的食用玫瑰滇红主要是鲜花饼和玫瑰糖的制作原料,其精油化学成分未见报道。紫枝玫瑰在山东,甘肃和陕西等地均有种植,安宁八街镇的紫枝玫瑰主要用于制作花茶。张海云曾经对山东产紫枝玫瑰精油进行了GC-MS分析,鉴定了55个香气成分[5]。本文主要分析比较安宁产的滇红玫瑰和紫枝玫瑰的出油率和化学成分差异,探讨云南产玫瑰花精油的香气成分,为滇红玫瑰和紫枝玫瑰的食用价值提供理论基础,拓宽两种玫瑰的使用和开发价值。
1 材料与方法
1.1 材料与仪器
玫瑰花样品 食用玫瑰滇红干花瓣、紫枝玫瑰干花瓣 安宁八街玫瑰种植示范基地。
DZTW型调温电热套10000 mL 北京市永光明医疗仪器有限公司;2W型(WZS 1型)阿贝折折仪 上海光学仪器厂;JA1003N型分析天平 上海菁海仪器有限公司;HP6890GC/5973MS气相色谱-质谱联用仪 美国Agilent Technologies公司。
1.2 实验方法
1.2.1 玫瑰精油的提取 准确称取云南食用滇红玫瑰干燥花瓣1000 g,分两次置于圆底烧瓶中,加入适量蒸馏水,连接挥发油测定器与球形冷凝管,以恒温电热套加热,控制电热套电压为200 V,温度控制在100~110 ℃之间保持水沸腾产生蒸汽,水蒸气蒸馏法连续提取8 h。停止加热后,挥发油测定器精油测量处收集精油,并用10 mL 二氯甲烷冲洗精油测量处,将提取液转移到分液漏斗中,摇匀后静置分层,收集二氯甲烷层,加入过量的无水硫酸钠干燥,保存于冰箱中过夜。第2 d,40 ℃蒸馏挥发完二氯甲烷,剩余得到黄色透明液体即滇红玫瑰精油,供物理分析及GC/MS 分析用[6]。紫枝玫瑰精油同法制得。
1.2.2 GC/MS分析 GC条件:HP-5MS石英毛细管柱(30 mm×0.25 mm×0.25 mm);柱温:起始温度80 ℃,程序升温3 ℃/min至280 ℃,保持20 min;柱流量为1.0 mL/min;进样口温度250 ℃;柱前压100 kPa;分流比30∶1;进样量0.4 mL;载气为高纯氦气。
MS条件:电离方式EI;电子能量70 eV;传输线温度250 ℃;离子源温度230 ℃;四极杆温度150 ℃;质量范围35~500 u;采用wiley7n.l标准谱库检索定性。
2 结果与分析
2.1 玫瑰精油产率
从表1中可见,紫枝玫瑰的出油率高于食用滇红玫瑰。

表1 紫枝玫瑰和食用滇红玫瑰精油产率对比Table 1 Comparison of oil yield of purple rose and Dianhong rose
2.2 物理特性
紫枝玫瑰精油颜色亮黄颜色略比食用滇红玫瑰深,同时紫枝玫瑰的折光率和密度也率大于食用滇红玫瑰[6]。
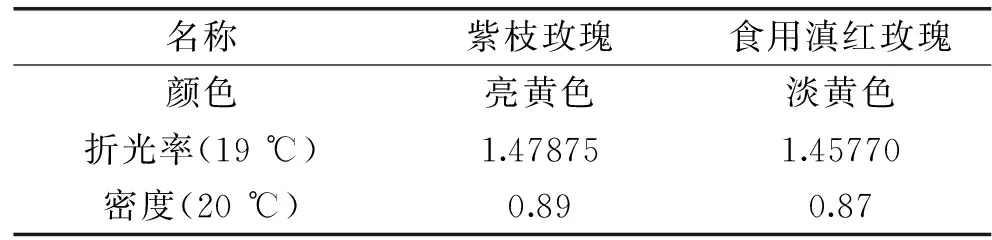
表2 紫枝玫瑰和食用滇红玫瑰精油物理特性对比Table 2 Comparison of physical properties of oil from purple rose and Dianhong rose
2.3 成分分析
2.3.1 两种玫瑰精油的香气成分分析 按照GC-MC条件获得了两个精油样品的总离子流色谱(见图1,图2),将总离子流色谱图的结果与计算机质谱库匹配,再根据分子量及人工解析确定精油样品化学组分的名称,采用峰面积归一化法计算出各组分含量(表3和表4,不含相对含量小于0.01%的成分)[7]。
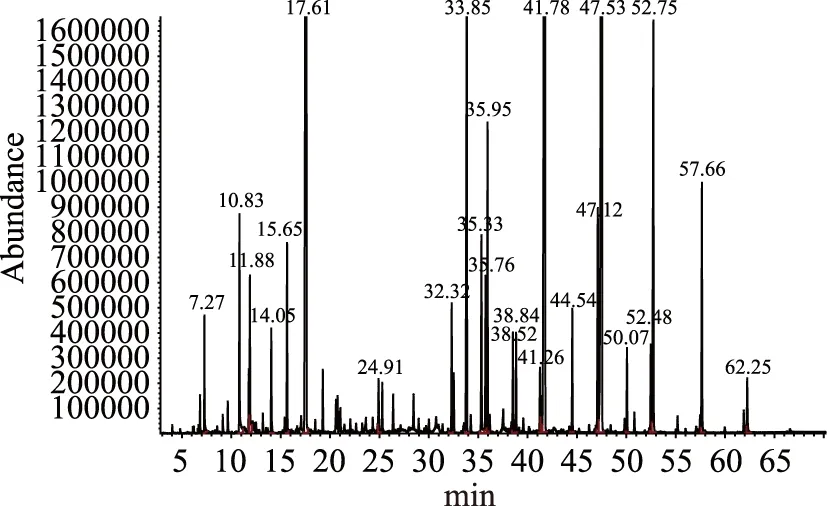
图1 食用滇红精油GC-MS总离子流图Fig.1 GC-MS total ion chromatogram of Dianhong rose oil
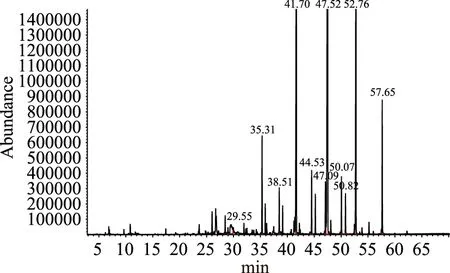
图2 紫枝玫瑰精油GC-MS总离子流图Fig.2 GC-MS total ion chromatogram of purple rose oil
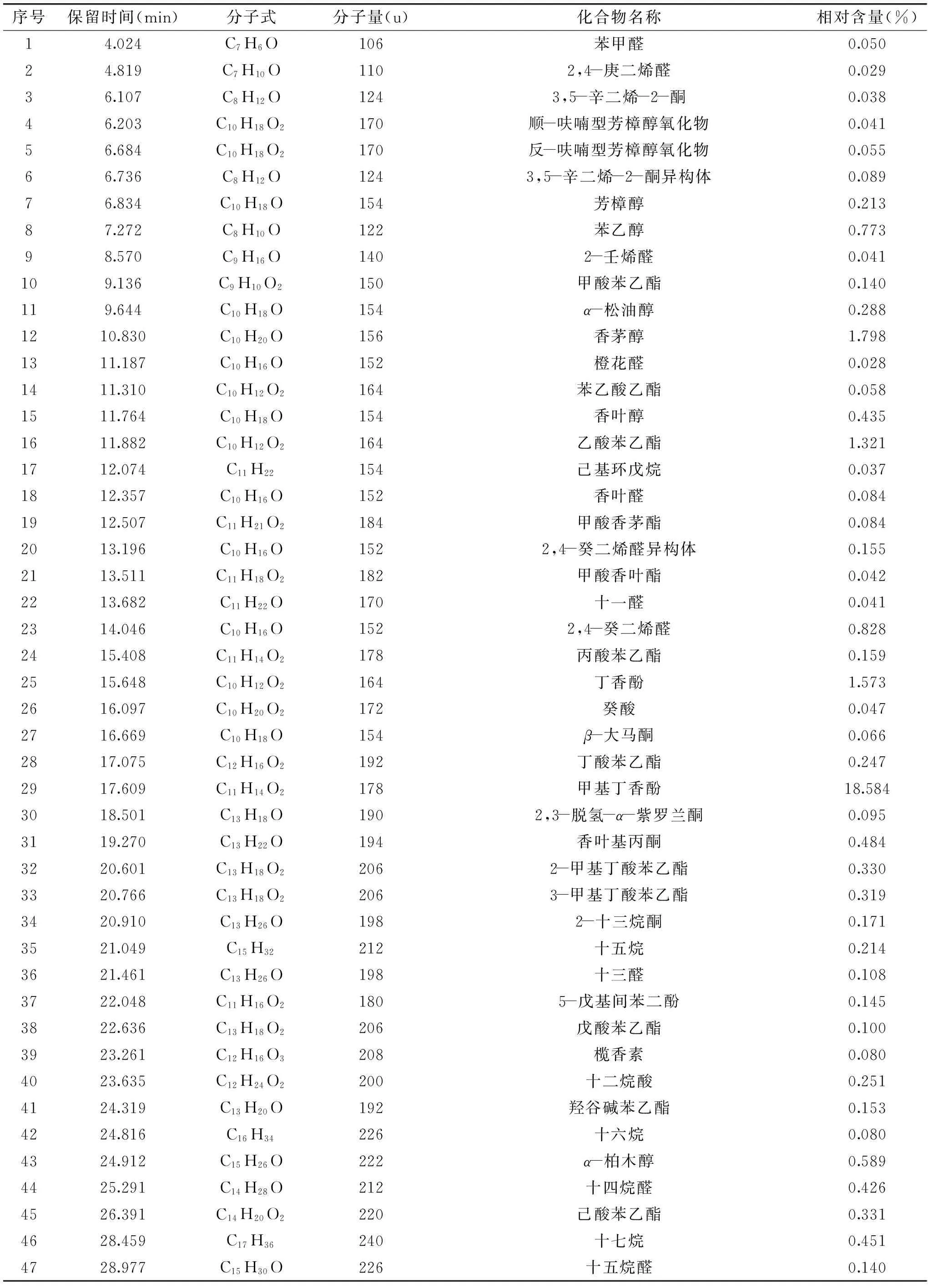
表3 食用滇红精油样品成分分析结果Table 3 Analysis results of aroma component essential oil of DianHong rose samples
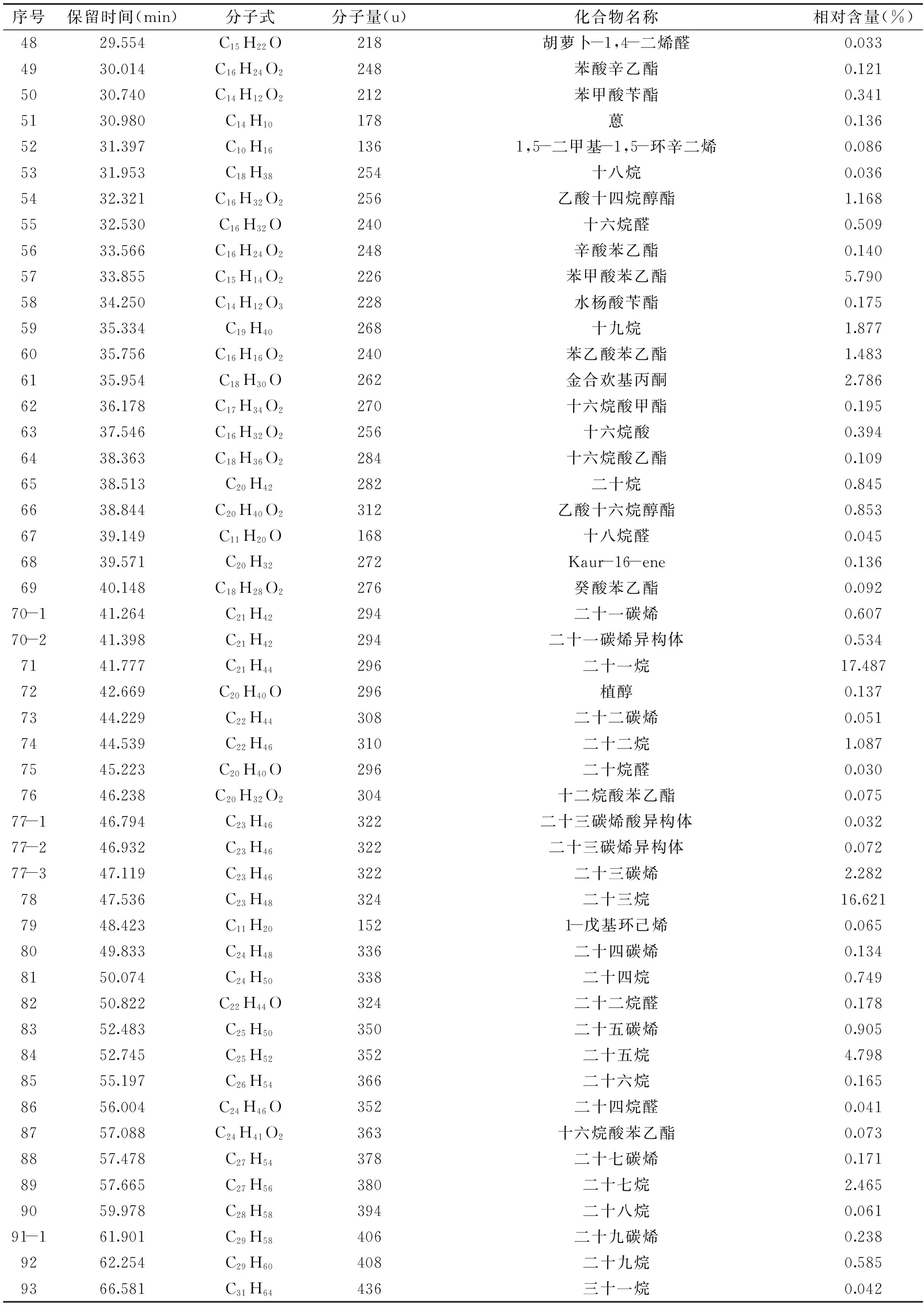
续表
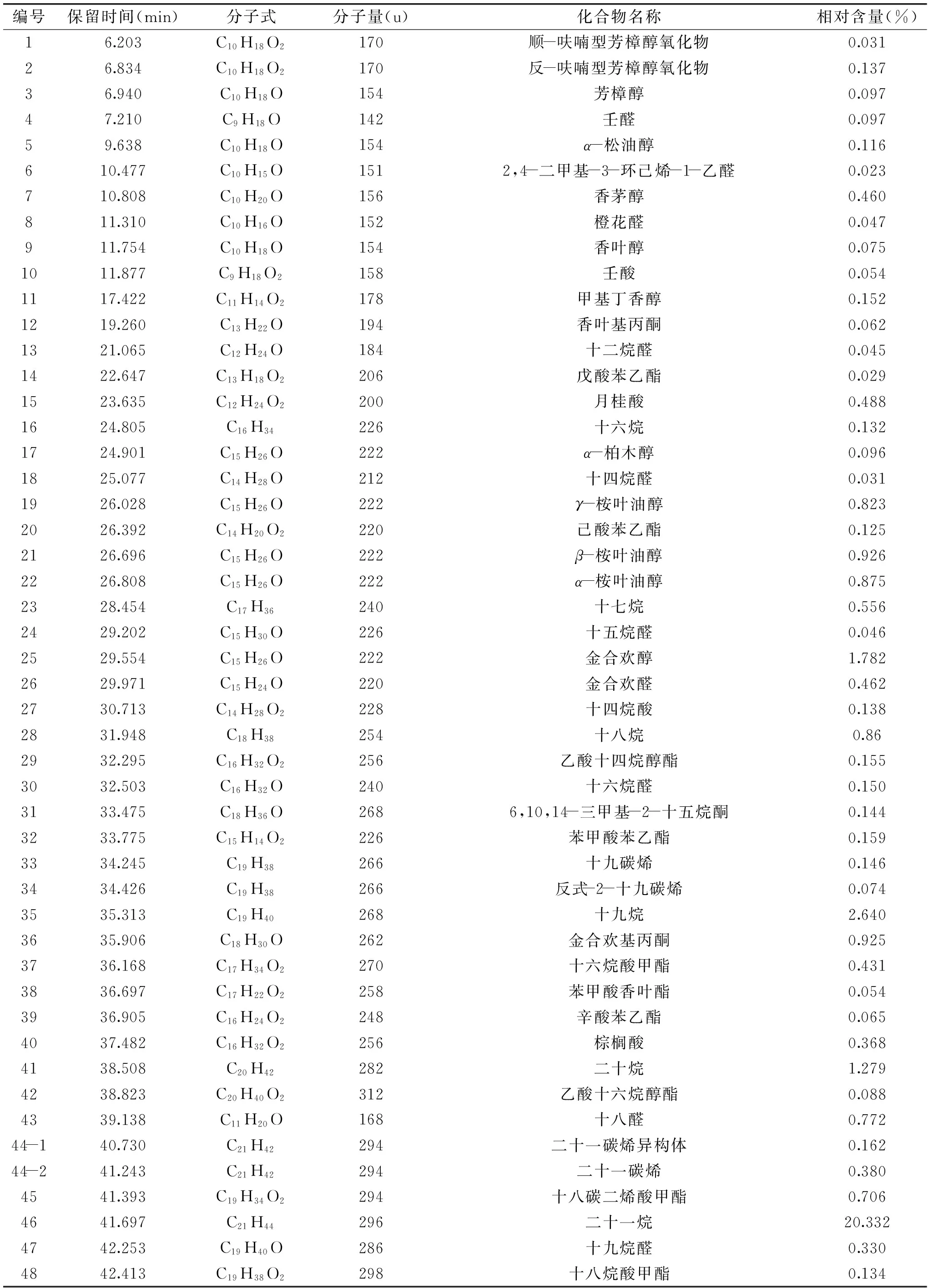
表4 紫枝玫瑰精油样品成分分析结果Table 4 Analysis results of aroma component essential oil of Purple Rose samples
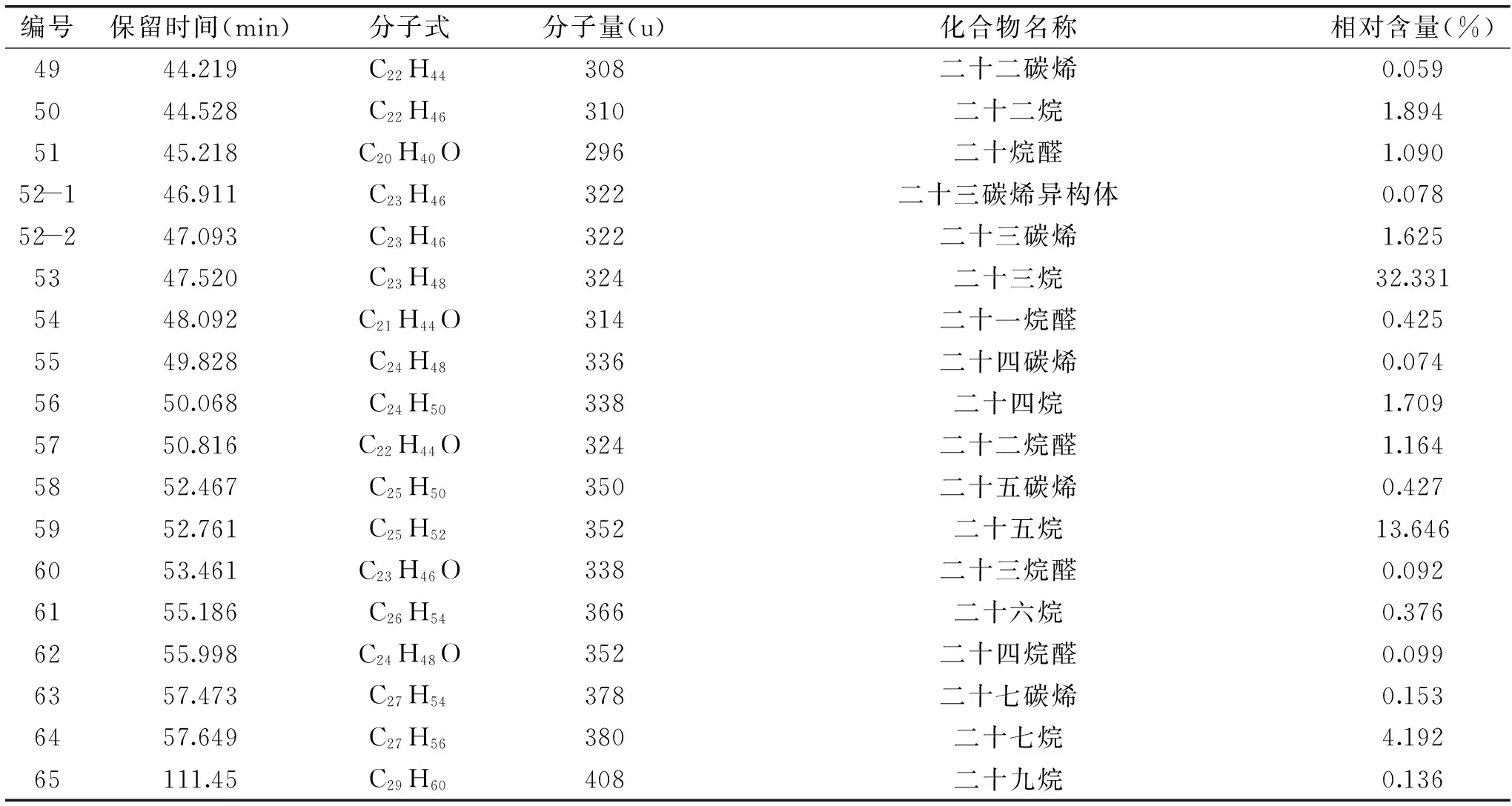
续表
从表3可见,食用滇红的香气组分中含量0.01%以上有93种,占香气总面积的98.85%。食用滇红主要的化学成分是烷烃类,共17种,占47.6%,其中十一烷含量为17.49%,二十三烷含量为16.62%;含量较高的组分是酚和酯,其中酯共25种,占13.899%;酚3种,占20.30%,酚主要成分是甲基丁香酚(18.584%)。含量较低的成分包括烯烃类共11种,含量5.145%;醛共17种,含量2.766%;酸共4种,含量0.724%;醇共9种,含量4.329%;酮共7种,含量3.729%[8]。
从表4可见,紫枝玫瑰含量0.01%以上的成分共65种,占香气总面积的97.829%。主要成分为烷烃类共13种,占80.083%,其中含量较高的烷烃类包括二十一烷含量为20.332%,二十三烷含量为32.331%,二十五烷含量为13.646%。其它烯烃类共10种,含量3.178%;醛共15种,含量4.873%;酯共10种,含量1.946%;酸共4种,含量1.048%;醇共12种,含量5.57%;酮共3种,含量1.131%。
3 结论
天然玫瑰精油的化学成分非常复杂,该实验报道的化学成分与文献报道一致,安宁产的两种食用玫瑰与其它品种食用玫瑰花一样,化学成分以烷烃类为主,其它次要成分包括酚,酯,烯烃,醇,酮,醛和酸类。云南虽然气候特殊,但除化学成分含量略有差异外,云南产玫瑰花的化学成分与其它产地的品种无明显的差异[9]。
值得注意的是,滇红玫瑰中含有较高的甲基丁香酚,而紫枝玫瑰中没有发现,甲基丁香酚可以作为区分滇红和紫枝玫瑰的一个化学成分指标。甲基丁香酚具有特异的香气,是一种常用食品调香剂,在很多的食品的均有添加[10]。很多香料植物如柠檬,香茅和胡椒均含有甲基丁香酚。除在大马士革玫瑰精油中发现甲基丁香酚含量较高外,国产的很多的玫瑰花中甲基丁香酚的含量均较低,滇红玫瑰花作为食品添加香料具有较好的应用价值和潜力。
[1]王晓霞,阴耕云,徐世涛,等. 云南食用玫瑰精油化学成分的GC-MS分析及其应用研究[J].云南大学学报(自然科学版),2011,33(S2):414-417.
[2]李延辉,薛晓丽,李林,等. 长白山玫瑰精油化学成分的分析[J]. 食品研究与开发,2013,34(9):65-68.
[3]彭艳丽,张炳桢,牟宗慧,等. 不同产地玫瑰花挥发油GC-MS分析[J].食品与药品,2009,11(3):35-38.
[4]柏斌. 安宁成云南食用玫瑰主产地[N].中国花卉报,2012-06-19(010).
[5]张海云,吕传润,孟宪水. 新品种丰花玫瑰与紫枝玫瑰出油率及成分的探讨[J].香料香精化妆品,2009(2):11-16.
[6]Khan M A,Rehman S U. Extraction and analysis of essential oil of rosa species[J]. International Journal of Agriculture & Biology,2005,7(6):973-974.
[7]Verma R S,Padalia R C,Chauhan A. Chemical investigation of the volatile components of shade-dride petals of damask rose(RosaDamascenaMill.)[J]. Arch Biol Sci,Belgrade,2011,63(4):1111-1115.
[8]余峰,张彬,周武,等. 玫瑰精油的提取和理化性质分析[J]. 天然产物研究与开发,2012,24:784-789.
[9]李延辉,薛晓丽,于连贵,等. 长白山玫瑰精油化学成分分析[J].食品研究与开发,2013,34(9):65-68.
[10]周慧秋,于滨,乔婉红,等. 甲基丁香酚药理作用研究[J].中医药学报,2000(2):79-80.
Oil yield and aroma component analysis of Anning Dianhong rose and purple rose essential oil
ZHU Yan-ling1,ZHAO Lei2,CHEN Xuan-qin3,YANG Yan1,*
(1.KunMing Medical University HaiYuan College,KunMing 650106,China; 2.The Third Affiliated Hospital of KunMing Medical University,The Tumor Hospital of YunNan province and The center of PET/CT,KunMing 650118,China; 3.Kunming University of Science and Technology,KunMing650504,China)
The essential oil of Dianhong rose and purple rose which planted in Anning city were obtained through steam distillation,with yield of 0.125‰ and 1.85‰. The physical properties of the two rose essential oils were basically the same. 93 compositions were identified using gas chromatography-mass spectro- metry(GC-MS)from Dianhong rose essential oil,and 65 compositions were identified using gas chromatography-mass spectrometry(GC-MS)from purple rose essential oil. The content of each component in Dianhong rose was from high to low:alkanes>phenols>esters>alkenes>alcohols>ketones>acids. The content of each component in Purple rose is from high to low:alkanes>alcohols>aldehydes>alkenes>esters>ketones>acids. Alkanes is the main components in essential oil of purple rose(47.600%)and dianhong rose(80.083%). Dianhong rose has high content of methyl eugenol(18.584%),it as the food add spices has good application value and potential.
Dianhong;purple rose;essential oil;GC-MS
2016-11-11
朱艳玲(1982-),女,硕士,讲师,主要从事天然产物化学研究,E-mail:516567220@qq.com。
*通讯作者:杨雁(1985-),女,硕士,讲师,主要从事天然产物化学研究,E-mail:516567220@qq.com。
云南省教育厅一般项目(2014Y664)。
TS207.3
A
1002-0306(2017)11-0299-06
10.13386/j.issn1002-0306.2017.11.049
