高纯度Nisin的制备及工业生产条件的优化
2017-06-23陈艺强李光进金陈斌洪超群
陈艺强,李光进,金陈斌,许 峰,叶 艇,洪超群
(浙江新银象生物工程有限公司,浙江台州 317200)
高纯度Nisin的制备及工业生产条件的优化
陈艺强,李光进,金陈斌,许 峰,叶 艇,洪超群
(浙江新银象生物工程有限公司,浙江台州 317200)
研究了一种制备高纯度Nisin的方法。该方法采用弱酸性离子交换树脂D113对Nisin浓缩液进行静态吸附和动态解吸,然后将解吸液进行盐析、抽滤、烘干、粉碎即得高纯度Nisin。结果表明pH为6,吸附时间为90 min,解吸剂为1 mol/L、V盐酸/V乙醇=1.25的盐酸乙醇溶液,解吸速率为1 BV/h,盐析所用氯化钠浓度为23%为最佳条件,获得的Nisin效价可达34000 IU/mg,收率达到67.45%,具有较好的工业应用前景。
高纯度,乳酸链球菌素,离子交换
乳酸链球菌素又为乳酸链球菌肽,是一种由34个氨基酸残基组成的抗菌肽[1],对Gram阳性菌有抑制作用,被认为是一种天然的,高效的食品防腐剂而广泛应用于各类食品[2-3]。但是目前市场上销售的都是纯度较低的乳酸链球菌素盐制剂,效价约为1000 IU/mg,杂质较多且盐含量高,对食品风味有一定的影响。而高纯度乳酸链球菌素可用于解决此类问题,例如高纯乳酸链球菌素应用于燕窝,海参,浓缩果汁等[4-5]。此外还可用于医药领域的研究。例如治疗奶牛乳房炎[6],进一步纯化可用于头、颈部鳞状细胞癌症的研究[7-8]。有关高纯度Nisin制备的专利及文献过去均有报导[9-11],但纯度不是很高,严宇媛等人的工艺中Nisin效价只有28000 IU/mg,或者收率较低,叶万荣等人的工艺收率只有30%,成本较高,不适合工业生产。本文研究的高纯度Nisin制备工艺在以期在保证纯度的同时保证较高的收率,适合于大规模工业化生产。
1 材料与方法
1.1 材料与仪器
Nisin标准品(sigma),Nisin浓缩液 浙江新银象生物工程有限公司,由发酵液过滤后浓缩而成;离子交换树脂110,D 113,122 安徽三星树脂科技有限公司;D M130,HZ-8,D61树脂 上海华震科技有限公司;乙醇 分析纯,杭州高晶精细化工有限公司;盐酸 分析纯,浙江中星化工试剂有限公司;氯化钠 分析纯,西陇化工股份有限公司;蒸馏水等试剂。
SHZ-88A水浴恒温振荡器 太仓市实验设备厂;DHG-9070A型恒温干燥箱 上海精宏实验设备有限公司;BT 100-2J型蠕动泵 longer pump;层析柱 5.3 cm×70 cm;DFY-300摇摆式高速万能粉碎机 温岭市林大机械有限公司。
1.2 静态吸附与解吸实验
1.2.1 树脂的筛选 准确量取预处理好的6种树脂各10 mL分别倒入250 mL锥形瓶中(其中110,D113,122均转为钠型树脂),加入pH为3的Nisin浓缩液50 mL,25 ℃下将锥形瓶置于振荡频率为60 r/min的摇床吸附4 h。然后抽滤,用蒸馏水洗涤树脂,滤液取样检测。然后将树脂加入到100 mL浓度为1 mol/L的盐酸乙醇溶液中在相同条件下解吸。4 h后抽滤,取解吸液检测。并按如下公式计算吸附量,吸附率,解吸率[12]。
式(1)
式(2)
式(3)
收率(%)=吸附解吸收率×盐析收率
式(4)
其中:C0为初始溶液中Nisin浓度;CP为吸附平衡时溶液中Nisin的浓度;m为树脂的质量;V为吸附液体积;Cj为解吸液中Nisin的浓度;Vj为解吸液体积。
1.2.2 吸附pH的影响 分别取4 L效价为100000 IU/mL左右的Nisin浓缩液6份,分别加入800 mL D113树脂,于常温下各自在pH为3、4、5、6、7、8下进行搅拌吸附。1.5 h后取样检测残液中Nisin含量并计算吸附率。吸附完全后,分别上柱,动态解吸。解吸液盐析、抽滤、烘干、粉碎并检测成品效价。
1.2.3 吸附时间的影响 分别取4 L效价约为100000 IU/mL左右的 Nisin浓缩液5份,加入800 mL D113树脂,常温下在pH6时分别搅拌15、30、45、60、90 min。分别取样检测残液中Nisin效价。
1.2.4 解吸剂配比实验 计算并量取不同浓度的盐酸与乙醇分别按体积比4∶1,2∶1,1.5∶1,1.25∶1,1.2∶1,1.1∶1,1∶1,1∶1.1,1∶1.3比例配成最终浓度为1 mol/L的盐酸乙醇溶液,采用动态解吸法对已吸附好树脂进行解吸,解吸时流速为1.0 BV/h,分别收集解吸液,检测并记录解吸收率。解吸液盐析、抽滤、烘干粉碎并检测成品效价。
1.2.5 解吸流速的影响 将V盐酸/V乙醇=1.25的解吸剂分别以0.5,0.75,1.0,1.25,1.5 BV/h流速进行解吸,分别收集解吸液,检测并记录解吸收率。吸液盐析、抽滤、烘干粉碎并检测成品效价。
1.2.6 吸附pH,解吸剂配比,解析流速的正交实验 考虑到吸附时间的交互作用较小,在单因素实验基础上分别以吸附pH,解吸剂配比,解吸流速进行L9(34)正交实验,因素水平如表1所示,分别以效价和收率为指标,得出高纯度Nisin制备的最佳工艺条件。

表1 因素水平表Table 1 Factors and levels of orthogonal test
1.3 盐析实验
在最佳条件下吸附解吸,然后将解吸液分别加入15%、20%、23%、25%、27%、30%的氯化钠盐析,搅拌2 h。然后静置12 h、抽滤、烘干、粉碎检测效价并计算盐析收率。
1.4 检测方法
液体浓度与Nisin成品均采用GB1886.231-2016中的方法进行检测。
2 结果与讨论
2.1 树脂筛选结果
不同树脂结果见表2。从表2中可以看出弱酸性树脂的吸附量均大于强酸性树脂的吸附量,这可能是由于Nisin以离子形式存在时,强酸性树脂吸附氢离子的能力要大于Nisin。而弱酸性阳离子树脂由于转为钠型之后,其对钠离子的吸附选择性要小于Nisin。从而造成它们的吸附容量差别很大。大孔吸附树脂DM130由于其物理吸附性能以及依靠其孔径大小而具有选择性,其吸附量介于强酸性树脂和弱酸性树脂之间,理论上我们可以根据孔径的大小选择一种更为合适的树脂,但是实验中发现大孔树脂解吸液中的杂质含量并没有降低,起不到除杂质的作用,而离子交换树脂能明显降低杂质的含量。弱酸性阳离子树脂中又以D113的吸附解吸性能较优,因为其兼备大孔树脂的吸附作用和离子交换能力,综合以上因素考虑,选择D113作为合适的吸附树脂。
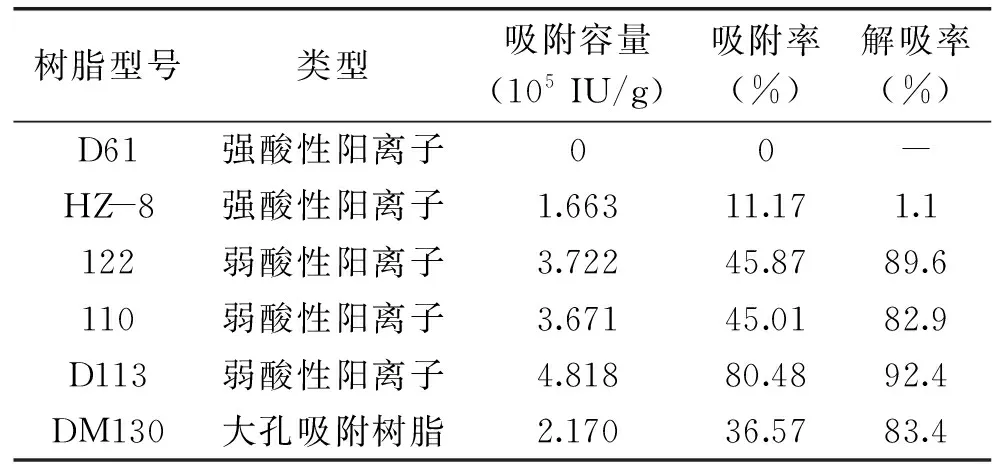
表2 树脂的吸附解吸性能参数Table 2 Performance parameters of resin adsorption and desorption
2.2 吸附pH的影响
从图1中看出随着pH升高,效价不断的升高,呈递增状态。实验中发现当pH在4~5之间的时候有大量絮状析出,絮状物经调pH重新溶解后检测到里面含有部分Nisin。
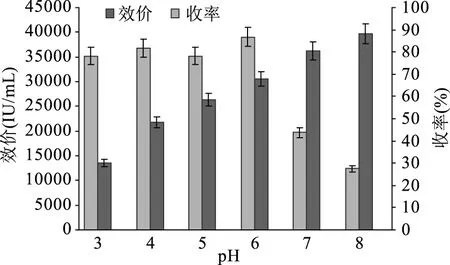
图1 吸附pH与效价、收率关系图Fig.1 Relationship of adsorption pH,yield and potency
此絮状物经烘干称量后发现其质量远大于相同效价的Nisin重量,推测其为杂蛋白,此pH区间为杂蛋白的等电点区间。而Nisin的等电点在9.5左右[13],当pH超过5时杂蛋白以阴离子形式存在,不被树脂吸附,相反Nisin却能继续被树脂吸附。因此,当pH3时,树脂的选择性很差,而pH从3升至4时其效价差别较大,同时由于Nisin的稳定性受pH影响[14],当pH大于6时,其收率急剧下跌,综合考虑pH6作为吸附pH比较合理。
2.3 吸附时间的影响
考虑到吸附时间对成品效价影响不大,主要考察了其对吸附残液效价的影响。结果如图2所示。吸附时间为15 min时,将近85%的Nisin已被吸附,之后延长吸附时间,吸附速度明显降低,90 min时溶液中的Nisin已被吸附完全。表明90 min作为最佳吸附时间较合理。

图2 吸附残液效价-时间图Fig.2 Time profile of adsorption raffinate potency
2.4 解吸剂配比对高纯度Nisin收率的影响
单纯采用酸水或者乙醇均不能很好地将吸附在树脂中的Nisin解吸下来。本文采用酸水与乙醇的混合溶液进行解吸,解吸效果如图3所示。V盐酸/V乙醇比例在1附近时,其收率较高,都在85%以上,比例为1.25时达到最高95.93%,比例大于1.25或小于0.91时均收率下降明显。可能是D113具备离子交换和大孔树脂的物理吸附能力,盐酸比例的升高,氢离子浓度增大,从而使Nisin更多的被交换下来,但同时又考虑到乙醇对大孔树脂的解吸能力,所以其比例过高或者过低均不利于解吸。同时V盐酸/V乙醇比例小于1.25时其效价较高,均在35000 IU/mL左右,比例大于1.25时效价下降明显。效价随着盐酸用量的加大呈下降趋势,可能是杂质所带电荷与Nisin相同,但其吸附能力较Nisin更强。考虑到效价与收率的因素,V盐酸/V乙醇=1.25是较为合适的解吸剂配比。
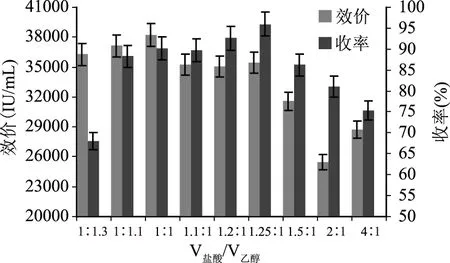
图3 解吸剂配比与收率、效价关系图Fig.3 Relationship of desorption rate,yield and potency
2.5 解吸流速对高纯度Nisin收率的影响
分别以0.5,0.75,1.0,1.25,1.5 BV/h流速进行解吸,结果如图4所示。从图中可以看出解吸速率对收率以及效价的影响并不是很大,但是在解吸速率为1.0 BV/h时收率为最高达到93.3%。

图4 Nisin解吸流速、收率、效价关系图Fig.4 Relationship of desorption flow,yield and potency
2.6 正交实验
考虑到多因素的交互关系,设计了相关的正交实验,实验结果如表3所示,对效价来说极差最大的是B,因素主次顺序为B>C>A,最优组合为B1C2A3。对收率来说因素主次顺序为B>A>C,最优组合为B1C2A2。考虑到A因素在两个指标中的主次顺序,我们选择B1C2A2作为最佳组合,即吸附pH为6,解吸剂比例V盐酸/V乙醇为1.25∶1,解吸流速为1.0 BV/h作为最佳工艺条件,此时,效价为35105 IU/mg,收率为90.79%。

表3 吸附,解吸正交实验表Table 3 Orthogonal experiment table of Adsorption and desorption
2.7 盐析实验
在以上正交实验最佳条件下吸附解吸,然后在解吸液中分别加入15%、20%、23%、25%、27%、30%的氯化钠进行盐析,盐析结果如图5所示。盐析成品效价随着氯化钠的加入量呈下降趋势,盐析收率随氯化钠的用量呈上升趋势,当氯化钠的用量大于23%时,收率变化不大,在23%时收率达到74.29%左右。总收率为90.79%×74.29%=67.45%,且此时Nisin效价达到34180 IU/mg,考虑到工业生产对收率的需求,选择浓度为23%的氯化钠来进行盐析。

图5 不同氯化钠浓度盐析图Fig.5 Effect of different NaCl concentration in salting out process
3 结论与讨论
综合以上实验结果分析,影响Nisin纯度的主要因素有树脂吸附时的pH、吸附剂配比、解吸速度以及盐析时氯化钠的用量,而这些因素均会影响到成品的收率,既考虑到纯度要求,同时又考虑到工业化生产的经济效益,所以本实验选择的工艺条件是:树脂采用D113弱酸性阳离子交换树脂,吸附pH为6,吸附时间90 min,解吸剂比例V盐酸/V乙醇为1.25∶1,解吸流速为1.0 BV/h,23%的氯化钠进行盐析。此工艺可获得效价大于34000 IU/mg的Nisin粉,同时总收率能达到67.45%。获得的Nisin可进一步提纯以用于医药领域,未来市场及其可观。
[1]郭本恒.功能性乳制品[M].中国轻工业出版社,2001:332-346.
[2]张玉华,孟一.天然食品防腐剂-nisin的应用[J].食品研究与开发,2003,24(2):109-110.
[3]石小琼,饶华明,张映斌,等.天然食品保鲜防腐剂nisin在豆腐保鲜上的研究应用[J].食品添加剂,2004,11:130-131.
[4]朱露露,农邵庄,李江阔,等. 两种生物保鲜液对鲜活海参贮藏品质的影响[J].食品工业,2015,36(6):128-132.
[5]夏云梯,潘立华,朱克美. 乳酸链球菌素(Nisin)的特性及在果汁钦料中的应用[J].饮料工业,2000,3(4):14-15.
[6]吴俊强,曹立婷,胡松华. 乳酸链球菌素治疗奶牛乳房炎效果观察[C].兽医临床学术会,2008:397-400.
[7]Pachiyappan Kamarajan,Takayuki Hayami,Bibiana Matte,et al. Nisin ZP,a Bacteriocin and Food Preservative,Inhibits Head and Neck Cancer Tumorigenesis and Prolongs Survival[J].PLOS ONE,2015 10(7):e0131008.
[8]Jae M. Shin,Islam Ateia,Jefrey R. Paulus,et al. Antimicrobial nisin acts against saliva derived multi-species biofilms without cytotoxicity to human oral cells[J]. Frontiers in Microbiology,2015,6:617.
[9]叶万荣,陈剑,许峰,等.一种高纯度乳酸链球菌素的制备方法:中国,101701034 B[P].2012-06-06.
[10]严宇媛,赵波,赵文杰,等. 一种高纯度乳酸链球菌素的制备方法:中国,102199200 B[P].2014-05-07.
[11]刘立毅,宁方红,徐环昕,等.乳酸链球菌素Z纯化脱色小试工艺研究[J].离子交换与吸附,2014,30(5):429-437.
[12]刘立毅,宁方红,徐环昕,等.吸附树脂对发酵上清液中nisin Z的吸附研究[J].中国调味品,2014(39):7-11.
[13]Yuan-Ching Tai,Pranav Joshi,Joseph McGuire,et al. Nisin adsorption to hydrophobic surfaces coated with the PEO-PPO-PEO triblock surfactant Pluronic ® F108[J]. NIH Public AccessAuthor Manuscript,2008 June 1;322(1):112-118.
[14]贾士儒.生物防腐剂[M].中国轻工业出版社,2009:34-35.
Preparation of high- purity Nisin and the optimization of industrial scale production conditions
CHEN Yi-qiang,LI Guang-jin,JIN Chen-bin,XU Feng,YE Ting,HONG Chao-Qun
(Zhe Jiang Silver-Elephant Bio-Engineering Company,Taizhou 317200,China)
In this study,a new method of preparation high-purity Nisin preparation was researched. The method adopted static adsorption and dynamic desorption of Nisin concentrated solution at a weak acidic ion exchange resin D113.The subsequent production process included salting out,suction filtration,drying and crushing to obtain high-purity Nisin. The results showed that the optimum condition was pH6,adsorption time 90 min,CDesorption agent=1 mol/L,VHCl/VEtOHl=1.25,desorption rate 1 BV/h,CNaCl=23% in salting out. The potency of Nisin attained through this procedure was 34000 IU/mg,total yield reached 67.45%.The method has bright prospect in industrial application.
high-purity;Nisin;ion exchange
2016-12-29
陈艺强(1966-),男,本科,工程师,研究方向:发酵产品工艺优化,E-mail:chenyiq8668@163.com。
TS202
A
1002-0306(2017)11-0281-04
10.13386/j.issn1002-0306.2017.11.045
