肝素抗凝治疗监测相关项目的性能验证*
2017-06-23胡欢荣李臣宾周文宾刘秀丽彭明婷
胡欢荣 李臣宾 周文宾 刘秀丽 彭明婷
肝素抗凝治疗监测相关项目的性能验证*
胡欢荣 李臣宾 周文宾 刘秀丽 彭明婷
目的 对低分子量肝素(low molecular weight heparin,LMWH)抗-Ⅹa活性、抗凝血酶(antithrombin, AT)活性和活化部分凝血活酶时间(activated partial thromboplastin time,APTT)检测系统的性能进行验证。方法 参考美国临床和实验室标准协会(CLSI)发布的多项指南、多项卫生行业标准和试剂厂家的要求,对LMWH抗-Ⅹa活性检测的批内精密度、日间精密度、线性、准确度和检出限,AT活性检测的批内精密度、日间精密度、线性和准确度,以及APTT检测的批内精密度、日间精密度和可比性进行验证。结果 LMWH抗-Ⅹa活性检测的批内精密度分别为0.03抗-Ⅹa IU/ ml和0.05抗-Ⅹa IU/ml,日间精密度分别为0.04 抗-Ⅹa IU/ml和0.05 抗-Ⅹa IU/ml,线性范围为0~1.83 抗-Ⅹa IU/ml,准确度百分偏差分别为4.3%和2.2%,检出限验证结果为0.05抗-Ⅹa IU/ml,均符合厂家要求。AT活性检测的批内精密度分别为2.0%和3.5%,日间精密度分别为2.7%和5.3%,线性范围为0~139%,准确度百分偏差分别为0.9%、–1.4%和–2.7%,均符合厂家要求。APTT活性检测的批内精密度分别为0.5%和0.4%,日间精密度分别为3.4%和4.4%,可比性验证结果符合行业标准的要求。结论 3个项目的性能能够满足厂家和行业标准的要求,性能验证方法和指标的研究有助于临床实验室实施质量改进。
肝素 实验室监测 抗-Ⅹa活性 抗凝血酶 性能验证
使用普通肝素(unfractionated heparin,UFH)和低分子量肝素(low molecular weight heparin,LMWH)对患者进行抗凝治疗时,临床医生常需要依靠实验室检测指标对抗凝治疗的强度进行监测。LMWH抗-Ⅹa活性、抗凝血酶(antithrombin,AT)活性和活化部分凝血活酶时间(activated partial thromboplastin time,APTT)是肝素抗凝治疗监测的相关项目,为保证检测结果的准确性和可靠性,本文参考美国临床和实验室标准协会(Clinical and Laboratory Standards Institute,CLSI)指南H57-A、H26-A2和EP17-A2[1-3]、卫生行业标准(WS/T 408-2012和WS/T 406-2012)[4,5]及试剂生产厂家的要求,对其检测性能进行验证,为临床实验室开展相关工作提供参考。
材料与方法
1 仪器 STA-R Evolution全自动血凝仪(法国Stago公司)。
2 试剂 抗-Ⅹa活性测定试剂盒STA®-Liquid Anti-Ⅹa(批号113504);LMWH校准品STA®-Multi Hep Calibrator(批号113897);LMWH质控品STA®-Quality HBPM/ LMWH(批号113064、114357和114896);APTT检测试剂STA®-PTTA(批号114631);AT活性检测试剂盒STA®-Stachrom® AT III(批号114915);通用定标品STA®-Unicalibrator(批号114319);凝血质控品STA®-Coag Control(批号114746和114876);氯化钙STA®-CaCl20.025 mol/L(批号114628);稀释液STA®-Owren-Koller(批号114803);特殊清洗液STA®-Desorb U(批号114647);清洗液STA®-Cleaner Solution(批号201602);以上试剂均为法国Stago公司生产。2016年全国凝血试验室间质评物(批号201611~201615和201621~201625)。
3 方法
3.1 批内精密度:参考H57-A[1]、H26-A2[2]和试剂厂家的要求,使用LMWH抗-Ⅹa活性、AT活性和APTT检测2个浓度水平质控品(低浓度水平L和高浓度水平H,或正常浓度水平N和异常浓度水平P)各1支,分别连续重复检测20次,计算检测结果的均值、标准差(s)和变异系数(CV)。评价标准:按厂家的要求,LMWH抗-Ⅹa活性检测的批内精密度(s)应≤0.10 抗-Ⅹa IU/ml;AT 活性检测正常和异常浓度水平的批内精密度(CV)应分别≤3.0%和5.0%;APTT检测的批内精密度(CV)应≤3.0%。
3.2 日间精密度:参考H57-A[1]、H26-A2[2]和试剂厂家的要求,使用LMWH抗-Ⅹa活性、AT活性和APTT检测2个浓度水平质控品(低浓度水平L和高浓度水平H,或正常浓度水平N和异常浓度水平P),分别于每周一和周四上午、下午各检测2次,连续检测1个月,分别计算检测结果的均值、s和CV。评价标准:按厂家的要求,LMWH抗-Ⅹa活性检测的日间精密度(s)应≤0.10 抗-Ⅹa IU/ ml;AT 活性检测正常和异常浓度水平的日间精密度(CV)应分别≤10.0%和15.0%。APTT检测的日间精密度(CV)应≤5.0%。
3.3 线性:参考卫生行业标准WS/T 408-2012[4]的线性验证方法,分别对LMWH抗-Ⅹa活性和AT活性检测的线性进行验证。对于LMWH抗-Ⅹa活性检测,使用STA®-Multi Hep Calibrator高、中、低值LMWH校准品两两等比例混合配制5个浓度水平的样本,每个样本分别检测2次;对于AT活性检测,使用0.8 ml无菌注射用水复溶通用定标品STA®-Unicalibrator获得高值样本(H),将缓冲液STA®-Owren-Koller液作为低值样本(L),按比例(4H、3H+1L、2H+2L、1H+3L和4L)配制5个浓度水平的样本,每个样本分别检测2次。计算2次检测结果的均值和每个浓度水平的理论值,将实测均值(Y轴)与理论值(X轴)进行线性回归分析,并计算实测值与理论值的百分偏差。评价标准:斜率按WS/T 406-2012[5]的要求,应在0.95~1.05范围内;相关系数(r)和偏差按厂家的要求,r2≥0.99,实测均值与理论值的百分偏差应在±10.0%范围内。
3.4 准确度或可比性
3.4.1 LMWH抗-Ⅹa活性和AT活性检测的准确度:参考卫生行业标准(WS/T 406-2012)[5]和厂家的要求。对于LMWH抗-Ⅹa活性检测,取STA®-Multi Hep Calibrator高、中值LMWH校准品各1支,分别检测1次;对于AT活性检测,取1支通用定标品STA®-Unicalibrator加入1 ml无菌注射用水复溶后,用STA®-Owren-Koller液按2∶3和1∶3稀释配制3个浓度水平的样本,每个样本分别检测1次。计算检测结果与理论值的百分偏差,要求百分偏差应在±10.0%范围内。
3.4.2 APTT检测的可比性:由于APTT无校准品,本研究采用检测质评物的方式评价其检测结果的可比性。分别检测2016年全国凝血试验室间质评物(批号201611~201615和201621~201625)各1次,计算检测结果与靶值(2016年全国室间质评中该试剂组实验室检测结果的中位数)的偏差。评价标准:参考WS/T 406-2012[5]的要求,质评物检测结果在该组范围内(靶值±15%)的比例应≥80%。
3.5 检出限 :参考CLSI EP17-A2[3]和厂家说明书的要求,对LMWH抗-Ⅹa活性的检出限(limit of detection,LoD)进行验证。选择10位男性和10位女性自愿者,按照标准操作程序采集静脉血液样本,离心分离血浆,将血浆进行等比例混合后作为空白样本。对空白样本连续重复检测30次,计算均值(和标准差(s),并根据公式“LoD=s”计算LoD;此外,计算检测结果超出厂家声称LoD的比例。评价标准:①按厂家的要求,LoD≤0.10 抗-Ⅹa IU/ml;②按EP17-A2的要求,检测结果超出厂家声称LoD的比例应≤15%。
结果
1 批内精密度 3个项目的批内精密度验证结果见表1,均符合要求。
2 日间精密度 3个项目的日间精密度验证结果见表2,均符合要求。
3 线性 LMWH抗-Ⅹa活性检测的线性验证结果见表3,线性回归方程为Y=1.05X+0.01,r2=1.00,符合斜率在0.95~1.05范围内、r2≥0.99的要求;除最低浓度水平外,其余4个浓度水平的偏差均在±10%的范围内,故可认为LMWH抗-Ⅹa活性在0~1.83 抗-Ⅹa IU/ml范围内线性良好。AT检测的线性验证结果见表4,线性回归方程为Y=0.99X+0.99,r2= 1.00,符合斜率在0.95~1.05范围内、r2≥0.99的要求;除最低浓度水平外,其余4个浓度水平的偏差均在±10%的范围内,故可认为AT活性检测在0~139%范围内线性良好。
4 LMWH抗-Ⅹa活性和AT活性检测结果的准确度验证结果见表5,各浓度水平实测值与理论值的百分偏差均在±10.0%的范围内,可认为2个项目的准确度均符合要求。
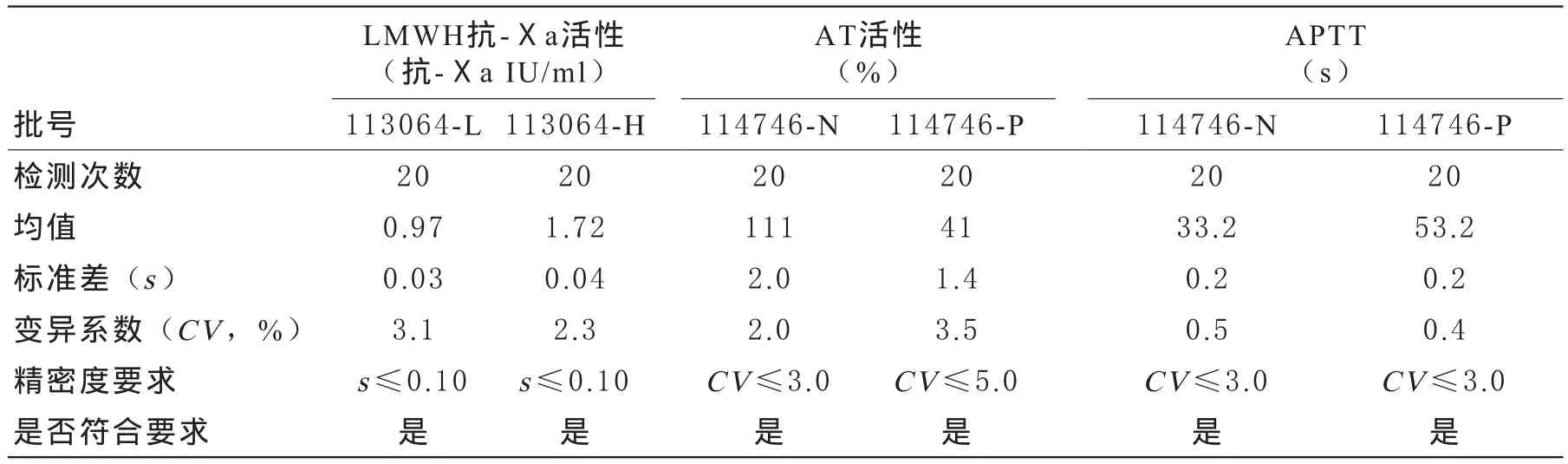
表1 LMWH抗-Ⅹa活性、AT活性和APTT检测批内精密度验证结果
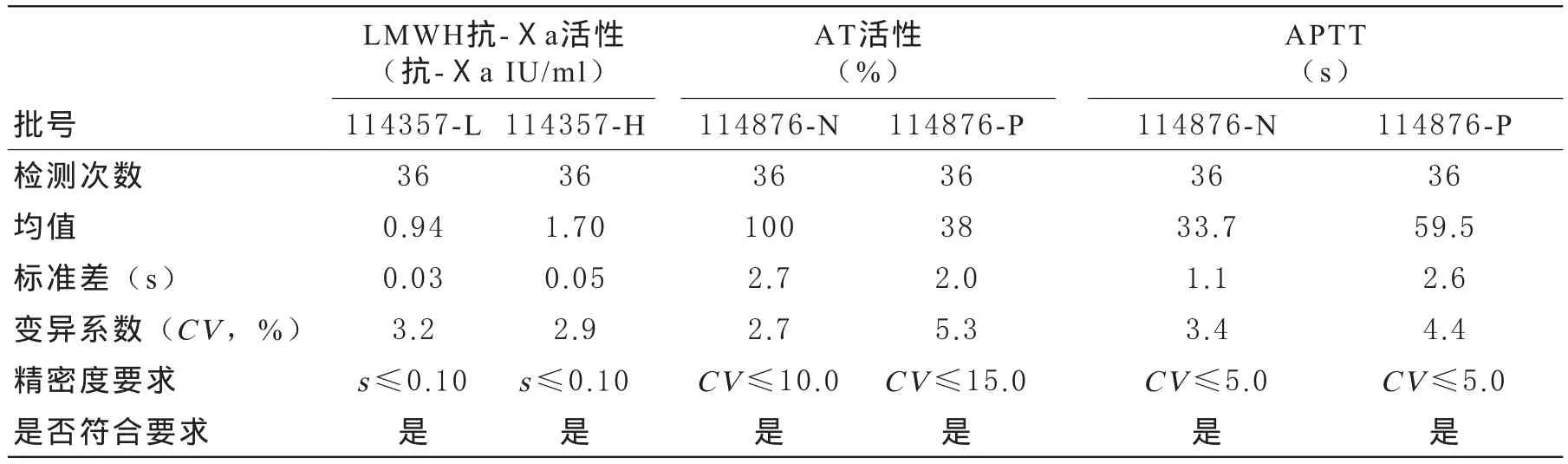
表2 LMWH抗-Ⅹa活性、AT活性和APTT检测日间精密度验证结果

表3 LMWH抗-Ⅹa活性检测线性验证结果
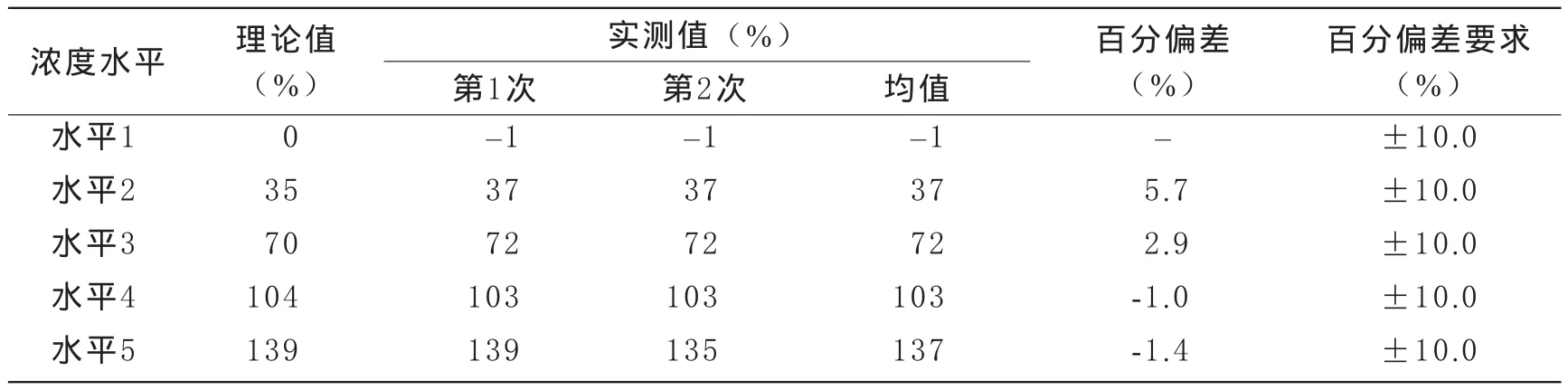
表4 AT活性检测线性验证结果
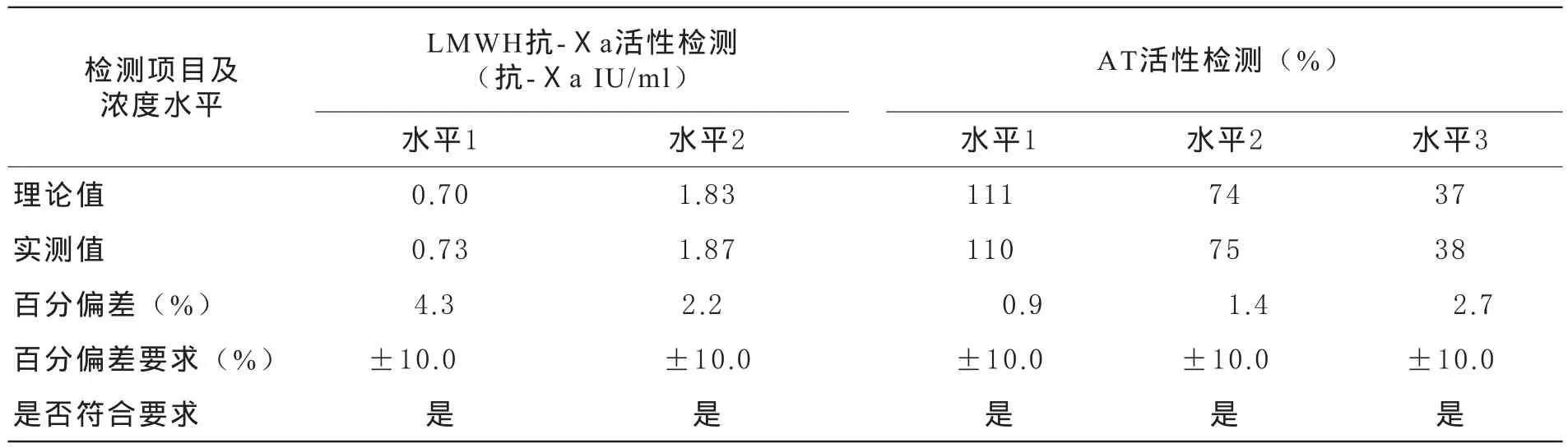
表5 LMWH抗-Ⅹa活性和AT活性检测准确度验证结果
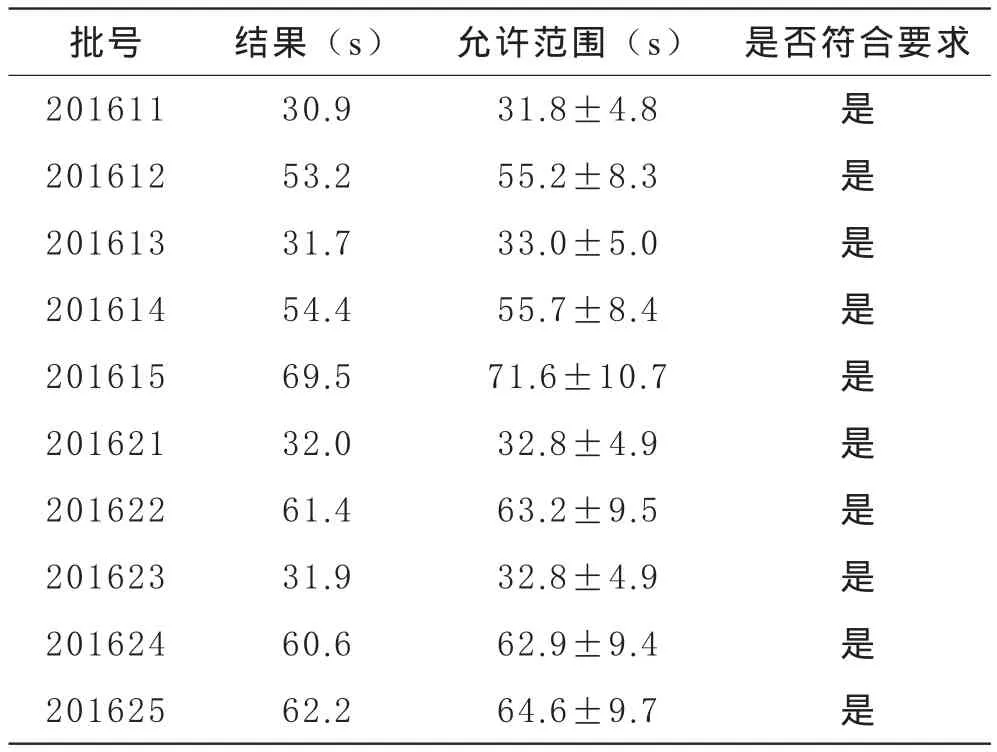
表6 APTT检测可比性验证结果
5 APTT检测结果的可比性 验证结果见表6,各批号质评物检测结果均在允许范围内(靶值±15%),可比性符合要求。
6 检出限 LMWH抗-Ⅹa活性LoD验证检测结果的均值为0.02 抗-Ⅹa IU/ml,标准差为0.01 抗-Ⅹa IU/ml,LoD=0.05 抗-Ⅹa IU/ml,小于厂家声称的LoD(0.10 抗-Ⅹa IU/ ml),所有检测结果均小于厂家声称的LoD,LoD验证结果符合要求。
讨 论
UFH和LMWH是临床常用的抗凝治疗药物,常用于预防和治疗血栓性疾病如肺栓塞、深静脉血栓、急性冠脉综合征以及继发于房颤的栓塞性脑卒中[6]。UFH因药代动力学不稳定、特异性结合力低等缺点,为了优化疗效、降低药物的副作用,目前主要使用APTT进行监测[7,8]。虽然一般情况下认为不需要监测LMWH,但目前多数指南和文献认为特定患者如老年、肥胖、孕妇、儿童和肾功能不全患者等需要进行监测[7-10]。抗-Ⅹa活性检测是美国胸科医师协会(American College of Chest Physicians,ACCP)[7]、英国血液学标准委员会(British Committee for Standards in Haematology,BCSH)[8]指南及加拿大[9]和中国[10]专家共识推荐的监测LMWH治疗药物浓度的方法。由于LMWH必须与AT结合才能发挥抗凝作用,AT缺乏会影响其抗凝效果[11],因此使用抗-Ⅹa活性监测LMWH药物浓度时,还需确认患者AT活性水平[7]。目前,关于肝素抗凝治疗监测相关项目(尤其是抗-Ⅹa活性和AT活性)性能验证的研究较少,故本研究参考CLSI指南、卫生行业标准和试剂厂家的要求,对上述3个项目的性能进行验证。
精密度验证结果显示,3个项目的批内精密度和日间精密度均符合厂家说明书要求。值得注意的是,对于LMWH抗-Ⅹa活性检测结果的精密度,本研究依据厂家建议以标准差(s)作为评价指标,2个浓度水平质控品检测结果的s均小于厂家的要求(s≤0.10抗-Ⅹa IU/ml)。若以变异系数(CV)表示,本研究CV为2.3%~3.5%,与相近浓度水平范围厂家试剂说明书给出的实测CV(3.0%~4.8%)和Suzuki等[12]研究结果(2.4%~6.4%)较接近。由于抗-Ⅹa活性数值较小,CV值的大小易受浓度水平的影响,如Houbouyan等[13]检测浓度水平为0.23~0.78 抗-Ⅹa IU/ml质控品的CV为1.9 %~16.7%。不同厂家的精密度评价指标存在差异,一般在低浓度水平时宜使用标准差,在较高浓度水平时宜使用变异系数。
LMWH抗-Ⅹa活性和AT活性检测结果在一定范围内呈线性且有配套校准品,故能够进行线性和准确度验证。线性验证方法主要参考行业标准WS/T 408-2012的方案,结果分析以回归方程的斜率和相关系数作为评价指标,简便易行。LMWH抗-Ⅹa活性检测厂家声称的线性范围为0.1~2.0抗-Ⅹa IU/ml,本研究结果显示,在0~1.83抗-Ⅹa IU/ml范围内线性良好;AT活性检测厂家声称的线性范围为9%~140%,本研究结果显示,在0~139%范围内线性良好。不足之处是本次验证的线性范围未能包括厂家声称线性范围的上限。APTT检测结果不呈线性且无配套校准品,故无法进行线性和准确度验证,其结果的可靠性常通过检测定值质控品、参加室间质量评价和结果比对等方式进行验证。本研究通过检测2016年全国室间质评10个批号质评物的方式进行可比性验证,结果符合要求。APTT检测结果易受试剂敏感度的影响,为保证检测结果的可靠性,实验室除规范做好室内质控外,在使用新批号试剂时还应对其参考区间和UFH治疗范围进行验证,必要时应建立新的参考区间和UFH治疗范围[1]。
正常人血浆LMWH抗-Ⅹa活性检测结果几乎为0,接受LMWH治疗的患者血浆抗-Ⅹa活性能够被检出,但水平仍然较低,故验证检测系统的抗-Ⅹa活性检出能力非常重要。本研究通过分析厂家声称的LoD对其检出能力进行验证。根据CLSI EP17-A2指南,LoD的验证方法是对空白样本进行至少20次检测,若检测结果超出厂家声称LoD的比例不超过15%,则可接受厂家声称的LoD。本研究以健康自愿者的血浆作为空白样本,为减少个体差异的影响,将20位自愿者(男女各半)的血浆进行等比例混合,并连续进行30次检测。结果显示,采用两种结果判断方法的LMWH抗-Ⅹa活性检测的LoD均符合要求。
为保证性能验证结果的可靠性,本研究在正式开始前首先严格按照标准操作程序进行试剂准备、建立了LMWH抗-Ⅹa活性和AT活性检测的定标曲线、规范开展了3个项目的室内质控。建立室内质控过程中发现LMWH抗-Ⅹa活性检测,个别批号质控品厂家给出的质控靶值和实际检测均值存在较大差异,实验室应按照《医疗机构临床实验室管理办法》实施细则的要求,使用一段时间内质控品实际检测的均值作为质控均值,否则易出现假失控。
综上所述,本研究对STA-R Evolution血凝仪LMWH抗-Ⅹa活性、AT活性和APTT检测性能进行了验证,结果符合厂家和卫生行业标准的要求。肝素抗凝治疗监测对于指导临床合理用药具有重要价值,只有检测系统的性能验证符合要求,才能保证检测结果准确可靠。不同厂家的性能验证方法和指标存在差异,探讨性能验证方法和指标对临床实验室的质量改进具有重要意义。
1 CLSI. Protocol for the Evaluation,Validation,and Implementation of Coagulometers; Approved Guideline:H57-A[S]. Wayne,PA: Clinical and Laboratory Standards Institute,2008.
2 CLSI. Validation,Verification,and Quality Assurance of Automated Hematology Analyzers; ApprovedStandard-Second Edition: H26-A2[S]. Wayne,PA:Clinical and Laboratory Standards Institute,2010.
3 CLSI. Protocols for Determination of Limits of Detection and Limits of Quantitation; Approved Guideline-Second Edition: EP17-A2[S]. Wayne,PA: Clinical and Laboratory Standards Institute,2012.
4 卫生部临床检验标准专业委员会.临床化学设备线性评价指南: WS/T 408-2012[S]. 北京: 中国标准出版社,2012.
5 卫生部临床检验标准专业委员会.临床血液学检验常规项目分析质量要求: WS/T 406-2012[S]. 北京: 中国标准出版社,2012.
6 Baglin T,Barrowcliffe TW,Cohen A,et al. Guidelines on the use and monitoring of heparin[J]. Br J Haematol,2006,133(1):19-34.
7 David A,Garcia MD,Trevor P,et al. Parenteral Anticoagulants: Antithrombotic Therapy and Prevention of Thrombosis,9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines [J]. Chest,2012,141(Suppl 2) :e419S-94S.
8 Kitchen S,Gray E,Mackie I,et al. Measurement of non-coumarin anticoagulants and their effects on tests of Haemostasis:Guidance from the British Committee for Standards inHaematology [J]. Br J Haematol, 2014,166(6): 830-841.
9 Easaw JC,Shea-Budgell MA,Wu CM,et al. Canadian consensus recommendations on the management of venous thromboembolism in patients with cancer. Part 1: prophylaxis[J]. Curr Oncol,2015,22(2):133-43.
10 中华医学会心血管病学分会肺血管病学组.急性肺栓塞诊断与治疗中国专家共识[J].中华心血管病杂志,2016,44(3):197-211.
11 Jeske WP,Walenga JM,Samama MM,et al. Functionality of fondaparinux (pentasaccharide)depends on clinical antithrombin levels[J]. Blood Coagul Fibrinolysis. 2011,22(3):206-210.
12 Suzuki T,Ishii-Watabe A,Hashii N,et al. The establishment and validation of efficient assays for anti-Ⅱa and anti-Ⅹa activities of Heparin sodium and heparin calcium[J]. Biologicals,2013,41(6):415-423.
13 Houbouyan L,Boutière B,Contant G,et al. Validation protocol of analytical hemostasis systems:measurement of anti-Ⅹa activity of low-molecularweight heparins[J]. Clin Chem,1996,42(8 Pt 1):1223-1230.
Verification of Assays for Heparin Therapy Monitoring
HU Huan-rong,LI Chen-bin,ZHOU Wen-bin,et al.
Graduate School of Peking Union Medical College,National Center for Clinical Laboratories,Beijing Engineering Technology Research Center of Clinical Laboratory,Beijing Hospital,National Center of Gerontology,Beijing 100730
Objective To verify the measurement performance of low molecular weight heparin(LMWH)anti-Ⅹa activity assay,antithrombin(AT)activity assay and activated partial thromboplastin time (APTT) test. Methods According to the Clinical and Laboratory Standards Institute (CLSI) guidelines,the professional standards and manufacturer's instructions,the performance characteristics of LMWH anti-Ⅹa activity assay,AT activity assay and APTT test were verified as follows: within-run precision,between-day precision,linearity,accuracy or comparability and the limit of detection (LoD,only for LMWH anti-Ⅹa activity assay). Results The within-run precision,betweenday precision,linear range,bias for accuracy and LoD of LMWH anti-Ⅹa activity assay were 0.03 anti-Ⅹa IU/ml and 0.05 anti-Ⅹa IU/ml,0.04 anti-Ⅹa IU/ml and 0.05 anti-Ⅹa IU/ml,0-1.83 anti-Ⅹ a IU/ml,4.3% and 2.2%,0.05 anti-Ⅹa IU/ml,respectively,all of which were acceptable following manufacturer’s instructions. The within-run precision,between-day precision,linear range and bias for accuracy of AT activity assay were 2.0% and 3.5%,2.7% and 5.3%,0%-139%,0.9%,-1.4% and -2.7%,respectively,all of which were acceptable following manufacturer's instructions. The within-run precision,between-day precision and bias for comparability of APTT test were 0.5% and 0.4%,3.4% and 4.4%,within ±15.0%,respectively,all of which were acceptable according to professional standards and manufacturer's instructions. Conclusion The verified data of the LMWH anti-Ⅹa activity,AT activity and APTT detection systems were acceptable according to the professional standards and manufacturer's instructions. It is very important to set up the methods and specifications of verification for clinical laboratories to implement quality improvement.
Heparin Laboratory monitoring Anti-Ⅹa activity Antithrombin Performance verification
R446.11
A
1671-2587(2017)03-0252-06
2017-02-01)
(本文编辑:王虹)
10.3969/j.issn.1671-2587.2017.03.013
*本课题受国家科技基础性工作专项基金(No.2013FY113800)资助
100730 北京协和医学院研究生院,北京医院,国家老年医学中心,卫生部临床检验中心,北京市临床检验工程技术研究中心(胡欢荣,刘秀丽,彭明婷);北京医院,国家老年医学中心,卫生部临床检验中心,北京市临床检验工程技术研究中心(李臣宾,周文宾)
胡欢荣(1990–),女,江西上饶人,在读硕士研究生,(E-mail)41232956@qq.com。
彭明婷,女,研究员,主要从事临床血液与体液检验标准化及质量控制研究,(E-mail)mtpeng@nccl.org.cn。
