高温高压CO2腐蚀环境中含Cr低合金钢耐蚀机理的研究进展
2017-06-19许立宁朱金阳
张 瑾,许立宁,朱金阳,王 贝
(北京科技大学 新材料技术研究院腐蚀与防护中心,北京 100083)
专论
高温高压CO2腐蚀环境中含Cr低合金钢耐蚀机理的研究进展
张 瑾,许立宁,朱金阳,王 贝
(北京科技大学 新材料技术研究院腐蚀与防护中心,北京 100083)
阐述了含Cr低合金钢耐CO2腐蚀的机理,并介绍了如何通过极化曲线来确定含Cr低合金钢是否耐蚀的方法,同时也列举了含Cr低合金钢腐蚀产物膜沉积机制的最新进展,并提出了含Cr低合金钢耐蚀机理研究中亟待解决的问题。
含Cr低合金钢;CO2腐蚀;耐蚀机理;极化曲线;腐蚀产物膜
石油管的CO2腐蚀现象是困扰石油、天然气生产的重要问题之一[1-3]。由于CO2溶于水所形成的H2CO3可以在碳钢表面直接发生还原反应,所以在相同的pH下,CO2水溶液的腐蚀性比强酸(如HCl)溶液更强[4]。此外,大多数油气田目前已进入开发的中后期,油气田中的CO2含量和含水率上升,再加上回注CO2强化采油等工艺[5]的广泛应用,致使高含水率、高矿化度的CO2介质对采油设备、油套管、输送管线的腐蚀更趋严重。
目前,针对管道CO2腐蚀所采取的防护措施主要有:对碳钢管线加注缓蚀剂,或采用比碳钢更耐蚀的材料(如不锈钢)[6-7]。由于缓蚀剂不能有效抑制局部腐蚀,因此,最安全的防护措施是使用耐蚀材料[8]。在国外,13Cr和超级13Cr马氏体不锈钢被广泛应用于CO2腐蚀控制。虽然13Cr、超级13Cr马氏体不锈钢以及22Cr双相不锈钢等耐蚀合金具有优异的抗CO2腐蚀性能,但是其价格较高,提高了油气田投资成本,对于产量较低的油气田来说,存在经济效益和投资比太低的问题[9]。另外,高合金含量的耐蚀材料还存在焊接性能、高Cl-条件下的抗点蚀性能以及抗H2S应力腐蚀开裂性能不理想等问题[10-11]。
大量研究发现,含Cr低合金管线钢是目前较为理想的兼具耐蚀性与经济性的抗CO2腐蚀管线钢。KERMANI等[12]发现,在CO2环境中,3% Cr钢的耐蚀性是相同强度级别碳钢的3倍甚至40多倍,而其成本仅为碳钢的1.5倍。由于具有力学性能良好、投资成本低、服役过程中无需加注缓蚀剂等优点,含Cr低合金钢正逐渐成为控制CO2腐蚀的热门材料。目前,含Cr低合金钢已成功应用于油田实际生产中,如宝钢BG80-3% Cr、BG110-3% Cr、BG80S-3% Cr、BG95S-3% Cr等油套管,已相继应用于中石化江汉油田、华东分公司、西南分公司、东北分公司以及中石油大庆油田和塔里木油田等含CO2、微量H2S腐蚀环境的油气井[8]。
许多学者对含Cr低合金钢抑制CO2腐蚀的机理进行了研究[13-15]。结果表明,含Cr低合金钢耐蚀性提高的主要原因是Cr元素在腐蚀产物膜中发生富集,明显改变了腐蚀产物膜的结构、致密性和保护性。尽管已经对含Cr低合金钢的腐蚀产物膜进行过大量的研究,但不同文献中给出的腐蚀产物膜的结构差别较大,对腐蚀产物膜的形成机制仍然缺乏系统、深入的研究[16]。本工作对国内外学者提出的含Cr低合金钢耐CO2腐蚀机理进行了阐述,同时介绍了如何通过极化曲线来确定含Cr低合金钢是否耐蚀的方法,列举了含Cr低合金钢腐蚀产物膜沉积机制的最新进展,并提出了含Cr低合金钢耐蚀机理研究中亟待解决的问题,为含Cr低合金钢后续的开发和应用提供参考。
1 含Cr低合金钢耐CO2腐蚀机理
在CO2环境中碳钢腐蚀的阴极反应如式(1)~(6)所示[17-20]。
(1)
(2)
(3)
(4)
(5)
(6)
碳钢腐蚀的阳极反应则主要是Fe通过一些多步反应的溶解过程[21-23],如式(7)~(9)所示。
(7)
(8)
(9)
当Fe2+和CO32-浓度的乘积超过了FeCO3的溶度积时,FeCO3会在基体表面析出并形成腐蚀产物膜,反应如式(10)~(11)所示。
(10)
(11)
但是,对于含Cr低合金钢来说,基体中含有Cr,所以还会增加一些阳极反应[24-29],如式(12)~(18)所示。
(12)
(13)
(14)
(15)
(16)
(17)
(18)
MURAKI等[30]研究发现,由于Cr的活性高于Fe,因此在腐蚀初期含Cr低合金钢的腐蚀速率比碳钢的大,当形成腐蚀产物膜后其腐蚀速率明显降低,可见含Cr低合金钢耐蚀性主要源于其腐蚀产物膜的保护作用。UEDA等[31]提出:腐蚀过程中形成了化学性质稳定的Cr(OH)3,同时由于腐蚀产物膜中FeCO3能够发生溶解,使得Cr元素在腐蚀产物膜中富集。FeCO3可通过式(19)~(20)所示反应溶解,而Cr(OH)3由于弱酸性将保留下来导致了Cr的富集[24]。
(19)
(20)
BROOKS等[32]认为,由于腐蚀产物膜中水合Cr(OH)3具有阳离子选择性,阻碍了阴离子穿过腐蚀产物膜到达金属表面,使得腐蚀速率降低;另外,CHEH等[26]发现,含Cr低合金钢腐蚀产物膜致密度的增大以及导电性的降低,也能提高其耐蚀性。基于以上两方面,含Cr低合金钢能有效抑制点蚀的发生[24,33]。2% Cr钢在50 ℃和0.8 MPa CO2的环境中腐蚀15 d后,表面会形成连续、均匀、致密的含非晶Cr化合物和Fe化合物的腐蚀产物膜层,而不是形成内嵌岛状FeCO3的不均匀膜或松散膜层,这层膜有效地阻隔了试样表面冷凝液膜中的腐蚀性成分到达基体表面,降低了腐蚀产物膜与基体界面处腐蚀性离子的浓度,从而提高了2% Cr钢在湿气CO2环境中的耐蚀性[34]。
2 含Cr低合金钢的极化曲线
判断材料耐蚀性的常用方法是通过失重法计算腐蚀速率,但通过极化曲线可以更快捷、高效地判断含Cr低合金钢的耐蚀性。
陈长风等[14]分别测试了5% Cr钢未腐蚀以及高温高压下腐蚀10 d后的极化曲线,发现腐蚀产物膜覆盖后,阳极反应的电流密度大大降低,表明该腐蚀产物膜对基体具有良好的保护作用。XU等[35]发现3% Cr钢(铁素体-珠光体)在80 ℃和0.8 MPa CO2环境中浸泡240 h后的极化曲线出现了如图1中所示的“半钝化”现象,即阳极极化曲线出现了电流密度的谷值(随着电位的升高电流密度减小),并指出3% Cr钢良好的耐蚀性与其具有半钝化特性的腐蚀产物膜密切相关。GUO等[36]在研究中发现:3% Cr钢在80 ℃和含0.5 MPa饱和CO2溶液中浸泡不同时间后,其阳极极化曲线有所不同。在浸泡32 h和96 h后,3% Cr钢仍然处于活化状态,但是浸泡96 h后电流密度相较于浸泡32 h明显减小;然而,浸泡252 h和312 h后,电位为-0.6~-0.5 V(SCE),出现了明显的半钝化现象。扫描电镜观察显示,在浸泡了252 h后,腐蚀产物膜的厚度快速增大,此时3% Cr钢处于半钝化状态,故极化曲线出现了电流密度的谷值。ZHU等[37]发现:在加入浓度小于200 mmol/L的苯甲酰胺缓蚀剂后,3% Cr的极化曲线均出现了明显的半钝化现象;但当缓蚀剂浓度达到600 mmol/L时,半钝化现象消失。他们指出半钝化现象消失是由于缓蚀剂浓度较高时,缓蚀剂分子快速地在基体表面吸附和聚集,形成了完整的缓蚀剂膜层,有效抑制了基体的腐蚀,从而阻止了钝化膜的形成。

图1 在80 ℃、0.8 MPa CO2环境中浸泡240 h后3% Cr钢的极化曲线[35]Fig. 1 Polarization curve of 3% Cr steel immersed for 240 h in condition of 80 ℃ and 0.8 MPa CO2[35]
3 含Cr低合金钢腐蚀产物膜的沉积机制
从腐蚀动力学角度来看,含Cr低合金钢腐蚀产物膜的形成机制较为复杂,而且膜的形态和成分决定了腐蚀的严重程度。FeCO3膜的沉积过程对钢在CO2环境中腐蚀产物膜的形成具有极其重要的影响[38]。
FeCO3膜的沉积离不开晶核形成以及晶粒长大过程。形核是沉积的第一步,形核速率受过饱和度的影响[39]。定义FeCO3的过饱和度S为离子浓度积与FeCO3溶度积Ksp的比值,如式(21)所示。[Fe2+]代表溶液中Fe2+的浓度;[CO32-]代表溶液中CO32-的浓度。
(21)
假设溶液为理想溶液,当过饱和度S=1时,溶液达到饱和状态;当过饱和度S>1时,出现沉积[40-42];但当S大于某个特定值时,结晶速率才会迅速增大[39]。这个特定值定义为FeCO3的临界过饱和度Sc,低于临界过饱和度,其形核速率几乎为零[43]。晶粒形核速率和晶体长大速率都与相对过饱和度σ有关[44],相对过饱和度σ和过饱和度S的关系如式(22)所示。
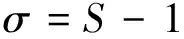
(22)
一般,形核速率随相对过饱和度的增长呈指数增长,而晶体长大速率随相对过饱和度的增长呈线性增长[22]。因此,在低的相对过饱和度下,晶体长大速率大于晶粒形核速率,FeCO3膜的沉积过程主要受晶体长大速率控制,腐蚀产物膜将由FeCO3大晶粒组成,该腐蚀产物膜疏松、多孔且耐蚀性差。相反,当相对过饱和度很高时,即离子浓度积远高于FeCO3溶度积Ksp时,以指数方式增长的晶粒形核速率远大于以线性方式增长的晶体长大速率,FeCO3膜的沉积过程主要受晶核形成速率控制,导致大量的晶粒密集形核而来不及长大,形成了由极为细小的FeCO3晶粒组成的腐蚀产物膜,甚至形成短程有序但长程无序的非晶态腐蚀产物膜[22]。该腐蚀产物膜只能依靠原子间的相互关联作用在小于几个原子间距的小区间内仍保持形貌和组分的某些有序特征。此时形成的腐蚀产物膜连续、致密且保护性好。所以,当FeCO3的临界过饱和度较高时,其相对过饱和度较大,晶粒形核速率远大于晶体长大速率,易形成由细小的FeCO3晶粒组成的腐蚀产物膜,甚至非晶腐蚀产物膜;当FeCO3的临界过饱和度较低时,情况则正好相反,易形成由FeCO3大晶粒组成的腐蚀产物膜。
众多学者对碳钢的腐蚀产物膜进行研究,得到的结果与上述形核和长大理论相符合[22-23,45-46],其腐蚀产物膜的沉积机制也与该理论密切相关。由式(12)~(18)可见,含Cr低合金钢中Cr的水解反应将改变基体或膜层表面溶液的pH。pH的改变会显著改变溶液中FeCO3的临界过饱和度,在近中性的环境中,pH每降低1,Fe2+含量需提高大约100倍才能达到临界过饱和度[44]。CHOKSHI等[45]研究发现:碳钢腐蚀19 h后,在低pH(pH为6.0)和FeCO3的过饱和度为9时,表面未沉积腐蚀产物膜;而在高pH(pH为6.3)和FeCO3的过饱和度为7时,表面却沉积了约10 μm厚的晶态FeCO3腐蚀产物膜。由此可知:pH为6.0时FeCO3的临界过饱和度大于9,而pH为6.3时FeCO3的临界过饱和度小于7,表明pH升高会使FeCO3的临界过饱和度降低。故对于含Cr低合金钢来说,由于Cr的水解反应而导致的溶液pH变化,将会显著改变溶液中FeCO3的临界过饱和度,进而间接影响腐蚀产物膜的沉积。
GUO等[27]通过试验推测了CO2环境中2% Cr钢腐蚀产物膜的形成机制,发现腐蚀产物膜的形成与2% Cr钢表面溶液的pH密切相关。他们还发现:2% Cr钢的腐蚀产物膜是两层结构。内层膜为完整覆盖整个基体表面的非晶态膜,由非晶态的Cr(OH)3和FeCO3组成;外层膜主要由FeCO3晶粒组成,呈条带状分布,且外层膜会随着pH的变化而发生溶解。监测结果显示,2% Cr钢表面pH处于周期性波动状态。内层膜中FeCO3呈现非晶态的原因为:腐蚀过程开始阶段试样表面溶液的pH急剧降低,导致了FeCO3的临界过饱和度升高,因此形核速率远远大于晶粒长大的速率,形成了非晶态的内层膜。外层膜的形成机制为:当2% Cr钢表面溶液的pH逐渐升高时,FeCO3的临界过饱和度降低,此时形核速率远远小于长大速率,非晶内层膜表面开始析出晶态的FeCO3,呈现出局部(呈条带状分布)被FeCO3晶粒覆盖的情况;当2% Cr钢表面溶液的pH再次降低时,FeCO3会发生溶解。
对于含Cr低合金钢来说,Cr的水解会导致基体或膜层表面溶液的pH发生变化,从而显著改变FeCO3的临界过饱和度;而临界过饱和度又决定着FeCO3的沉积机制,随着pH的降低,晶粒尺寸逐渐减小,当pH降低至一定程度时,甚至转变为非晶态FeCO3。
4 展望
含Cr低合金钢凭借其良好的抗CO2腐蚀性能以及经济性成为了目前较为理想的抗CO2腐蚀的材料,具有十分广阔的应用前景。生成富Cr腐蚀产物膜是含Cr低合金钢在高温高压CO2下耐蚀的主要原因,但如何提高富Cr腐蚀产物膜的耐蚀性等关键问题,如富Cr腐蚀产物膜中Cr的存在形式、Cr的化合物与FeCO3的结合方式等,还没有形成统一的认识。同时,对含Cr低合金钢发生的阴极反应以及pH出现波动的根本原因等仍需进行深入的探讨。
[1] 赵国仙,严密林. 石油天然气工业中CO2腐蚀的研究进展[J]. 腐蚀与防护,1998,19(2):51-54.
[2] 路民旭,白真权. 油气采集储运中的腐蚀现状及典型案例[J]. 腐蚀与防护,2002,23(3):105-113.
[3] 陈长风,路民旭,赵国仙,等. N80钢CO2腐蚀产物膜研究[J]. 中国腐蚀与防护学报,2002,22(3):143-147.
[4] NESIC S,NYBORG R,STANGELAND A,et al. Mechanistic modeling for CO2corrosion with protective iron carbonate films[C]//Corrosion 2001. Houston:NACE,2001:40.
[5] 郝敏,宋永臣. 利用CO2提高石油采收率技术研究现状[J]. 钻采工艺,2010,33(4):59-63.
[6] 王彬,杜敏,张静. 油气田中抑制CO2腐蚀缓蚀剂的应用及其研究进展[J]. 腐蚀与防护,2010,31(7):503-507.
[7] 潘一,孙林,杨双春,等. 国内外管道腐蚀与防护研究进展[J]. 腐蚀科学与防护技术,2014,26(1):77-80.
[8] 张忠铧,黄子阳,孙元宁,等. 3Cr抗CO2和H2S腐蚀系列油套管开发[J]. 宝钢技术,2006(3):5-8.
[9] NOSE K,ASAHI H,NICE P I,et al. Corrosion properties of 3% Cr steels in oil and gas environments[C]//Corrosion 2001. Houston:NACE,2001:82.
[10] SMITH L M,JORDAN D E. Ensuring corrosion properties of CRA welds meet requirements for the oil and gas industry[C]//Corrosion 2003. San Diego:NACE,2003:91.
[11] LINNNE C P,BLANCHARD F,GUNTZ G C,et al. Corrosion performances of modified 13Cr for OCTG in oil and gas environments[C]//Corrosion 1997. New Orleans:NACE,1997:28.
[12] KERMANI B,GONZALES J C,TURCONI G L,et al. In-field corrosion performance of 3% Cr steels in sweet and sour downhole production and water injection[C]//Corrosion 2004. New Orleans:NACE,2004:111.
[13] 孙建波,柳伟,路民旭. 成分和组织影响钢CO2腐蚀的研究进展[J]. 中国腐蚀与防护学报,2008,28(4):246-248.
[14] 陈长风,路民旭,赵国仙,等. 腐蚀产物膜覆盖条件下油套管钢CO2腐蚀电化学特征[J]. 中国腐蚀与防护学报,2003,23(3):139-143.
[15] 胡丽华,俞曼丽,常炜,等. Cr含量对低合金管线钢CO2腐蚀性能的影响[J]. 腐蚀科学与防护技术,2011,23(3):256-260.
[16] 陈太辉,许立宁,常炜,等. 耐CO2腐蚀低Cr管线钢的研究进展[J]. 腐蚀科学与防护技术,2011,23(5):451-452.
[17] ZHANG G A,CHENG Y F. Corrosion of X65 steel in CO2-saturated oilfield formation water in the absence and presence of acetic acid[J]. Corrosion Science,2009,51(8):1589-1595.
[18] PALACIOS C A,SHADLEY J R. CO2corrosion of N80 steel at 71 ℃ in a two-phase flow system[J]. Corrosion,1993,49(8):686-693.
[19] OGUNDELE G I,WHITE W E. Some observations on corrosion of carbon steel in aqueous environments containing carbon dioxide[J]. Corrosion,1986,42(2):71-78.
[20] CHENG Y F,NIU L. Mechanism for hydrogen evolution reaction on pipeline steel in near-neutral pH solution[J]. Electrochemistry Communications,2007,9(4):558-562.
[21] BOCKRIS J O M,DRAZIC D. The kinetics of deposition and dissolution of iron:effect of alloying impurities[J]. Electrochimica Acta,1962,7(3):293-313.
[22] GAO M,PANG X,GAO K. The growth mechanism of CO2corrosion product films[J]. Corrosion Science,2011,53(2):557-568.
[23] DUGSTAD A. Fundamental aspects of CO2metal loss corrosion-part 1:mechanism[C]//Corrosion 2006. San Diego:NACE,2006:111.
[24] CHEN C F,LU M X,SUN D B,et al. Effect of chromium on the pitting resistance of oil tube steel in a carbon dioxide corrosion system[J]. Corrosion,2005,61(6):594-601.
[25] CHEN T H,XU L N,LU M X,et al. Study on factors affecting low Cr alloy steels in a CO2corrosion system[C]//Corrosion 2011. Houston:NACE,2011:74.
[26] CHEN C F,LU M X,ZHAO G X,et al. The ion passing selectivity of CO2corrosion scale on N80 tube steel[C]//Corrosion 2003. San Diego:NACE,2003:342.
[27] GUO S Q,XU L N,ZHANG L,et al. Corrosion of alloy steels containing 2% chromium in CO2environments[J]. Corrosion Science,2012,63:246-258.
[28] ZHU J,XU L,LU M. Electrochemical impedance spectroscopy study of the corrosion of 3Cr pipeline steel in simulated CO2-saturated oilfield formation waters[J]. Corrosion,2015,71(7):854-864.
[29] 陈太辉. 3% Cr管线钢CO2腐蚀的影响因素及耐蚀机理研究[D]. 北京:北京科技大学,2010.
[30] MURAKI T,HARA T,ASAHI H. Effects of chromium content up to 5% and dissolved oxygen on CO2corrosion[C]//Corrosion 2002. Denver:NACE,2002:272.
[31] UEDA M,TAKABE H. The formation behavior of corrosion protective films of low Cr bearing steels in CO2environments[C]//Corrosion 2001. Houston:NACE,2001:66.
[32] BROOKS A R,CLAYTON C R,DOSS K,et al. On the role of Cr in the passivity of stainless steel[J]. Journal of the Electrochemical Society,1986,133(12):2459-2464.
[33] 王磊. CO2腐蚀产物膜微观结构与离子选择性研究[D]. 北京:中国石油大学,2007.
[34] 许立宁,朱金阳,谢云,等. 含Cr管线钢的力学性能和耐蚀性能[J]. 北京科技大学学报,2014,36(2):200-205.
[35] XU L N,GUO S Q,GAO C L,et al. Influence of microstructure on mechanical properties and corrosion behavior of 3% Cr steel in CO2environment[J]. Materials and Corrosion,2012,63(11):997-1003.
[36] GUO S Q,XU L N,CHANG W,et al. The anti-pitting mechanism of low Cr alloy steel in CO2corrosion environment[C]//Corrosion 2012. Salt Lake City:NACE,2012:1357.
[37] ZHU J Y,XU L N,LU M X,et al. Interaction effect between Cr(OH)3passive layer formation and inhibitor adsorption on 3Cr steel surface[J]. RSC Advances,2015,5(24):18518-18522.
[38] GULBRANDSEN E,NESIC S,STANGELAND A,et al. Effect of pre-corrosion on the performance of inhibitors for CO2corrosion of carbon steel[C]//Corrosion 1998. Houston:NACE,1998:13.
[39] MULLIN J W. Crystallization[M]. 3版. 北京:世界图书出版社公司北京公司,2000:123-129.
[40] SÖHNEL O,MULLIN J W. Interpretation of crystallization induction periods[J]. Journal of Colloid and Interface Science,1988,123(1):43-50.
[41] TANTAYAKOM V,SREETHAWONG T,FOGLER H S,et al. Scale inhibition study by turbidity measurement[J]. Journal of Colloid and Interface Science,2005,284(1):57-65.
[42] NIELSEN A E. Kinetics of precipitation[M]. Oxford:Pergamon Press,1964.
[43] DRELA I,FALEWICZ P,KUCZKOWSKA S. New rapid test for evaluation of scale inhibitors[J]. Water Research,1998,32:3188-3191.
[44] DUGSTAD A. Mechanism of protective film formation during CO2corrosion of carbon steel[C]//Corrosion 1998. San Diego:NACE,1998:31.
[45] CHOKSHI K,SUN W,NESIC S. Iron carbonate scale growth and the effect of inhibition in CO2corrosion of mild steel[C]//Corrosion 2005. Houston:NACE,2005:285.
[46] RUZIC V,VEIDT M,NESIC S. Protective iron carbonate films-part 2:chemical removal by dissolution in single-phase aqueous flow[J]. Corrosion,2006,62(5):598-612.
Research Progress of Corrosion Resistance Mechanism for Low Alloy Steels Containing Cr in High Temperature, High Pressure and CO2Corrosion Environments
ZHANG Jin, XU Lining, ZHU Jinyang, WANG Bei
(Corrosion and Protection Center, Institute for Advanced Materials and Technology, University of Science and Technology Beijing, Beijing 100083, China)
The corrosion resistance mechanism of low alloy steels containing Cr is summarized. The method of determining the corrosion resistance of low alloy steels containing Cr through polarization curves is introduced. The latest progress in the growth mechanism of corrosion product scales is listed. And the urgent issues of corrosion resistance mechanism research of low alloy steels containing Cr are put forward.
low alloy steel containing Cr; CO2corrosion; corrosion resistance mechanism; polarization curve; corrosion product scale
10.11973/fsyfh-201706010
2015-11-27
国家科技支撑计划(2012BAK13B04)
许立宁(1976-),副教授,博士,从事金属腐蚀与防护、马氏体不锈钢含Cr低合金钢的研究,18910957210,xulining@ustb.edu.cn
TG174.2
A
1005-748X(2017)06-0456-05
