108例胃肠道间质瘤患者复发转移危险因素分析
2017-06-05高志芳
高志芳, 高 青
重庆医科大学附属第一医院消化内科,重庆 400016
108例胃肠道间质瘤患者复发转移危险因素分析
高志芳, 高 青
重庆医科大学附属第一医院消化内科,重庆 400016
目的探讨胃肠道间质瘤(gastrointestinal stromal tumor,GIST)复发转移危险因素。方法回顾性分析108例经手术证实的GIST患者的临床资料,并分析影响其复发转移的危险因素。结果108例患者4年累计复发转移率为29.63%,单因素分析显示肿瘤大小、核分裂象数、肿瘤原发部位、术后服用伊马替尼、Ki67指数与GIST复发转移有关(P<0.05),多因素分析显示肿瘤大小、核分裂象数、肿瘤原发部位、术后服用伊马替尼是影响GIST复发转移的独立危险因素。结论肿瘤大小、核分裂象、肿瘤原发部位是GIST复发转移的独立危险因素,术后伊马替尼分子靶向治疗可明显降低GIST复发转移风险。
胃肠道间质瘤;复发转移;伊马替尼
胃肠道间质瘤(gastrointestinal stromal tumor,GIST)是胃肠道最常见的间叶源性肿瘤,从食管到直肠及腹膜的任何地方均可发生[1],一般将肿瘤大小、核分裂象、肿瘤原发部位作为可靠的预后指标[2]。手术治疗是GIST的首选方式[3],伊马替尼分子靶向治疗使GIST患者的预后得到了明显改善。随着诊断技术的提高,GIST患者逐渐增多,但预后相关因素报道不一,本研究旨在探讨GIST复发转移危险因素,以期为临床治疗提供有效价值。
1 资料与方法
1.1 一般资料选取2011年5月-2015年6月在重庆医科大学附属第一医院收治的108例GIST患者的临床资料,进行回顾性分析,男47例(43.52%),女61例(56.48%),年龄23~84岁,中位年龄58岁。纳入标准:(1)手术完整切除,经病理和免疫组化确诊为GIST,按NIH危险性分级为中、高危[4];(2)无严重术后并发症;(3)无心、肝、肾重要器官功能障碍。
1.2 方法
1.2.1 研究项目:记录患者的年龄、性别、肿瘤原发部位、肿瘤大小、核分裂象数、CD117、CD34、Dog-1、Ki67指数、术后服用伊马替尼资料。其中肿瘤大小为测量所得的肿瘤最大的径线值,核分裂象数是根据核分裂象较丰富的50个高倍视野下计算所得的核分裂数。
1.2.2 随访:采用电话进行随访,截止随访日期为2015年12月,随访时间定义为自患者确诊日期至截访日期,复发时间为患者确诊日期至复发时间。
1.3 统计学处理采用SPSS 22.0软件进行统计学分析,影响复发转移的单因素分析采用χ2检验,多因素分析采用Logistic回归分析,P<0.05为差异有统计学意义。
2 结果
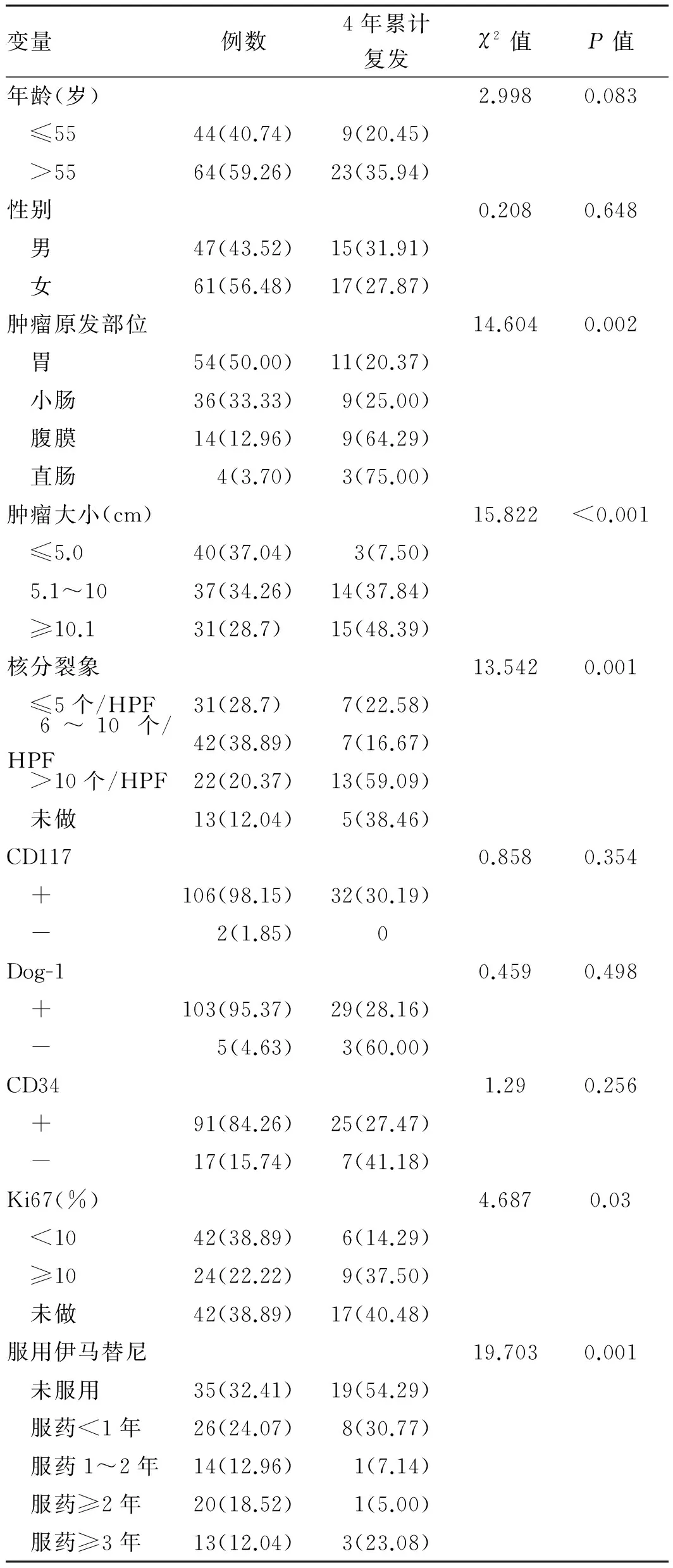
2.1 单因素分析单因素分析显示肿瘤大小、核分裂象数、肿瘤原发部位、Ki67指数、术后服用伊马替尼与GIST复发转移有关(P<0.05)。而年龄、性别、CD117、CD34、Dog-1等因素对预后无明显影响(P>0.05,见表1)。
表1 108例GIST一般资料与单因素分析[例数(%)]
Tab 1 Single factor analysis and general data of GIST in 108 cases [n(%)]
变量例数4年累计复发χ2值P值年龄(岁)2.9980.083 ≤5544(40.74)9(20.45) >5564(59.26)23(35.94)性别0.2080.648 男47(43.52)15(31.91) 女61(56.48)17(27.87)肿瘤原发部位14.6040.002 胃54(50.00)11(20.37) 小肠36(33.33)9(25.00) 腹膜14(12.96)9(64.29) 直肠4(3.70)3(75.00)肿瘤大小(cm)15.822<0.001 ≤5.040(37.04)3(7.50) 5.1~1037(34.26)14(37.84) ≥10.131(28.7)15(48.39)核分裂象13.5420.001 ≤5个/HPF31(28.7)7(22.58) 6~10个/HPF42(38.89)7(16.67) >10个/HPF22(20.37)13(59.09) 未做13(12.04)5(38.46)CD1170.8580.354 +106(98.15)32(30.19) -2(1.85)0Dog-10.4590.498 +103(95.37)29(28.16) -5(4.63)3(60.00)CD341.290.256 +91(84.26)25(27.47) -17(15.74)7(41.18)Ki67(%)4.6870.03 <1042(38.89)6(14.29) ≥1024(22.22)9(37.50) 未做42(38.89)17(40.48)服用伊马替尼19.7030.001 未服用35(32.41)19(54.29) 服药<1年26(24.07)8(30.77) 服药1~2年14(12.96)1(7.14) 服药≥2年20(18.52)1(5.00) 服药≥3年13(12.04)3(23.08)
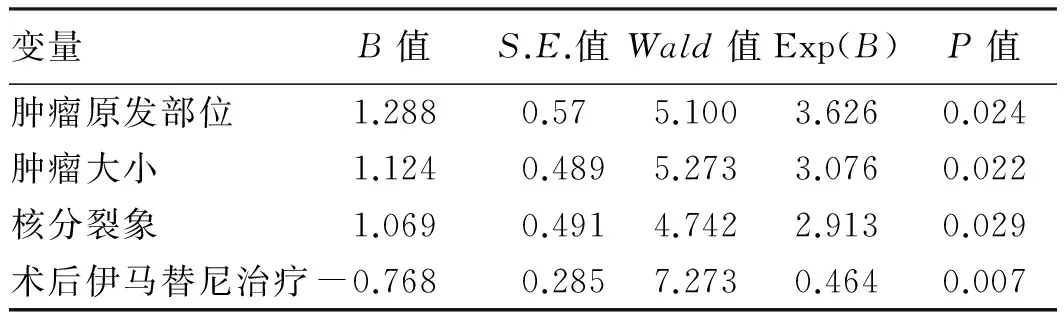
2.2 多因素分析因Ki67数据缺失值较多,未纳入多因素分析。分析结果显示肿瘤大小、核分裂象数、肿瘤原发部位、术后服用伊马替尼是GIST复发转移的独立因素(见表2)。
2.3 随访随访时间6~55个月,中位时间22个月。共32例经CT或剖腹探查证实复发转移,复发转移率为29.63%。平均复发转移周期为22个月,最常见复发转移部位为肝脏和腹膜。
表2 108例GIST复发转移危险因素多因素分析
Tab 2 Multiple factors analysis of risk factors of recurrence and metastasis in 108 cases of GIST
变量B值S.E.值Wald值Exp(B)P值肿瘤原发部位1.2880.575.1003.6260.024肿瘤大小1.1240.4895.2733.0760.022核分裂象1.0690.4914.7422.9130.029术后伊马替尼治疗-0.7680.2857.2730.4640.007
3 讨论
GIST是最常见的间叶源性肿瘤,好发于中老年,肿瘤原发部位最常见为胃,其次为小肠,也可发生于胃肠道外,如网膜、肠系膜、腹膜后、盆腔[5]。GIST起病隐匿,临床上表现常见有腹痛、消化道出血、腹胀、恶心呕吐、食欲下降等,缺乏特异性表现,部分患者没有临床症状,而在体检或其他手术中偶然发现[6],本组有17例无临床症状,且术前难以获得病理诊断,故GIST复发转移危险因素的研究对指导治疗、判断预后具有重要意义。
影响GIST预后的因素较多,本研究显示肿瘤原发部位、肿瘤大小、核分裂象、术后服用伊马替尼均为影响GIST复发转移的独立危险因素,这与多数报道一致[7]。肿瘤大小、核分裂象数、肿瘤原发部位的B值均为正,提示肿瘤越大、核分裂象数越多则术后复发转移可能性越大,肿瘤原发于胃预后相对较好,而原发于小肠、直肠、胃肠外等非胃部位复发转移可能性则较高。术后伊马替尼靶向治疗可明显降低复发转移风险,B值为负提示术后服药的时间越长,则复发的可能性越小。通过比较独立危险因素,上述4个独立影响因素与复发转移关系的密切程度依次为:术后伊马替尼靶向治疗>肿瘤大小>肿瘤原发部位>核分裂象数。
肿瘤直径越大,肿瘤复发转移风险较高。多数学者认为肿瘤直径>5 cm较容易发生复发转移,恶性潜能较高[8]。但也有报道小肠间质瘤多为浸润性生长,常早期出现腹膜转移,完全切除率较低,小肠直径>2 cm提示预后不良[9]。报道认为上消化道GIST其恶性潜能较低,肿瘤直径≤2 cm的上消化道 GIST,宜选择临床随访观察;2~3 cm的GIST 恶性潜能介于低和中度之间,可进行密切随访、EUS-FNA 结合细胞学检查或外科及内镜切除;>3 cm的GIST 恶性潜能较高,应采取外科或内镜切除[10]。本文显示核分裂象是GIST复发转移的重要影响因素,报道认为原发于胃的GIST核分裂象≤10个/50 HPF与非胃GIST≤5个/50 HPF的复发转移风险最低;胃GIST核分裂象11~50个/50 HPF与非胃6~20个/50 HPF的复发转移风险为中等,胃GIST核分裂象>50个/50 HPF与非胃>20个/50 HPF的复发转移风险最高[11],但本文也有核分裂象计数较小的GIST患者发生复发。同时本文证实肿瘤原发于胃复发转移风险较低,而原发于小肠、直肠及腹膜等复发转移风险高,与美国国立卫生研究院(NIH) GIST危险度分级体系内容基本相符。
单因素分析Ki67指数与GIST复发转移有关,提示Ki67指数可能为GIST复发转移的危险因素,有文献[12]报道Ki67指数≥10复发转移可能性较高。但因本文Ki67指数缺失值较多(缺失42例),未纳入多因素分析,尚需进一步的研究。也有报道[13-14]认为P53突变、周围组织浸润、肿瘤细胞类型、基因分型等可对GIST复发转移产生影响,但由于临床及病例资料局限,本文未能深入分析。
一直以来手术切除是最有效的治疗方案,原则上尽可能地完整切除,保证切缘肉眼及镜下无肿瘤细胞浸润,防止术中肿瘤破裂。随着分子靶向治疗的深入研究,NIH分级中高危患者术后服用伊马替尼可明显改善预后。本研究显示NIH分级中高危患者术后服用伊马替尼可明显降低复发转移风险,且服用时间越长,复发转移风险越低。目前以NIH分级为基础,推荐中高危复发风险GIST进行伊马替尼分子靶向治疗,一般推荐剂量为400 mg/d[15],高危GIST或复发风险>50患者至少接受36个月的伊马替尼辅助治疗,中危患者辅助治疗应1年或以上。至于辅助治疗的最佳时限是多少,目前尚不明确[16],需大规模的临床试验研究。伊马替尼常见不良反应有水肿、恶心、腹泻、皮疹、皮肤瘙痒、白细胞下降、血小板下降、肌肉抽搐、脱发等,严重不良反应少见,随着治疗时间的延长,上述不良反应可能得到改善[17]。但对于伊马替尼耐药患者,可增加剂量或选择舒尼替尼、瑞格菲尼等二三线药物治疗,但均难以获得长期的肿瘤稳定的控制[16]。
综上所述,GIST复发转移危险因素需综合评估,肿瘤大小、肿瘤原发部位是独立危险因素,术后服用伊马替尼可降低复发转移风险。所有GIST均具有恶性潜能,早期发现、综合治疗是降低复发转移、提高生存率的关键。
[1]Bauer S, Rutkowski P, Hohenberger P, et al. Long-term follow-up of patients with GIST undergoing metastasectomy in the era of imatinib-Analysis of prognostic factors (EORTC-STBSG collaborative study) [J].Eur J Surg Oncol, 2014, 40(4): 412-419.
[2]Yeh CN, Hwang TL, Huang CS, et al. Clinical practice guidelines for patients with gastrointestinal stromal tumor in Taiwan [J].World J Surg Oncol, 2012, 10: 246.
[3]Berney CR. Laparoscopic resection of locally advanced gastrointestinal stromal tumor (GIST) of the stomach following neoadjuvant imatinib chemoreduction [J]. Int J Surg Case Rep, 2015, 8C: 103-106.
[4]Jang SH, Kwon JE, Kim JH, et al. Prediction of tumor recurrence in patients with non-gastric gastrointestinal stromal tumors following resection according to the modified national institutes of health criteria [J]. Intest Res, 2014, 12(3): 229-235.
[5]Beham AW, Schaefer IM, Schüler P,et al. Gastrointestinal stromal tumors [J]. Int J Colorectal Dis, 2012, 27(6): 689-700.
[6]Rubin BP, Heinrich MC, Corless CL. Gastrointestinal stromal tumour [J].Lancet, 2007, 369(9574): 1731-1741.
[7]杨健, 于健春, 马志强, 等. 胃肠道间质瘤558例临床病理特征及预后分析[J]. 中华外科杂志, 2015, 53(4): 274-279. Yang J, Yu JC, Ma ZQ, et al. Clinical pathological features and prognosis analysis of gastrointestinal stromal tumor:a series of 558 cases [J]. Chin J Surg, 2015, 53(4): 274-279.
[8]Chan KH, Chan CW, Chow WH, et al. Gastrointestinal stromal tumors in a cohort of Chinese patients in Hong Kong [J]. World J Gastroenterol, 2006, 12(14): 2223-2228.
[9]Jie ZG, Xie XP, Qin KW, et al. Clinical analysis of prognostic factors for patients with gastrointestinal stromal tumors [J]. Chin J Gastrointest Surg, 2005, 8(3): 8210-8212. 揭志刚, 谢小平, 秦克旺, 等.胃肠道间质瘤预后因素的临床分析[J].中华胃肠外科杂, 2005, 8(3): 8210-8212.
[10]Zhou X, Chen Y, Wu Y, et al. Analysis of related factors of tumors invasion risk in patients with upper gastrointestinal stromal tumors [J]. J Third Mil Med Univ, 2014, 36(8): 816-820. 周雪, 陈瑶, 吴玥, 等. 上消化道间质瘤的随访及侵袭危险性的相关因素分析[J]. 第三军医大学学报, 2014, 36(8): 816-820.
[11]Joensuu H, Eriksson M, Hall KS, et al. Risk factors for gastrointestinal stromal tumor recurrence in patients treated with adjuvant imatinib[J]. Cancer, 2014, 120(15): 2325-2333.
[12]Artigiani Neto R, Logullo AF, Stávale JN, et al. Ki-67 expression score correlates to survival rate ingastrointestinal stromal tumors(GIST) [J]. Acta Cir Bras, 2012, 27(5): 315-321.
[13]Huang H, Liu YX, Zhan ZL, et al. Different sites and prognoses of gastrointestinal stromaltumors of the stomach:report of 187 cases [J]. World J Surg, 2010, 34(7):1523-1533.
[14]石素胜, 孙耘田, 白月奎, 等.胃肠道间质瘤多因素预后分析 [J].诊断病理学杂志, 2006, 13(1): 21-25. Shi SS, Sun GT, Bai YK, et al.Gastrointestinal stromal tumors:a multivariate prognostic analysis [J]. J Diag Pathol, 2006, 13(1): 21-25.
[15]Li J, Gong JF, Li J, et al. Efficacy of imatinib dose escalation in Chinesegastrointestinal stromal tumor patients [J]. World J Gastroenterol, 2012, 18(7): 698-703.
[16]He YL. Review of Chinese consensus and NCCN guidelines of surgical management of ingastrointestinal stromal tumor [J]. Chin J Colorec Dis (Electronic Edition), 2013, 2(2): 54-57. 何裕隆. 胃肠间质瘤外科诊治的中国专家共识与NCCN 指南解读[J]. 中华结直肠疾病电子杂志, 2013, 2(2): 54-57.
[17]曹晖, 汪明.NCCN《软组织肉瘤—胃肠间质瘤临床实践指南(2015年第1版)》 更新介绍与解读[J]. 中国实用外科杂志, 2015, 35(6): 599-603. Cao H, Wang M. Updates and interpretations of the NCCN Clinical Practice Guidelines 2015 on gastrointestinal stromal tumor [J].Chinese Journal of Practical Surgerry, 2015, 35(6): 599-603.
(责任编辑:马 军)
Risk factors of recurrence and metastasis in 108 cases of gastrointestinal stromal tumor
GAO Zhifang, GAO Qing
Department of Gastroenterology, the First Affiliated Hospital of Chongqing Medical University, Chongqing 400016, China
Objective To investigate the risk factors of recurrence and metastasis in patients with gastrointestinal stromal tumor (GIST). Methods The clinical data of 108 cases of GIST having undergone surgery and confirmed by pathology were reviewed retrospectively and the risk factors of recurrence and metastasis were evaluated. Results The 4-year cumulative recurrence and metastasis rate was 29.63%. Univariate analysis showed that tumor size, mitotic count, primary tumor location, use of imatinib treatment, Ki67 were related to recurrence and metastasis of GIST (P<0.05). Multivariate analysis showed that tumor size, mitotic count, primary tumor location, use of imatinib treatment were the independent influencing factors. Conclusion Tumor size, mitotic count, primary tumor location are the independent influencing factors of GIST. Adjuvant imatinib therapy after surgery can reduced recurrence and metastasis rate of GIST.
Gastrointestinal stromal tumor; Recurrence and metastasis; Imatinib
10.3969/j.issn.1006-5709.2017.03.012
高志芳,在读硕士研究生,研究方向:胃肠道肿瘤。E-mail:zhifang-gao@126.com
高青,主任医师,硕士生导师,研究方向:胃肠道肿瘤。E-mail:gaoqing27@aliyun.com
R735
A 文章编号:1006-5709(2017)03-0289-03
2016-07-07
