含锌、硒羟基磷灰石的制备及其载药性能研究
2017-06-01徐祥华张万东王永兰
徐祥华,张万东,王永兰
(1.天津大学理学院化学系,天津300354;2.天津医科大学口腔医院)
含锌、硒羟基磷灰石的制备及其载药性能研究
徐祥华1,张万东1,王永兰2
(1.天津大学理学院化学系,天津300354;2.天津医科大学口腔医院)
通过共沉淀法制备了一系列Zn2+和SeO32-共同掺杂的羟基磷灰石(HAP),并研究了Zn2+的掺入对HAP微粒的形貌、化学组成、表面电荷的影响,对ZnSeHAP作为载体对牛血清白蛋白(BSA)的负载与释放性能进行了研究。结果显示:所制备的ZnSeHAP是颗粒长为60~80 nm、宽度为20~30 nm的纳米棒,并且随着锌含量的增加,纳米粒子逐渐减小。随着锌掺杂到HAP晶格内,其表面电势逐渐变小,并且由正转负。负载实验表明:随锌掺杂量的增加,BSA的负载量逐渐减小,说明通过锌掺杂可以调变HAP的表面电荷,以达到控制HAP吸附量的目的。
羟基磷灰石;共沉淀;负载;释放
近年来,人工合成的纳米羟基磷灰石[Ca10(PO4)6(OH)2,HAP]因其良好的生物相容性、生物活性及可生物降解性越来越受到人们的广泛关注[1-2]。另外,由于HAP的化学组成及晶体结构与天然骨的无机部分相似,因此被作为载体用于药物的负载与释放[3]。不同合成方法制备的HAP具有不同的形貌,如棒状、针状、纤维状、片状和球状等,而组成人体硬组织如骨骼和牙齿的“建筑模块”呈棒状或针状,因此人工合成的棒状和针状的HAP受到更深入的研究[4]。目前,阴、阳离子掺杂HAP的制备和应用是生物材料研究的另一热点。通过阴离子或阳离子的掺杂可以改变HAP的晶格参数,进而影响其形貌、热稳定性、溶解性、表面电荷和其对药物蛋白的吸附能力等。V.Aina等[5]研究了镁和锶阳离子共同掺杂HAP,结果表明共同掺杂制备的HAP要比单个元素掺杂制备的HAP更加稳定。N.Y.Mostafa等[6]制备了系列Na+、SiO44-、CO32-复合掺杂的HAP,结果表明HAP的热稳定性和机械性能有了明显的提高。硒是人体不可缺少的微量元素之一,尽管其在人体中的质量不足0.1%,但其在新陈代谢过程中起非常重要的作用。欧洲食物安全局建议人体每日硒的摄入量为55 μg。硒还可以降低癌症的发病率,预防心血管病,治疗肌肉紊乱等[7]。锌也是人体中不可缺少的微量元素,它可以促进成骨细胞的增殖和分化[8]。欧洲食物安全局建议男女每日锌的摄入量分别为7 mg和9.5 mg。锌还可以提高人体免疫力、促进蛋白质消化和碳水化合物的新陈代谢。考虑到硒和锌的独特作用,笔者制备了系列Zn2+和SeO32-共同掺杂的HAP,并主要研究了随锌含量的增加,HAP的形貌、表面电荷和化学组成的变化,进而研究了将其作为药物蛋白载体对牛血清白蛋白(BSA)吸附与释放的影响。
1 实验方法
1.1 ZnSeHAP的制备及表征
本实验采用共沉淀法制备系列ZnSeHAP样品。Ca(NO3)2·4H2O,(NH4)2HPO4,Zn(NO3)2·6H2O,Na2SeO3分别为钙源、磷源、锌源和硒源。各试剂的用量见表1,在保证(Ca+Zn)与(P+Se)的物质的量比等于1.67的前提下,将硒的质量分数固定为4.72%,锌的质量分数分别为13.02%、6.51%、0.651%、0.065 1%、0.006 51%和 0%,并分别命名为 Zn0.2Se0.1HAP,Zn0.1Se0.1HAP,Zn0.01Se0.1HAP,Zn0.001Se0.1HAP,Zn0.0001Se0.1HAP和Zn0Se0.1HAP。在烧瓶中加入钙锌混合溶液,并恒温在80℃;在剧烈搅拌下将(NH4)2HPO4和Na2SeO3的混合溶液慢慢滴加到上述混合液中,并用氨水调节混合液的pH>10,混合液滴加完毕继续恒温搅拌2.5 h;然后,常温下老化36 h,将所得沉淀物用去离子水多次洗涤,并在120℃下干燥36 h;最后将样品在600℃下煅烧4 h后研磨备用。
用BD 3000 X射线衍射仪(XRD)分析样品的物相,测试条件为:铜靶(λ=0.154 18 nm),管电压为30 kV,管电流为30 mA;用Bruker ALPHA-E Fourier红外光谱仪(FTIR)分析样品组分;用JEM-2100F透射电镜(TEM)观察样品的形貌;用S4 Pioneer射线荧光(XRF)测试样品中的元素含量;用 Malvern Nano-ZS电位仪分析样品的表面电荷。
1.2 蛋白质的负载与释放
在pH为7.40的模拟体液(SBF)中制备ZnSeHAP系列载体对牛血清白蛋白(BSA)的负载样品[9]。称取0.2 g载体浸入20 mL用SBF配制的1 mL/mg的BSA溶液中,常温下吸附6 h后,移取上清液用紫外分光光度计在280 nm处测量样品的吸光度并根据上清液中蛋白浓度与初始蛋白浓度的差计算吸附于载体上的载药量。重复实验3次。载药样品真空干燥之后,精密称量0.100 g的样品并加入20 mL的释放介质SBF溶液,置水浴恒温摇床中(37℃),每隔一定时间移取4 mL上清液,并补充相同体积的SBF溶液,用紫外分光光度法测定取出液的吸光度,计算药物释放量。

表1 样品配制的物质的量比
2 结果与讨论
2.1 X射线衍射分析
图1为系列ZnSeHAP样品的XRD谱图,与标准HAP(JCPDS 09-432)具有相同的衍射峰,没有其他杂峰,只是随着锌含量的增加,ZnSeHAP的峰位微微向高角度偏移,Zn含量越多,偏移量越大,这是由于HAP晶体中Zn2+(0.074 nm)进入了HAP晶体的晶格内部,取代了Ca2+(0.099 nm),使晶间距减小,进而引起了晶格畸变,随着掺入量的增大,取代越多,畸变也就越明显[10]。

图1 样品的XRD谱图
2.2 红外光谱分析
图2是ZnSeHAP晶体的红外谱图,系列样品的主要官能团吸收峰基本相同。3 565、629 cm-1处吸收峰是OH-伸缩振动峰;3 425、1 643 cm-1附近的峰为吸附水的特征峰;1 418、1 465 cm-1附近为CO32-反对称伸缩振动的双分裂峰,此峰不同于碳酸盐的红外吸收谱在此波段的表达,表明在样品制备过程中有CO32-取代了部分的 PO43-;963、1 036、1 104 cm-1是PO43-的伸缩振动峰,602、566 cm-1是PO43-的弯曲振动峰;869、775 cm-1是SeO32-的弯曲振动峰[11]。随着锌掺杂量的增加,PO43-的峰越来越宽。
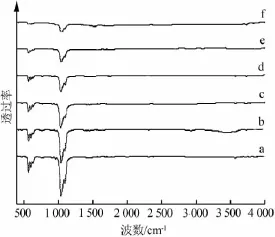
图2 样品的红外谱图
2.3 颗粒形貌分析
图3为合成的ZnSeHAP晶体的TEM照片。

图3 样品的TEM图
由图3可以看出,制备的ZnSeHAP均在纳米范围内,是一种单分散的棒状晶体。合成的ZnSeHAP晶体长度约为60~80 nm,宽度在20~30 nm,形状为棒状,具有良好的结晶度,HAP随Zn2+掺入量的增加,晶体颗粒尺寸逐渐减小,这是因为Zn离子取代部分Ca离子抑制了晶体的生长。区域电子衍射显示衍射花样为同心圆环,说明测试粉体为多晶材料,属于多种晶形共存的晶体。G.S.Kumar等[12]研究锌和二氧化碳复合掺杂的HAP也发现了类似的结果。
2.4 样品的成分及表面Zeta电位分析
通过X射线荧光光谱(XRF)测出样品中钙、锌及磷、硒的含量,并计算出(Ca+Zn)/(P+Se)的物质的量比,其值列于表2。所有样品的钙磷比都高于化学计量HAP的钙磷比,这是因为部分PO43-被CO32-取代的结果,红外谱图亦给出了相同的结论。
Zeta电位是反映固体表面带电性质和大小的指标,是固体粒子电行为的一个重要参数。本实验通过Malvern Nano-ZS Zeta电位仪测量了系列ZnSeHAP样品在BSA溶液中的表面电荷。表2列出了ZnSeHAP在模拟体液中的Zeta电位,其结果表明随着Zn含量的增加,Zeta电位逐渐减小,并由表面带正电变为表面带负电,这主要是因为越来越多的Ca2+被Zn2+取代。

表2 样品的XRF结果、Zeta电位值和BSA的负载量
2.5 系列ZnSeHAP样品对BSA的吸附及其在模拟体液中的释放行为
表2列出了系列ZnSeHAP载体对BSA的负载量,结果表明,随着Zn含量的增加,载体对BSA的负载量逐渐减少,其主要原因是由于载体表面电荷的多少决定的,根据Zeta电势的测试结果,在SBF溶液中,ZnSeHAP颗粒表面的电荷随Zn含量的增加呈下降的趋势,并且由正变负,而BSA在pH为7.40时显负电性,因此通过电荷间的相互作用导致载体对BSA的负载量逐渐减少。
图4为系列ZnSeHAP/BSA载药样品在模拟体液(SBF)中的累积释放曲线图。从图4可以看出,系列ZnSeHAP载体对BSA均具有良好的缓释作用。在初始的12 h内发生了药物突释现象,这是由于部分药物通过物理吸附结合在ZnSeHAP纳米颗粒表面,随着释放时间的增加,蛋白药物释放趋于平缓,这是由于载体与BSA蛋白间的静电引力起到了主导作用。从图4还可以观察到,在相同的释放时间上,随着载体中Zn含量的增加,其累积释放量同样是增加的,这同样是由于载体表面的电荷不同造成的,从Zeta电位的数据可以看出,Zn含量的增加导致载体表面的电荷减少,载体表面电荷的大小导致通过静电引力吸附于其表面的蛋白药物的多少。因此,在羟基磷灰石的制备过程中,通过掺杂不同的离子或含量不同的离子可以调控HAP表面的电荷,使其对不同的药物蛋白有选择性的吸附,以期达到对药物的有效控释。
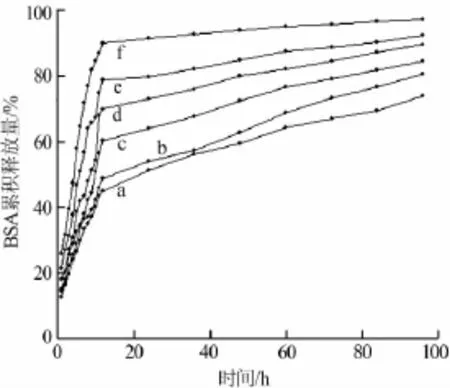
图4 系列ZnSeHAP/BSA载药样品在模拟体液中的累积释放曲线图
3 结论
本实验以Ca(NO3)2·4H2O,(NH4)2HPO4,Zn(NO3)2· 6H2O,Na2SeO3为前驱体,通过共沉淀法制备了硒、锌复合掺杂的HAP粉体,并应用XRD、FTIR、TEM、XRF和Zeta电位等技术对样品进行了表征。结果表明Zn2+和SeO32-能成功地掺入HAP晶格中,并随Zn含量的增加其纳米粒子逐渐减小,其表面电势逐渐变低。负载与释放实验表明:随Zn的掺杂时增加,BSA的负载量逐渐减小,在释放实验中ZnSeHAP/ BSA表现出了良好的缓释效果,说明通过Zn掺杂可以调变HAP的表面电荷,以达到控制HAP吸附量的目的。
[1] 顾雪梅,安燕,杨雪艳,等.含锶纳米羟基磷灰石的制备及性能研究[J].无机盐工业,2015,47(1):30-32.
[2] 曹娜娜,张万东,王永兰.羟基磷灰石湿法制备技术及应用研究进展[J].无机盐工业,2012,44(12):9-12.
[3] Zhao Q F,Wang T Y,Wang J,et al.Template-directed hydrothermal synthesis of hydroxyapatite as a drug delivery system for the poorly water-soluble drug carvedilol[J].Appl.Surf.Sci.,2011,257(23):10126-10133.
[4] Amer W,Abdelouahdi K,Ramananarivo H R,et al.Synthesis of mesoporous nano hydroxyapatite by using zwitterions surfactant[J]. Mater.Lett.,2013,107:189-193.
[5] Aina V,Lusvardi G,Annaz B,et al.Magnesium-and strontium-cosubstituted hydroxyapatite:the effects of doped-ions on the structure and chemico-physical properties[J].J.Mater.Sci.Mater.Med.,2012,23:2867-2879.
[6] Mostafa N Y,Hassan H M,Mohamed F H.Sintering behavior and thermal stability of Na+,SiO44-and CO32-co-substituted hydroxyapatites[J].J.Alloy.Comp.,2009,479:692-698.
[7] Kongsri S,Janpradit K,Buapa K,et al.Nanocrystalline hydroxyapatite from fish scale waste:Preparation,characterization and application for selenium adsorption in aqueous solution[J].Chem. Eng.J.,2013,215:522-532.
[8] Ito A,Otsuka M,Kawamura H,et al.Zinc-containing tricalcium phosphate and related materials for promoting bone formation[J].Curr. Appl.Phys.,2005,5:402-406.
[9] Zhang W D,Chai Y M,Xu X H,et al.Rod-shaped hydroxyapatite with mesoporous structure as drug carriers for proteins[J].Appl. Surf.Sci.,2014,322:71-77.
[10] Tank K P,Sharma P,Kanchan D K,et al.FTIR,powder XRD,TEM and dielectric studies of pure and zinc doped nano-hydroxyapatite[J].Cryst.Res.Technol.,2011,46(12):1309-1316.
[11] Zhang W D,Chai Y M,Cao N N,et al.Synthesis and characterization of selenium substituted hydroxyapatite via a hydrothermal procedure[J].Mater.Lett.,2014,134:123-125.
[12] Kumar G S,Thamizhavel A,Yokogawa Y,et al.Synthesis,charac
terization and in vitro studies of zinc and carbonate co-substituted nano-hydroxyapatite for biomedical applications[J].Mater.Chem. Phys.,2012,134:1127-1135.
联系方式:zhangwandong@tju.edu.cn
Preparation and drug loading properties of zinc and selenite co-substituted hydroxyapatite
Xu Xianghua1,Zhang Wandong1,Wang Yonglan2
(1.Department of Chemistry,School of Science,Tianjin University,Tianjin 300354,China;2.Stomatological Hospital,Tianjin Medical University)
Series of synthetic hydroxyapatites(HAP)containing both Zn2+and SeO32-were synthesized via co-precipitation method and the effects of the zinc ion doping concentrations on the morphology,surface charge,and chemical composition of the HAP were studied.The drug loading release properties of using the zinc and selenite co-substituted hydroxyapatite(ZnSeHAP)as drug carrier material and bovine serum albumin(BSA)as model drug were investigated.Results showed that the synthetic product exhibited an uniform rod-like morphology,with diameters of 20~30 nm and lengths of 60~80 nm,and the particles size decreased with increasing the content of Zn.An increase in Zn into the HAP lattice also led to a decrease in the surface charge when ZnSeHAP was suspended in simulated body fluid.In addition,the amount of loaded BSA decreased with increasing the zinc-doped content,which meant the surface charge of HAP could be adjusted by zinc doping,so as to achieve the purpose of controlling the adsorption amount of HAP.
hydroxyapatite;co-precipitations;loading;release
TQ132.41
A
1006-4990(2017)01-0025-04
2016-07-11
徐祥华(1989— ),男,硕士研究生,主要从事生物纳米材料制备技术及应用研究。
张万东
