栽培稻和普通野生稻居群根表铁膜形成能力的比较研究
2017-05-30黄剑冰任杰唐璐但建国
黄剑冰 任杰 唐璐 但建国
摘 要 根表铁膜形成能力反映了水稻根系氧化力的强弱。为了了解普通野生稻根系氧化力,采用水培铁胁迫试验对5个水稻品种和2个普通野生稻居群根表铁膜形成能力进行评价。结果表明:同亚洲栽培稻相比,普通野生稻拥有较高的根孔隙度,但其根表铁膜含量较低;供试植株的根孔隙度与根表铁膜含量之间没有相关性,这很可能与侧根的数量有关。
关键字 铁膜;根孔隙度;亚洲栽培稻;普通野生稻
中图分类号 S511 文献标识码 A
Abstract Iron plaque on roots is an indicator of root oxidation potential of Asian cultivated rice, Oryza sativa L. In order to determine the root oxidation potential of O. rufipogon Griff., iron plaque formation on the roots of five rice cultivars and two populations of O. rufipogon was investigated using hydroponic experiments. Iron plaque was induced by exposing the roots to a Kimura B nutrient solution supplemented with 0.532 mmol/L FeSO4 for 12 h. The results indicated that the O. rufipogon populations had higher root porosity, but lower content of iron plaque on roots compared with the rice cultivars. The root porosity of all tested plants was not correlated with the content of iron plaque on their roots, which was possibly attributed to difference in number of lateral roots on primary roots.
Key words iron plaque; root porosity; Oryza sativa; Oryza rufipogon
doi 10.3969/j.issn.1000-2561.2017.03.006
水稻是世界上最重要的粮食作物之一,亚洲栽培稻(Oryza sativa L.)为主要栽培种。亚洲栽培稻属湿生植物,其根系是由胚根、不定根及各次分枝的侧根所构成[1-2]。亚洲栽培稻的根系对淹水环境有2种适应对策[3]。其一,稻根具有发达的通气组织,以便将氧气快速、有效地转运到地下,满足根生长发育以及根际环境的耗氧所需。其二,胚根和不定根的中部和基部(从距根尖5~7 cm处起)有泌氧屏障(barrier to radial oxygen loss)[4-5],主要得益于木栓质在根外层组织的沉积[6-7]。该屏障能有效限制根内通气组织的氧气径向扩散到根际,有利于氧气纵向运输至根尖,从而促进根在厌氧环境中的伸长生长,同时还能阻止根际毒素、甲烷和乙烯等气体进入根内[3,7]。水稻根系分泌的氧气能使厌氧土壤中的Fe2+被氧化成Fe3+,并在根表沉积,形成根表铁膜(iron plaque)[8]。铁膜的主要组分为水铁矿,其次为纤铁矿,有时还有少量的针铁矿[9-10]。根表铁膜具有两性胶体的性质,可通过吸附和共沉淀等作用影响水稻植株对磷、锌以及镉、铬、铅、砷等重金属的吸收及其转运,故这一领域的研究备受国内外的关注[11-12]。水稻根系分泌的氧气和土壤溶液中Fe2+浓度是影响根表铁膜形成的2个主要因素[13-16]。水稻根系泌氧能力跟品种有关,不同水稻品种的根表铁膜形成能力是有差异的[17-21]。因此,根表铁膜形成能力可用来表征水稻根系的氧化力[22-23]。
普通野生稻(Oryza rufipogon Griff.)是亚洲栽培稻的野生祖先种[24-26]。在中国,普通野生稻仅分布于广东、广西、海南、云南、江西、湖南、福建和台湾等省(区)。普通野生稻为多年生水生植物,喜栖息在常年有水的沼泽、湖泊、沟渠附近[26-29]。普通野生稻拥有更丰富的遗传多样性和更复杂的遗传背景,蕴藏着极其丰富的优异基因,是水稻栽培品种改良的重要遗传资源[25-26]。但是,迄今为止,国内外对普通野生稻根系的研究报道比较少。有关普通野生稻根表铁膜的研究尚处空白。本研究拟对不同水稻品种和普通野生稻居群根表铁膜形成能力进行评价和比较,所得结果将有助于普通野生稻资源的保护与利用。
1 材料与方法
1.1 材料
以5个水稻品种和2个普通野生稻居群作为供试材料。水稻品种包括‘特籼占25、‘新黄占、‘海香占、‘琼糯和‘63选。普通野生稻采自海南省琼海市中原普通野生稻自然保护区和海南省万宁市东澳普通野生稻自然保护区西部,分别称为‘琼海居群和‘万宁居群。
1.2 方法
1.2.1 水稻和普通野生稻的培养 水稻:挑选饱满的水稻种子,用54 ℃热水浸种,放置室内。24 h后将种子移至湿润滤纸上催芽。萌芽后第7天的幼苗用1/2木村B营养液进行沙培12 d。接着,将稻苗转移到圆口塑料桶(桶深18.5 cm、直徑20 cm)中,用木村B营养液进行水培31.5 d。将稻株插入泡沫板小孔中,以海绵固定植株,让根茎交界处距离水面2.5 cm。每3 d更换一次营养液。每桶8株稻苗,每个品种共计24株。沙培和水培均在自然光照和变温(21~33 ℃)条件下进行。木村B营养液配方是[30]:(NH4)2SO4 0.37 mmol/L,MgSO4·7H2O 0.55 mmol/L,KNO3 0.18 mmol/L,CaNO3·4H2O 0.37 mmol/L,KH2PO4 0.21 mmol/L,Na2EDTA-Fe(Ⅱ) 90 μmol/L,MnCl2·4H2O 7.3 μmol/L,H3BO3 9.3 μmol/L,(NH4)6Mo7O24·4H2O 0.015 μmol/L,ZnSO4·7H2O 0.15 μmol/L,CuSO4·5H2O 0.16 μmol/L,其pH调至5.5。
普通野生稻:采自野外的普通野生稻用木村B营养液培养。当新芽萌发后第14天,将幼苗从母株分离,然后进行沙培和水培,方法同前。
1.2.2 铁胁迫试验 挑选长势一致的水稻和普通野生稻植株供试。将供试植株转移到室内[培养温度为(26±1)℃, 每日光照14 h,光强330 lx,相对湿度60%±5%]。用去离子水培养0.5 d,然后用含高浓度Fe2+的营养液对植株进行铁胁迫处理。配置该营养液时,将木村B营养液配方中的Na2EDTA-Fe(Ⅱ)90 μmol/L替换为FeSO4·7H2O 0.532 mmol/L。胁迫处理时水稻和普通野生稻植株年龄分别为50 d和57 d,均处于分蘖期。铁胁迫24 h后,收获植株。随机挑选3株,测定根生物量。剪下其他植株的根用去离子水清洗3次,然后用吸水纸吸干根表面的水分。最后,将根装入封口袋中,置于4 ℃保存,这些根被用来测定根含水量、根孔隙度和根表铁膜。
1.2.3 根含水量和根生物量的测定 测定根含水量或根生物量时,将根置于105 ℃烘干30 min后,在70 ℃烘干72 h至恒重,然后称重。
1.2.4 根孔隙度的测定与计算 参照Kludze等[31]和Mei等[17]报道的方法。称取0.5~1.0 g根,放入盛满去离子水的100 mL比重瓶,擦干瓶称重。取出根,剪成1 cm长的根段,放入装有40 mL去離子水的离心管(50 mL)中,抽真空处理2次,每次持续2 h。最后,将根段取出,再放入比重瓶,擦干瓶称重。每处理设3次重复。按下列公式计算根孔隙度:
POR=[(pvr-pr)/(r+p-pr)]×100
其中,POR为根孔隙度(%);r为根重(g);p为盛满水时比重瓶的重量(g);pr为完整稻根装入满水比重瓶时比重瓶的重量(g);pvr为经抽真空处理后的根段装入满水比重瓶时比重瓶的重量(g)。
1.2.5 根表铁膜的提取、测定和计算 采用DCB(Dithionite-Citrate-Barbonate)法提取铁膜[32]。将0.5~1.0 g 根放入250 mL蓝盖广口瓶中,添加45 mL DCB提取液(含Na3C6H5O7·2H2O 0.27 mol/L,NaHCO3 0.11 mol/L,Na2S2O4 3.0 g,pH值调至6.5),于26 ℃震荡3 h。用去离子水将提取液定容至100 mL。经孔径0.45 μm滤网过滤后,取5 mL于15 mL离心管中,再添加1 mL浓硝酸,摇匀后于4 ℃保存待测。样品铁含量用原子吸收分光光度计(AA6401F,日本岛津)测定。每处理设3次重复。根据提取液铁含量、根重和根含水量计算根表铁膜含量(以每克干根含多少毫克Fe计,mg/g。下同)。用每处理根表铁膜含量的平均值乘以根生物量即得到单株根表铁膜数量(以每株含多少毫克Fe计,mg/株。下同)。
1.3 数据分析
采用Excel 2003进行数据处理和作图。采用SPSS 18.0统计软件进行统计分析和Duncan多重比较。
2 结果与分析
2.1 根孔隙度和根生物量
在供试的5个水稻品种和2个普通野生稻居群中,普通野生稻拥有较高的根孔隙度(表1)。‘琼海居群的根孔隙度最高,为35.05%,‘万宁居群和‘新黄占分列第2和第3位,但三者之间没有显著差异(p>0.05)。‘琼海居群根孔隙度同其他4个水稻品种的差异均达显著水平(p<0.05)。‘琼糯根孔隙度最低,仅为21.67%。
同样地,普通野生稻的根生物量也比水稻高(表1)。‘琼海居群根生物量高达337.96 mg,显著高于其他供试材料的根生物量(p<0.05)。‘特籼占25根生物量最低,只有105.10 mg,与‘万宁居群之间的差异也达到显著水平(p<0.05)。5个水稻品种的根生物量之间都没有显著差异(p>0.05)。
2.2 根表铁膜
由表2可见,普通野生稻的根表铁膜含量比部分水稻品种低。水稻‘海香占的根表铁膜含量最高,为6.30 mg/g。‘琼海居群的根表铁膜含量最低,只有3.86 mg/g,其铁膜形成能力同水稻‘63选近似,但同‘万宁居群和其他水稻品种均有显著差异(p<0.05)。但是,由于普通野生稻拥有较高的根生物量,其单株根表铁膜含量大于水稻。普通野生稻‘琼海居群单株根表铁膜数量最多,为1.31 mg/株,‘海香占次之,而‘万宁居群和其余4个水稻品种的单株根表铁膜数量相似,为0.50~0.68 mg/株,彼此之间没有显著差异(p>0.05)。
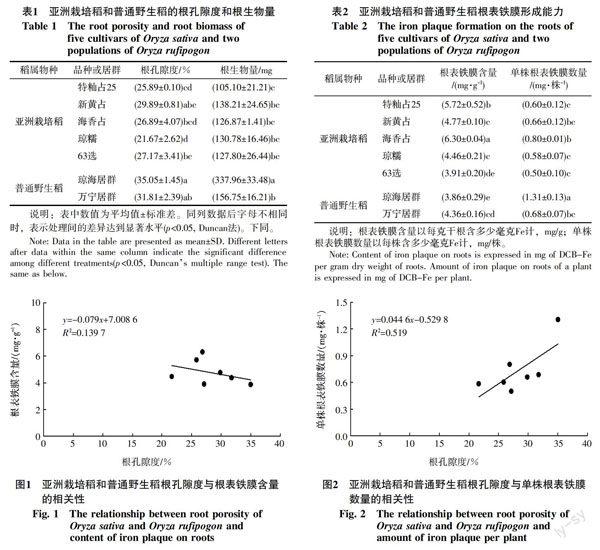
5个水稻品种和2个普通野生稻居群的根孔隙度与根表铁膜含量之间没有相关性(图1)。虽然根孔隙度与单株根表铁膜数量之间有一定程度的正相关(图2),但其相关性仍未达显著水平(p>0.05)。
3 讨论
本文首次对2个普通野生稻居群根表铁膜形成能力进行了研究,并同5个水稻品种做对比分析。结果发现,同亚洲栽培稻相比,普通野生稻拥有较高的根孔隙度,但其根表铁膜含量较低;所有供试材料的根孔隙度与根表铁膜含量之间没有相关性。
根孔隙度可用来表征根内通气组织的发达程度。普通野生稻的根孔隙度比亚洲栽培稻要高一些,主要跟它们的生境有关。作为一种多年生植物,普通野生稻生长于长期淹水的环境中[25-26,28];而亚洲栽培稻为一年生作物,在其生育期内,稻田土壤并非一直处于淹水状态,因高产需要,分蘖后期的稻田常常进行排水晒田。淹水是导致水稻等湿地植物的根部形成发达通气组织的主要环境因子之一[3-4]。所以,终年淹水促使普通野生稻具有更高的根孔隙度。在本研究中,供试水稻品种的根孔隙度介于21.67%~29.89%之间,通气组织处于中等水平。Wu等[33]对20个水稻品种根孔隙度的测定结果为12.4%~33.2%。稻根泌氧能力在一定程度上取决于根孔隙度的大小。不同水稻品种的泌氧速率随根孔隙度的提高而增大[17]。水稻泌氧的增多更有利于根表铁膜的形成。本研究中5个水稻品种的根表铁膜含量介于3.9~6.30 mg/g,其值小于Wu等[18]的水培试验结果(11.2~25.1 mg/g),这种差异主要归功于试验条件的不同。本研究对植株进行铁胁迫试验时光强较弱。在Wu等[18]的研究中,采用了自然光照加钠灯补光和充氮气处理。光强的提高能使水稻根系泌氧增多[34]。铁胁迫试验时充氮气能使根表铁膜增厚[35]。
在水稻根表铁膜的研究中,根表铁膜形成能力有3种评价指标,即根表铁膜含量[17-20]、单株根表铁膜数量[36-38]和根表铁膜厚度[21]。其中最常用的是根表铁膜含量,指的是每单位干根上铁膜所含铁的重量。单株根表铁膜数量是指每株根系上铁膜所含铁的重量,可用根生物量乘以根表铁膜含量即可得到该值。显然,根系的形态和结构特征,以及根生物量都会影响单株根表铁膜数量。根表铁膜含量和单株根表铁膜数量这2个指标均没有考虑根表面积对根表铁膜形成能力的影响。有人曾报道,水稻根孔隙度与根表铁膜含量呈正相关[18-19]。但是,本研究未观测到此现象,供试材料根孔隙度与根表铁膜含量之间没有相关性。这种不一致性可能与试验材料的侧根数量有关。侧根可分为粗大侧根和细小侧根。细小侧根没有通气组织[2],也没有泌氧屏障,但拥有更大的根表面积,所以,细小侧根是根系泌氧的重要场所[39-40]。曾有人应用圆筒状金属铂电极(cylindrical Pt cathodes)技术[5]和二维平面光极(planar-optode)技术[34],从空间尺度证实了水稻侧根的泌氧潜力。本研究中没有对侧根进行测定,但肉眼观察发现,2个普通野生稻居群根系的侧根极少,而供试水稻品种中有的品种侧根多,有的侧根较少。根表铁膜厚度是指每单位根表面积上铁膜所含铁的重量。Holzschuh等[21]曾报道距根尖6 cm水稻不定根根段的根孔隙度與根表铁膜厚度呈正相关。但是,Wu等[18]发现水稻根系的根孔隙度与根表铁膜厚度没有相关性。可见,基于单位根表面积的根表铁膜厚度也没有涵盖整个根系的根表面积对根表铁膜形成的贡献。所以,在未来的研究中,有必要提出新的评价指标,以综合表征根孔隙度和根表面积对根系铁膜形成能力的影响。
致 谢 海南省农业科学院粮食作物研究所孟卫东研究员和王效宁研究员提供水稻种子。
参考文献
[1] Suralta R R, Inukai Y, Yamauchi A. Genotypic variations in responses of lateral root development to transient moisture stresses in rice cultivars[J]. Plant Production Science, 2008, 11: 324-335.
[2] Rebouillat J, Dievart A, Verdeil J L, et al. Molecular genetics of rice root development[J]. Rice, 2009, 2: 15-34.
[3] Nishiuchi S, Yamauchi T, Takahashi H, et al. Mechanisms for coping with submergence and waterlogging in rice[J]. Rice, 2012, 5: 1-14.
[4] Colmer T D. Aerenchyma and an inducible barrier to radial oxygen loss facilitate root aeration in upland, paddy and deep-water rice (Oryza sativa L.)[J]. Annals of Botany, 2003, 91: 301-309.
[5] Armstrong J, Armstrong W. Rice: sulfide-induced barriers to root radial oxygen loss, Fe2+ and water uptake, and lateral root emergence[J]. Annals of Botany, 2005, 96: 625-638.
[6] Schreiber L, Franke R, Hartmann K D, et al. The chemical composition of suberin in apoplastic barriers affects radial hydraulic conductivity differently in the roots of rice (Oryza sativa L. cv. IR64) and corn (Zea mays L. cv. Helix)[J]. Journal of Experimental Botany, 2005, 56: 1 427-1 436.
[7] Shiono K, Yamauchi T, Yamazaki S, et al. Microarray analysis of laser-microdissected tissues indicates the biosynthesis of suberin in the outer part of roots during formation of a barrier to radial oxygen loss in rice (Oryza sativa)[J]. Journal of Experimental Botany, 2014, 65: 4 795-4 806.
[8] Chen C C, Dixon J B, Turner F T. Iron coatings on roots: Mineralogy and quantity influencing factors[J]. Soil Science Society of America, 1980, 44: 635-639.
[9] Liu W J, Zhu Y G, Hu Y, et al. Arsenic sequestration in iron plaque, its accumulation and speciation in mature rice plants (Oryza sativa L.)[J]. Environmental Science and Technology, 2006, 40: 5 730-5 736.
[10] Seyfferth A L, Webb S M, Andrews J C, et al. Arsenic localization, speciation, and co-occurrence with iron on rice (Oryza sativa L.) roots having variable Fe coatings[J]. Environmental Science and Technology, 2010, 44: 8 108-8 113.
[11] Seyfferth A L. Abiotic effects of dissolved oxyanions on iron plaque quantity and mineral composition in a simulated rhizosphere[J]. Plant Soil, 2015, 397: 43-61
[12] Khan N, Seshadri B, Bolan N, et al. Root iron plaque on wetland plants as a dynamic pool of nutrients and contaminants[J]. Advances in Agronomy, 2016, 138: 1-96.
[13] Mendelssohn I A, Kleiss B A, Wakeley J S. Factors controlling the formation of oxidized root channels - a review[J]. Wetlands, 1995, 15: 37-46.
[14] Snowden R E D, Wheeler B D. Chemical changes in selected wetland plant species with increasing Fe supply, with specific reference to root precipitates and Fe tolerance[J]. New Phytologist, 1995, 131: 503-520.
[15] 劉文菊, 朱永官. 湿地植物根表的铁锰氧化物膜[J]. 生态学报, 2005, 25(2): 359-363.
[16] Zhou X B, Shi W M, Zhang L H. Iron plaque outside roots affects selenite uptake by rice seedlings (Oryza sativa L.) grown in solution culture[J]. Plant and Soil, 2007, 290: 17-28.
[17] Mei X Q, Ye Z H, Wong M H. The relationship of root porosity and radial oxygen loss on arsenic tolerance and uptake in rice grains and straw[J]. Environmental Pollution, 2009, 157: 2 550-2 557.
[18] Wu C, Ye Z H, Li H, et al. Do radial oxygen loss and external aeration affect iron plaque formation and arsenic accumulation and speciation in rice[J]. Journal of Experimental Botany, 2012, 63: 2 961-2 970.
[19] Cheng H, Wang M, Wong M, et al. Does radial oxygen loss and iron plaque formation on roots alter Cd and Pb uptake and distribution in rice plant tissues[J]. Plant and Soil, 2014, 375: 137-148.
[20] Pereira E G, Oliva M A, Siqueira-Silva A I, et al. Tropical rice cultivars from lowland and upland cropping systems differ in iron plaque formation[J]. Journal of Plant Nutrition, 2014, 37: 1 373-1 394.
[21] Holzschuh M J, Carlos F S, Carmona F C, et al. Iron oxidation on the surface of adventitious roots and its relation to aerenchyma formation in rice genotypes[J]. Revista Brasileira de Ciência do Solo, 2014, 38: 185-192.
[22] 傅友强, 吴道铭, 申守营, 等. 一种定量测定水稻根系氧化力的新方法[J]. 土壤, 2013, 45(6): 1 133-1 136.
[23] Atulba S L, Gutierrez J, Kim G W, et al. Evaluation of rice root oxidizing potential using digital image analysis[J]. Journal of the Korean Society for Applied Biological Chemistry, 2015, 58: 463-471.
[24] Huang X, Kurata N, Wei X, et al. A map of rice genome variation reveals the origin of cultivated rice[J]. Nature, 2012, 490: 497-501.
[25] Sang T, Ge S. Understanding rice domestication and implications for cultivar improvement[J]. Current Opinion in Plant Biology, 2013, 16: 139-146.
[26] 杨庆文, 黄 娟. 中国普通野生稻遗传多样性研究进展[J]. 作物学报, 2013, 39(4): 580-588.
[27] 王效宁, 韩东飞, 云 勇, 等. 利用SSR标记分析海南普通野生稻的遗传多样性[J]. 植物遗传资源学报, 2007, 8(2): 184-188.
[28] 刘 迪, 孟卫东. 海南野生稻的遗传多样性及其保护与利用[J]. 杂交水稻, 2010, S1: 525-527.
[29] Liu W, Shahid M Q, Bai L, et al. Evaluation of genetic diversity and development of a core collection of wild rice (Oryza rufipogon Griff.) populations in China[J]. PLoS One, 2015, 10(12), e0145990.
[30] Ma J F, Takahashi E. Effect of silicon on the growth and phosphorus uptake of rice[J]. Plant Soil, 1990, 126: 115-119.
[31] Kludze H K, DeLaune R D, Patrick W H. A colorimetric method for assaying dissolved oxygen loss from container-grown rice roots[J]. Agronomy Journal, 1994, 86: 483-487.
[32] Chen R F, Shen R F, Gu P, et al. Response of rice (Oryza sativa) with root surface iron plaque under aluminium stress[J]. Annals of Botany, 2006, 98: 389-395.
[33] Wu C, Ye Z H, Shu W S, et al. Arsenic accumulation and speciation in rice are affected by root aeration and variation of genotypes[J]. Journal of Experimental Botany, 2011, 62: 2 889-2 898.
[34] Larsen M, Santner J, Oburger E, et al. O2 dynamics in the rhizosphere of young rice plants (Oryza sativa L.) as studied by planar optodes[J]. Plant Soil, 2015, 390: 279-292.
[35] Xu B, Yu S. Root iron plaque formation and characteristics under N2 flushing and its effects on translocation of Zn and Cd in paddy rice seedlings (Oryza sativa)[J]. Annals of Botany, 2013, 111: 1 189-1 195.
[36] Lee C H, Hsieh Y C, Lin Z H, et al. Iron plaque formation and its effect on arsenic uptake by different genotypes of paddy rice[J]. Plant and Soil, 2013, 363(1-2): 231-241.
[37] 傅友強, 杨旭健, 吴道铭, 等. 磷素对水稻根表红棕色铁膜的影响及营养效应[J]. 中国农业科学, 2014, 47(6): 1 072-1 085.
[38] 丁汉卿, 赖聪玲, 沈 宏. 干湿交替和过氧化物对水稻根表铁膜及养分吸收的影响[J]. 生态环境学报, 2015, 24(12): 1 983-1 988.
[39] Kirk G J D. Rice root properties for internal aeration and efficient nutrient acquisition in submerged soil[J]. New Phytologist, 2003, 159: 185-194.
[40] Kirk G J D, Greenway H, Atwell B J, et al. Adaptation of rice to flooded soils[J]. Progress in Botany, 2014, 75: 215-253.
