焦炉气转化制甲醇原料气工艺简析
2017-05-30李霞
李霞
摘要:利用焦炉气制取甲醇合成气是焦化厂利用焦炉气经济效益最好的工艺方法之一,也是焦炉气综合利用和深加工的先进技术。文章简要分析了焦炉气组成及转化工艺,结果表明,在投资复杂性、能量消耗方面,非催化转化工艺经济效益优于催化转化。
关键词:焦炉气;非催化转化;甲醇
焦炉气是焦化企业在炼焦过程中,除了产出焦炭和焦油外,获得的可燃气体,其中含有55%~60%的氢气,23%~27%的甲烷,5% ~8%的一氧化碳和少量的二氧化碳、氧气及不饱和烃。是炼焦过程的重要副产品。据统计,截至2015年,我国已是世界上最大的焦炭供应国和消费国,同时伴随有大量的焦炉气资源产生。目前我国焦炉气的利用状况是:一部分作为加热原料返回炼焦炉,一部分用作城市燃料气,还有一部分通过火炬烧掉,这样不仅浪费了资源,更污染了环境,造成了较大的损失。因此,焦炉气的综合利用具有重大的经济和环境效益,而焦炉煤气制甲醇就是一条很好的利用途径。
1 焦炉气转化制甲醇原料气工艺
焦炉气制甲醇主要流程是:焦炉气预处理→焦炉气压缩→转化→净化→甲醇合成。
1.1焦炉气的组成
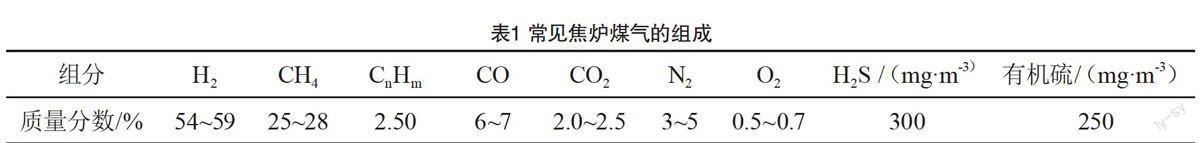
焦炉煤气是煤干馏过程中释放的小分子气体。根据干馏温度分为低温干馏(550~650℃)、中温干馏(700~900℃)和高温干馏(900~1100℃),干馏终温不同,气体成分差别较大,焦化属于高温干馏范畴,副产的煤气中除含有一氧化碳、二氧化碳、氢气、甲烷、氧氮外,还有大量的硫化氢、硫氧化碳、二硫化碳、氨、苯、焦油等,典型的焦炉气成分如表1所示[1-2]。
1.2焦炉气预处理
从焦化装置来的焦炉气中含有焦油、苯、萘、硫化物、粉尘等物质,由于温度、压力等生产条件的改变,改变了各物质的分压,造成一部分此类物质凝结为液滴或固体颗粒,该类物质对后续工段造成一定的危害,必须将这些物质清除。因此,焦炉煤气在送到后续工段之前先要进行预处理,以除去苯、萘、焦油、粉尘等易凝或易结晶的物质,避免对后续工段造成危害。
焦炉气预处理的主要任务是将从炼焦厂来的焦炉气依次通过洗涤塔(洗涤除去焦炉气中的大部分焦油、苯、萘和大颗粒粉尘等),焦炉气过滤器(过滤吸附洗涤塔未脱除的萘、苯、焦油等),电捕焦油器(除去洗涤塔、过滤器未除去的微米等级的雾滴或粉尘)进行脱苯、脱焦油及降尘处理,达标后将气体压缩送至转化工段。
1.3转化
一般焦化企业副产的焦炉气量较大,据估算,每生产一吨焦炭,大致产生420m?左右的焦炉气。其中大约一半作为燃料气回炉,剩余部分需使用專门的装置进行回收,否则就只有通过火炬烧掉。
焦炉气含有25%左右的CH4,其在甲醇合成过程中作为惰性气体存在,对合成不利,可以将其与水蒸气在一定的温度、压力下,运用特定催化剂转化为氢气和一氧化碳(甲醇原料气),提高焦炉气利用价值。因此,将焦炉气转化,转变为更高效的甲醇合成气是焦炉气制备甲醇工艺中重要一环。
1.3.1焦炉气转化工艺
焦炉气转化工艺可分为催化蒸气转化法、催化部分氧化法、非催化部分氧化法3种。
(l)催化蒸汽转化法。催化蒸汽转化法是指在一定温度、压力条件下,运用催化剂镍,通过甲烷一水蒸气重整反应,生成一氧化碳和氢气的工艺,主要参与的反应式有:
CH4+H20 =C0+3H2 △H298=206.4 kj/mol
(l)
CH4+2H20=C02+4H2△H298=165.4 kj/mol
(2)
CH4+C02=2C0+2H2 △H298=247.4 kj/mol
(3)
CO+H20=C02+H2
△H298= - 41.2 kj/mol
(4)
催化转化后,转化气变为以一氧化碳、氢气和二氧化碳为主的混合物,反应式(4)决定着三者的化学平衡关系。(1-3)式为蒸汽转化的主反应,反应过程吸热。
催化蒸汽转化法早前常用于天然气间歇转化制合成气(如以天然气为原料的小型合成氨厂),尽管该工艺简单,投资小,但因其高能耗,生产强度不够,需经常更换催化剂,该工艺逐渐被淘汰。此外,催化蒸汽转化技术应用的对象需含有较多的甲烷气体(如天然气),而焦炉煤气中甲烷含量约为25%左右,含量偏低,且还满足不了单程转化后甲烷残余量小于l.O%的要求,因此,催化蒸汽转化法不易用于焦炉煤气转化。
(2)催化部分氧化法。催化部分氧化法是原料气和氧气发生部分燃烧,放出的热量被甲烷转化所利用的工艺。具体过程为:原料气部分氧化产生热量,部分氧化后的混合物进入催化剂床层,在一定温度下、压力下发生甲烷转化。该工艺所用反应器由燃烧室和反应室两部分组成,原料气部分氧化发生在燃烧室,甲烷转化在反应室,从而进一步获得合成气。
以天然气为原料时,氧化燃烧的主要反应有(5~7)式:
CH4+202=C02+2H2O
△H298= - 802.6 kj/mol (5)
CH4+02=CO+H2+H20 △H298= - 278.0 kj/mol
(6)
2CH4+02=2C0+4H2
△H298= - 71.2 kj/mol
(7)
H2+1/202=H2O
△H298= - 241.0 kj/rriol
(8)
以一段反应器出口气或焦炉煤气为原料时,由于混合气中含有大量的氢气,氢气的燃烧速率远远大于一氧化碳和甲烷,所以原料气部分氧化主要发生的是氢气和氧气的燃烧反应(反应式8)。生成水的同时产生大量的热。
在燃烧过程中,可能伴有少量的CH4和CO燃烧反应。也可能有少量水蒸气发生(1)和(4)反应。整个反应中也伴有副反应的发生,当水蒸气量不足或温度过高时,有甲烷裂解和炭黑与水蒸气的气化反应。
CH4=C+2H2-77.9 kJ
(9)
C+H2O=CO+H2-127.7 kJ
(10)
以上主反应是放热反应,结果使整个反应体系温度升高。当部分氧化后的混合气到达反应室催化剂床层时,99%以上的氧气己消耗。此时的主要反应为(1~4)式。因此,燃烧室和反应室的总反应为(11、12)式。
CH4+(1/2) 01=C0+2H1 △H298= - 36 kj/rriol
(II)
CH4+(3/2) 02=_C0+2H20△H298= - 519 kj/mol (12)
此类工艺为部分氧化工艺。焦炉煤气CH4含量相对较低,可以采用该工艺进行转化。
专利CN138550IA以镍化合物为催化剂、2.07 MPa、950~1150℃条件下[3],采用部分氧化工艺对焦炉气进行了转化,结果表明,该技术优于常规的甲烷蒸汽转化法。主要体现在节能、投资小、能安全运行、保护镍催化剂等方面。
但由于该工艺中副反应产生的积碳易使催化剂中毒失活,因此,这就要求催化剂在使用中要具有较高的活性、稳定性、选择性及抗积碳能力。
(3)非催化部分氧化法。该方法于20世纪50年代中期實现工业化,天然气非催化部分氧化制合成气工艺技术成熟后,以焦炉煤气为代表的富甲烷气体作为新洁净能源被逐渐重视。非催化部分氧化转化工艺中的主要反应物有CH4、H20和02。主要的反应有(1-8)式。
甲烷非催化部分氧化转化是热力学控制过程,反应温度升高,反应速率加快。一般此反应操作温度达l300~1500℃。
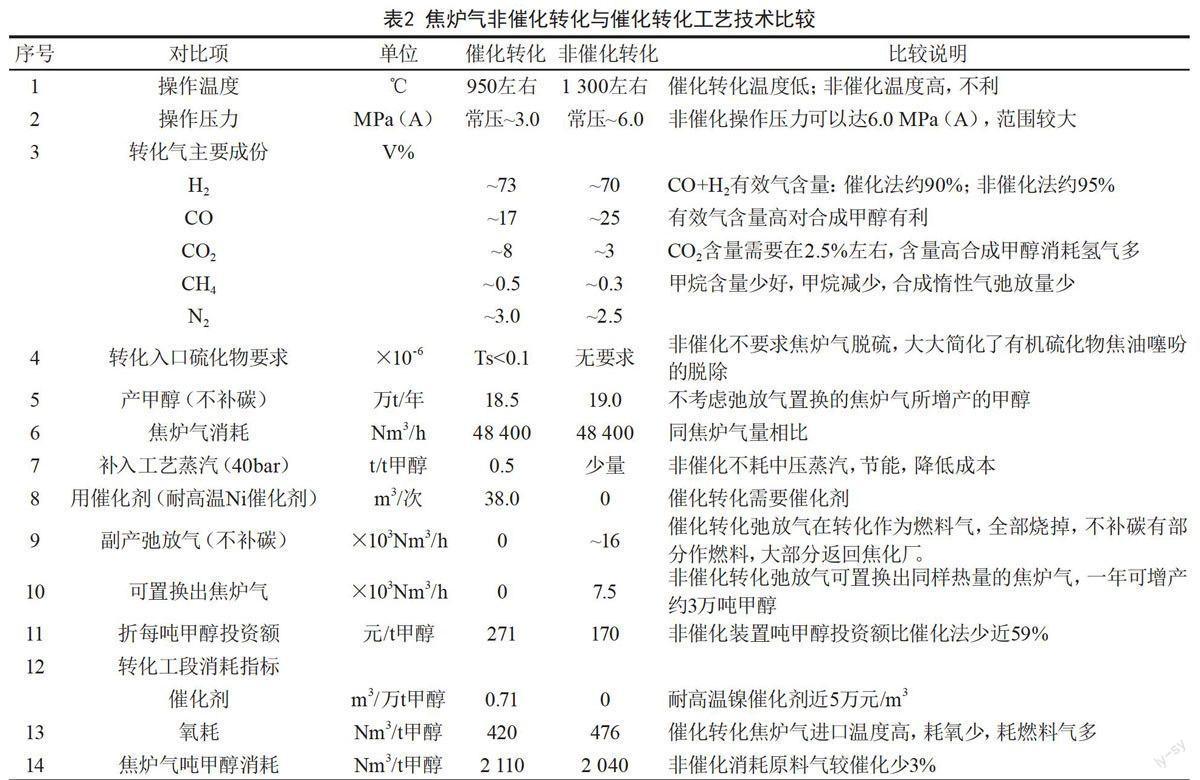
非催化部分氧化工艺对原料气要求低,无需深度脱硫,无催化剂中毒问题;工作过程主要是通过高温裂解反应,将烷烃、烯烃及芳烃转化成炭和氢气;该方法操作温度高,所以能耗相对也高,l300℃高的转化温度,对转化炉和废热锅炉设计要求难度也相应增加;且产品气中有积碳生成,所以后续需有净化处理设备。为抑制炭黑的生成,在甲烷转化时通常加入一定量的蒸汽,使甲烷进行蒸汽转化反应。焦炉气非催化转化与催化转化工艺技术比较如表2所示。
