羟考酮用于缺血后处理对家兔心肌缺血再灌注损伤的影响
2017-05-25高宏博申文增贾辛未牛培赵文萍付立强尚雪飞彭燕杨旭
高宏博,申文增,贾辛未,牛培,赵文萍,付立强,尚雪飞,彭燕,杨旭
(1河北大学附属医院,河北保定071000;2河北大学;3保定市第一医院)
羟考酮用于缺血后处理对家兔心肌缺血再灌注损伤的影响
高宏博1,申文增2,贾辛未1,牛培2,赵文萍1,付立强1,尚雪飞3,彭燕3,杨旭3
(1河北大学附属医院,河北保定071000;2河北大学;3保定市第一医院)
目的 探讨羟考酮用于缺血后处理对缺血再灌注家兔心肌的保护作用,并观察κ受体在羟考酮缺血后处理中的作用。方法 将48只雄性家兔随机分为4组,假手术组开胸后左前降支只穿线,不结扎;缺血再灌注组开胸后左前降支结扎心肌缺血 30 min,再灌注 180 min,建立缺血再灌注模型;羟考酮后处理组于再灌注起始前5 min开始缓慢静脉给予羟考酮0.3 mg/kg;κ受体拮抗剂+羟考酮后处理组于再灌注起始前10 min给予κ受体拮抗剂3 mg/kg,余处理同羟考酮后处理组。于再灌注末测定各组血清CK-MB、cTnI水平,TTC法测定心肌梗死面积(IS),计算心肌梗死面积百分比(IS/LVS)。留取心肌组织,免疫组化染色法检测细胞缝隙连接蛋白43(CX43)表达。结果 与假手术组比较,缺血再灌注组、羟考酮后处理组、κ受体拮抗剂+羟考酮后处理组血清CK-MB、cTnI水平升高,CX43表达降低(P均<0.05)。与缺血再灌注组比较,羟考酮后处理组IS/LVS降低,血清CK-MB、cTn-I水平降低,CX43表达升高(P<0.05或<0.01)。与羟考酮后处理组比较,κ受体拮抗剂+羟考酮后处理组IS/LVS及血清CK-MB、cTn-I水平升高,CX43表达降低(P均<0.05)。结论 羟考酮缺血后处理能够降低血清CK-MB、cTn-I,减少IS,具有减轻心肌缺血再灌注损伤的作用;其机制可能是通过激动κ受体后调节CX43表达来发挥心肌保护作用。
羟考酮;再灌注损伤;心肌;缺血后处理;κ受体;缝隙连接蛋白43;兔
造成急性心肌梗死患者的心肌损伤有两个过程,即冠状动脉阻塞导致的心肌缺血损伤和冠状动脉再通后的心肌再灌注损伤,两者合称为缺血再灌注损伤(IR)[1]。减少再灌注期间的心肌损伤对改善患者预后、提高患者生存质量具有重要意义。研究表明,缺血后处理及吗啡、瑞芬太尼、美沙酮等阿片受体激动剂后处理可减轻实验动物心肌缺血再灌注损伤[2~4]。羟考酮为半合成蒂巴因类衍生物,属阿片类强效镇痛药,具有较强的κ受体激动作用。研究表明,羟考酮可减轻大鼠肠缺血再灌注诱发的肝损伤[5],但其对心肌缺血再灌注损伤的影响尚无定论。细胞缝隙糖蛋白43(CX43)是心肌组织表达的主要缝隙连接蛋白,是决定冠状动脉阻塞后心肌梗死面积(IS)大小的因素之一。2016年6~9月,我们对家兔心肌缺血再灌注损伤模型给予羟考酮后处理,观察其对血清cTnI及CK-MB、IS、心肌组织CX43表达的影响,探讨羟考酮对心肌缺血再灌注损伤的影响及其可能的作用机制。
1 材料与方法
1.1 材料 健康清洁级雄性家兔48只,2~3月龄,体质量2.2~2.8 kg,由河北大学动物实验中心提供。实验前禁食12 h、禁水2 h。盐酸羟考酮注射液(BJ940,Hamol公司,英国),κ受体拮抗剂nor-binaltorphimne(Tocris公司,英国),CK-MB试剂盒、cTnI试剂盒、UniCel DxI 800免疫分析系统(贝克曼·库尔特公司,美国),一抗为小鼠抗大鼠CX43单克隆抗体(BD公司,美国),二抗为山羊抗小鼠抗体(中杉金桥),SP9002生物素-链霉卵白素免疫组化检测试剂盒(中杉金桥),DAB显色剂(迈新试剂),氯化三苯基四氮唑(TTC),BL-420S生物机能实验系统(成都泰盟)。
1.2 动物分组与处理 将家兔随机分为假手术组、缺血再灌注组、缺血后处理组、羟考酮后处理组、κ受体拮抗剂+羟考酮后处理组各12只。参照文献[6]方法制备心肌缺血再灌注损伤模型。向家兔耳缘静脉注射25%氨基甲酸乙酯麻醉后,仰卧位固定。于左侧胸壁第3、4肋间距离胸骨左缘约0.5 cm处逐层钝性分离开胸,剪开心包膜,暴露心脏。在左心耳下方1~2 mm处,以5-0无损伤缝合线在左冠状动脉前降支下穿线,进针深度约1.5 mm。将缝线两端穿过内径0.1 cm、长2 cm的硅胶管,稳定10 min后束紧结扎线,行左冠状动脉缺血30 min,然后松开结扎线进行再灌注180 min。缺血成功的标准:结扎线以下心肌组织发绀,ECG示胸导联ST段抬高>0.3 mV;再灌注成功的标准:心肌局部反应性充血,ECG示胸导联抬高的ST段下降1/2以上。假手术组仅穿线不结扎;缺血再灌注组左前降支结扎心肌缺血30 min,再灌注180 min;羟考酮后处理组于再灌注起始前5 min开始缓慢静脉给予羟考酮0.3 mg/kg;κ受体拮抗剂+羟考酮后处理组于再灌注起始前10 min给予κ受体拮抗剂3 mg/kg,余处理同羟考酮后处理组。
1.3 血清cTnI、CK-MB水平检测 于再灌注3 h时,用EDTA抗凝管经颈静脉采集血样2~3 mL,离心取上清。采用UniCel DxI 800免疫分析系统、磁粒子化学发光法检测血清cTnI、CK-MB水平。
1.4 IS测定 采集颈静脉血后处死家兔,快速取出心脏,用冰生理盐水冲洗。将左心室-20 ℃冷冻15 min取出,自心尖向心底部垂直心室长轴方向切2 mm厚切片5~6片,加入含1% TTC的PBS溶液中温育15 min,中性甲醛固定。用数码相机自心底向心尖方向照相,Image-Pro Plus 6.0图像分析软件计算白色梗死区的总面积,即IS。以IS占总面积的百分比计算心肌梗死面积百分比(IS/LVS),重复测量3次取平均值。
1.5 心肌组织CX43表达检测 采用免疫组化方法。在家兔心脏左冠状动脉前降支下穿线处下方,横向切取厚约0.2 cm的心肌切片,中性甲醛溶液固定,石蜡包埋、切片,常规脱蜡至水。将切片置于柠檬酸盐缓冲液中高压加热,冷却,PBS冲洗。3% H2O2去离子水孵育10 min,PBS冲洗。滴加封闭用山羊血清,室温孵育15 min。依次加入一抗(小鼠抗大鼠CX43单克隆抗体)、二抗(山羊抗小鼠抗体),PBS冲洗。滴加辣根标记链霉卵白素,室温孵育15 min。DAB显色,苏木素复染,脱水,透明,中性树胶封片,显微镜下观察。每张切片随机选取3个400×不重叠代表性视野拍照,利用Image-Pro Plus 6.0图像分析软件测定平均光密度OD值,作为CX43表达量的半定量分析。

2. 结果
2.1 各组血清cTnI、CK-MB水平比较 排除实验过程中死亡的家兔,假手术组、缺血再灌注组、羟考酮后处理组、κ受体拮抗剂+羟考酮后处理组各剩余11、10、11、10只。各组血清cTnI、CK-MB水平比较见表1。
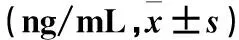
表1 各组血清cTnI、CK-MB水平比较
注:与假手术组比较,*P<0.05;与缺血再灌注组比较,△P<0.05;与羟考酮后处理组比较,#P<0.05。
2.2 各组IS/LVS比较 假手术组、缺血再灌注组、羟考酮后处理组、κ受体拮抗剂+羟考酮后处理组的IS/LVS分别为0、18.28%±2.89%、12.85%±1.77%、16.13%±2.60%。与假手术组比较,其他三组IS/LVS均升高(P均<0.05);羟考酮后处理组较缺血再灌注组、κ受体拮抗剂+羟考酮后处理组明显减少(P均<0.05),缺血再灌注组与κ受体拮抗剂+羟考酮后处理组比较无统计学差异(P>0.05)。
2.3 各组心肌组织CX43表达比较 假手术组可见CX43棕黄色阳性信号密集,表达分布规律,呈条索状和簇状;缺血再灌注组阳性信号呈弱的弥散或点状样改变,表达不清晰、无规则;羟考酮后处理组阳性信号分布相对均一,接近假手术组;κ受体拮抗剂+羟考酮后处理组阳性信号不清晰、分布零乱、无规律,与缺血再灌注组相似。假手术组、缺血再灌注组、羟考酮后处理组、κ受体拮抗剂+羟考酮后处理组CX43表达OD值分别为28.28±3.50、10.55±2.25、15.74±3.77、11.09±1.70。与假手术组比较,其他三组OD值均降低(P均<0.05);羟考酮后处理组较缺血再灌注组、κ受体拮抗剂+羟考酮后处理组升高(P均<0.05),缺血再灌注组与κ受体拮抗剂+羟考酮后处理组比较无统计学差异(P>0.05)。
3 讨论
心肌缺血再灌注损伤是指在短时间内心肌血供中断,一定时间内恢复血供后,原缺血心肌发生较缺血时更为严重的损伤[7,8]。临床表现为再灌注后血压下降,PCI术中发生无再流或慢血流现象[9],不能实现心肌细胞微循环的再灌注,胸痛症状反复发作,术后发生梗死后的心肌功能丧失、心室重塑、心功能不全、梗死后心衰及恶性心律失常,近期及远期死亡率增加,严重影响急性心肌梗死患者的预后。
缺血后处理是通过再灌注起始给予3次30 s缺血/30 s再灌注干预,来减轻再灌注损伤,减少心肌梗死面积。研究表明,再灌注期间给予他汀类药物、钾离子通道开放剂类药物、M胆碱受体阻滞剂药物、阿片肽类镇痛药等可对心肌缺血再灌注损伤起到保护作用,即药物后处理。药物后处理可避免缺血后处理操作上带来的机械性损伤,拥有更好的临床应用价值。目前许多新型阿片类受体激动剂如芬太尼、瑞芬太尼、舒芬太尼等广泛用于围手术期的心肌保护,阿片样物质可以模拟心肌缺血预处理和后处理的方式减轻缺血再灌注,减少心肌梗死面积,降低心律失常的发生率,具有明确的心肌保护作用。羟考酮是一种强效阿片类受体激动剂,与吗啡、瑞芬太尼、舒芬太尼等阿片类药物相比,羟考酮除有强效的μ受体激动作用外,还有较强的κ受体激动作用[10]。激动κ受体可通过PI3K通路开放线粒体膜ATP依赖的钾离子通道,抑制细胞内钙超载与氧自由基的释放,最终减少心肌细胞的坏死与凋亡,在阿片类药物的心肌保护机制中占用重要的地位[11]。此外,羟考酮对内脏痛和神经病理性疼痛的抑制作用更强[12],与吗啡等相比,羟考酮可能更好地抑制心肌梗死患者因疼痛所带来的应激反应,从而降低心肌氧耗。CK-MB、CTnI均为心肌细胞内的特异蛋白,当心肌坏死时释放入血,可反映心肌受损的程度。一般认为CTnI最具特异性,CK-MB在心肌再梗死时敏感性更佳。本研究显示,羟考酮后处理组可显著减少心肌梗死面积、降低血清CK-MB、CTnI释放,具有确切的减轻心肌缺血再灌注损伤的作用。而加入κ受体拮抗剂后,羟考酮的上述心肌保护作用则被消除。提示羟考酮的心肌保护作用与κ受体激活有关。
缝隙连接由相邻细胞膜上2个连接子构成,是细胞间电信号直接传递和胞质物质交换的结构基础,并参与缺血再灌注心肌的保护作用。CX43是心肌组织表达的主要缝隙连接蛋白,是决定冠状动脉阻塞后IS大小的因素之一。生理状态下,CX43主要呈簇状位于细胞膜闰盘处呈端端连接,少量位于侧侧连接或存在于线粒体内,CX43的分布和结构改变对缝隙连接的活性有重要影响。当心肌发生缺血再灌注损伤时,缝隙连接蛋白的表达、分布和功能都将发生变化[13]。本研究显示,羟考酮后处理可改善家兔缺血再灌注心肌CX43表达,使CX43分布相对均一,接近假手术组。提示羟考酮后处理可改善CX43表达与分布。而加入κ受体拮抗剂后,CX43分布不规律,与缺血再灌注组相似。提示羟考酮的作用可能与激活心肌细胞的κ受体有关。阿片受体激动剂激动κ受体可抑制CX43重构,稳定CX43的合成与降解,从而发挥抗缺血再灌注损伤的作用[14]。
综上所述,羟考酮后处理可减轻家兔心肌缺血再灌注损伤,其保护作用可能由κ受体介导,通过改善心肌组织CX43表达,减少心肌梗死面积。
[1] Ibanez B, Heusch G, Ovize M. Evolving therapies for myocardial ischemia/reperfusion injury[J]. J Am Coll Cardiol, 2015,65(14):1454-1471.
[2] Katsaya T, Judy RK, Matthias LR. Opioid-induced cardioprotection[J]. Curr Pharm Des, 2014,20(36):5697-5705.
[3] Wong GT, Li R, Jiang LL, et al. Remifentanil post-conditioning attenuates cardiac ischemia-reperfusion injury via kappa or delta opioid receptor activation[J]. Acta Anaesthesiol Scand, 2010,54(4):510-518.
[4] Gross ER, Hsu AK, Gross GJ. Acute methadone treatment reduces myocardial infarct size via the delta-opioid receptor in rats during reperfusion[J]. Anesth Analg, 2009,109(5):1395-1402.
[5] 靖庆国,范钧钊,任瑶瑶,等.羟考酮预处理对大鼠肠缺血再灌注诱发肝损伤的影响及不同阿片受体在其中的作用[J].中华麻醉学杂志,2015,35(10):1271-1273.
[6] Fujita M, Morimoto Y, Ishihara M, et al. A new rabbit model of myocardial infarction without endotracheal intubation[J]. J Surg Res, 2004,116(1):124-128.
[7] Yellon DMD. Myocardial reperfusion injury[J]. N Engl J Med, 2007,357(11):1121-1135.
[8] Frohlich GM, Meier P, White SK, et al. Myocardial reperfusion injury: looking beyond primary PCI[J]. Eur Heart J, 2013,34(23):1714-1722.
[9] Niccoli G, Burzotta F, Galiuto L, et al. Myocardial no-reflow in humans[J]. J Am Coll Cardiol, 2009,54(4):281-292.
[10] Kokki H, Kokki M, Sjövall S. Oxycodone for the treatment of postoperative pain[J]. Expert Opin Pharmacother, 2012,13(7):1045-1058.
[11] Xu YC, Li RP, Xue FS, et al. kappa-Opioid receptors are involved in enhanced cardioprotection by combined fentanyl and limb remote ischemic postconditioning[J]. J Anesth, 2015,29(4):535-543.
[12] Olesen AE, Staahl C, Arendt-Nielsen L, et al. Different effects of morphine and oxycodone in experimentally evoked hyperalgesia: a human translational study[J]. Br J Clin Pharmacol, 2010,70(2):189-200.
[13] He H, Li N, Zhao Z, et al. Ischemic postconditioning improves the expression of cellular membrane connexin 43 and attenuates the reperfusion injury in rat acute myocardial infarction[J]. Biomed Rep, 2015,3(5):668-674.
[14] Zhang QY, Wang W, Shi QX, et al. Antiarrhythmic effect mediated by κ-opioid receptor is associated with Cx43 stabilization[J]. Crit Care Med, 2010,38(12):2365-2376.
贾辛未(E-mail: jxw1967@126.com)
10.3969/j.issn.1002-266X.2017.06.010
R542.2
A
1002-266X(2017)06-0032-03
2016-10-11)
