缺血性二尖瓣反流患者冠状动脉介入治疗术前后的超声定量分析
2017-05-19白文娟刘丹唐红饶莉
白文娟 刘丹 唐红 饶莉
·临床研究·
缺血性二尖瓣反流患者冠状动脉介入治疗术前后的超声定量分析
白文娟 刘丹 唐红 饶莉
目的应用二维斑点追踪成像技术评价缺血性二尖瓣反流(IMR)患者冠状动脉介入治疗术前后左室心肌功能及二尖瓣反流容积的变化。方法选取亚急性心肌梗死患者41例,所有患者于冠状动脉介入治疗术前72 h内及术后6个月采集超声图像,并进行二尖瓣反流容积定量和心肌应变定量分析。根据二尖瓣反流容积变化情况将41例患者分为非恶化组(Ⅰ组)和恶化组(Ⅱ组),对比分析两组术前、术后超声检测情况。结果41例患者分别为Ⅰ组28例和Ⅱ组13例。Ⅰ组患者术后二尖瓣反流容积较术前明显减少,左室射血分数较术前升高(P<0.05);各节段及总体径向应变、纵向应变均较术前改善(均P<0.05)。Ⅱ组患者术后二尖瓣反流容积较术前增加(P<0.05),左室射血分数较术前升高不明显,差异无统计学意义;短轴基底段径向应变较术前恶化(P<0.05)。结论二维斑点追踪成像技术可以较敏感地评价左室心肌功能;冠状动脉介入治疗术通过改善左室收缩功能可以减少IMR的发生。
斑点追踪成像,二维;二尖瓣反流;缺血性;心肌应变
缺血性二尖瓣反流(ischemic mitral regurgitation,IMR)是指由冠状动脉疾病引起,二尖瓣瓣叶及瓣下结构功能异常而非器质性病变导致的功能性二尖瓣反流[1]。研究[2]表明IMR患者5年病死率较未合并者高,且IMR的严重程度与心力衰竭的发生率呈正相关。对于IMR的治疗有人工瓣环成形术、二尖瓣缘对缘钳夹术及药物治疗等,但由于IMR的发生发展机制尚未完全阐明,IMR的治疗指征和时间不明确,远期复发率较高[3]。近年来二维斑点追踪成像技术广泛应用于临床,通过高帧频的二维灰阶超声图像,能较准确地反映心肌运动力学信息。本研究应用二维斑点追踪成像技术评价IMR患者冠状动脉介入治疗术前后左室心肌功能及二尖瓣反流容积变化,初步研究IMR的发病机制,为临床制定治疗方案及预后评估提供依据。
资料与方法
一、研究对象
选取2012年9月至2013年3月我院心血管内科收治的亚急性心肌梗死患者41例,其中男31例,女10例,年龄40~84岁,平均(61.78±12.30)岁。纳入标准:窦性心律,且符合WHO冠状动脉粥样硬化性心脏病诊断标准(2010)的亚急性心肌梗死患者。排除标准:合并心瓣膜病、心肌病及先天心脏病等非缺血性因素引起心脏改变的患者;单纯右室心肌梗死、梗死后心绞痛的患者;频发早搏、房颤、束支传导阻滞等心律失常患者;高血压病未控制及合并其他重要内脏器官功能不全的患者;声窗不佳的患者。
二、仪器与方法
1.仪器:使用P hili p si E 33彩色多普勒超声诊断仪,X5-1三维矩阵探头,频率1~5M Hz。
2.方法:所有患者于冠状动脉介入治疗术前72 h内及术后6个月采集超声图像,取左侧卧位,连接同步胸导联心电图。首先采集胸骨旁左室长轴、左室基底段、中间段、心尖段短轴及心尖四腔、三腔、两腔切面连续4个心动周期的二维超声图像;然后采集心尖四腔、三腔及两腔切面彩色多普勒图像,调节彩色多普勒量程和基线,以最佳显示二尖瓣口反流血流的等流速面。以上图像均由高年资超声医师按照统一采图标准完成,并以D I CO M格式储存。将D I CO M数据导入P hili p s QLAB 9.0工作站,选取心律稳定且受呼吸影响小的心动周期进行测量。进入心肌运动定量模式,勾勒心内膜及心外膜边界,根据美国超声心动图学会标准划分左室17节段,应用二维斑点追踪成像技术定量分析左室节段运动。获得参数包括:左室各节段应变,左室短轴基底段、中间段及心尖段切面总体应变,以及心尖四腔、三腔、两腔切面总体应变。以上所有数值均连续测量3次并取平均值。于心尖四腔、三腔、两腔切面采用近端等速面积汇聚法测量二尖瓣反流容积,取平均3个切面获得二尖瓣反流容积平均值。
依据美国超声心动图学会指南(2003)对IMR程度进行分级[4],将二尖瓣反流容积变化15m l作为分组指标:非恶化组为术后反流量减少或增加<15 m l的患者(Ⅰ组);恶化组为术后反流量增加≥15ml的患者(Ⅱ组)。比较两组术前、术后各参数的变化。
患者入院后均接受抗血小板、降脂及改善心室重构等药物治疗。将冠状动脉大致分为左前降支、左回旋支及右冠状动脉,根据冠状动脉造影结果将狭窄>75%的血管定义为病变冠状动脉。收集患者临床资料,包括脑钠肽等实验室指标、冠状动脉造影结果及内科合并症情况。
三、统计学处理
应用S P SS 17.0统计软件,计量资料以±s表示,组间比较行配对t检查;计数资料比较行χ2检验。两变量间相关性研究采用P earson线性相关分析。P<0.05为差异有统计学意义。
结果
41例患者分为Ⅰ组28例和Ⅱ组13例。两组一般资料比较差异无统计学意义。
一、两组术前与术后左室17节段应变比较
Ⅰ组患者术后各节段及总体径向应变、纵向应变均较术前改善,其中心尖段径向应变和左室总体径向应变与术前比较差异均有统计学意义(P<0.05);Ⅱ组患者术后短轴中间段及心尖段径向应变较术前改善,但差异无统计学意义,短轴基底段径向应变较术前恶化,差异有统计学意义(P<0.05)。术后各节段纵向应变较术前稍改善,但差异无统计学意义。见表1,2。
表1 Ⅰ组患者术前与术后左室17节段应变、二尖瓣反流容积、左室容积及射血分数比较(±s)
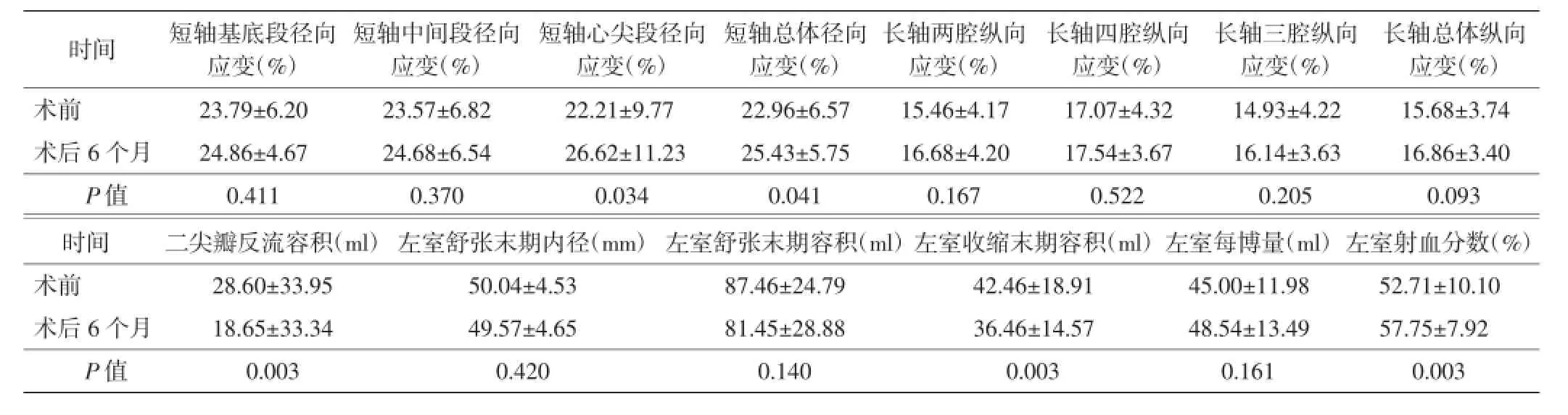
表1 Ⅰ组患者术前与术后左室17节段应变、二尖瓣反流容积、左室容积及射血分数比较(±s)
长轴总体纵向应变(%)术前23.79±6.20 23.57±6.82 22.21±9.77 22.96±6.57 15.46±4.17 17.07±4.32 14.93±4.22 15.68±3.74术后6个月24.86±4.67 24.68±6.54 26.62±11.23 25.43±5.75 16.68±4.20 17.54±3.67 16.14±3.63 16.86±3.40 P值0.411 0.370 0.034 0.041 0.167 0.522 0.205 0.093时间短轴基底段径向应变(%)短轴中间段径向应变(%)短轴心尖段径向应变(%)短轴总体径向应变(%)长轴两腔纵向应变(%)长轴四腔纵向应变(%)长轴三腔纵向应变(%)时间二尖瓣反流容积(m l)左室舒张末期内径(mm)左室舒张末期容积(ml)左室收缩末期容积(m l)左室每博量(m l)左室射血分数(%)术前28.60±33.95 50.04±4.53 87.46±24.79 42.46±18.91 45.00±11.98 52.71±10.10术后6个月18.65±33.34 49.57±4.65 81.45±28.88 36.46±14.57 48.54±13.49 57.75±7.92 P值0.003 0.420 0.140 0.003 0.161 0.003
二、两组术前与术后二尖瓣反流容积及左室收缩功能比较
Ⅰ组患者术后二尖瓣反流容积较术前明显减少,左室收缩末期容积降低,左室射血分数较术前提高,差异均有统计学意义(均P<0.05),左室舒张末期内径和舒张末期容积有减小趋势,差异均无统计学意义。Ⅱ组患者术后二尖瓣反流容积较术前增加,差异有统计学意义(P<0.05),左室射血分数较术前升高不明显,左室舒张末期内径有增大趋势,但差异均无统计学意义。见表1,2和图1,2。
表2 Ⅱ组患者术前与术后左室17节段应变、二尖瓣反流容积、左室容积及射血分数比较(±s)
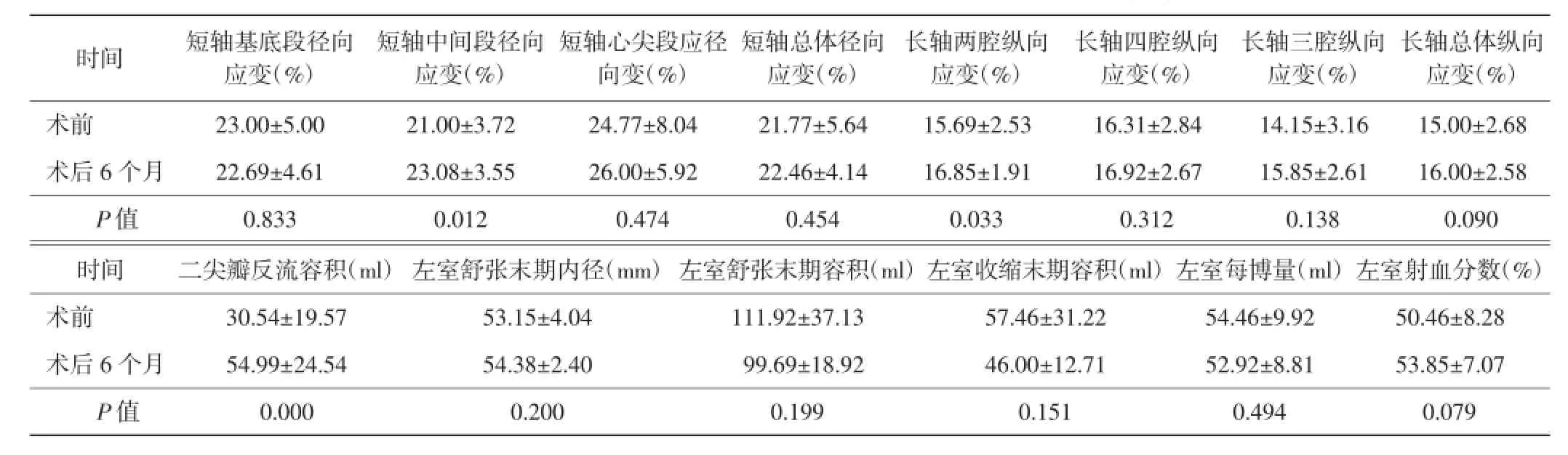
表2 Ⅱ组患者术前与术后左室17节段应变、二尖瓣反流容积、左室容积及射血分数比较(±s)
长轴总体纵向应变(%)术前23.00±5.0021.00±3.7224.77±8.0421.77±5.6415.69±2.5316.31±2.8414.15±3.1615.00±2.68术后6个月22.69±4.6123.08±3.5526.00±5.9222.46±4.1416.85±1.9116.92±2.6715.85±2.6116.00±2.58 P值0.8330.0120.4740.4540.0330.3120.1380.090时间短轴基底段径向应变(%)短轴中间段径向应变(%)短轴心尖段应径向变(%)短轴总体径向应变(%)长轴两腔纵向应变(%)长轴四腔纵向应变(%)长轴三腔纵向应变(%)时间二尖瓣反流容积(ml)左室舒张末期内径(mm)左室舒张末期容积(ml)左室收缩末期容积(ml)左室每博量(ml)左室射血分数(%)术前30.54±19.5753.15±4.04111.92±37.1357.46±31.2254.46±9.9250.46±8.28术后6个月54.99±24.5454.38±2.4099.69±18.9246.00±12.7152.92±8.8153.85±7.07 P值0.0000.2000.1990.1510.4940.079
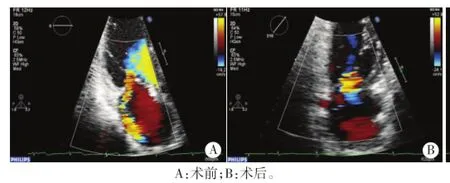
图1 Ⅰ组患者冠状动脉介入治疗术前后二尖瓣反流的超声图像
三、相关性分析
将术前及术后二尖瓣反流容积与左室各节段应变及左室射血分数行直线相关性分析,结果显示各变量与二尖瓣反流容积均无相关,差异均无统计学意义。
讨论
近年来广泛应用于临床的二维斑点追踪成像技术可以基于高帧频的二维灰阶超声图像,实时跟踪心肌内回声斑点的空间运动,能定性、定量地显示心肌运动速度、应变、应变率及位移等,无角度依赖且排除周围组织对心肌运动的影响,从而较准确地反映局部心肌的运动力学信息[5-6]。本研究应用二维斑点追踪成像技术评估亚急性心肌梗死患者左室17节段应变及二尖瓣反流容积,并在患者血运重建后6个月进行随访,通过对比分析得出,Ⅰ组患者术后左室整体应变及射血分数均较术前显著改善(均P<0.05),而左室大小与术前比较有减小趋势,提示这部分患者冠状动脉血运重建后,可改善梗死区存活心肌的功能,使左室收缩功能及运动同步性提高,降低二尖瓣反流量。而IMR的减轻又进一步降低了左心室前负荷,增加左心室做功效能,从而改善左室重构。Ⅱ组患者术后短轴基底段径向应变较术前恶化(P<0.05),其余节段应变及左室射血分数较术前改善不明显,且左室大小与术前相比有增大趋势,提示该部分患者冠状动脉血运重建后,心肌再灌注可挽救的存活心肌少,心脏梗死范围大,也表明对缺血性心肌病患者而言,左室收缩功能下降及左室心肌重构是导致IMR发展的重要原因。
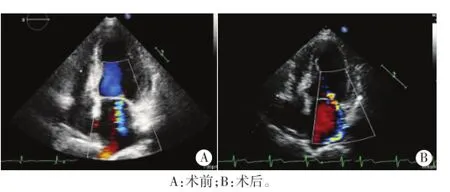
图2 Ⅱ组患者冠状动脉介入治疗术前后二尖瓣反流的超声图像
有研究[2]报道,心肌梗死后IMR的发生率为20%~25%,其中有50%的患者合并心力衰竭。研究[2,7]认为IMR是心肌梗死后患者死亡率的预测指标。早期研究认为IMR是由牵拉二尖瓣的乳头肌缺血重构所致,后期研究认为IMR是由解剖及功能上的多种异常综合引起[8-10]。一方面,局部心室重构和单组乳头肌的移位,可导致瓣叶闭合点向单侧移位,引起偏心性IMR;而左室整体重构时,两组乳头肌及瓣叶移位程度相同,瓣叶闭合点向心尖移位,往往导致中心性IMR;另一方面,瓣叶关闭的多种力量失衡是影响IMR的重要因素;再者,左室心肌功能下降及左室运动失同步性可能通过瓣叶关闭力下降及乳头肌收缩欠协调等机制导致IMR的发生。
左室容积和左室心肌质量可以反映左室重构。Stanle y等[11]认为IMR的治疗应该包括冠状动脉的再灌注、二尖瓣装置的修复及左室形态和容积的恢复,而冠状动脉的再灌注在改善患者左室收缩功能中起着重要的作用。本研究发现,冠状动脉介入治疗术后IMR减轻患者的左室容积指标减小,提示部分患者治疗后可以有效缓解左室重构过程,通过恢复部分左室及二尖瓣装置的空间结构,减少IMR;而IMR的减少又减轻了左室前负荷,增加左室做功效能,从而改善左室重构。
本研究存在一定的局限性:①随访时间短,患者远期预后及IMR的变化情况需要进一步观察;②病例数较少,未能将患者按照心肌梗死部位进行分组,尚不能阐述罪犯血管与IMR之间的联系,且未能得到IMR反流量与各应变指标的相关关系。因此未来我们将在此基础上扩大样本量,进行一系列的随访研究。
综上所述,二维斑点追踪成像技术可以较敏感地评估左室各节段心肌的运动功能;IMR的发生与左室重构及左室收缩力下降有密切关系,有效的血运重建及心室重构改善可以减少IMR的发生。
[1]Tahta SA,Oury JH,Maxwell JM,et al.Outcome after mitral valve repair for functional ischemic mitral regurgitation[J].JHeart Valve Dis,2002,11(1):11-19.
[2]Aronson D,Goldsher N,Zukermann R,et al.Ischemic mitral regurgitation and risk of heart failure aftermyocardial infarction[J]. Arch Intern Med,2006,166(11):2362-2368.
[3]Mishra YK,Mittal S,Jaguri P,et al.Coapsys mitral annuloplasty for chronic functional ischemic mitral regurgitation:1-year results[J]. Ann Thorac Surg,2006,81(1):42-46.
[4]Zoghbi WA,Enriquez-Sarano M,Foster E,et al.Recommendations for evaluation of the severity of native valvular regurgitation with two-dimensional and Doppler echocardiography[J].J Am Soc Echocardiogr,2003,16(7):777-802.
[5]Shudo Y,Nakatani S,Sakaguchi T,et al.Left ventricular mechanics following restrictive mitral annuloplasty for functional mitral regurgitation:two-dimensional speckle tracking echocardiographic study[J].Echocardiography,2012,29(4):445-450.
[6]Kamperidis V,Marsan NA,Delgado V,et al.Left ventricular systolic function assessment in secondarymitral regurgitation:left ventricular ejection fraction vs.speckle tracking global longitudinal strain[J].Eur Heart J,2016,37(10):811-816.
[7]Crabtree TD,BaileyMS,Moon MR,etal.Recurrentmitral regurgitation and risk factors forearly and latemortality aftermitralvalve repair for functional ischemic mitral regurgitation[J].Ann Thorac Surg,2008,85(5):1537-1543.
[8]Sadeghpour A,Abtahi F,Kiavar M.Echocardiographic evaluation of mitral geometry in functionalmitral regurgitation[J].JCardiothorac Surg,2008,3(10):54-61.
[9]Bigi R,Cortigiani L,Bovenzi F.Assessing functional mitral regurgitation with exercise echocardiography:rationale and clinical applications[J].Cardiovasc Ultrasound,2009,7(12):57-64.
[10]Szymanski P,Klisiewicz A,Hoffman P.Asynchronous movement of mitral annulus:an additional mechanism of ischaemic mitral regurgitation[J].Clin Cardiol,2007,30(10):512-516.
[11]Stanley AW,Athanasuleas CL,Buckberg GD,et al.Left ventricular remodeling and functional mitral regurgitation:mechanisms and therapy[J].Semin Thorac Cardiovasc Surg,2001,13(4):486-495.
Echocardiograph ic com parison of i schem icm itralregurgitation beforeand after percutaneous coronary intervention
BAIWenjuan,LIUDan,TANGHong,RAOLi Departmentof Echocardiography,WestChina Hospital,Sichuan University,Chengdu 610041,China
ObjectiveTo assess the variation of left ventricular function and ischem ic m itral regurgitation(IMR)volume before and after percutaneous coronary intervention(PCI)by echocardiography.M ethods Forty-one subacute myocardial infarction patients who were prepared to undergo PCIwere enrolled.The left ventricular function and IMR were evaluated 72 h before PCT and 6 months after PCI by echocardiography.Then the patients were divided into two groups by the variation ofmitral regurgitation volume(groupⅠ:IMR volume diminish or increase less than 15 ml;groupⅡ:IMR volume increasemore than or equal to 15ml).Results In 41 patients,there were 28 cases of groupⅠ,and 13 cases of groupⅡ. In groupⅠ,the IMR volume decreased and the left ventricular ejection fraction(LVEF)increased after PCI(P<0.05),and the regional and global radial strain,longitudinal strain were better than preoperative status(all P<0.05).In groupⅡ,the IMR volume increased PCI(P<0.05),the LVEF had no significant improvement,the postoperative basal regional radial strain was worse compared to preoperative status(P<0.05).Conclusion Echocardiography can evaluate left ventricular muscle function sensitively.PCI can help reduce IMR by improving leftventricular systolic function.
Speckle tracking imaging,two-dimeonsional;Mitral regurgitation;Ischem ic;Myocardialstrain
R542.5;R540.45
A
2016-02-08)
四川省科技计划项目(2014SZ0004-8)
610041成都市,四川大学华西医院心内科(白文娟、唐红、饶莉);四川大学华西临床医学院内科学(刘丹)
饶莉,E mail:lrl z1989@163.com
