基于化学成分含量变化的金银花药材保质期预测Δ
2017-05-16葛朝晖张海娟临沂大学药学院山东临沂276000
葛朝晖,张海娟(临沂大学药学院,山东临沂 276000)
基于化学成分含量变化的金银花药材保质期预测Δ
葛朝晖*,张海娟#(临沂大学药学院,山东临沂 276000)
目的:建立测定金银花药材中绿原酸和木犀草苷含量的方法,以探讨金银花在常温密封环境下的保质期。方法:采用高效液相色谱法。色谱柱为Agilent Zorbax SB-C18(绿原酸)、Agilent Zorbax SB-Phenyl(木犀草苷),流动相为乙腈-0.4%磷酸溶液(13∶87,V/V,绿原酸)、乙腈-0.5%冰醋酸溶液(梯度洗脱,木犀草苷),流速为1.0 mL/min,检测波长为327 nm(绿原酸)、350 nm(木犀草苷),柱温为30,进样量为10 μL。结果:绿原酸、木犀草苷检测质量浓度线性范围分别为10~100 μg/mL(r=0.998 6)、5~ 50 μg/mL(r=0.999 3);精密度、稳定性、重复性试验的RSD<4.0%;加样回收率分别为95.78%~99.70%(RSD=1.46%,n=6)、96.30%~104.31%(RSD=2.93%,n=6)。滚简杀青、烤房烘干、自然晾晒的药材样品中绿原酸和木犀草苷的含量在贮藏12个月后普遍降低了30%~40%。结论:该方法操作简便,精密度、稳定性、重复性好,可用于金银花药材中绿原酸和木犀草苷含量的测定;金银花在贮藏1年后有效成分的含量显著下降,有必要建立金银花保质期规范,以保证临床用药的有效性。
金银花;绿原酸;木犀草苷;保质期
金银花为忍冬科Caprifoliaceae植物忍冬Lonicera japonica Thunb的干燥花蕾或带初开的花,其具有清热解毒、疏散风热之功效,可用于痈肿疗疮、喉痹、丹毒、热毒血痢、风热感冒、温病发热等症的治疗[1]。近年来,由于其市场需求增大,质量难以保持稳定[2]。经化学和药理研究证实,绿原酸和木犀草苷是主要活性成分,其含量高低是评价金银花药材质量优劣的重要标志[3-6]。2015年版《中国药典》(一部)规定:金银花含绿原酸不得少于1.5%,木犀草苷不得少于0.050%。目前,对金银花药理作用的研究比较广泛和深入,但其稳定性的研究较少,在贮藏过程中多凭借经验进行,没有可靠的质控方法。
为考察金银花的有效期,笔者通过留样观察,以绿原酸和木犀草苷为指标,采用高效液相色谱法(HPLC)测定其含量,为评价金银花药材质量提供试验依据。
1 材料
1.1 仪器
SURVEYOR型HPLC仪,包括DAD检测器(美国Thermo Finnigan公司);KQ2200B型超声波清洗器(昆山市超声仪器有限公司,功率:250 W,频率:35 kHz);TG16-WS型高速台式离心机(长沙湘仪离心机仪器有限公司);FA2004N型电子分析天平(上海精密科学仪器有限公司)。
1.2 试剂
绿原酸对照品(中国食品药品检定研究院,批号:110753-201314,纯度:≥98%);木犀草苷对照品(天津一方科技有限公司,批号:20121227,纯度:≥98%);乙腈为色谱纯,磷酸为分析纯,乙酸、无水乙醇为优级纯,水为重蒸水。
1.3 药材
金银花药材源自全国不同省市,采用不同加工方式,由山东九间棚药业有限公司提供,经山东医学高等专科学校冯丽娟教授鉴定为真品。样品收集之后研磨过4号筛,密封贮藏。取药材样品18份,每份约50 g,以密封袋封口室温贮藏。分别于贮藏1个月(Y1)和12个月(Y2)时测定药材样品相关指标。

表1 金银花药材信息Tab 1 Information of L.japonicae
2 方法与结果
2.1 绿原酸的含量测定
2.1.1 色谱条件与系统适用性试验 色谱柱:Agilent Zorbax SB-C18(250 mm×4.6 mm,5 μm);流动相:乙腈-0.4%磷酸溶液(13∶87,V/V);流速:1.0 mL/min;检测波长:327 nm,柱温:30 ,进样量:10 μL。在上述色谱条件下,理论板数以绿原酸峰计不少于1 000;各成分基线分离良好,分离度>1.5,详见图1。
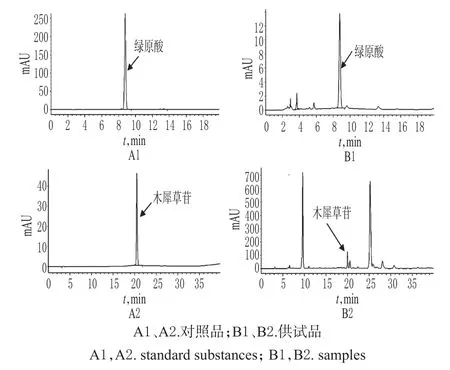
图1 高效液相色谱图Fig 1 HPLC Chromatograms
2.1.2 对照品溶液的制备 取绿原酸对照品适量,精密称定,置于棕色量瓶中,加50%甲醇溶液制成质量浓度为1 mg/mL的对照品溶液。
2.1.3 供试品溶液的制备 取药材样品粉末约0.5 g,精密称定,置于具塞锥形瓶中,精密加50%甲醇溶液50 mL,称定质量,超声处理30 min,放冷,再次称定质量,用50%甲醇溶液补足减失的质量,摇匀,滤过,精密量取续滤液5 mL,置于25 mL棕色量瓶中,加50%甲醇溶液定容,摇匀,即得。
2.1.4 线性关系考察 分别精密量取“2.1.2”项下对照品溶液0.2、0.4、0.6、0.8、1.0、1.2、1.4 mL,分别置于10 mL量瓶中,加50%甲醇溶液定容,制成系列对照品溶液。精密量取上述系列对照品溶液各10 μL,按“2.1.1”项下色谱条件进样测定,记录峰面积。以绿原酸质量浓度(x,g/L)为横坐标、峰面积(y)为纵坐标进行线性回归,得绿原酸回归方程为y=28 061x-46 304(r=0.998 6)。结果表明,绿原酸检测质量浓度线性范围为10~100 μg/mL。
2.1.5 精密度试验 取“2.1.2”项下对照品溶液适量,按“2.1.1”项下色谱条件连续进样测定6次,记录峰面积。结果,绿原酸峰面积的RSD=0.15%(n=6),表明仪器精密度良好。
2.1.6 稳定性试验 取“2.1.3”项下供试品溶液(编号:S1)适量,分别于室温下放置0、2、4、8、12、24 h时按“2.1.1”项下色谱条件进样测定,记录峰面积。结果,绿原酸峰面积的RSD=0.81%(n=5),表明供试品溶液在室温放置24 h内基本稳定。
2.1.7 重复性试验 精密称取同一批样品(编号:S1)适量,按“2.1.3”项下方法制备供试品溶液,共6份,再按“2.1.1”项下色谱条件进样测定并计算平均含量。结果,绿原酸平均含量为2.19%,RSD=0.25%(n=6),表明本方法重复性良好。
2.1.8 加样回收率试验 取已知含量样品(编号:S1)适量,共6份,分别加入一定质量的绿原酸对照品,按“2.1.3”项下方法制备供试品溶液,再按“2.1.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表2。
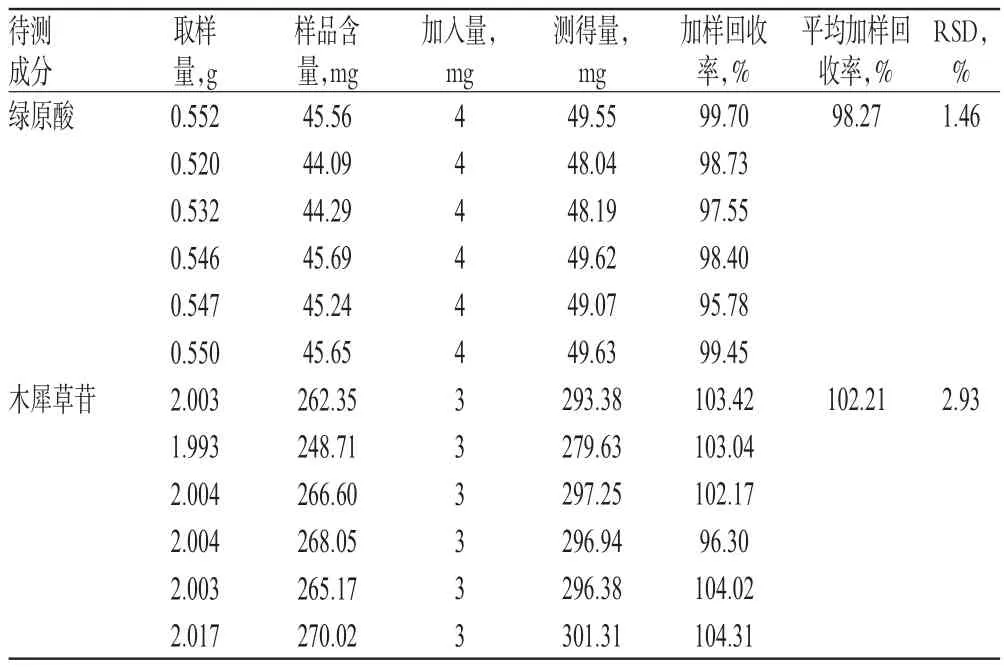
表2 加样回收率试验结果(n=6)Tab 2 Results of recovery test(n=6)
2.1.9 样品中绿原酸含量测定 取18批药材样品各适量,分别按“2.1.3”项下方法制备供试品溶液,再按“2.1.1”项下色谱条件进样测定,记录峰面积并计算样品中绿原酸含量,结果见表3。

表3 样品含量测定结果(n=3,%)Tab 3 Results of contents determination of samples (n=3,%)
2.2 木犀草苷的含量测定
2.2.1 色谱条件与系统适用性试验 色谱柱:Agilent Zorbax SB-Phenyl(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.5%冰醋酸溶液(B),梯度洗脱(0~15 min,10%→20%A;15~30 min,20%A;30~40 min,20%→30%A);流速:1.0 mL/min;检测波长:350 nm;柱温:30 ;进样量:10 μL。在上述色谱条件下,理论板数以木犀草苷峰计不少于20 000;各成分基线分离良好,分离度>1.5,详见图1。
2.2.2 对照品溶液的制备 取木犀草苷对照品适量,精密称定,加70%乙醇溶液制成质量浓度为1 mg/mL的对照品溶液。
2.2.3 供试品溶液的制备 取药材样品粉末约2 g,精密称定,置于具塞锥形瓶中,精密加70%乙醇溶液50 mL,称定质量,超声处理60 min,放冷,再次称定质量,加70%乙醇溶液补足减失的质量,摇匀,滤过,精密量取续滤液10 mL,回收溶剂至干,残渣用70%乙醇溶液溶解,移至5 mL量瓶中,加70%乙醇溶液定容,摇匀,即得。
2.2.4 线性关系考察 分别精密量取“2.2.2”项下对照品溶液0.6、0.8、1.0、1.2、1.4 mL,分别置于10 mL量瓶中,加70%乙醇溶液定容,制成系列对照品溶液。精密量取上述系列对照品溶液各10 μL,按“2.2.1”项下色谱条件进样测定,记录峰面积。以木犀草苷质量浓度(x,g/L)为横坐标、峰面积(y)为纵坐标进行线性回归,得木犀草苷回归方程为y=29 771x-13 725(r=0.999 3)。结果表明,木犀草苷检测质量浓度线性范围为5~50 μg/mL。
2.2.5 精密度试验 取“2.2.2”项下对照品溶液适量,按“2.2.1”项下色谱条件连续进样测定6次,记录峰面积。结果,木犀草苷峰面积的RSD=3.36%(n=6),表明仪器精密度良好。
2.2.6 稳定性试验 取“2.2.3”项下供试品溶液(编号:S1)适量,分别于室温下放置0、2、4、8、12、24 h时按“2.2.1”项下色谱条件进样测定,记录峰面积。结果,木犀草苷峰面积的RSD=1.37%(n=6),表明供试品溶液在室温放置24 h内基本稳定。
2.2.7 重复性试验 精密称取同一批样品(编号:S1)适量,按“2.2.3”项下方法制备供试品溶液,共6份,再按“2.2.1”项下色谱条件进样测定并计算平均含量。结果,木犀草苷平均含量为0.05%,RSD=2.36%(n=6),表明本方法重复性良好。
2.2.8 加样回收率试验 取已知含量样品(编号:S1)适量,共6份,分别加入一定质量的木犀草苷对照品,按“2.2.3”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表2。
2.2.9 样品中木犀草苷含量测定 取18批药材样品各适量,分别按“2.2.3”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样测定,记录峰面积并计算样品中木犀草苷含量,结果见表3。
3 讨论
笔者采用HPLC法测定金银花不同炮制品中绿原酸和木犀草苷的含量,结果显示其含量顺序为滚筒杀青>烤房烘干>自然晾晒。这表明,金银花采用烘干和晒干炮制方法的有效成分含量较低,采用滚筒杀青方法的有效成分含量最高。这可能是由于滚筒杀青能使金银花瞬间高速受热,多酚氧化酶迅速失活,再快速烘干,使水分迅速失散,避免了有效成分的损失[7-8]。在传统的自然晾晒或烤房烘干的炮制方法中,需时较长且更易受外界环境影响,故有效成分含量显著降低。
本试验中,3种炮制方法的药材样品中绿原酸和木犀草苷的含量在贮藏12个月后普遍降低了30%~40%。药材样品粉粹后比表面积增大会使成分降解速率增加,因此药材的贮藏期应该大于本试验数据结果,但本试验结果可作为参考[9]。
研究表明,金银花药材中有效成分的含量受物种、生态环境、栽培措施、物候期、采收、加工、贮藏时间及炮制方法等多种因素影响[8],本试验只对贮藏时间和炮制方法对药材的影响进行了探讨。为了确定中药材的保质期,应该在综合考虑影响中药材的产地、采收加工、晾晒贮藏、炮制过程及包装等前提下,通过试验得到各种数据,经过统计分析,得到各种影响因素与中药材质量变化的相关性,为中药材保质期的确定提出科学依据;且因为中药材的有效成分复杂,不能单一用某种成分来衡量其有效期,应寻找更全面适合中药有效期的确定方法,结合药效评价和临床应用实际,制订出科学合理的中药材保质期。
[1] 国家药典委员会.中华人民共和国药典:一部[S].2015年版.北京:中国医药科技出版社,2015:221.
[2] 李红霞,王雪芹,李振国,等.不同产地金银花与山银花主要成分的含量比较[J].中国药房,2011,22(31):2395-2397.
[3] 朱丹,李琼,张春花,等.不同产地金银花中绿原酸、木犀草苷和总黄酮含量的比较研究[J].广西医科大学学报,2016,33(1):15-19.
[4] 牛晓雪,崔旭盛,苏贺,等.高效液相色谱法同时测定忍冬中7种成分[J].色谱,2012,30(2):211-214.
[5] 欧水平,张文志,陈灵.金银花与山银花抗病毒酚酸类和黄酮类成分的差异性研究[J].中国药房,2015,26(33):4750-4752.
[6] 彭素琴,刘郁林.不同品种金银花不同花期绿原酸含量比较[J].安徽农业科学,2010,38(14):7296-7298.
[7] 宋健,张会敏,石俊英.金银花最佳产地加工方法:杀青烘干干燥法[J].中药材,2008,31(4):489-491.
[8] 胡璇,李卫东,李欧,等.滚筒杀青烘干加工方法对四倍体金银花药材质量的影响[J].中国中药杂志,2012,37 (17):2554-2557.
[9] 薛志平,王金梅,刘杰,等.初均速法预测金银花的有效期[J].中国中药杂志,2012,37(21):3179-3181.
Forecast on Shelf Life of Lonicerae japonicae Based on Its Chemical Components Variation
GE Zhaohui,ZHANG Haijuan(School of Pharmacy,Linyi University,Shandong Linyi 276000,China)
OBJECTIVE:To establish a method for determining the contents of chlorogenic acid and luteoloside in Lonicerae japonicae,and to explore the shelf life of L.japonicae under ordinary temperature and sealed environment.METHODS:HPLC method was adopted.The determination was performed on Agilent Zorbax SB-C18(chlorogenic acid)column and Agilent Zorbax SB-Phenyl(galuteolin)with mobile phase consisted of acetonitrile-0.4%phosphoric acid(13∶87,V/V),acetonitrile-0.5%glacial acetic acid(gradient elution,galuteolin)at the flow rate of 1.0 mL/min.The detection wavelength was set at 327 nm(chlorogenic acid)and 350 nm(galuteolin).The column temperature was 30 ,and sample size was 10 μL.RESULTS:The linear range of chlorogenic acid and galuteolin were 10-100 μg/mL(r=0.998 6),5-50 μg/mL(r=0.999 3),respectively.RSDs of precision,stability and reproducibility tests were all lower than 4.0%.Recoveries were 95.78%-99.70%(RSD=1.46%,n=6)、96.30%-104.31% (RSD=2.93%,n=6).The contents of chlorogenic acid and galuteolin in roller method,baking method and natural drying method of processed L.japonicae were all decreased by 30%-40%after stored for 12 months.CONCLUSIONS:The method is simple,precise,stable and repeatable,and can be used for simultanoue determination of chlorogenic acid and luteoloside in L.japonicae. The contents of active components in L.japonicae decrease significantly after stored for 12 months.It is necessary to establish shelf life standard of L.japonicae,so as to guarantee the effectiveness of drug use in the clinic.
Lonicerae japonicae;Chlorogenic acid;Luteoloside;Shelf life
R917;R927.2
A
1001-0408(2017)12-1677-04
2016-05-09
2016-07-02)
(编辑:张 静)
国家自然科学基金资助项目(No.41201526);山东省教育厅高校科研发展计划项目(No.J12LM59)
*博士研究生。研究方向:中药质量控制。E-mail:gezhaohui@lyu.edu.cn
#通信作者:副教授。研究方向:天然活性物质。电话:0539-8766716。E-mail:hjzhang2004@126.com
DOI10.6039/j.issn.1001-0408.2017.12.26
