盐酸兰地洛尔原料药中3-[4-(3-硝基苯磺酰氧基)苯基]丙酸的检测方法学研究
2017-05-10王珊珊王丽娟李卓瓦宁凡盛王晓利陈跃陈相峰
王珊珊,王丽娟,李卓瓦,宁凡盛,王晓利,陈跃,陈相峰*
(1.山东省分析测试中心,山东 济南250014;2.枣庄学院,山东 枣庄277000)
盐酸兰地洛尔原料药中3-[4-(3-硝基苯磺酰氧基)苯基]丙酸的检测方法学研究
王珊珊1,王丽娟1,李卓瓦2,宁凡盛1,王晓利1,陈跃1,陈相峰1*
(1.山东省分析测试中心,山东 济南250014;2.枣庄学院,山东 枣庄277000)
为了检测并控制合成盐酸兰地洛尔原料药物的质量,依托高效液相色谱-三重串联四级杆质谱建立了一种测定其中痕量基因毒性杂质3-[4-(3-硝基苯磺酰氧基)苯基]丙酸的方法。方法采用多级反应监测模式,检测灵敏度可达到0.50 mg/kg,加标回收率在91.9% ~ 97.8%之间,且精密度的相对标准偏差为3.28%(n=6),均能满足杂质检测的需要。该研究方法操作简单、结果可靠,可实现快速、低成本检测。
盐酸兰地洛尔;液相色谱-三重串联四级杆质谱;3-[4-(3-硝基苯磺酰氧基)苯基]丙酸;痕量检测
Study on detecting method of 3-[4-(3-nitrobenzene sulfonyl oxygen radicals)
盐酸兰地洛尔是在艾司洛尔的基础上进行结构改进而获得的化合物[1-3],是一种选择性的β1-肾上腺素能受体阻断剂,主要拮抗存在于心脏的β1受体,通过抑制儿茶酚胺引起的心搏增加而改善心动过速性心律失常,具有超短效、高选择性的优点。临床应用于手术时和手术后心动过速性心律失常的紧急治疗[4-6],具有起效快,半衰期短,不良反应较其他同类产品少,疗效可靠的特点[7]。此外,兰地洛尔在改善心肌缺血以及血液动力学方面表现出显著优势[8-12]。目前,该药在国内还处于研究阶段,主要针对国外过期专利进行工艺改造,匹配相应的药物分析手段,以达到降低用药成本的目的。
3-[4-(3-硝基苯磺酰氧基)苯基]丙酸(图1)是合成盐酸兰地洛尔的必备原料,如果采用常规的液相色谱方法检测,不仅检测灵敏度达不到要求,其中的主成分盐酸兰地洛尔还对检测有比较大的干扰。因此,为了检测并控制合成盐酸兰地洛尔原料药物中3-[4-(3-硝基苯磺酰氧基)苯基]丙酸的含量,保证该原料药的质量,本研究依托液相色谱-三重串联四级杆质谱建立了一种可对其进行定量检测的方法[13-14]。该研究的样品前处理方法简便,检测快速、准确且灵敏度高,可实现对盐酸兰地洛尔原料药物中痕量3-[4-(3-硝基苯磺酰氧基)苯基]丙酸的检测。

图1 3-[4-(3-硝基苯磺酰氧基)苯基]丙酸的分子式Fig.1 The molecular structure of 3-[4-(3-nitrobenzene sulfonyl oxygen radicals) phenyl] propionic acid
1 仪器与试剂
1.1 仪器
Agilent-1200型快速分离高效液相色谱仪,6410型三重串联四级杆质谱仪(QQQ)(美国安捷伦科技有限公司);Vortex-5型涡旋振荡器(海门市其林贝尔仪器制造有限公司);Heraeus Multifuge X1R型高速冷冻离心机(美国赛默飞世尔科技公司);AL104型天平(梅特勒-托利多仪器上海有限公司); 0.5~10 μL移液器(德国艾本德公司);20~200 μL移液器(德国艾本德公司);100~1 000 μL移液器(德国艾本德公司)。
1.2 试剂
色谱级甲酸(美国ROE科技公司);色谱级甲醇(瑞典OceanPak公司);色谱级乙腈(瑞典OceanPak公司);娃哈哈饮用纯净水(杭州娃哈哈集团有限公司);3-[4-(3-硝基苯磺酰氧基)苯基]丙酸(批号20140917,辰欣药业股份有限公司)。
2 实验方法
2.1 液相色谱-质谱的检测条件优化
2.1.1 液相色谱检测条件
本研究首先对3-[4-(3-硝基苯磺酰氧基)苯基]丙酸的液相检测条件进行优化,包括色谱柱型号、流动相选择(甲醇、乙腈)、梯度洗脱条件等,以保证其在色谱柱上有较好的保留时间及良好的峰型,最终优化后的条件为:XDB-C18色谱柱(4.6×50 mm,1.8 μm);进样量:5 μL;柱温:30 ℃ ;流速:0.4 mL/min;流动相A:含0.1%(体积分数)甲酸的水溶液;流动相B:乙腈溶液;柱后平衡3 min。流动相梯度条件见表1。

表1 流动相梯度洗脱条件
2.1.2 质谱检测条件
利用浓度为500 ng/mL 的3-[4-(3-硝基苯磺酰氧基)苯基]丙酸的标准品,对其质谱检测的母离子质荷比、子离子质荷比、碎裂电压(Fragmentor)、碰撞能量(CE)等条件及参数进行优化,优化后的检测条件为:电喷雾离子源(ESI源),负离子模式检测,毛细管电压4 000 V,四极杆温度100 ℃,雾化压力241 kPa,干燥气温度330 ℃,干燥气流量12 L/min。具体MRM参数设置为:母离子质荷比350;定量离子质荷比为185.5,碎裂电压100 V,碰撞能量15 eV;定性离子质荷比为121.4,碎裂电压100 V,碰撞能量25 eV。
2.2 样品前处理方法
准确称取盐酸兰地洛尔原料约40.0 mg,置10 mL容量瓶中,加入色谱甲醇10 mL,摇匀后超声10 min,冷却至室温,加入色谱甲醇定容至刻度,作为盐酸兰地洛尔供试品溶液,浓度为4.00 mg/mL,取5.0 μL进入液相色谱-质谱检测。
2.3 专属性实验
精密称定盐酸兰地洛尔样品40.0 mg,置于10 mL容量瓶中,加色谱甲醇定容至刻度,摇匀后超声10 min,冷却至室温,加色谱甲醇定容至刻度,作为盐酸兰地洛尔空白样品溶液(4.0 mg/mL)。
准确量取2.0 mL 10.0 mg/mL的3-[4-(3-硝基苯磺酰氧基)苯基]丙酸标准储备液,置于100 mL量瓶中加甲醇稀释至刻度,摇匀,作为标准溶液。
准确称取盐酸兰地洛尔样品40.0 mg,置于10 mL量瓶中,准确加入浓度为4.0 mg/mL的3-[4-(3-硝基苯磺酰氧基)苯基]丙酸标准溶液1.0 mL,加甲醇至刻度。摇匀后超声10 min,作为盐酸兰地洛尔空白样品加标溶液。
取上述溶液各5.0 μL进入液相色谱质谱检测,记录总离子流图。
2.4 系统适用性实验
准确配制浓度为100 ng/mL的3-[4-(3-硝基苯磺酰氧基)苯基]丙酸标准溶液,重复进样6次,每次5.0 μL,记录目标化合物质谱检测峰面积,考察检测方法的精密度。
2.5 标准曲线的测定
3-[4-(3-硝基苯磺酰氧基)苯基]丙酸标准储备液的配制:准确称取3-[4-(3-硝基苯磺酰氧基)苯基]丙酸标准品0.010 0 g,利用校准后的移液器准确加入1 000 μL的色谱级甲醇溶液溶解,配成浓度为10.0 mg/mL的标准溶液。将1 000 μL的10.0 mg/mL的标准溶液转移至10 mL容量瓶中,加入色谱级甲醇溶液稀释并定容至刻度,配成浓度为1.00 mg/mL的标准溶液储备液I。准确移取1 000 μL浓度为1.00 mg/mL的标准溶液储备液至100 mL容量瓶中,加入色谱级甲醇至刻度,配成浓度为10.0 μg/mL的标准储备液II,备用。
精密量取标准储备液II 1.0 mL于10 mL容量瓶中,用甲醇稀释至刻度,配成浓度为1.00 μg/mL的对照品溶液,然后用甲醇逐级稀释配置成浓度分别为300、200、160、100、80、40、20 ng/mL的3-[4-(3-硝基苯磺酰氧基)苯基]丙酸标准曲线溶液。精密量取上述溶液各5.0 μL注入液相色谱质谱联用仪,记录峰面积。以目标物浓度为横坐标,以相应目标物峰面积为纵坐标做回归曲线,计算回归方程及相应的线性回归系数。
2.6 定量限及检出限的测定
用甲醇逐级稀释浓度为10.0 μg/mL的3-[4-(3-硝基苯磺酰氧基)苯基]丙酸标准储备液,配制浓度为20 ng/mL的标准溶液,作为3-[4-(3-硝基苯磺酰氧基)苯基]丙酸的定量限浓度,平行做3组,各进样5.0 μL检测。
用甲醇逐级稀释浓度为10.0 μg/mL的3-[4-(3-硝基苯磺酰氧基)苯基]丙酸标准储备液,配制浓度为2.0 ng/mL的标准溶液,作为3-[4-(3-硝基苯磺酰氧基)苯基]丙酸的检出限浓度,平行做3组,各进样5.0 μL检测。
2.7 加标回收率的考察
精密称取盐酸兰地洛尔样品40.0 mg,置10 mL量瓶中,加甲醇至刻度,摇匀后超声10 min,冷却至室温,加色谱甲醇至刻度,作为空白样品溶液。平行制备3份。
称取3份盐酸兰地洛尔样品40.0 mg,置于10 mL量瓶中,分别加入1.00 μg/mL的 3-[4-(3-硝基苯磺酰氧基)苯基]丙酸标准溶液2.0、1.0、0.4 mL,再加甲醇溶解并稀释至刻度,摇匀后超声10 min,作为加标浓度200、100、40 ng/mL的加样回收率试验溶液。每个浓度平行制备3份。
精密量取上述供试品溶液5.0 μL注入液相色谱质谱联用仪,记录样品峰面积,并计算回收率。
2.8 方法精密度
由于样品中无目标物检出,取盐酸兰地洛尔样品40.0 mg,置10 mL量瓶中,精确加入1.0 mL浓度为1.00 μg/mL的3-[4-(3-硝基苯磺酰氧基)苯基]丙酸标准溶液,加甲醇溶解并稀释至刻度,摇匀后超声10 min,作为供试品溶液,平行测定3次,计算相对标准偏差。
2.9 溶液稳定性
2.9.1 对照品溶液稳定性
制备浓度为10 ng/mL的3-[4-(3-硝基苯磺酰氧基)苯基]丙酸的标准对照品溶液,分别于室温放置0、2、4、8、12、24 h,精密量取5.0 μL注入液相色谱质谱联用仪检测,记录各目标化合物的质谱检测峰面积。
2.9.2 供试品溶液稳定性
由于样品溶液中无目标物检出,参照样品加标溶液的制备方法制备一份浓度为10 ng/mL的加标溶液,分别于室温放置0、2、4、8、12、24 h,精密量取5.0 μL注入液相色谱质谱联用仪检测,记录各目标化合物的质谱检测峰面积。
2.10 实际样品检测
按照标准曲线配制方法制备标准曲线,并检测盐酸兰地洛尔样品3批。3-[4-(3-硝基苯磺酰氧基)苯基]丙酸的线性回归方程为:Y=1 305.140 9X+79 700.654 4,相关系数R2=0.993。
准确称取样品各40.0 mg(每批各2份),置10 mL容量瓶中,精密加入甲醇至刻度,摇匀后超声10 min,进样5.0 μL,依法测定,代入标准曲线计算样品中目标化合物的含量。
3 结果与分析
3.1 专属性实验
利用建立的方法分别进样检测空白溶剂(甲醇)、盐酸兰地洛尔样品及加标后的样品,空白溶剂及盐酸兰地洛尔样品中目标物均未出峰,加标后的样品目标物的峰形良好,且空白溶剂、空白样品对杂质测定无干扰,见表2,图2~3。

表2 专属性实验结果

图2 盐酸兰地洛尔空白样品检测质谱图Fig.2 The mass spectrogram of landiolol blank sample

图3 盐酸兰地洛尔空白样品加标3-[4-(3-硝基苯磺酰氧基)苯基]丙酸的检测质谱图Fig.3 The mass spectrogram of landiolol sample spiked with target analyte
3.2 系统适用性实验
3-[4-(3-硝基苯磺酰氧基)苯基]丙酸标准品溶液重复进样6次的检测峰面积如表3所示,结果重复性良好,相对标准偏差为3.20%,符合精密度实验要求。

表3 3-[4-(3-硝基苯磺酰氧基)苯基]丙酸精密度实验结果
3.3 标准曲线
分别进样浓度为300、200、160、100、80、40、20 ng/mL的3-[4-(3-硝基苯磺酰氧基)苯基]丙酸标准曲线溶液,以目标物浓度为横坐标,以目标物峰面积为纵坐标做回归曲线,得线性回归方程为y=447.3x+30 018(R2=0.996),如图4所示。实验结果表明,在20~300 ng/mL范围内,3-[4-(3-硝基苯磺酰氧基)苯基]丙酸浓度与峰面积呈良好线性关系。

图4 3-[4-(3-硝基苯磺酰氧基)苯基]丙酸标准曲线Fig.4 The calibration curve of target analyte obtained by the developed method
3.4 定量限及检出限
根据表4中3-[4-(3-硝基苯磺酰氧基)苯基]丙酸定量限及检出限的峰面积检测结果显示,定量限浓度为20.0 ng/mL,换算到盐酸兰地洛尔样品中的检测定量限为5.00 mg/kg;检测限浓度为2.0 ng/mL,换算到盐酸兰地洛尔样品中的检测定量限为0.50 mg/kg。
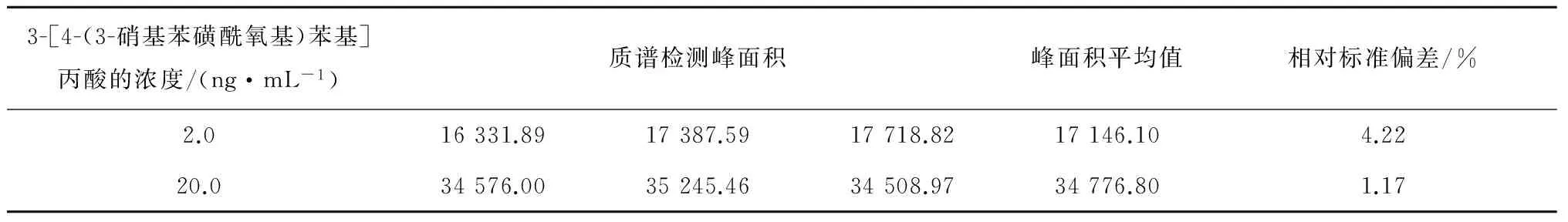
表4 3-[4-(3-硝基苯磺酰氧基)苯基]丙酸定量限与检出限检测质谱峰面积及标准偏差
3.5 加标回收率的考察
低、中、高3个浓度的样品加标回收率结果见表5,数据显示,样品的加标回收率在92.47%~99.19%之间,平行3个样品的相对标准偏差在0.70%~5.59%之间,表明该方法回收率良好,符合方法学实验的要求。

表5 3-[4-(3-硝基苯磺酰氧基)苯基]丙酸加标回收率实验的检测结果
3.6 方法精密度
3-[4-(3-硝基苯磺酰氧基)苯基]丙酸的方法精密度结果如表6所示,此方法3次加标的相对标准偏差为3.28%,结果重现性良好。

表6 方法精密度实验结果
3.7 溶液稳定性
3.7.1 对照品溶液稳定性
对照品溶液稳定性实验结果如表7所示,对照品溶液在室温放置下各目标物峰面积无明显变化,符合稳定性要求。

表7 对照品溶液稳定性试验结果
3.7.2 供试品溶液稳定性
加标后的原料药供试品溶液稳定性实验结果如表8所示,供试品溶液在室温放置下目标物峰面积无明显变化,符合稳定性要求。
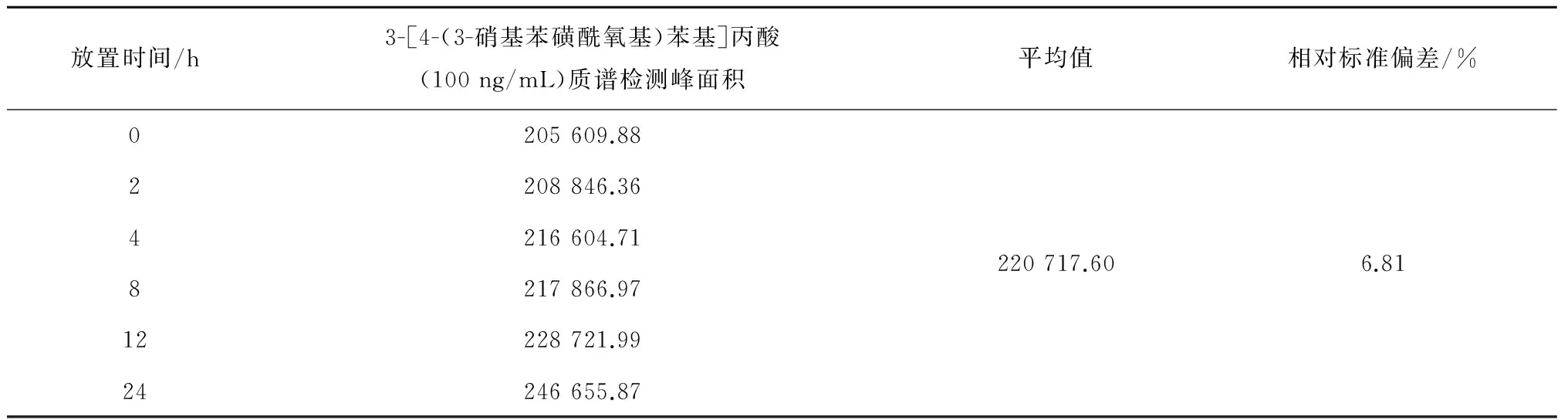
表8 样品加标溶液稳定性实验结果
3.8 样品检测结果
利用本文建立的方法,分别对企业提供的批号为1、2、3号的盐酸兰地洛尔原料药物中3-[4-(3-硝基苯磺酰氧基)苯基]丙酸的含量进行检测,结果显示,3批样品中3-[4-(3-硝基苯磺酰氧基)苯基]丙酸的含量均低于0.50 mg/kg。
4 结论
本研究利用高效液相色谱-三重串联四级杆质谱,建立了盐酸兰地洛尔原料药物中痕量3-[4-(3-硝基苯磺酰氧基)苯基]丙酸的检测方法。本方法的检测灵敏度可达到0.50 mg/kg,且方法的精密度和回收率均能满足检测要求。该研究操作简单、结果可靠,可实现对盐酸兰地洛尔原料药物中痕量3-[4-(3-硝基苯磺酰氧基)苯基]丙酸的快速、低成本检测。
[1]叶惠珍. β1受体阻断剂盐酸兰地洛尔[J]. 世界临床药物, 2004, 25(3): 189-190.
[2]赫冠男, 吕黄伟, 王俊科. 兰地洛尔的药理作用及其围手术期的应用[J]. 中国新药与临床杂志, 2007, 26(12): 942-945.
[3]庾莉菊, 黄海伟, 李秀梅, 等. 超高效合相色谱法测定盐酸兰地洛尔中立体异构体的含量[J]. 分析化学, 2016, 44(9): 1348-1353.
[4] 卢定强, 李衍亮, 凌岫泉, 等. 手性药物拆分技术的研究进展[J]. 时珍国医国药, 2009, 20 (7): 1731-1734.
[5] 张倩, 冯明声, 曹于平, 等.超短效 β-1-肾上腺素受体阻断剂:盐酸兰地洛尔的研发和临床应用[J].中国医药指南,2012, 10(9): 7-9.
[6] KIDO T, MOCHIZUKI T, HIRANO M, et al. Radiation-dose-lowering effects of landiolol hydrochloride in coronary angiography using computed tomography (Delight):A prospective multicenter study[J].Circ J, 2016,80(5):1225-1231.
[7] 李梅, 孙政, 庄儒麟, 等.兰地洛尔和艾司洛尔抗实验性心律失常作用和安全性评价的比较研究[J].中国临床药理学杂志, 2015, 31(8): 640-644.
[8]SAKANASHI M, SAKANASHI M,SUGAHARA K, et al. Effects of landiolol on mechanical and metabolic changes in rat reperfused ischaemic hearts[J]. Clin Exp Pharmacol Physiol, 2007, 34(1/2): 55-60.
[9] YU SC, KATOH T, OKADA H, et al. Landiolol does not enhance the effect of ischemic preconditioning in isolated rat hearts[J]. J Anesth, 2010, 24(2): 208-214.
[10] KAWAGUCHI M, KAWARAGUCHI Y, YAMAMOTO Y, et al. Effects of landiolol on systemic and cerebral hemodynamics and recovery from anesthesia in patients undergoing craniotomy[J]. J Anesth, 2010, 24(4): 503-510.
[11] GOTO K,SHINGU C,MIYAMOTO S,et al.The effect of landiolol on hemodynamics and left ventricular function in patients with coronary artery disease[J]. J Clin Anesth,2007,19(7):523-529.
[12]KADOI Y,HORIUCHI T,UCHIDA S,et al.A dequacy of control of preoperative hypertension can affect landiolol-induced hemodynamic changes in elderly patients during emergence from anesthesia[J]. J Anesth, 2011, 25(2): 271-277.
[13]梁键谋, 傅聪, 陈悦. LC-MS/MS 测定草酸右旋西酞普兰中对甲苯磺酸酯类基因毒性杂质的含量[J].中国现代应用药学, 2016, 33 (11):1436-1440.
[14]周长朋, 王东武, 张曼玉, 等. 高效液相色谱-四极杆/线性离子阱质谱仪测定盐酸决奈达隆中两种基因毒性杂质的痕量残留[J]. 分析测试学报, 2016, 35 (9):1111-1115.
phenyl] propionic acid in the landiolol hydrochloride crude drug
WANG Shan-shan1,WANG Li-juan1, LI Zhuo-wa2, NING Fan-sheng1, WANG Xiao-li1, CHEN Yue1, CHEN Xiang-feng1*
(1. Shandong Analysis and Test Center, Jinan 250014, China; 2.Zaozhuang College,Zaozhuang 277000, China)
∶To detect and control the content of trace toxic impurity 3-[4-(3-nitrobenzene sulfonyl oxygen radicals) phenyl] propionic acid, which isessential material in the synthesis of landiolol hydrochloride drug, a HPLC with tandem mass spectrometry method was developed to determine the 3-[4-(3-nitrobenzene sulfonyl oxygen radicals) phenyl] propionic acid in the landiolol hydrochloride crude drug. The multiple reaction monitor mode was used to eliminate the matrix effect and increase the sensitivity of the method. The limit of detection of the target analyte was 0.50 mg/kg. The recoveries of spiked samples were between 91.9% and 97.8%. The relative standard diviation value of precision experiment was 3.28%(n=6). The established method was simple, reliable, fast and low cost,which is able to meet the demand of impurities determination in crude drugs.
∶landiolol hydrochloride; high performance liquid chromatography with tandem mass spectrometry; 3-[4-(3-nitrobenzene sulfonyl oxygen radicals)phenyl]propionic acid;trace detection
10.3976/j.issn.1002-4026.2017.02.017
2017-01-18
山东省自然科学基金(ZR2012BQ009)
王珊珊(1983—),女,博士,研究方向为分析化学。
*通信作者,陈相峰(1981—),男,博士,副研究员,研究方向为质谱分析。E-mail:xiangfchensdas@163.com
O656.31
A
1002-4026(2017)02-0113-08
