清血八味片中钙离子的含量测定
2017-05-09王宝丽李思茹徐柯心林瑞超
王宝丽 李思茹 徐柯心 林瑞超
·论著·
清血八味片中钙离子的含量测定
王宝丽 李思茹 徐柯心 林瑞超
目的 建立清血八味片中钙离子的含量测定方法。方法 采用化学鉴别法进行清血八味片的钙盐与硫酸盐的鉴别反应;分别对清血八味片样品的处理方法及测定方法进行考察;将样品经炭化后灰化,采用乙二胺四乙酸二钠络合滴定法测定钙离子含量。结果 确定样品最佳处理条件:在调压电炉上炭化1小时至炭化完全后,置于马弗炉中在700~800℃下灰化6小时;测定方法的重复性试验RSD值为0.32%(n=6),加样回收率为98.67%~101.25%,RSD值为0.97%(n=6),均符合定量分析要求;3批清血八味片样品的钙离子含量分别为17.40%、19.34%及20.69%。结论 该方法操作简便,准确,重复性好,可用于清血八味片中钙离子的含量测定。
清血八味片; 寒水石; 石膏; 钙离子; 含量测定
清血八味片(蒙名:琪孙黑木拉-8)是常用的蒙医药复方制剂,具有清讧血功效,用于血热头痛、口渴目赤、中暑等病症,临床上主要治疗高血压、高脂血症、高血脂、中暑。处方是由寒水石(凉制)340 g、紫草340 g、土木香52 g、人工牛黄44 g、栀子140 g、瞿麦60 g、石膏42 g、甘草20 g八味药组成。《中国人民共和国卫生部药品标准》(蒙药分册)1998年版中收载清血八味胶囊及清血八味散,均缺乏鉴别项和含量测定项[1]。2009年国家食品药品监督管理局发布清血八味片的质量标准,建立了紫草、土木香、人工牛黄的薄层鉴别及栀子苷的含量测定,未对寒水石及石膏成分作定量测定。清血八味的散剂、胶囊及颗粒等制剂中,植物药化学成分的薄层色谱鉴别及高效液相色谱法的含量测定已有文献报道[2-6],但目前尚无关于制剂中矿物药寒水石及石膏的定性及定量测定方法的报道。矿物药寒水石作为方中君药用量较大,且石膏与寒水石主成分相同,有必要对两者的含量测定制定检测方法。预实验中按照《中华人民共和国卫生部药品标准》(中药材)理化鉴别试验[7]及《中华人民共和国药典》(2015版)通则0301项下的一般鉴别试验[8]证明方中寒水石为北寒水石,主含二水硫酸钙(CaSO4·2H2O)。经凉制后的寒水石[9]失去结晶水,主含硫酸钙(CaSO4)。方中石膏主含二水硫酸钙[10],经水煎后入药,且石膏在水中的溶解度较低。寒水石及石膏均含有钙离子,故考虑以钙离子总量作为控制清血八味片中寒水石及石膏成分的控制指标。本研究利用EDTA络合滴定法测定清血八味片中钙离子的含量。
1 材料与方法
1.1 药物
清血八味片由内蒙古蒙奇药业有限公司提供,批号分别为20150602、20150901、20160302,3批样品均为市售样品。
1.2 试剂
二水硫酸钙为分析纯(北京化工厂,批号20140516,CaSO4·2H2O含量不少于99.0%);乙二胺四乙酸二钠(EDTA-2Na)标准试剂(0.05 mol/L,国家化学试剂质检中心,批号201608);钙黄绿素指示剂(天津市福晨化学试剂厂,批号20150520;按药典规定,取钙黄绿素0.1 g,加氯化钾10 g,研磨均匀,即得);甲基红指示剂(天津市福晨化学试剂厂,批号20160102),取甲基红0.05 g,加3.7 mL的0.05 mol/L氢氧化钠溶液使溶解,加水稀释至100 mL,即得。氢氧化钾、氢氧化钠均为分析纯AR,购自西陇化工股份有限公司。氯化钾、草酸铵、氯化钡、醋酸铅、醋酸铵、氨水、硝酸、醋酸、盐酸(HCL含量为36%~38%)均为分析纯AR,购自北京化工厂,水为屈臣氏蒸馏水。
1.3 仪器
马弗炉,1/万型电子天平,带调压器电炉(1000 W,220 V),250 mL锥形瓶,25 mL酸式滴定管,50 mL瓷质坩埚、试管等。
1.4 理化鉴别
取供试品粉末0.2 g,加稀盐酸10 mL,加热使溶解,过滤,取续滤液作为供试品溶液。
1.4.1 检查钙盐 取供试品溶液2 mL,加甲基红指示液2滴(溶液呈粉红色),用氨试液中和(溶液呈黄色),再滴加盐酸至恰呈酸性(溶液呈粉红色),加草酸铵试液,即生成白色沉淀;分离,沉淀不溶于醋酸,但可溶于稀盐酸。上述鉴别反应呈阳性,结果证明供试品中存在钙盐。
1.4.2 检查硫酸盐 (1)取供试品溶液2 mL,滴加氯化钡试液,即生成白色沉淀;分离,沉淀在盐酸或硝酸中均不溶解。(2)取供试品溶液2 mL,滴加醋酸铅试液,即生成白色沉淀;分离,沉淀在醋酸铵试液或氢氧化钠试液中溶解。(3)取供试品溶液1 mL,加盐酸,不生成白色沉淀(与硫代硫酸盐区别)。上述三个鉴别反应均为阳性,结果证明供试品中存在硫酸盐。
1.5 含量测定
1.5.1 供试品的制备 取供试品细粉约0.24 g,精密称定,置50 mL瓷质坩埚内,敞口置于带调压器电炉上(1000 W,220 V),炭化1小时,至炭化完全,所有操作均在通风橱中进行。将样品炭化完全的坩埚盖上盖,至马弗炉中,700~800℃灰化6小时,至灰化完全,放冷,备用。
1.5.2 测定方法 将坩埚内的灰分加稀盐酸10 mL,加热使溶解,将溶液转移至250 mL锥形瓶中,用蒸馏水洗坩埚3~4次,最终加水总量为100 mL,滴加甲基红指示液1滴,滴加氢氧化钾试液至溶液显浅黄色,再继续多加5 mL,加钙黄绿素指示剂少量(约0.1 g),用乙二胺四乙酸二钠滴定液(0.05 mol/L)滴定,至溶液的黄绿色荧光消失,并显橙色,按照2015版《中华人民共和国药典》(一部)石膏项下的测定方法[10]进行。
1.5.3 空白试验 按照1.5.1项下的方法制备不加入供试品的空白溶液,测得消耗乙二胺四乙酸二钠滴定液(0.05 mol/L)0 mL。
1.5.4 重复性试验 平行称取6份供试品细粉(批号20150602)各0.24 g,精密称定,按照1.5.1项下方法制备供试品,按照1.5.2项下方法进行测定,按供试品制备方法进行制备及含量测定,计算RSD值。结果表明重复性良好,见表1。
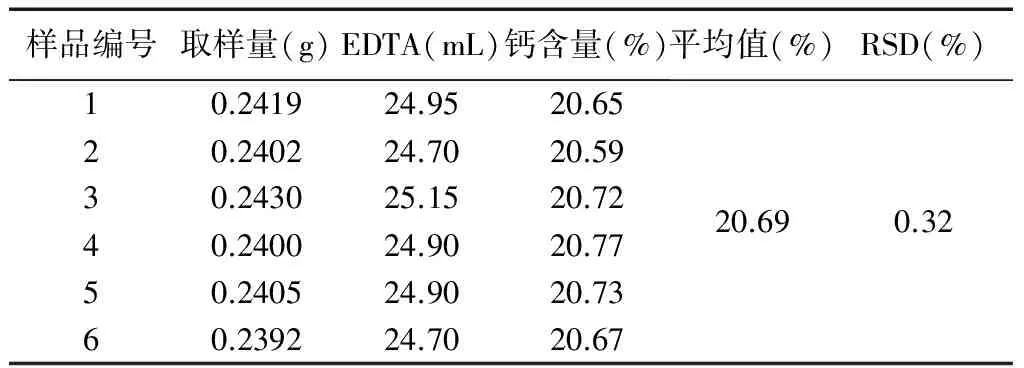
表1 重复性试验(n=6)
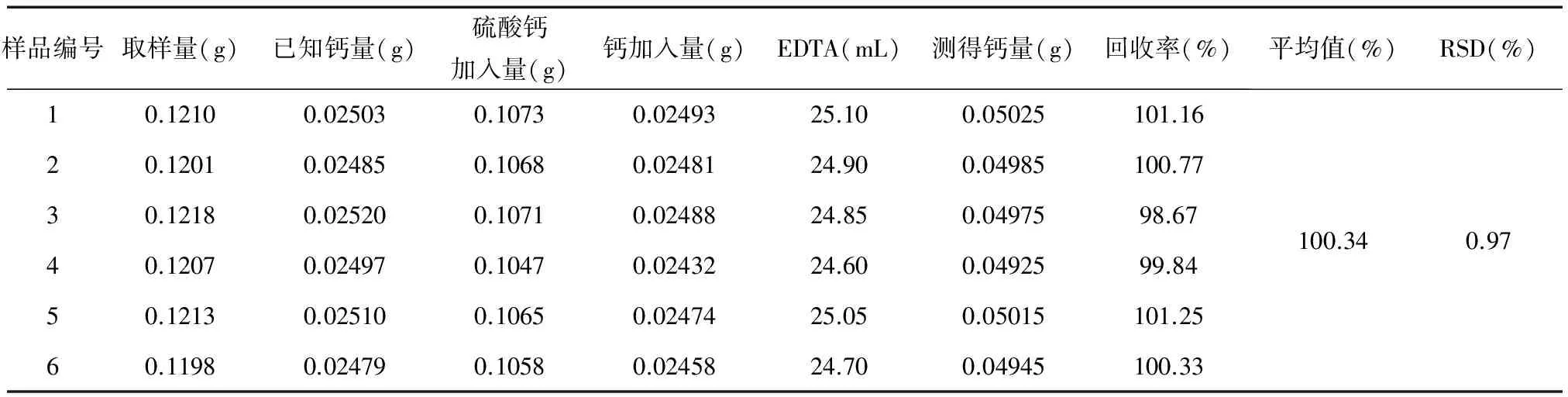
表2 加样回收率试验(n=6)
1.5.5 加样回收率试验 精密称取6份已知含量的清血八味片样品(批号20150602)各0.12 g,精确加入一定量的二水硫酸钙对照品,按1.5.1供试品制备方法制备,按1.5.2测定方法测定每份含量,计算加样回收率及RSD值。结果表明该方法准确度高,见表2。
2 结果
取清血八味片样品按照1.5.1项下的方法处理,按照1.5.2项下的方法进行含量测定,3批样品的测定结果见表3。
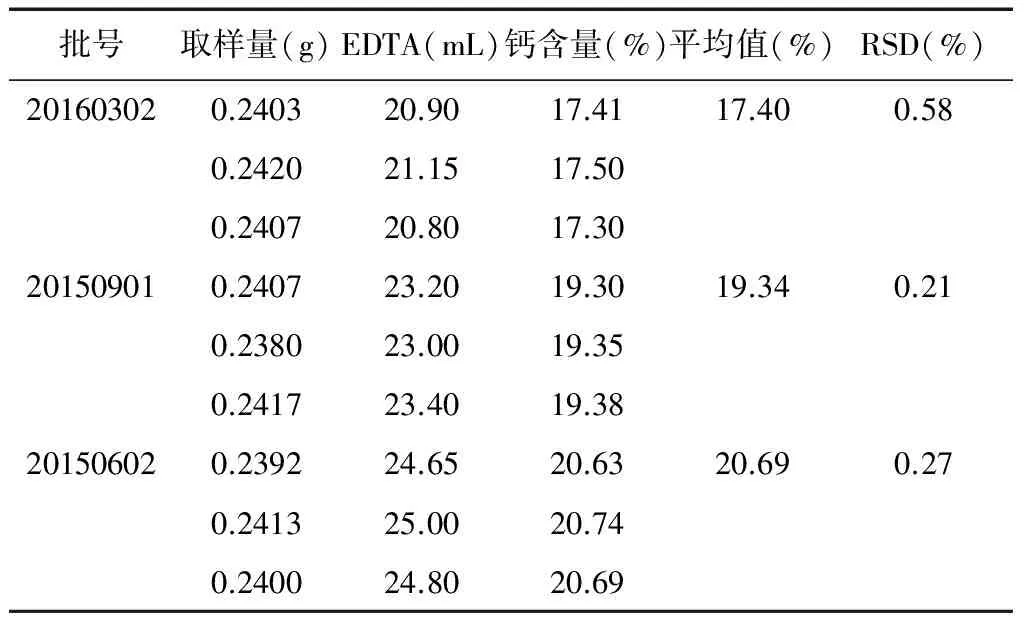
表3 清血八味片中钙含量测定结果(n=3)
3 讨论
3.1 供试品制备方法考察
实验中首先对供试品取样量进行了考察,比较了0.1 g、0.2 g、0.3 g、0.5 g对试验结果的影响,为了满足消耗的滴定液体积大于20 mL[11],并尽量减小滴定误差,最终选择0.24 g的取样量。清血八味片中有机物成分较多,对钙离子络合滴定的干扰较为严重,故样品处理方法的选择显得尤为关键。参考有关文献报道[11-14],尝试了不同的样品处理方法,若将样品细粉直接加入稀盐酸,溶液较浑浊,无法观察到滴定终点;另外,若将样品细粉加入稀盐酸后,过滤取滤液或离心取上清液,溶液显棕黄色,与滴定终点颜色接近,影响滴定终点的判别。实验发现采用先炭化后灰化的处理方法,可有效减少其他化学成分对滴定方法的干扰。进一步优化样品处理条件,样品炭化1小时后炭化完全(即无烟),灰化温度选择700~800 ℃,灰化时间第一次选择6小时,第二次选择2小时,第三次选择2小时,三次称重结果表明第二、三次灰分重量并未减少,故只需灰化6小时即可。
3.2 含量测定的方法学考察
络合滴定过程中,溶液的酸碱度对络合物的稳定性影响很大,所以本实验对稀盐酸用量、加水总量及氢氧化钾试液用量分别进行了考察。
3.2.1 稀盐酸用量的选择 取供试品细粉3份,按“1.5.1”项下的方法制备样品,分别加入5、10、15 mL的稀盐酸,按照“1.5.2”项下的方法测定钙含量。结果表明,加入10 mL稀盐酸的样品钙含量明显高于加入5 mL的样品,加入15 mL稀盐酸的样品钙含量没有增加。为保证最大限量的溶解样品,故选择加入10 mL的稀盐酸。
3.2.2 加水总量的选择 取供试品细粉3份,按“1.5.1”项下的方法制备样品,分别加入50、100、150 mL的水进行试验。结果表明,加水总量100 mL和150 mL测得结果相近,而加水总量50 mL的测得结果略低,故选择加入100 mL的水。
3.2.3 氢氧化钾试液用量的选择 取供试品细粉3份,按“1.5.1”项下的方法制备样品,测定过程中在滴加氢氧化钾试液至溶液显浅黄色后,再分别继续加入5、10、15 mL的氢氧化钾试液进行试验。观察发现,加入过量氢氧化钾试液5 mL时滴定终点明显且变色敏锐,未出现可逆反应。结果表明3种氢氧化钾试液用量的测定结果基本相同,故选择加入过量氢氧化钾试液为5 mL。
4 结语
中国矿物药的研究基础薄弱,尤其在安全标准及质量标准上尚存在较大的问题,因此亟需制定和完善矿物药的安全标准和质量标准,以便提高临床用药的安全性和质量可控性。近年来,矿物药检测技术随着科技的飞速发展而不断提高,偏光显微镜、X射线衍射仪、红外光谱仪及电感耦合等离子体质谱仪等分析测试仪器均在矿物药的质量研究中得到广泛应用[15]。利用偏光显微镜可观察矿物的光学性质,矿物的化学成分及结构决定了其红外光谱特征,矿物的晶体结构会产生相应的X射线衍射图谱,但由于方中的寒水石及石膏经过粉碎、炮制及煎煮过程,其光学性质及晶体构型已被破坏,所以目前无法应用上述方法对制剂中的寒水石及石膏进行相关的质量分析。电感耦合等离子体质谱法(ICP-MS)和电感耦合等离子体原子发射光谱法(ICP-AES)均具有灵敏度高、检测限低、分析速度快和多元素同时测定等优点,是分析微量和痕量无机元素的常规分析技术,但对于只测定钙离子这一常量元素来说,仪器价格相对昂贵,经济成本较高。《中华人民共和国药典》中的EDTA 滴定法是目前测定石膏中钙离子含量的主要方法,该方法操作简便,准确度高且重复性好,具有一定的实际应用价值。故本研究采用了EDTA滴定法对清血八味片中钙离子含量进行测定。
寒水石和石膏均为临床常用的矿物药,在2015版《中华人民共和国药典》中收载的六味安消散、清咽丸、紫雪散等11种成方制剂中均以寒水石入药,小儿感冒颗粒、牛黄解毒片、连花清瘟胶囊等60余种成方制剂中均以石膏入药,可见以寒水石或石膏入药方剂之多,应用范围之广泛。前期实验初步鉴定该方中寒水石为北寒水石(主成分为二水硫酸钙,经凉制后失去结晶水),并非南寒水石(主成分为碳酸钙)。由于寒水石和石膏的主成分相同,均为二水硫酸钙,两者相互干扰钙离子的检测,无法专属性地测定寒水石或石膏单味药材在清血八味片中的钙含量,故对制剂中钙总量进行含量测定。本实验初步建立了EDTA滴定法测定清血八味片中总钙离子含量的方法,可用于清血八味片中矿物药的质量控制,亦为清血八味片质量标准的提高与完善提供参考资料,对以寒水石或石膏入药的成方制剂中钙离子含量测定具有实际意义。
[1] 中华人民共和国卫生部药典委员会.中华人民共和国卫生部药品标准(蒙药分册)[S]. 北京:人民卫生出版社,1998:164-165.
[2] 杜娟,武桂芝,白音夫,等.清血八味散的薄层色谱鉴别[J].中国民族医药杂志,2008,14(1):43-44.
[3] 高钢,徐华.清血八味胶囊的薄层色谱鉴别[J].北方药学,2014,11(2):17-18.
[4] 李改莲.HPLC法测定蒙药清血八味散中甘草酸含量[J].中国民族医药杂志,2013,19(8):58-59.
[5] 王秀梅,包明兰.HPLC测定蒙药清血八味散中异土木香内酯和土木香内酯含量[J].辽宁中医药大学学报,2014,16(9):80-82.
[6] 许莉勇.清血八味颗粒质量标准的研究[J].中华中医药杂志,2010,25(6):942-944.
[7] 中华人民共和国卫生部药典委员会.中华人民共和国卫生部药品标准(中药材)(第一册)[S].北京:人民生出版社, 1992:29.
[8] 国家药典委员会.中华人民共和国药典(四部)[S].北京:中国医药科技出版社,2015:35-36.
[9] 陆景坤,周昊菲,陈朝军,等.不同产地寒水石炮制前后主成分、微量元素含量对比分析[J].中药材,2011,34(3):357-361.
[10] 国家药典委员会.中华人民共和国药典(一部)[S].北京:中国医药科技出版社,2015:94-95.
[11] 夏振江,魏立新,杜玉枝,等.北寒水石质量标准研究[J].时珍国医国药,2010,21(7):1658-1659.
[12] 李晓明,陈敏,邵爱娟,等.清咽六味散中石膏的含量测定[J].中国实验方剂学杂志,2011,17(9):72-73.
[13] 李晓明,邵爱娟,陈敏,等.小儿清热止咳口服液中石膏的含量测定[J].中国实验方剂学杂志,2011,17(19):72-73.
[14] 李敬芬,王栋,林燕.蒙成药寒水石小灰散中含水硫酸钙的含量测定[J].中国民族医药杂志,2007,(12):47,75.
[15] 林瑞超.矿物药检测技术与质量控制[M].北京:科学出版社,2013.
(本文编辑: 董历华)
Content determination of calcium inQingxueBaweiPill
WANGBaoli,LISiru,XUKexin,etal.
BeijingKeyLaboratoryofTraditionalChineseMedicineQualityEvaluation,SchoolofChinesePharmacy,BeijingUniversityofChineseMedicine,Beijing100102,China
Corresponingauthor:LINRuichao,E-mail:linrch307@sina.com
Objective To establish the method for content determination of calcium inQingxueBaweiPill. Methods To detect calcium salt and sulfate by chemical identification method. The sample treatment methods and determination method were studied respectively. Samples were charred and incinerated to ash, and the content of calcium was determined by EDTA complex metric titration method. Results The optimal processing conditions were 2-step heating: carbonized 1 hour on the electric stove, incinerated 6 hours under the 700~800℃ in the muffle furnace. The RSD value of the repeatability was 0.32%(n=6), the recovery was 98.67%~101.25% with RSD of 0.97%(n=6). They all met the demands of quantitative analysis. The content of calcium in three batches ofQingxueBaweiPill was 17.40%, 19.34%, 20.69% respectively. Conclusion The method was simple, accurate and reproducible. It can be used for the content determination of calcium inQingxueBaweiPill.
QingxueBaweiPill; Gypsum Rubrum; Gypsum; Calcium; Content determination
公益性行业科研专项(201507004)
100102 北京中医药大学中药学院 中药品质评价北京市重点实验室[王宝丽(硕士研究生)、李思茹(硕士研究生)、徐柯心(硕士研究生)、林瑞超]
王宝丽(1992- ),女,2014级在读硕士研究生。研究方向:民族药品质评价研究。E-mail:wblego@163.com
林瑞超(1954- ),博士,教授,研究员,博士生导师。研究方向:中药与民族药的品质评价研究。E-mail:linrch307@sina.com
R284.1
A
10.3969/j.issn.1674-1749.2017.05.003
2016-11-22)
