甲醇溶液中五氮唑负离子的制备与表征
2017-05-08徐冰韬王鹏程胡炳成
徐冰韬, 王鹏程, 王 乾, 章 冲, 胡炳成, 陆 明
(南京理工大学化工学院, 江苏 南京 210094)
1 引 言
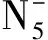

基于此,本研究以3,5-二甲基-4-羟基苯基五唑为原料,采用“先还原后氧化”的方法,在保持N—N键稳定的情况下,切断C—N键。该方法反应条件温和,危险性较小。运用质谱仪监测反应的进行程度,并通过同位素标记来研究五唑负离子的性质。
2 实验部分
2.1 仪器和试剂
仪器: EYELA公司PSL-1810型磁力搅拌低温恒温槽,Coolingway公司-86 ℃超低温冰箱,Bruker公司Avance III 500 MHz核磁共振仪,Finnigan公司TSQ Quantum Ultra AM高分辨液质联用仪。
试剂: 对氨基苯磺酸、2,6-二甲基苯酚、叠氮化钠、亚硝酸钠、连二亚硫酸钠、七水合硫酸亚铁、四水合氯化亚铁、四水合氯化铁、四水合氯化锰、氯化亚铜、30%过氧化氢水溶液、过氧叔丁醇,阿拉丁试剂有限公司,分析纯; 氢氧化钠、无水碳酸钠、无水硫酸钠,成都市科龙化工试剂厂,分析纯; 36.5%浓盐酸、四氢呋喃、甲醇,上海凌峰化学试剂有限公司,分析纯; 85%间氯过氧苯甲酸,上海萨恩化学技术有限公司,分析纯。
2.2 3,5-二甲基-4-羟基苯胺盐酸盐的合成
在250 mL三口瓶中依次加入12 g对氨基苯磺酸(69 mmol,1.0 e.q.),3.7 g碳酸钠(35 mmol,0.5 e.q.),50 mL水。磁力搅拌下降温至0 ℃,加入20 mL NaNO2水溶液(7.2 g,104 mmol,1.5 e.q.),滴加过程中保持温度稳定,反应30 min。加入14.6 mL 36.5% 浓盐酸(175 mmol,2.5 e.q.),反应30 min后置于冰箱中低温保存。
在另一个500 mL三口瓶中加入7.8 g 2,6-二甲基苯酚(64 mmol,0.93 e.q.),0 ℃下加入50 mL NaOH水溶液(14 g,350 mmol,5.0 e.q.),反应10 min后加入之前制备好的重氮盐溶液,加入过程中保持温度恒定在0 ℃,反应1 h。
将反应液升温至80 ℃,加入30.5 g Na2S2O4(175 mmol,2.5e.q.),反应1 h。冷却至室温后抽滤,滤饼水洗两次后用50 mL THF溶解,滤去不溶物,在所得澄清THF溶液中加入浓盐酸至强酸性(pH<2),搅拌析出大量固体,抽滤并用THF洗涤滤饼一次,晾干后得9 g粉色固体,产率75%。m.p. 230~235 ℃。1H NMR (CD3OD-d4, 500 MHz)δ: 6.95(s, 2H), 2.25(s, 6H)。ESI-MS/MS(m/z, 10 eV): 138.01 [M+H]+。
合成路线见Scheme 1。
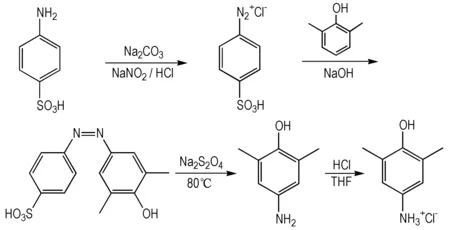
Scheme 1 Synthetic route of 3, 5-dimethyl-4-hydroxy aniline hydrochloride
2.3 3,5-二甲基-4-羟基苯基五唑(R1)的合成
3,5-二甲基-4-羟基苯基五唑为含能化合物,室温易分解,具有一定危险性,注意采取必要防护措施,保存在-50 ℃低温冰箱中[22]。
在250 mL单口瓶中加入3 g 3,5-二甲基-4-羟基苯胺盐酸盐(17.3 mmol,1.0 e.q.),加入30 mL水溶解,磁力搅拌下降温至0 ℃,加入1.52 mL 36.5% 浓盐酸(18.2 mmol,1.05 e.q.)。充分搅拌后加入15 mL NaNO2水溶液(1.25 g,18.2 mmol,1.05 e.q.),反应30 min。
重氮化完成后加入80 mL甲醇,降温至-50 ℃后,加入20 mL 预先冷冻至-50 ℃的NaN3的甲醇水混合溶液(1.22 g,18.2 mmol,1.05 e.q.),反应2 h。
低温抽滤,滤饼低温真空干燥,得2 g粉色固体,产率66.7%。1H NMR(CD3OD-d4, 500 MHz)δ: 6.95 (s, 2H), 2.25 (s, 6H)。ESI-MS/MS(m/z, 10 eV): 190.07 [M-H]-,225.99 [M+Cl]-。
合成路线见Scheme 2。

Scheme 2 Synthetic route of 3,5-dimethyl-4-hydroxy phenyl-pentazole
2.4 五唑负离子(P1)的合成
R1在-50 ℃下合成并保持稳定,故以R1为底物的反应也在-50 ℃下进行。鉴于五唑溶液的稳定性尚不明确,故所得产品也保存于-50 ℃低温冰箱中。
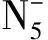
合成路线见Scheme 3。
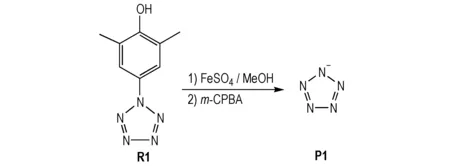
Scheme 3 Synthetic route of pentazole anion
3 结果与讨论
3.1 还原剂和氧化剂的选择
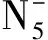
表1 不同还原剂和氧化剂的反应结果
Table 1 Results of using different reductants react with oxidants

entryreductantoxidantyield/%1FeSO4a1/a2/a3-2FeSO4a4trace3MnCl2a1/a2/a3/a4-4CuCla1/a2/a3/a4-

图1 五唑溶液的质谱图
Fig.1 Mass spectrum of pentazole solution
图1中主要峰的归属如下:m/z=155为m-CPBA的还原产物间氯苯甲酸 (m-CBA);m/z=190为R1离去H+得到的负离子[R1-H]-;m/z=226为[R1+Cl]-;m/z=261为[R1+N5]-;m/z=311为m-CBA的二聚;m/z=381为R1的二聚。

表2 氯化亚铁和氯化铁的测试
Table 2 Test of ferrous chloride and ferric chloride

entryreductantoxidantyield/%1FeCl2a1/a2/a3-2FeCl2a4trace3-FeCl3-4-FeCl3+a4-
3.2 五唑负离子的分离浓缩
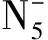

a. mass spectrum

b. mass/mass spectrum
图2 五唑浓缩溶液的质谱图
Fig.2 Mass spectrum of the concentrated solution of pentazole
3.3 同位素标记实验
假如五唑负离子具有芳香性,那么其N原子的化学环境应完全相同。由于尚未得到五唑的晶体,其N—N键键长键角无法测定,故设计同位素标记实验。以普通NaNO2为原料,可以得到R1,P1,为方便分析,将5个N原子分别编号为N(1),N(2),N(3),N(4),N(5),后续的分析均使用此编号; 使用15N标记的NaNO2作为原料,则可以得到三种15N标记的3,5-二甲基-4-羟基苯基五唑,分别为R2,R3,R4; 分别以R2,R3,R4为原料,制备对应的五唑,编号为P2,P3,P4,如图3所示。
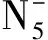

图3 不同位置15N标记的3,5-二甲基-4-羟基苯基五唑和五唑负离子
Fig.3 3, 5-dimethyl-4-hydroxy phenyl-pentazole and pentazole anion with15N in different position

a. 15N NMR spectrum of P2

b. 15N NMR spectrum of P3

c. 15N NMR spectrum of P4
图4 不同位置15N标记五唑的15N NMR图谱
Fig.415N NMR spectrum of pentazole with15N in different position
4 结 论
(1)以对氨基苯磺酸和2,6-二甲基苯酚为起始原料,依次合成3,5-二甲基-4-羟基苯胺盐酸盐(收率75%),3,5-二甲基-4-羟基苯基五唑(收率66.7%),操作简单,危险性较低。
(2)以亚铁盐为还原剂,间氯过氧苯甲酸为氧化剂,可以切断3,5-二甲基-4-羟基苯基五唑中的C—N键,得到五唑负离子(m/z=70,141; 10 eV)。五唑负离子在甲醇溶液中稳定,但由于提纯难度较大,尚未得到其固体,未能测定其热稳定性等性质。
(3)五唑负离子的15N NMR图谱证明,其环上5个N原子的化学环境相同(δN=309.4),并且在同一平面上,认为五唑负离子极有可能具有芳香性。
参考文献:
[1] 李玉川, 庞思平. 全氮型超高能含能材料研究进展[J]. 火炸药药学报. 2012, 35(1): 1-7.
LI Yu-chuan, PANG Si-ping. Progress of all-nitrogen ultrahigh-energetic macterials[J].ChineseJournalofExplosives&Propellants, 2012, 35(1): 1-7.
[2] Kim F Ferris, Rodney J Bartlett. Hydrogen pentazole: does it exist?[J].JournaloftheAmericanChemicalSociety, 1992, 114 (21): 8302-8303.
[3] Burke L A, Butler R N, Stephens J C. Theoretical characterization of pentazole anion with metal counter ions. Calculated and experimental15N shifts of aryldiazonium, -azide and-pentazole systems[J].JournaloftheChemicalSociety, 2001(9): 1679-1684.

[5] Straka M, PyykköP. One metal and forty nitrogens. Ab initio predictions for possible new high-energy pentazolides[J].InorganicChemistry, 2003, 42(25): 8241-8249.
[6] Müller R, Wallis J D, von Philipsborn W. Direct structural proof for the pentazole ring system in solution by15N NMR spectroscopy[J].AngewandteChemieInternationalEditioninEnglish, 1985, 24(6): 513-515.
[7] Wallis J D, Dunitz J D. An all-nitrogen aromatic ring system: structural study of 4-dimethyl-aminophenylpentazole[J].JournaloftheChemicalSociety,ChemicalCommunications, 1983 (16): 910-911.
[8] Ugi I, Huisgen R. Pentazole, II. Die zerfallsgeschwindigkeit der aryl-pentazole[J].ChemischeBerichte, 1958, 91(3): 531-537.
[9] Ugi I, Perlinger H, Behringer L. Pentazole, III.Kristallisierte aryl-pentazole[J].ChemischeBerichte, 1958, 91(11): 2324-2329.
[10] Huisgen R ,Ugi I.Mittlere Ringe X I. Polycyclische systeme mit heteroatomen[J].EuropeanJournalofOrganicChemistry, 1957, 610(1): 57-66.
[11] Benin V, Kaszynski P, Radziszewski G. Arylpentazoles revisited: experimental and theoretical studies of 4-hydroxyphenylpentazole and 4-oxophenylpentazole anion[J].TheJournaloforganicChemistry, 2002, 67(4): 1354-1358.

[14] 毕福强, 许诚, 樊学忠, 等. 对叔丁基苯基五唑的合成及分解动力学[J]. 火炸药学报, 2012(2): 002.
BI Fu-qiang, XU Cheng, FAN Xue-zhong, et al. Synthesis and decomposition kinetics of p-tert-butylphenylpentazole[J].ChineseJournalofExplosives&Propellants, 2012(2): 002.
[15] 沈梦楠, 申程, 王鹏程, 等. 多供电子基苯胺类化合物的合成及其芳基五唑衍生物稳定性[J]. 精细化工, 2014, 31(12): 1531-1536.
SHEN Meng-nan, SHEN Cheng, WANG Peng-cheng, et al. Synthesis of anilines with multi-electron-donating groups and the stability of arylpentazole derivatives[J].FineChemicals, 2014, 31(12): 1531-1536.
[16] Carlqvist P, Östmark H, Brinck T.The stability of arylpentazoles[J].TheJournalofPhysicalChemistryA, 2004,108(36): 7463-7467.
[17] Lein M, Frunzke J, Timoshkin A, et al. Iron Bispentazole Fe(η5-N5)2, a theoretically predicted high-energy compound: Structure, bonding analysis, metal-ligand bond strength and a comparison with the isoelectronic ferrocene[J].Chemistry-AEuropeanJournal, 2001, 7(19): 4155-4163.
[18] Frunzke J, Lein M, Frenking G. Structures, metal-ligand bond strength, and bonding analysis of ferrocene derivatives with group-15 heteroligands Fe (η5-E5)2and FeCp (η5-E5)(E= N, P, As, Sb). A theoretical study[J].Organometallics, 2002, 21(16): 3351-3359.
[19] Vij A, Pavlovich J G, Wilson W W, et al. Experimental detection of the pentaazacyclopentadienide(pentazolate) anion, cyclo-N5[J].AngewandteChemie,2002, 114(16): 3177-3180.
[20] Butler R N, Stephens J C, Burke L A. First generation of pentazole (HN5, pentazolic acid), the final azole, and a zinc pentazolate salt in solution: a newN-dearylation of 1-(p-methoxyphenyl) pyrazoles, a 2-(p-methoxyphenyl) tetrazole and application of the methodology to 1-(p-methoxyphenyl) pentazole[J].ChemicalCommunications, 2003, (8): 1016-1017.
[22] 章冲, 胡炳成, 刘成, 等. 对羟基苯基五唑及其衍生物的合成与稳定性[J]. 含能材料, 2016, 24(8): 769-773.
ZHANG Chong, HU Bing-cheng, LIU Cheng, et al. Synthesis and stability of p-hydroxylphenylpentazole and its derivatives[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2016, 24(8): 769-773.
[23] Guisado-Barrios G, Zhang Y, Harkins A M, et al.Low temperature reaction of [Fe(TPA)(CH3CN)2]2+with excess 3-chloroperoxybenzoic acid in semi-frozen acetonitrile; EPR detection of an acylperoxo iron (Ⅲ) adduct[J].InorganicChemistryCommunications, 2012, 20: 81-85.
[24] 徐敏, 毕福强, 张皋, 等. 对二甲氨基苯基五唑和对羟基苯基五唑的低温合成与NMR表征[J]. 含能材料, 2012, 20(5): 596-600.
XU Min, BI Fu-qiang, ZHANG Gao, et al. Synthesis and NMR characterization of p-dimethylaminophenylpentazole andp-hydroxyphenylpentazole at low temperature[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2012, 20(5): 596-600.
