小剂量多巴酚丁胺负荷超声心动图在低流速低压差伴心功能不全的主动脉瓣狭窄患者中的初步应用分析
2017-05-02赵振燕宋光远张文佳裴汉军王建德肖明虎杨跃进吴永健
赵振燕,宋光远,张文佳,裴汉军,王建德,肖明虎,杨跃进,吴永健
小剂量多巴酚丁胺负荷超声心动图在低流速低压差伴心功能不全的主动脉瓣狭窄患者中的初步应用分析
赵振燕,宋光远,张文佳,裴汉军,王建德,肖明虎,杨跃进,吴永健
目的:探讨小剂量多巴酚丁胺负荷超声心动图(LDDSE)检查在主动脉瓣狭窄伴左心室功能不全、低流速低压差患者行经皮主动脉瓣置换术(TAVR)的应用价值和安全性。
方法:2013-10至2016-07,在我院连续入选列为常规外科换瓣手术禁忌,且准备行TAVR适应证评估的重度主动脉瓣狭窄患者,同时合并严重左心室功能不全伴低流速低压差者,共纳入有效病例5例。记录LDDSE检查前、过程中的平均跨瓣压差、最大流速、每搏输出量、射血分数,对判定为真性重度主动脉瓣狭窄且具有左心收缩储备功能患者行TAVR治疗,无左心收缩储备功能者采取药物治疗或酌情行TAVR治疗。观察TAVR治疗后心功能和N末端B型利钠肽原(NT-proBNP)变化。
结果:5例患者均表现为LDDSE检查阳性,平均跨瓣压差均≥40 mmHg(1 mmHg=0.133 kPa),每搏输出量增加≥20%,提示患者为真性重度主动脉瓣狭窄且有心脏收缩储备功能。LDDSE过程中、结束后无明显不良反应。其中4例行经TAVR治疗,1例因暂无瓣膜等待TAVR或球囊扩张术。TAVR术后患者心功能逐渐好转或恢复至正常,NT- proBNP持续下降。
结论:低流速低压差且伴左心功能不全的重度主动脉瓣狭窄患者,可考虑行LDDSE检查明确心功能储备情况和主动脉瓣狭窄程度;如有心脏收缩功能储备,建议行TAVR治疗。TAVR是此类患者的有效治疗手段。
超声心动描记术,压力;主动脉瓣狭窄;心脏瓣膜假体植入
在重度主动脉瓣狭窄患者中,大约5%~10%的患者伴有严重左心室功能不全(左心室射血分数<40%)、低流速低压差,平均跨瓣压差<40 mmHg(1 mmHg=0.133 kPa)定义为低流速低压差,虽然比例小,但治疗方面最有争议[1,2]。此类患者心功能差,如药物保守治疗,预期寿命小于2年;即使行外科换瓣手术治疗,与正常射血分数的重度主动脉瓣狭窄患者相比,具有极高的死亡率,但经外科换瓣手术后存活的患者却有着良好的远期生存率。如何从心功能差的患者中识别行换瓣手术获益的患者具有重大意义。国际上推荐采用小剂量多巴酚丁胺负荷超声心动图(LDDSE)检查指导此类患者的治疗[2,3]。尤其是随着经皮主动脉瓣置换术(TAVR)的发展,此检查越来越引起重视,但国内尚少见相关研究报道。本研究对5例重度主动脉瓣狭窄患者伴左心室功能不全伴低流速低压差的临床资料进行分析,初步探讨LDDSE在此类患者应用的安全性及指导TAVR治疗的价值。
1 资料与方法
研究对象:2013-10至2016-07在我院连续入选列为外科换瓣手术禁忌,且准备行TAVR适应证评估的重度主动脉瓣狭窄患者,其中合并严重左心室功能不全伴低流速低压差者,共8例,有3例因心功能左心室射血分数<20 %且合并中大量返流排除。其中男性3例,女性2例,年龄范围74岁~85岁,平均年龄(76.2±6.1)岁,左心室射血分数平均(34.0±3.5)%,NHYA分级Ⅲ级4例,Ⅳ级1例。心力衰竭病史平均(10.8±8.9)个月,体重指数(21.5±0.9)kg/m2,其中劳力性呼吸困难2例,心绞痛2例,冠心病史2例(无心肌梗死病史),高血压病史3例,慢性阻塞性肺疾病2例,慢性肾功能不全1例,脑卒中2例,吸烟史1例,均无黑朦史、晕厥史,胸骨左缘第2、3肋间均可闻及2/6级以上收缩期杂音,STS积分均大于8分。LDDSE试验阳性的患者均进行TAVR治疗。
主动脉瓣重度狭窄诊断标准[4]:主动脉瓣最大血流速度(Vmax)>4.0 m/s,平均跨瓣压差≥40 mmHg,一般情况下主动脉瓣口面积(AVA)≤1.0 cm2。入选条件需符合以下超声心动图诊断标准:(1)主动脉瓣瓣口面积≤1.0 cm2;(2)伴左心室射血分数<40%;(3)伴Vmax<4 m/s或静息平均跨瓣压差<40 mmHg。排除标准:(1)超声心动图测得主动脉瓣瓣口面积>1 cm2;(2)超声心动图静息平均跨瓣压差>40 mmHg。(3)主动脉瓣中大量返流。(4) 左心室射血分数<20%。
测试方法:由具备丰富经验的超声科医师、心脏病医生和护士共同完成。(1)超声心动图检查:静息状态:使用Philips iE 33型彩色多普勒超声诊断仪,配备经胸探头S5-1,于TAVR术前及术后1、6、12个月分别行超声心动图检查,探头频率2.5~3.5 MHz。于心尖五腔心切面以连续多普勒测量主动脉瓣最大血流速度、平均压差;二维Simpson法测量左心室射血分数。(2)LDDSE检查方法和操作流程:检查前通知病房,护士配好多巴酚丁胺液体备用,即50mg多巴酚丁胺与0.9%的生理盐水50ml配液在50ml注射器上,然后装载至微量输液泵上。检查期间全程行血压、心电监测,除颤器备用,同时备好抢救物品。LDDSE具体流程[5]:先记录用药前静息状态下的心率、血压、瓣口面积、平均跨瓣压差、最大流速、每搏输出量、射血分数等。然后静脉泵入多巴酚丁胺,以5 μg/(min·kg)为起始剂量,之后每隔5 min根据患者耐受情况或超声结果增加5 μg/(min·kg),最大剂量20 μg/(min·kg)。每一剂量泵入3 min后进行超声心动图检查,检查内容同上。如LDDSE达到阳性,则停止下一剂量检查。检查结束后观察5 min,患者如无明显不适则返回病房。(3)LDDSE阳性标准:心脏每搏输出量增加≥20%或主动脉瓣瓣口面积≤1.0 cm2且任何流量下Vmax≥4 m/s或平均跨瓣压差≥40 mmHg。心脏每搏输出量增加≥20%提示心脏有收缩储备功能;主动脉瓣瓣口面积≤1.0 cm2且任何流量下Vmax≥4 m/s或平均跨瓣压差≥40 mmHg提示主动脉瓣为重度主动脉瓣狭窄。如达多巴酚丁胺最大剂量20 μg/(min·kg),心脏每搏输出量增加<20%,提示心脏无收缩储备功能;如结果为心脏每搏输出量增加≥20%,平均跨瓣压差<40 mmHg同时Vmax<4 m/s,则认为心脏有收缩储备功能,主动脉瓣狭窄为非重度狭窄;心脏每搏输出量增加<20%,平均跨瓣压差<40 mmHg同时Vmax<4 m/s,则进一步行主动脉瓣CT检查钙化积分判定狭窄程度。如钙化积分女性>1200分或男性>2000分则为重度主动脉瓣狭窄,否则为非重度主动脉瓣狭窄[2,6]。检查终止指标:(1)出现阳性标准;(2)心率增加≥10次/min或心率>140次/min;(3)左心室射血分数增加到50%;(4)患者无法耐受或出现严重副反应如严重心律失常。对于判定为重度主动脉瓣狭窄且具有左心收缩储备功能患者采取TAVR治疗,如无左心收缩储备功能酌情行TAVR治疗或仅采取抗心力衰竭治疗。
术后观察和随访:对确定能行TAVR的患者术后1、6、12个月时返回我院行超声心动图检查,测定平均跨瓣压差、最大流速、射血分数等,同时行生化全套、血常规、N末端B型利钠肽原(NT-proBNP)化验等。
统计学处理:所有数据用统计学软件包SPSS20.0处理,计量资料以均数±标准差表示,计数资料采用频数(百分比)表示。本分析因纳入样本例数少,不进行统计检验。所有比较为绝对数值的直接比较。
2 结果
LDDSE结果及安全性分析:5例患者均表现为LDDSE检查阳性。多巴酚丁胺以5 μg/(min·kg)、10 μg/(min·kg)剂量激发时患者平均跨瓣压、最大跨瓣流速、血压、心率较静息状态变化不明显,见图1。多巴酚丁胺10 μg/(min·kg)剂量激发时每搏输出量较静息状态稍有增加,但增量小于20%。多巴酚丁胺以15 μg/(min·kg)激发时5例患者心脏每搏输出量增加分别为24%、25%、21%、27%、28%,平均跨瓣压差增加至40 mmHg以上,提示患者为真性主动脉瓣狭窄且具备收缩储备功能;5例患者最大跨瓣流速较静息状态增加15.7%~61.7%(绝对值增加0.6~2.1 m/s);左心室射血分数较静息状态增加12.5%~31.8%(绝对值增加4%~12%);1例患者血压稍有下降,无不适;心率较静息状态增加3~13次/min。LDDSE过程中、结束后患者均无明显胸痛、胸闷气短不适,无室性期前收缩、室性心动过速及其他心律失常。其中4例进行了TAVR,1例因暂无瓣膜等待行TAVR或球囊扩张术。

图1 5例患者在不同剂量多巴酚丁胺泵入时变量变化情况

表1 4例经皮主动脉瓣置换术前后LVEF、NT-proBNP变化情况
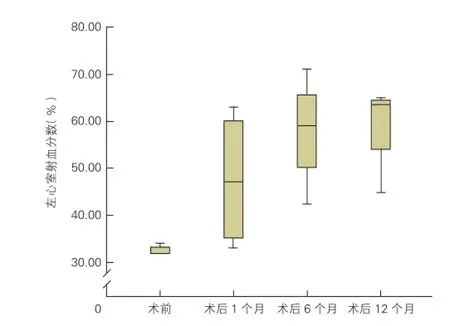
图2 经皮主动脉瓣置换术前后左心室射血分数变化

图3 经皮主动脉瓣置换术前后N末端B型利钠肽原(NT-proBNP) 变化
TAVR治疗前后左心室射血分数、NT-proBNP结果分析(表1):4例患者行TAVR治疗,其中1例随访尚未满6个月。左心室射血分数方面:术后1个月时2例患者由严重降低恢复正常,1例患者较术前有好转但未恢复正常(34%→37%),1例患者改善不明显;术后6个月时左心室射血分数继续好转,恢复正常者增加1例;术后12个月时左心室射血分数较术后6个月时继续改善,变化趋势(图2)。NT-proBNP方面,术后持续下降,术后1个月时下降最明显(图3)。
3 讨论
临床上对于重度主动脉瓣狭窄患者伴严重心功能不全、低流速低压差的治疗策略一直存有争议。国外指南中,LDDSE被推荐为判断低流速低压差伴左心室功能不全患者的瓣膜狭窄严重性和评估左心室收缩功能储备的工具[2]。本次分析显示,低流速低压差伴左心功能不全的重度主动脉瓣狭窄患者,即使属于外科换瓣高危风险或外科换瓣手术禁忌证,可考虑行多巴酚丁胺负荷超声心动图检查,了解主动脉瓣狭窄真实程度,明确心功能储备情况;如重度主动脉瓣狭窄患者有心脏收缩功能储备,建议积极行TAVR治疗。如无心脏收缩储备功能,可酌情行TAVR或单纯药物保守治疗。
由于多巴酚丁胺具有起效快、体内代谢时间短、静脉给药容易控制剂量、价格低及小剂量无明显副作用等优点,LDDSE广泛在临床开展。本次分析显示LDDSE是一种较为安全的筛查手段,亦有指导远期治疗的作用。研究报道,左心室功能和主动脉瓣口平均跨瓣压差是影响外科换瓣手术结局的独立预测因子[7,8]。心功能愈差,外科手术风险愈高,远期预后不佳。主动脉瓣狭窄患者左心功能不全通常是因为后负荷长期过大所致,另一部分是因为合并心肌梗死或心肌病变所致。在左心功能不全患者评估主动脉瓣狭窄有时比较困难,因为瓣口面积与每搏输出量相关[9,10],并且在低流量状态和正常流量状态使用Gorlin’s方程有差异[5,11]。此外,跨瓣压差与流量高度相关,因此在左心功能不全的患者有可能低估瓣膜真实狭窄程度。LDDSE可用来鉴别是固定性的重度狭窄还是流量依赖性的狭窄(相对性的)。如主动脉瓣口有固定性狭窄,行LDDSE时,患者会表现出每搏输出量增加,但瓣口的固定压差无变化。对于相对性狭窄,会表现出瓣口面积增加但跨瓣压差无明显增加。最终,无收缩储备功能的主动脉瓣狭窄患者因多巴酚丁胺不能增加每搏输出量就无法确定主动脉瓣狭窄程度。对于这部分患者需行主动脉瓣的CT检查钙化积分情况来判断瓣口狭窄严重程度[7]。正确鉴别主动脉瓣狭窄伴左心功能不全、低流速低压差患者有重要治疗和预后意义,有左心收缩储备功能的重度主动瓣狭窄患者换瓣手术后心功能可有良好恢复;无左心收缩功能储备的患者多由于长期心肌纤维化造成心肌不可逆性病变所致,行外科换瓣或TAVR治疗,效果改善不佳,故建议保守抗心力衰竭治疗。在本分析中,5例高龄重度主动脉瓣狭窄患者合并严重左心功能不全,被列为外科换瓣手术禁忌,行LDDSE检查提示有心脏收缩储备功能,建议积极行TAVR治疗。在LDDSE检查过程中和结束后,无明显不良反应,提示严重左心功能不全者可考虑行LDDSE检查明确心脏收缩储备功能情况。
由于高龄、合并其他系统疾患、左心室功能严重减低等多个原因导致约30%~40%的重度主动脉瓣狭窄患者无法耐受外科换瓣手术。而TAVR对于这些无法进行主动脉瓣置换的患者提供了一种全新的治疗方案。PARTNER、CorVlave等研究证实,TAVR已成为存在外科手术禁忌或STS评分高危患者的有效替代治疗手段[12,13]。在本分析中,5例患者无外科换瓣手术机会,如单纯药物保守治疗,预后极差。经LDDSE检查后,提示有心脏收缩储备功能,其中4例患者成功行TAVR治疗,术后心功能有明显好转甚至恢复正常,NT-proBNP持续下降,术后1个月时下降最明显。本次分析亦提示TAVR是重度主动脉瓣狭窄伴严重左心功能不全患者的有效替代治疗手段。
低流速低压差且伴左心功能不全的重度主动脉瓣狭窄患者,如有心功能储备,行TAVR较药物保守治疗心功能恢复明显,预后良好。本次分析描述了LDDSE检查在高龄、低流速低压差且伴左心功能不全的重度主动脉瓣狭窄患者的安全性及指导TAVR治疗的应用,希望能对临床工作给予提示和指导。
本研究尚存在一些不足,纳入例数稀少,因目前国内TAVR尚处于起步阶段,且只能适用于高龄、衰弱、心功能差或合并其他系统异常而不宜行外科手术治疗的患者,需行TAVR评估和治疗的例数目前非常有限。其次,缺乏对照研究,未设立药物保守治疗组和外科手术组,仅TAVR治疗前后行对比观察。第三,缺乏因心功能极差而未行LDDSE检查的患者行TAVR治疗的资料,无法完全明确LDDSE的应用价值。相信随着TAVR的发展和适应证的推广,会有更多的患者行LDDSE检查,可为临床决策提供大量的循证依据。
总之,低流速低压差且伴左心功能不全的重度主动脉瓣狭窄患者,可考虑行LDDSE检查明确有无心功能储备;如有心功能储备,在无外科换瓣的条件下建议积极行TAVR治疗改善心功能和预后。
[1] Clavel MA, Fuchs C, Burwash IG, et al. Predictors of outcomes in lowflow, low-gradient aortic stenosis: results of the multicenter TOPAS Study. Circulation, 2008, 118(14 Suppl): S234-S242.
[2] Clavel MA, Magne J, Pibarot P. Low-gradient aortic stenosis. Eur Heart J, 2016, 37: 2645-2657.
[3] Burwash IG. Low-flow, low-gradient aortic stenosis: from evaluation to treatment. Curr Opin Cardiol, 2007, 22: 84-91.
[4] Nishimura RA, Otto CM, Bonow RO, et al. 2014 AHA/ACC guideline for the management of patients with valvular heart disease: executive summary: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol, 2014, 63: 2438-2488.
[5] Defilippi CR, Willett DL, Brickner ME, et al. Usefulness of dobutamine echocardiography in distinguishing severe from nonsevere valvular aortic stenosis in patients with depressed left ventricular function and low transvalvular gradients. Am J Cardiol, 1995, 75: 191-194.
[6] Pibarot P, Dumesnil J G. Low-flow, low-gradient aortic stenosis with normal and depressed left ventricular ejection fraction. J Am Coll Cardiol, 2012, 60: 1845-1853.
[7] Clavel MA, Magne J, Pibarot P. Low-gradient aortic stenosis. Eur Heart J, 2016, 37: 2645-2657.
[8] Tribouilloy C, Levy F, Rusinaru D, et al. Outcome after aortic valve replacement for low-flow/low-gradient aortic stenosis without contractile reserve on dobutamine stress echocardiography. J Am Coll Cardiol, 2009, 53: 1865-1873.
[9] Paulus WJ, Sys SU, Heyndrickx GR, et al. Orifice variability of the stenotic aortic valve: evaluation before and after balloon aortic valvuloplasty. J Am Coll Cardiol, 1991, 17: 1263-1269.
[10] Burwash IG, Thomas DD, Sadahiro M, et al. Dependence of Gorlin formula and continuity equation valve areas on transvalvular volume flow rate in valvular aortic stenosis. Circulation, 1994, 89: 827-835.
[11] Segal J, Lerner DJ, Miller DC, et al. When should Doppler-determined valve area be better than the Gorlin formula?: Variation in hydraulic constants in low flow states. J Am Coll Cardiol, 1987, 9: 1294-1305.
[12] Smith CR, Leon MB, Mack MJ, et al. Transcatheter versus surgical aortic-valve replacement in high-risk patients. N Engl J Med, 2011,364: 2187-2198.
[13] Kappetein AP, Head SJ, Genereux P, et al. Updated standardized endpoint definitions for transcatheter aortic valve implantation: the valve academic research consortium-2 consensus document. Eur Heart J, 2012, 33: 2403-2418.
Preliminary Study of Low-dose Dobutamine Stress Echocardiogram in Patients With Low-flow/Low-gradient Aortic Stenosis Combining Ventricular Dysfunction
ZHAO Zhen-yan, SONG Guang-yuan, ZHANG Wen-jia, PEI Han-jun, WANG Jian-de, XIAO Ming-hu, YANG Yue-jin, WU Yong-jian.
Department of Cardiology, Cardiovascular Institute and Fu Wai Hospital, CAMS and PUMC, Beijing (100037), China Corresponding Author: WU Yong-jian, Email: fuwaiwyj@163.com
Objective: To explore the application value and safety of low-dose dobutamine stress echocardiogram (LDDSE) in patients of low-flow/low-gradient aortic stenosis combining left ventricular dysfunction with transcatheter aortic valve replacement (TAVR).
Methods: A total of 5 eligible consecutive patients with contradiction of routine surgical valve replacement and going to receive TAVR in our hospital from 2013-10 to 2016-07 were enrolled. The mean aortic valvegradient, maximum flow velocity, each stroke volume and ejection fraction were recorded before and during LDDSE examination. The patients having confirmed diagnosis of true severe aortic stenosis with left ventricular contractile reserve received TAVR, for those without left ventricular contractile reserve received drug therapy or TAVR conditionally. The changes of cardiac function and NT-proBNP level were observed after TAVR.
Results: All 5 patients showed positive finding in LDDSE; the mean aortic valve gradient ≥40mmHg and stroke volume≥20% implied that the patients had true severe aortic stenosis with left ventricular contractile reserve. No adverse reaction occurred during and after LDDSE. TAVR was performed in 4 patients and 1 was waiting for TAVR or balloon dilatationsince temporary lacking of valve. The post-operative cardiac function was improved in all patients and NT-proBNP level was declined continuously.
Conclusion: LDDSE examination could be considered in patients of aortic stenosis combining left ventricular dysfunction, low-flow and low-gradient to clarify ventricular contractile reserve and the severity of aortic stenosis. If the patients with ventricular contractile reserve, TAVR was recommended which was the effective treatment for relevant patients.
Echo cardiography, pressure; Aortic valve stenosis; Heart valve prosthesis implantaion
(Chinese Circulation Journal, 2017,32:372.)
2016-12-16)
(编辑:汪碧蓉)
100037 北京市,中国医学科学院 北京协和医学院 国家心血管病中心 阜外医院 冠心病诊治中心(赵振燕、宋光远、张文佳、裴汉军、杨跃进、吴永健),心脏超声诊治中心(王建德、肖明虎)
赵振燕 主治医师 博士研究生 主要从事冠心病和TAVR临床研究 Email: zhaozhenyan-82@163.com 通讯作者:吴永健 Email: fuwaiwyj@163.com
R541
A
1000-3614(2017)04-0372-05
10.3969/j.issn.1000-3614.2017.04.015
