改良DAL-HX83/90方案治疗儿童朗格汉斯细胞组织细胞增生症的疗效及预后因素
2017-04-28苗丽霞李彦珊孙岩峰金德奎张向兰刘秋玲
周 云,苗丽霞,李彦珊,孙岩峰,王 军,赵 扬,金德奎,张向兰,刘秋玲
改良DAL-HX83/90方案治疗儿童朗格汉斯细胞组织细胞增生症的疗效及预后因素
周 云,苗丽霞,李彦珊,孙岩峰,王 军,赵 扬,金德奎,张向兰,刘秋玲
目的分析改良DAL-HX83/90方案治疗儿童朗格汉斯细胞组织细胞增生症(langerhans cell histocytosis,LCH)的疗效及预后因素。方法回顾性分析武警某三甲医院儿科2003-07至2014-12采用改良DAL-HX83/90方案初治的34例LCH患儿的病例及随访资料。应用Kaplan-Meier方法计算其总体生存率(overall survival,OS)和无事件生存率(event free survival,EFS),采用Log-rank检验及多因素COX回归模型分析EFS的影响因素。结果(1)诱导治疗有效率为82.4%(28/34),化疗结束初治有效率为88.2%(30/34)。(2)所有患儿均获得有效随访,中位随访时间 48个月(13~155个月);患儿1、3、5年OS分别为100.0%、97.1%、93.7%,1、3、5年EFS分别为82.4%、70.3%、70.3%。全组复发率为26.5%(9/34),中位复发时间8个月(1~72个月)。(3)单因素分析显示,多系统受累(χ2=10.213,P=0.001)和6周诱导治疗无效(χ2=9.744,P=0.002)是影响LCH患儿EFS的因素;多因素分析表明,多系统受累是影响LCH患儿EFS的独立危险因素[相对危险度(relative risk,RR)=9.933,P=0.037]。结论改良DAL-HX 83/90方案对于单系统、无脏器功能受损LCH患儿疗效较好,不良反应少,可耐受,但对于多系统脏器功能受损者复发率仍较高,疗效有待提高。多系统受累是影响LCH患儿EFS的独立危险因素。
改良DAL-HX83/90方案;朗格汉斯细胞组织细胞增生症;预后
朗格汉斯细胞组织细胞增生症(langerhans cell histocytosis,LCH)是一种少见的以单核-吞噬细胞系统特定的树突细胞增生为特点的疾病[1],为儿童最常见的组织细胞疾病。该病发病高峰年龄为1~4岁,也可出生即发病[2],男女发病比例1.2~2∶1[3]。研究报道儿童发病率不一,为3.5~7.0/100万[4]。LCH临床表现具有异质性,除膀胱、肾上腺和性腺目前尚无受累的报道,其他器官均可累及。轻者仅累及皮肤、单一骨损害,重者可累及多器官系统并造成重要脏器(如肝、脾、肺和造血系统)功能损害。LCH患儿的总体病死率约为15.0%,相当一部分患儿病情进展或反复,远期后遗症发生率30.0%~40.0%[5]。近年来,随着临床分类分型标准的完善,基于危险度分层治疗策略的实行,化疗方案的不断优化,LCH患儿的预后得到明显改善,多系统LCH的5年生存率从81.0%提高到94.0%,但复发率和尿崩症的发生率未见明显降低[6]。因此,加强对LCH患儿长期无事件生存率(event free survival,EFS)影响因素的认识,对于改善LCH患儿的远期疗效尤为重要。本研究回顾性分析武警某三甲医院2003-07至2014-12采用改良DAL-HX83/90方案初治的34例LCH患儿治疗、转归等情况,旨在为改善儿童LCH的疗效和预后提供一定的临床依据。
1 资料与方法
1.1一般资料 LCH患儿共43例,其中3例确诊后放弃治疗,3例未完成诱导治疗,3例复发后改变化疗方案,最终34例应用改良DAL-HX83/90方案完成治疗并获得完整随访。
1.2诊断及分组标准 按照2009年国际组织细胞协会提出的LCH三级诊断标准[7],经病理、免疫组化染色(CD1a和/或CD207)或电镜找到具有Birbeck颗粒的组织细胞以明确诊断。
依据完整的病史、症状、体征、实验室检查(血常规、肝肾功能、内分泌功能)、影像学检查如X线片、计算机X线断层扫描(computed tomography,CT)、头颅磁共振成像(magnetic resonance imaging,MRI)、B型超声及骨髓细胞形态学等相关辅助检查评估器官功能,将所有患儿分为三组治疗,I组:骨骼或软组织的单部位损害,无器官功能异常;Ⅱ组:骨骼或软组织两个以上部位损害,无器官功能异常;Ⅲ组:有器官功能异常(肝脏、肺或骨髓)[8]。
1.3治疗方案 本研究采用改良奥地利/德国的DAL-HX83/90方案作为治疗方案[9],并在原方案基础上做了如下调整:诱导阶段三组患儿均加服6-巯基嘌呤;Ⅲ组患儿在原诱导方案基础上加用甲氨蝶呤和环磷酰胺;维持治疗阶段Ⅱ、Ⅲ组患儿加用甲氨蝶呤;予以鬼臼噻酚甙和足叶乙甙交替使用;长春新碱代替长春花碱。具体化疗方案为:三组均先给予6周诱导治疗,然后维持治疗至52周,维持治疗期间每3周1次强化治疗,治疗结束后停药观察。所有患儿于化疗期间均给予水化、碱化、止吐、保心、保肝等对症支持治疗。
1.4疗效评价 参照1991 年国际组织细胞协会制定的LCH 疗效判定标准[9]。治愈:症状和(或)客观征象完全消失;好转:症状和(或)客观征象消退,无新病灶出现;稳定:症状和(或)客观征象持续存在,但无新病灶出现;进展或恶化:症状和(或)客观征象较确诊时有进展,(或)出现新病灶或旧病灶复发。治愈及好转判定为有效。
1.5生存分析 通过查阅住院病历资料、复诊和电话随访,随访起始时间为首次治疗时间,随访终点为2016-06-30。EFS时间指化疗开始到第1次事件发生或末次随访日期的时间间隔;事件包括:复发、进展、死亡或继发肿瘤。总生存时间指化疗开始到死亡的时间间隔。截至随访日期未复发或死亡的以截尾数据纳入分析。依据2009年国际组织细胞协会发布的LCH评估与治疗指南中的分类标准和器官受累标准[7],按照发病年龄、性别、有无皮肤及淋巴结受累、有无多部位骨质受累、有无危险器官受累(累及肝脏、脾、肺和造血系统)、有无中枢受累、多系统是否受累、诱导治疗疗效9个临床因素对34例患儿进行分组,分析各组生存曲线分布和各临床因素的关系,了解影响LCH患儿EFS的相关因素。
1.6安全性评价 每个疗程治疗前均测体重、血尿常规、肝功能(谷丙转氨酶、转肽酶)、肾功能(肌酐)、心电图、胸片;每次治疗结束后复测体重、血常规、小儿生化。体重评判参照实用儿科学儿童身高体重生长量表[4];毒副反应参考化疗药物毒性反应分级标准(national cancer institute common terminology criteria adverse events,NCI-CTCAE)[10]。
1.7统计学处理 采用SPSS 17.0软件进行数据分析,调用Kaplan-Meier方法进行生存分析,单因素分析采用Log-rank检验,多因素分析采用COX比例风险模型分析,以双侧P<0.05为差异有统计学意义。
2 结 果
2.1一般资料 34例患儿中,男23例,女11例,男女比例为2.1∶1。发病年龄6个月~15岁,中位年龄4岁;三个治疗组Ⅰ组9例,Ⅱ组19例,Ⅲ组6例。其中皮肤受累5例(14.7%),淋巴结受累10例(29.4%),多部位骨质受累19例(55.9%),危险器官受累5例(14.7%),垂体受累4例(11.8%),其中发生尿崩症3例(8.8%),多系统者18例(52.9%)。
2.2疗效 34例患儿经6周诱导治疗结束时28例病情好转,4例稳定,2例进展,早期有效率(完全缓解+好转)为82.4%(28/34);化疗结束时治愈8例,好转22例,稳定2例,死亡2例,总的初治有效率为88.2%(30/34)。所有患儿均获得有效随访,随访时间13~155个月,中位随访时间 48个月。Kaplan-Meier生存分析显示,全组病例1、3、5年总体生存率(overall survival,OS)分别为100.0%、97.1%、93.7%,1、3、5年EFS分别为82.4%、70.3%、70.3%(图1,图2)。

图1 34例LCH患儿总生存函数曲线

图2 34例LCH患儿无事件生存曲线
全组共9例复发,复发率26.5%(9/34),中位复发或进展时间为8个月(1~72个月)。Ⅰ组、Ⅱ组、Ⅲ组复发率分别为11.1%(1/9)、36.8%(7/19)、16.7%(1/6)。8例为原发部位复发,6例在原发部位以外出现了新病灶,5例在原发部位及其以外均出现了病灶,新病灶包括包括新发骨损害、新发包块、尿崩症状、外耳道流脓血、脑白质脱髓鞘变、下牙槽骨萎缩、皮疹。4例复发了1次,5例复发了2次。复发的9例中,3例予以再诱导、维持和强化治疗,至随访截止期2例获得好转,1例病情稳定;4例诱导结束后出现进展,升级为Ⅲ组方案维持治疗,治疗结束后3例好转,1例稳定;2例复发后继续予以维持治疗疗程结束后均好转;2例诱导无效因病情进展而死亡。随访截止,共发生后遗症6例,脑白质脱髓鞘变1例,扁平椎1例,患侧视力下降1例,尿崩症3例,其中1例合并牙槽骨萎缩。本组随访无继发肿瘤发生。
2.3预后相关因素分析 对纳入的9个预后相关临床因素进行单因素分析显示:单系统受累组3年EFF为100.0%明显高于多系统受累组的47.4%,差异有统计学意义(χ2=10.213,P=0.001);诱导治疗有效组3年EFS为82.1%明显高于无效组的16.7%,差异有统计学意义(χ2=9.744,P=0.002)。发病年龄、性别、皮肤及淋巴结是否受累、多部位骨质是否受累、有无危险器官受累、有无中枢受累对EFS影响无统计学意义(表1)。采用COX逐步回归模型对EFS单因素分析中有统计学意义的2个临床因素进行多因素分析,结果显示多系统受累是影响LCH患儿EFS的独立危险因素[相对危险度(relative risk,RR)=9.933,P=0.037,表2]。
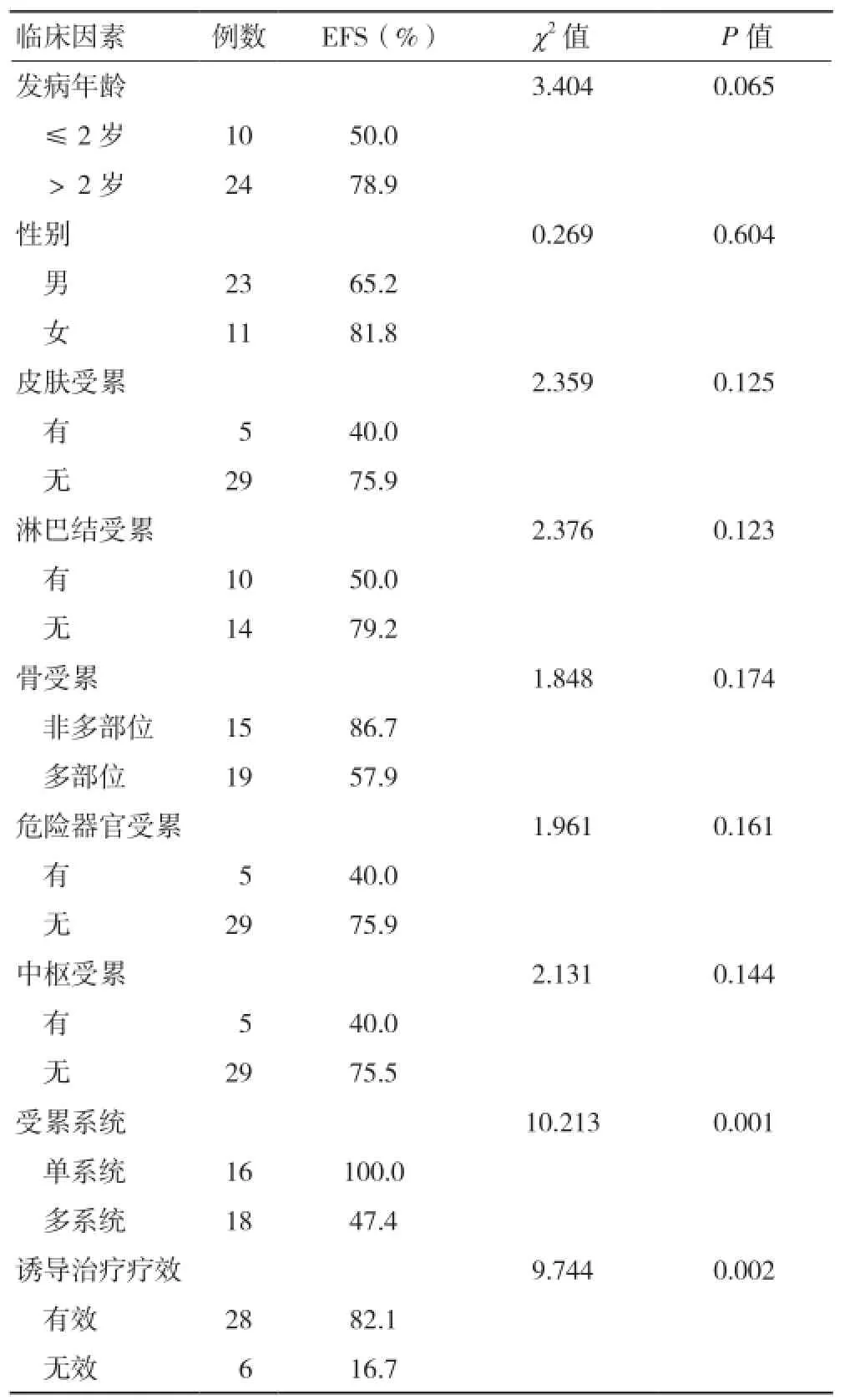
表1 34例LCH患儿3年EFS单因素分析
2.4安全性评价 32例存活患儿体重均在同龄儿童正常体重范围内;血常规均发现0~4级的三系降低,经对症治疗或化疗间期自行恢复正常;小儿生化及心电图等检查示肝、心功能损伤均为0~2级,肾功能损伤为0~1级,经保心、保肝、碱化、水化治疗和随着化疗药物的停用均恢复正常,为可逆性损伤。

表2 34例LCH患儿EFS多因素分析结果
3 讨 论
LCH是一组以朗格汉斯细胞克隆性增生和聚集为特点的疾病,临床表现多样,病灶可呈孤立局限或弥漫增生,可仅限于单个器官,也可多脏器侵润,治疗后轻者自发消退,重者全身播散甚至危及生命。由于本病相对罕见,关于其究竟是免疫系统失调导致的反应性增生还是肿瘤性疾病尚未定论,目前国内外尚缺乏统一的诊疗指南,多药联合化疗是目前本病的主要治疗措施。
DAL-HX83/90方案和LCH-I方案均为早期治疗LCH患儿的代表性方案。LCH-I方案6周诱导治疗反应率为49.0%,复发率55.0%,5年存活率可达80.0%。DAL-HX83/90方案将诱导治疗的反应率提高至80.0%,复发率降至30.0%,5年存活率为81.0%[11],即DALHX83/90 方案的疗效优于LCH-I方案。因此本研究从2003-07至2014-12对收治的34例LCH患儿采用改良DAL-HX83/90方案治疗,发现改良方案的总体治疗效果较好,甚至优于原方案。但治疗分组方面,由于本方案较原方案稍作修改:将单部位骨质受损者者也纳入Ⅰ组(原方案为多部位骨质受累)化疗,可能对治疗结果的改善产生一定的影响。
本研究中所有患儿总的初治有效率为88.2%,复发率26.5%,3年OS为97.1%,3年EFS为70.3%,与蒋俊晔等[12]研究结果相似。但本组患儿Ⅱ组、Ⅲ组复发率分别为36.8%、16.7%,Ⅲ组复发率明显低于Ⅱ组,分析原因为Ⅲ组仅6例患儿,可能由于例数较少,造成了结果的偏差;而Ⅱ组复发率高,可能与该组患儿家属的就诊意识差、院外治疗的依从性较差等有关。
目前关于LCH患儿预后影响因素的研究较多,本研究将纳入对象的发病年龄、性别、受累部位(有无皮肤、淋巴结、多部位骨质、危险器官、中枢)、有无多系统受累、诱导治疗疗效等预后相关临床因素进行单因素分析,并对其中有统计学意义的因素进行多因素分析。结果发现以2岁为分界点,≥2岁与<2岁患儿3年EFS差异无统计学意义,即年龄不是影响LCH患儿EFS的因素,目前对于发病年龄是否为LCH的预后影响因素尚存在争议[13,14],需扩大样本量进一步验证;另外还发现性别、皮肤受累、淋巴结受累不是LCH患儿EFS的影响因素。既往研究对于多部位骨质是否影响LCH患儿EFS观点尚未统一[15,16],本研究结果显示多部位骨质受累不是影响患儿EFS 的危险因素;同时无危险器官受累者3年EFS为75.9%高于危险器官受累患儿的40.0%,但差异无统计学意义,与Totadri等[17]的研究结论不一致,考虑与本研究为单中心研究,样本量较少有关。另外发现中枢神经系统受累不是影响患儿预后的危险因素,与文献[18]报道相一致。
多系统受累被证实是儿童LCH重要的预后不良因素。单器官系统病灶可自发消退,缓慢进展,而多系统病变具有侵袭性。本研究单因素分析显示,多系统LCH患儿3年EFS显著低于单系统LCH组,多因素分析进一步证实多系统受累是影响LCH患儿EFS的独立危险因素,该结论与Kim等[14]的研究结果一致。诱导治疗疗效被认为是LCH患儿的重要预后因素。患儿对诱导治疗疗效的反应一定程度上反映了其对化疗药物的敏感性、耐药性和疾病本身的严重程度。本研究中2例死亡患儿均为诱导结束反应为病情进展,且本组资料统计分析生存曲线显示诱导治疗有效组较无效组EFS更高,表明诱导治疗疗效是EFS的影响因素,这与吴方方等[19]的研究发现一致。然而多因素分析无统计学意义,可能与本研究样本例数较少有关,差异未能显现,也可能与人群的选择偏倚有关。
另外,本组患儿最常见的不良反应包括不同程度的骨髓抑制、轻度的肝肾功能损伤、心脏毒性,经对症治疗后均恢复正常;且所有患儿体格生长发育均正常,未发生治疗相关性死亡,随访时间最长为155个月无继发肿瘤发生,提示本方案安全可行。
总之,本研究发现采用改良DAL- HX 83 /90方案治疗儿童LCH患者,对于单系统、无脏器功能受损者疗效较好,不良反应少可耐受,但对于多器官系统、脏器功能受损者复发率仍较高,疗效有待提高。多系统受累是影响LCH患儿EFS的独立危险因素。近年来,关于BRAF V600E基因突变与LCH患儿临床相关性研究逐步受到重视。因此今后的研究中,将开展BRAF V600E基因的检测,更合理化危险度分层,也期望有更多的多中心、大样本研究进一步证实相关因素对LCH预后的影响意义。
[1]Bakry O A, Samaka R M, Kandil M A,et al. Indeterminate cell histiocytosis with naive cells [J]. Rare Tumors, 2013, 5(1): e13. DOI: 10.4081/rt.2013.e13.
[2]Degar B A, Rollins B J. Langerhans cell histiocytosis: malignancy or inflammatory disorder doing a great job of imitating one?[J]. Dis Model Mech, 2009, 2(9-10): 436-439. DOI: 10.1242/dmm.004010.
[3]Horibe K, Saito A M, Takimoto T,et al. Incidence and survival rates of hematological malignancies in Japanese children and adolescents( 2006-2010): based on registry data from the Japanese Society of Pediatric Hematology [J]. Int J Hematol, 2013, 98(1): 74-88. DOI: 10.1007/ s12185-013-1364-2.
[4]胡亚美, 江载芳. 诸福棠实用儿科学[M]. 8版. 北京:人民卫生出版社, 2015: 1945-2893.
[5]Haupt R, Minkov M, Astigarraga I,et al. Langerhans cell histiocytosis( LCH): guidelines for diagnosis, clinical work-up,and treatment for patiems till the age of 18 years [J]. Pediatr Blood Cancer, 2013, 60(2): 175-184. DOI: 10.1002/pbc.24367.
[6]Morimoto A, Ikushima S, Kinugawa N,et al. Improved outcome in the treatment of pediatric multifocal Langerhans cell histiocytosis: results from the Japan Langerhans Cell Histiocytosis Study Group-96 protocol study [J]. Cancer, 2006,107(3): 613-619. DOI:10.1002/cncr.21985.
[7]Wu S H. Introduction of guidelines on evaluation and treatment of langerhans cell histiocytosis [J]. Zhonghua Er Ke Za Zhi, 2012, 50(2):155-158. DOI: 10.3760/cma. j.issn.0578-1310.2012.02.016.
[8]The Writing Group of the Histiocyte Society. Histiocytosis syndromes in children [J]. Lancet, 1987, 329(8526): 208-209. DOI: 10.1016/S0140-6736(87)90016-X.
[9]Gadner H, Grois N, Arico M,et al. A randomized trial of treatment for multisystem Langerhans' cell histiocytosis [J]. J Pediatr, 2001, 138(5): 728-734. DOI: 10.1067/ mpd.2001.111331.
[10]Trotti A, Golevas A D, Setser A,et al. CTCAE v3.0: develoment of a comprehensive grading system for the adverse effects of cancer treatment [J]. Semin Radiat Oncol, 2003, 13(3): 176-181. DOI: 10.1016/S1053-4296(03) 00031-6.
[11]吴 鹏, 方拥军, 何璐璐, 等. 儿童郎格罕斯细胞组织细胞增生症83例临床分析[J]. 南京医科大学学报(自然科学版), 2015, 35(1): 86-89. DOI:10.7655/ NYDXBNS20150121.
[12]蒋俊晔, 高怡瑾, 王宏胜, 等. 82例朗格罕斯细胞组织细胞增生症临床分析[J]. 中国小儿血液与肿瘤杂志, 2014, 19(1): 21-25. DOI : 10.3969 /j.issn.1673-5323. 2014.01.006.
[13]Lee J W, Shin H Y, Kang H J,et al. Clinical characteristics and treatment outcome of Langerhans cell histiocytosis: 22 years' experience of 154 patients at a single center [J]. Pediatr Hematol Oncol, 2014, 31(3): 293-302. DOI: 10.3109/08880018.2013.865095.
[14]Kim B E, Koh K N, Suh J K,et al. Clinical features and treatment outcomes of Langerhans cell histiocytosis: a nationwide survey from Korea histiocytosis working party [J]. J Pediatr Hematol Oncol, 2014, 36(2): 125-133. DOI: 10.1097/MPH.0000000000000054.
[15]Jubran R F, Marachelian A, Dorey F,et al. Predictors of outcome in children with Langerhans cell histiocytosis [J]. Pediatr Blood Cancer, 2005, 45(1): 37-42. DOI: 10.1002/pbc.20364.
[16]张 莉, 廉红云, 马宏浩, 等. 单器官受累朗格罕细胞组织细胞增生症112例[J]. 中华实用儿科临床杂志, 2016, 31(15): 1172-1174. DOI: 10.3760/cma.j.issn. 2095-428X.2016.15.014.
[17]Totadri S, Bansal D, Trehan A,et al. The 5-Year EFS of multisystem LCH with risk-organ involvement is suboptimal: A single-center experience from India [J]. J Pediatr Hematol Oncol, 2016, 38(1): e1-e5. DOI: 10.1097/MPH.0000000000000414.
[18]Chellapandian D, Shaikh F, van den Bos C,et al. Management and outcome of patients with Langerhans cell histiocytosis and single-bone CNS-risk lesions: A multiinstitutional retrospective study[J]. Pediatr Blood Cancer, 2015, 62(12): 2162-2166. DOI: 10.1002/pbc.25645.
[19]吴方方, 高怡瑾, 潘 慈, 等. 儿童多脏器受累朗格汉斯细胞组织细胞增生症131例临床研究[J]. 中华儿科杂志, 2016, 54(5): 349-353. DOI: 10.3760/cma.j.issn. 0578-1310.2016.05.008.
(2016-11-27收稿2017-03-12修回)
(本文编辑 付 辉)
Eff i cacy and prognostic factors of langerhans cell histocytosis in children treated with modif i ed DAL-HX 83/90 protocol
ZHOU Yun, MIAO Lixia, LI Yanshan, SUN Yanfeng, WANG Jun, ZHAO Yang, JIN Dekui, ZHANG Xianglan, and LIU Qiuling. Department of Pediatrics, General Hospital of Chinese People's Armed Police Force, Beijing 100039, China
Corresponding author: LIU Qiuling, E-mail: wj670@vip.sina.com
ObjectiveThis study objective was to analyse the efficacy and prognostic factors of modified DAL-HX 83/90 protocol in treatment of langerhans cell histocytosis (LCH) in children.MethodsA retrospective analysis was conducted on the clinical records and follow-up data of 34 children with LCH treated with modified DAL-HX 83/90 protocol in a third-grade class-A hospital of PAP from July 2003 to December 2014. The Kaplan-Meier estimator was applied to calculate the overall survival (OS) and event free survival (EFS), log-rank test and multivariate Cox proportion hazard regression model were used for the analysis of the factors impacting on EFS.Results(1) The effective rate of inductive treatment was 82.4% (28/34), the effective rate of the initial treatment after chemotherapy was 88.2% (30/34). (2) All the children with LCH were followed up effectively, the median follow-up time was 48 months (13~155 months); among the 34 children with LCH, the 1-year OS, 3-year OS and 5-year OS were 100.0%, 97.1% and 93.7% and 1-year EFS, 3-year EFS and 5-year EFS were 82.4%, 70.3% and 70.3%, respectively. The recurrence rate was 26.5% (9/34), the median time to relapse was 8 months (1~72 months). (3) The univariate analysis showed that multisystem involvement (χ2=10.213,P=0.002) and ineffective inductive treatment (χ2=10.213,P=0.001) were the risk factors of EFS in children with LCH. The multivariate analysis revealed that multisystem involvement was the independent risk factor of EFS in children with LCH (RR=9.933,P=0.037).ConclusionsThe modified DAL-HX 83/90 protocol is an effective and tolerable therapy for LCH children without organ dysfunction and has less adverse reactions, while its curative effect on patients with multiple organ dysfunction needs to be improved. Multisystem involvement is the independent risk factor of EFS in children with LCH.
modified DAL-HX 83/90 protocol; langerhans cell histiocytosis; prognosis
R725.5
10.13919/j.issn.2095-6274.2017.04.005
100039 北京,武警总医院儿科
刘秋玲,E-mail:wj670@vip.sina.com
