pH值对酚醛树脂性能的影响*
2017-04-27高士帅赵临五刘美红陈日清储富祥
高士帅 赵临五 刘美红 陈日清 储富祥
木材工业中使用的酚醛树脂是由甲醛和苯酚在碱性条件下经羟甲基化和缩聚过程合成的热固性甲阶酚醛树脂,具有较好的胶接性能[1]、优良的耐候性、耐沸水性和耐化学腐蚀性,在木材工业中被广泛应用于制造室外级胶合板、集装箱底板等人造板[2,3]。在合成过程中,催化剂的种类和用量对酚醛树脂的结构和性能会产生很大的影响。Ning Yan[4]等通过研究不同pH值条件下合成的酚醛树脂的固化行为,发现随着pH值升高,固化后的树脂中亚甲基醚键含量逐渐减少。PIZZI A[5]研究了高碱性条件下,pH值对酚醛树脂的结构和固化速度的影响,发现pH值高于10以后,树脂的凝胶时间反而明显变长。Luukko P[6]等分别研究了氢氧化钠的用量对浸渍用酚醛树脂和胶合板用酚醛树脂的羟甲基化阶段和缩聚反应阶段的影响,结果表明氢氧化钠对合成过程中的两个阶段均有影响,氢氧化钠用量越大,酚羟基邻位的缩聚反应活性越高,羟甲基的含量呈略微升高的趋势,树脂的固化温度却呈降低趋势。Wang Jian和Zhang Yifan[7]通过实验对比了氯化钙、氢氧化钡和氯化镁对酚醛树脂的催化作用,发现在中性或接近中性的条件下氯化钙和氢氧化钡的催化作用明显强于氯化镁的催化作用。该实验探究了合成阶段和固化阶段的pH值对PF树脂的理化性能及其压制的胶合板性能的影响。
1 试验方法
1.1 主要原料与试剂
甲醛溶液、苯酚、尿素、氢氧化钠及氧化钙均为分析纯,南京化学试剂有限公司。
1.2 试验仪器
Dv-Ⅱ+Pro型旋转黏度测定仪,美国BROOKFIELD公司;IS10 型傅里叶变换红外光谱仪(FT-IR),美国尼高力公司;Bruker AVANCE3 400 MHz核磁共振仪;新三思(SANS)CMT4000系列万能材料试验机,深圳新三思材料检测有限公司。
1.3 不同pH值PF的制备
1.3.1 配方
甲醛与苯酚的物质的量之比为2.27,尿素、氧化钙分别为苯酚质量的14%和0.24%,氢氧化钠溶液适量。
1.3.2 制备工艺
将苯酚及氧化钙加入到四口烧瓶中,并加入少量的水,升高温度至75 ℃保温15~20 min,;加入第一批甲醛(此时甲醛和苯酚的物质的量之比约为1.0),升温至90 ℃,反应60 min;加入第二批甲醛(此时甲醛和苯酚的物质的量之比约为1.5),控制反应温度为90 ℃,依据不同pH值要求,滴加不同量的氢氧化钠水溶液,反应70 min;加入第三批甲醛(此时甲醛和苯酚的物质的量之比约为2.27),控制反应温度为85~88 ℃,以氢氧化钠水溶液分别调节树脂最终pH值为10、11、12和13,反应50 min;加入苯酚质量14%的尿素,控制温度为85℃,反应至树脂黏度为(150±20)mPa.s,降温至40 ℃出料,并调节固含量为44.0%。
1.4 杨木和桉木三层胶合板的制备
单板:杨木、桉木单板均为400 mm×400 mm×1.5 mm,含水率8 %~12 %;调胶工艺:加入酚醛树脂质量20 %~35 % 的面粉,搅拌均匀;施胶量:280~320 g/m2(双面) 。
压板工艺:室温下0.8 MPa预压1 h,闭合陈放1~2 h,热压温度:125~130 ℃,热压压力1.0 MPa(杨木)、1.2 MPa(桉木),热压时间:60 s/mm。
1.5 树脂及胶合板性能测试
1.5.1 树脂性能测试
pH值、黏度、固体含量、游离苯酚含量、游离甲醛含量均按GB/T 14074—2006《木材胶粘剂及其树脂检验方法》测定。
1.5.2 胶合板性能检测
压制的胶合板室内放置5~6 d后检测。胶合强度采用新三思(SANS)CMT4000系列万能材料试验机按GB/T 9846.3—2004《胶合板》第3部分:普通胶合板通用技术条件Ⅰ类胶合板标准测试。甲醛释放量按GB/T 17657—2013《人造板及饰面人造板理化性能试验方法》干燥器法进行检测。
1.6 红外光谱
冷冻干燥后不同pH值的PF树脂在Nicolet 550 型FT-IR红外分析仪上采用KBr压片法测定。
1.7 核磁共振碳谱
以D2O为溶剂、TMS为内标,通过Bruker AVANCE3 400 MHz核磁共振仪对不同pH值的PF树脂进行测定,扫描频率为100 MHz。
1.8 树脂固化速度
利用HAAK MARS Ⅱ旋转流变仪,采用动态温度扫描模式,频率为1 Hz,升温速度5 ℃/min,升温范围80~200℃。
2 结果与讨论
2.1 树脂理化性能分析
为了对比研究pH值对PF树脂的游离甲醛、游离苯酚、凝胶时间和贮存时间等理化性能的影响,该实验控制PF树脂的最终黏度及固含量不变,合成了最终pH值分别为10、11、12和13四种PF树脂,分别记为PF1、PF2、PF3和PF4,并对其理化性能进行了分析。
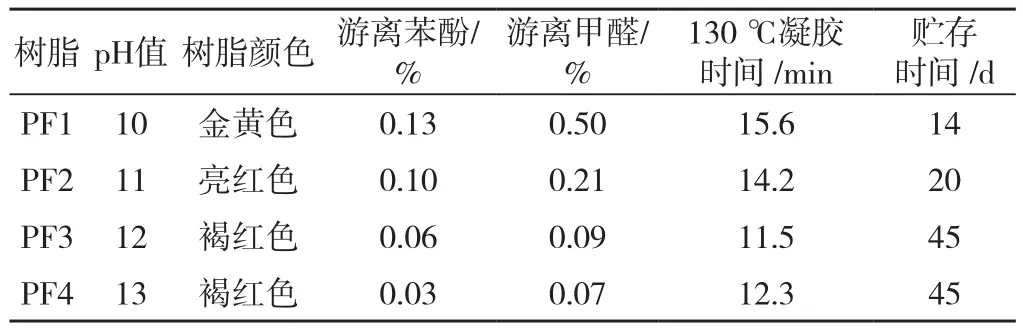
表1 不同pH值PF树脂的理化性能Tab.1 Physical and chemical properties of PF resin with different pH
由表1可以看出, PF树脂随着pH值的升高,树脂的颜色由金黄色逐渐变深,pH值较高的PF3和PF4呈现褐红色,游离苯酚和游离甲醛的含量均呈不同程度的下降趋势。树脂PF1、PF2和PF3的凝胶时间依次递减,但是,树脂PF4的凝胶时间比PF3的凝胶时间增长。pH值相对较低的树脂PF1和PF2的游离甲醛含量分别高达0.50%和0.21%,pH值为12和13的树脂游离甲醛含量均远低于PF1和PF2的游离甲醛含量。高pH值有利于降低树脂中的游离苯酚,造成这一现象的原因可能是高碱性条件有利于酚羟基中的氢被氢氧根离子夺取,形成反应活性较高的酚盐形式,使甲醛的亲电加成更易发生。甲醛在碱性条件下除了主要和苯酚发生反应外,还可以发生Cannizzaro[8]反应,并且pH值越高,反应速度越快,导致游离甲醛含量的降低速度快于游离苯酚含量。中性或弱碱性环境有利于尿素与甲醛发生加成反应,生成羟甲基脲,树脂PF1、PF2、PF3和PF4的pH值依次升高,树脂中羟甲基脲的含量依次降低。在室温中羟甲基脲容易导致PF树脂发生凝胶,所以树脂的pH值越低,贮存时间越短。
2.2 胶合板性能检测
2.2.1 pH值对胶合板性能的影响
为了对比研究pH值对PF树脂胶合强度和甲醛释放量的影响,将pH值为10的PF树脂的pH值分别调节为11、12和13,分别记为 PF5、PF6和PF7,并利用PF1~PF7七个PF树脂分别压制了杨木和桉木两种不同材质的三层胶合板。取4次重复压板的胶合强度和甲醛释放量平均值列于表2。
由表2可以看出,不同pH值PF树脂压制的杨木和桉木三层胶合板均能满足我国Ⅰ类胶合板要求,并且杨木三层胶合板的胶合强度均高于桉木三层胶合板,其原因分为两个方面,一方面杨木的密度小于桉木,其细胞壁较为松散,在冷压和固化过程中有利于树脂通过细胞壁深入细胞腔生成更多、更大的胶钉,从而增大了胶合强度;另一方面与杨木和桉木表面的pH值有关,杨木表面呈碱性,有利于树脂固化,而桉木表面呈酸性,不利于树脂固化。观察PF1~PF3可知pH值由10升高到12时,胶合板的胶合强度逐渐增大,但是当pH值升高到12以上后胶合强度开始出现减小趋势。另外,当PF树脂的pH值为10时,杨木和桉木三层胶合板及pH值11时的杨木胶合板的甲醛释放量只能勉强达到我国E2级胶合板甲醛释放量要求。但是,PF3和PF4压制的杨木三层胶合板和桉木三层胶合板的甲醛释放量均迅速下降,达到我国E0级胶合板要求,与PF树脂中游离甲醛含量的变化趋势相一致。

表2 pH值对三层胶合板性能的影响Tab.2 Effect of pH on the performance of three-layers plywood
对比树脂PF1、PF5、PF6和PF7压制的杨木三层胶合板和桉木三层胶合板的胶合强度及甲醛释放量的变化规律,可以发现胶合板胶合强度变化不大,说明pH值主要通过改变合成过程中PF树脂的结构影响胶合强度;甲醛释放量的变化趋势与树脂PF1、PF2、PF3和PF4压制的胶合板的甲醛释放量变化趋势相一致,但是对比同等pH值水平PF树脂的甲醛释放量可以发现,树脂PF5、PF6和PF7压制的胶合板的甲醛释放量明显偏高,说明树脂的甲醛释放量除了与游离甲醛的含量有关,还与树脂结构相关。
2.2.2 热压时间的影响
为了探究pH值与树脂的固化速度之间的关系,该实验中每毫米单板的热压时间分别设置为30、60、90 s和120 s,以得到不同固化程度的杨木三层胶合板。不同热压时间的杨木胶合板的胶合强度的变化情况如图1所示。
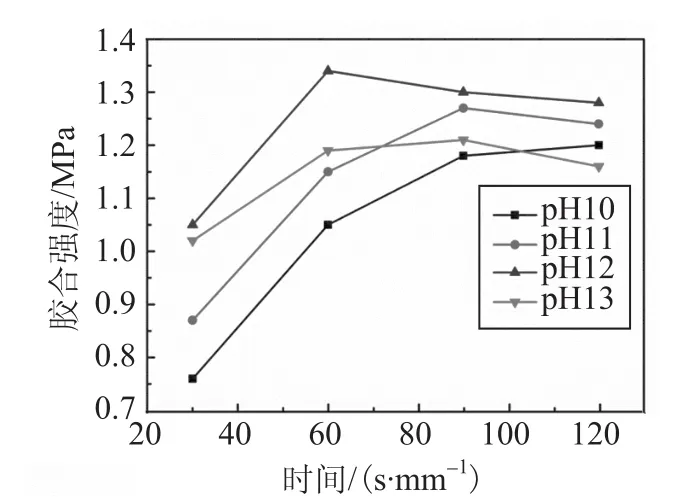
图1 热压时间对胶合板性能的影响Fig.1 Effect of pressing time on the performance of plywood
由图1可以发现pH值为10的PF在热压时间为120 s/mm单板的条件下,才能基本实现完全固化;pH值为11的PF在热压时间为90 s/mm单板的条件下,可以实现完全固化;pH值为12、13的PF在热压时间为60 s/mm单板的条件下,就已经实现完全固化,并且当热压时间延长后,pH值为12、13的PF胶合强度均出现不同程度的衰减。另外,对比完全固化后不同pH值的PF树脂的实验结果,发现其胶合强度呈现出先增大后减小的变化规律,与2.2.1的实验结果相一致。
2.3 红外光谱分析
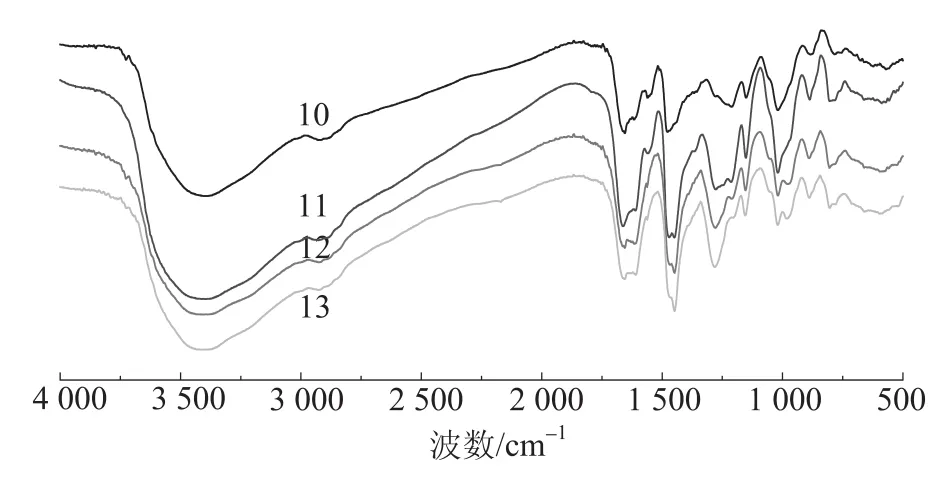
图2 不同pH值PF树脂红外光谱Fig.2 FT-IR spectra of phenolic resin with different pH
根据相关文献[9-11]可知,3 400 cm-1附近是羟基的伸缩振动吸收峰,2 910 cm-1附近为亚甲基的碳氢伸缩振动吸收峰,1 650 cm-1附近是尿素和羟甲基脲的羰基伸缩振动吸收峰,1 600 cm-1和1 580cm-1两处是苯环C=C双键的振动吸收峰,1 477 cm-1附近是亚甲基桥以邻-对位连接方式产生的变形振动吸收,1 211 cm-1附近是酚羟基的C—O的伸缩振动吸收峰,1 151 cm-1附近是醚键CH2—O—CH2的对称伸缩振动吸收峰;1 020 cm-1附近是羟甲基的C—O伸缩振动吸收峰,883 cm-1和786 cm-1附近分别是对位取代苯和邻位取代苯的—CH—面外弯曲振动吸收峰。由图2可知,随着pH值的升高,1 477 cm-1附近的邻-对位亚甲基桥的变形振动吸收逐渐增强,说明pH值升高促进了邻-对位亚甲基桥的生成;786 cm-1处的吸收峰逐渐增强,这说明高碱性条件更有利于邻位取代的发生。
2.4 核磁共振碳谱分析
图3是不同pH值酚醛树脂的13C-NMR谱图,结合相关文献报道[12-15]将大部分化学位移对应的化学结构依次列于表3。由图3可以发现pH值为10和11的PF树脂的13C-NMR谱图十分相近,这表明pH值10~11之间酚醛树脂的结构基本保持一致。特别值得注意的有以下4点:

图3 不同pH值PF树脂的核磁共振碳谱Fig.3 13C-NMR spectra of phenolic resin with different pH
1)无论酚羟基邻、对位是否发生取代,随着pH值由10升高到13,苯环中与酚羟基相连的C1的核磁共振峰均向低场方向移动,造成这一现象的原因是随着pH值的升高,酚羟基转变为氧负离子,诱导催化作用增加,这种变化有利于加成和缩聚过程,苯环中其他位置的碳也呈现出微弱的向低场移动的趋势,颜宁等在研究尿素改性酚醛树脂的过程中有着相同的发现[4];
2)观察pH值为12和13的两种树脂的核磁共振碳谱,可以发现118.7~118.9ppm和124.6 ppm位置出现了少量的未被取代的苯环C2/C6和C4;
3)与Ning Yan[4]和Bunichiro Tomita[16]的研究结果类似, pH值为10和11的两种树脂的核磁共振碳谱中81.8 ppm处的信号峰对应为HOCH2OH(甲醛与水发生图4所示的反应生成的甲二醇),说明PF树脂的pH值越高,游离甲醛含量越低,与表1中化学滴定法测定的结果一致;
4)四种树脂的核磁共振碳谱在170.7~171.1 ppm处均存在一个尖锐的信号峰,可能是甲醛发生Cannizzaro反应以及甲醛被空气中的氧气氧化生成甲酸,甲酸在碱性条件下生成COONa的信号峰。
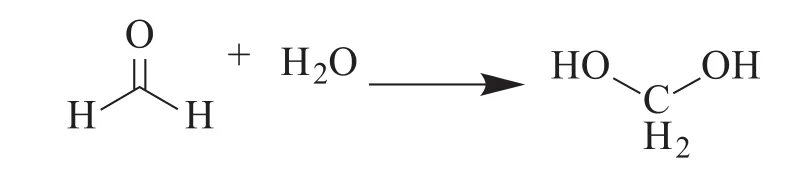
图4 甲醛和水的加成反应Fig.4 Addition reaction of formaldehyde and H2O
2.5 树脂固化速度分析
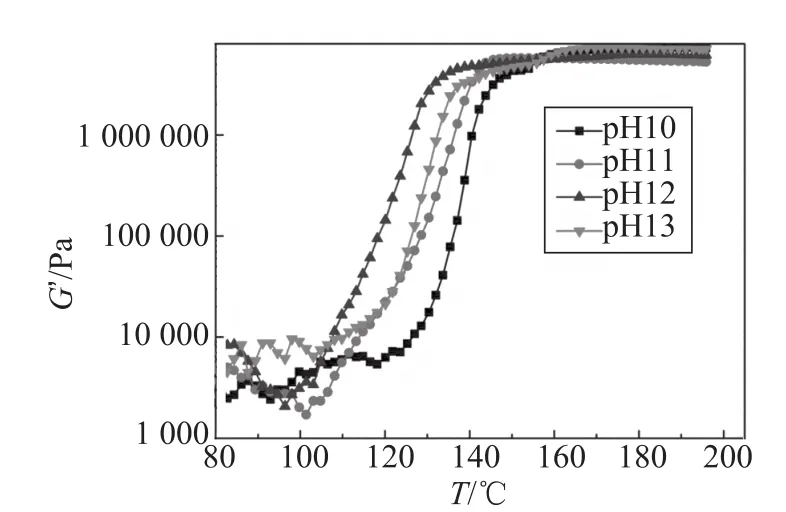
图5 不同pH值PF树脂升温固化过程弹性模量变化曲线Fig.5 G 'curves of temperature curing process of phenolic resin with different pH
图5展示了相同温度变化过程中不同pH值PF树脂的弹性模量变化情况,由图可知pH值为10~13的酚醛树脂的起始固化温度分别为118、103、96 ℃和105℃,固化基本完成的温度分别为145、140、130 ℃和135℃。由树脂固化曲线可以发现树脂固化速度由快到慢的顺序是pH值为12、13、11、10的PF树脂,但是固化后的树脂弹性模量区别不大。pH值为12的PF树脂固化速度最快,它的起始固化温度和固化基本完成时的温度分别比固化速度最慢的pH值为10的PF树脂降低了22 ℃和15 ℃。 pH值为13的PF树脂的固化速度介于pH值为12、11的PF树脂之间,且更接近于pH11的PF树脂的固化速度。该实验结果与测定的树脂的凝胶时间及胶合板的胶合强度的变化趋势相似,充分说明了pH值对酚醛树脂固化速度的影响。
3 结论
1)随着PF树脂pH值升高,树脂的游离甲醛、游离苯酚的含量逐渐降低,凝胶时间呈先缩短后变长的趋势,固化速度先加快后变慢。
2)随着PF树脂pH值升高,胶合板的胶合强度先升高后下降,甲醛释放量逐渐下降,pH值为12时,胶合板的性能达到最佳。
[1]Sanjay Sarkar,Basudam Adhikari.Lignin-modified phenolic resin:synthesis optimization,adhesive strength,and thermal stability[J].Journal of adhesion science and technology,2000,14(9):1179-1193.
[2]Zhao Y,Cheng L,Jiang J X,et al.Pyrolysis kinetics of tannin-phenolformaldehyde resin by non-isothermal thermogravimetric analysis[J].Journal of Thermal Analysis and Calorimetry,2015,121(2):867-876.
[3]Zhang W,Ma Y F,Wang C P,et al.Preparation and properties of ligninphenol-formaldehyde resins based on different biorefinery residues of agricultural biomass[J].Industrial Crops and Products,2013(43):326-333.
[4]He Guangbo,Ning Yan.13C NMR study on structure,composition and curing behavior of phenol-urea-formaldehyde resole resins[J].POLYMER,2004 (20):6813-6822.
[5]Pizzi A,Stephanou A.On the chemistry,behavior,and cure acceleration of phenol-formaldehyde resins under very alkaline conditions[J].Journal of applied polymer science,1993,49(12):2157-2170.
[6]Luukko P,Alvila L,Holopainen T,et al.Effect of alkalinity on the structure of phenol-formaldehyde resol resins[J].Journal of applied polymer science,2001,82(1):258-262.
[7]Wang Jian,Zhang Yi Fan.The Study of Divalent Metal Ion Catalysts on Phenol-Formaldehyde Resol Resins[J].Applied Mechanics & Materials,2011 (71-78):818-821.
[8]胡岚方,高士帅,赵临五,等.羟甲基化秸秆乙醇残渣脲醛复合树脂的制备与应用性能[J].林产化学与工业,2015 (6):21-26.
[9]Timo Holopainen,Leila Alvila,Jouni Rainio,et al.IR spectroscopy as a quantitative and predictive analysis method of phenol-formaldehyde resol resins[J].Journal of Applied Polymer Science,1998 (11):2175-2185.
[10]Krystyna Roczniak,Teresa Biernacka,Maciejski.Some properties and chemical structure of phenolic resins and their derivatives[J].Journal of Applied Polymer Science,1983 (2): 531-542.
[11]Holopainen H,Alvila L,Pakkanen T T,et al.Determination of the formaldehyde-to-phenol molar ratios of resol resins by infrared spectroscopy and multivariate analvsis[J].Journal of Applied Polymer Science,2003 (13):3582-3586.
[12]Bunichiro Tomita,Chung-Yun Hse.Cocondensation of urea with methylolphenols in acidic conditions[J].Journal of Polymer Science Part A:Polymer Chemistry,1992,30(8):1615-1624.
[13]Bunichiro Tomita,Chung-Yun Hse.Phenol-urea-formaldehyde (PF) cocondensed wood adhesives[J].International journal of adhesion and adhesives,1998,18(2): 69-79.
[14]Bunichiro Tomita,Masahiko Ohyama,Chung-Yun Hse.Synthesis of Phenol-Urea-Formaldehyde Cocondehsed Resins from UFConcentrate and Phenol[J].Holzforschung.1994,48(6):522-526.
[15]MO X F,FAN D B,Qin T F,et al.13C NMR study on the structure of ZnO-catalyzed phenol-urea-formaldehyde resin during its synthesis process[J].Journal of Adhesion Science and Technology,2014,28(22-23):2316-2326.
[16]Bunichiro Tomita,Chung-Yun Hse.Analysis on cocondensation of melamine and urea through carbon 13 enriched formaldehyde with carbon 13 nuclear magnetic resonance spectroscopy[J].Mokuzai Gak.taishi,1995,41(5):490-497.
