漂白竹浆疏水改性纳米纤丝化纤维素的制备和表征
2017-04-24周静沈葵忠房桂干李漫林艳邓拥军
周静,沈葵忠,2*,房桂干,2,李漫,林艳,2,邓拥军,2
(1.江苏省生物质能源与材料重点实验室,国家林业局林产化学工程重点开放性实验室,生物质化学利用国家工程实验室,中国林业科学研究院林产化学工业研究所,南京210042; 2.南京林业大学林业资源高效加工利用协同创新中心,南京210037)
漂白竹浆疏水改性纳米纤丝化纤维素的制备和表征
周静1,沈葵忠1,2*,房桂干1,2,李漫1,林艳1,2,邓拥军1,2
(1.江苏省生物质能源与材料重点实验室,国家林业局林产化学工程重点开放性实验室,生物质化学利用国家工程实验室,中国林业科学研究院林产化学工业研究所,南京210042; 2.南京林业大学林业资源高效加工利用协同创新中心,南京210037)
纳米纤丝化纤维素(NFC)通过化学改性的方法可以赋予其特殊表面性质。研究以漂白竹浆为原料,采用机械(球磨机和高压均质机)和化学改性相结合的方法,制备改性纳米纤丝化纤维素(m-NFC)。在球磨中使用丁酰氯为酰基化试剂,N,N-二甲基甲酰胺(DMF)为分散剂,降低纤维尺寸的同时对纸浆纤维进行化学改性,再经高压均质机处理制备了取代度为2.07的m-NFC。利用激光粒度分析仪、原子力显微镜(AFM)、傅里叶红外光谱(FTIR)、X射线衍射仪(XRD)对m-NFC的结构和形态进行表征。均质20次最高压力80 MPa制备的m-NFC微纤丝长度为316.9 nm,直径分布在25~80 nm范围内,强物理机械力作用改变了m-NFC的晶体结构。改性后的m-NFC在低极性溶剂丙酮中具有较好的分散稳定性。研究结果可为纳米纤丝化纤维素应用于疏水性生物基质材料制备提供依据。
纳米纤丝化纤维素;纳米纤丝化纤维素改性;取代度;分散性
自1947年Nickerson和Habrle首次制备得到纳米纤维素以来,纳米纤维素因具有优异的性能受到广大研究者关注。制备纳米纤维素的方法可分为化学法[1]、生物法[2-3]、机械法[4-5]等。由机械法制备的纳米纤维素又叫纳米纤丝化纤维素(NFC)。NFC是对纤维反复进行高强度均质化处理后得到的具有纳米尺度的纤维素产品(直径一般为10~40 nm,长径比为100~150)[6]。NFC具有可再生、可完全生物降解的特点,并具有极其优异的力学性能和高度有序的晶体结构。NFC的纵向弹性模量在140~250 GPa之间,拉伸强度高达2~3 GPa[7],与目前力学性能较为优异的合成有机纤维聚对苯撑苯并二噁唑纤维(PBO)相当;其线性热膨胀系数只为1.0×10-7K-1[8],与石英相当。植物体中的天然纤维素实际是以直径2~10 nm,长度数十微米的纤维素聚集结构纳米纤维素纤丝的形式存在。将NFC从植物中分离出来,并用于高分子增强材料的添加剂,可以制备出高力学性能、高热尺寸稳定性的新型高分子复合材料。因此,NFC的制取与应用被认为是林产品业较有市场前景,较有可能率先取得突破的关键领域。
由于NFC表面存在丰富的羟基,有较强的极性,并具有天然亲水性的特点,使其在亲水性材料中有较好的分散性,但若将其分散在疏水性为基质的材料中则会出现团聚、分散不均匀等问题。目前,多数研究均局限在以亲水性材料为基质的纳米复合材料方面[9-10],其在疏水性基质材料中的应用研究较少。笔者采用球磨研磨切断纤维素长链的同时加入化学改性试剂,利用机械研磨与表面化学反应协同效应,在不加入任何催化剂的条件下,即可制备出较高取代度的疏水改性微米级纤维素;经过高压均质处理可得到在极性溶剂丙酮中能稳定分散的改性纳米纤丝化纤维素(m-NFC)。本实验过程简便,所用试剂均常见易获得,为绿色环保地制备疏水性纳米纤维素提供新途径。
1 材料与方法
1.1 原料、试剂和仪器
1.1.1 原料与试剂
原料竹浆取自贵州赤天化纸业股份有限公司;N,N-二甲基甲酰胺(DMF)、丁酰氯、叔丁醇、氢氧化钠、盐酸、丙酮、无水乙醇、亚氯酸钠、苯、氢氧化钾均为分析纯。
1.1.2 仪 器
QM-QX4全方位行星式球磨机,南京南大仪器厂;GYB40-10S高压均质机,上海东华高压均质机厂;H1850R型离心机,湖南湘仪离心机仪器有限公司;LGJ-12冷冻干燥机,北京松源华兴科技发展有限公司;DF-101SA-H集热式恒温加热磁力搅拌器;原子力显微镜(AFM);马尔文激光粒度仪,英国马尔文仪器有限公司;D8 FOCUS 型X射线衍射(XRD)仪,BRUKE; 傅里叶红外光谱(FTIR)仪,THERMO SCIENTIFIC; 加拿大纤维质量分析仪(FQA),型号LDAO2140。
1.2 实验方法
1.2.1 竹浆的漂白提纯
使用综纤维素制备方法去除残留木质素提纯纸浆[11]。竹浆原料在索式抽提器中以苯与乙醇(体积比2∶1)的混合液抽提6 h,除去部分抽提物。自然晾干后置于75℃水浴锅中,用pH为4.8的酸性亚氯酸钠溶液浸泡样品,反复处理6次,每次1 h,以除去其中的木质素,用蒸馏水洗净至中性后得到综纤维素。将综纤维素在室温下用质量分数为5%的KOH溶液浸泡24 h后转移到80℃的水浴锅中保温浸泡2 h,最后用蒸馏水洗净样品至中性,冷冻干燥后即得纯度较高的α-纤维素。
1.2.2 球磨处理制备微米级竹纤维
将1.7 g提纯竹浆和50 mL DMF分别加入两个300 mL 玛瑙球磨罐中(30颗粒径为18 mm的大球和50颗粒径为8 mm的小球),命名为1号罐和2号罐。另取4.7 mL丁酰氯加入到2号罐中作为改性试剂,1号罐为空白对照。球磨机转速设置为360 r/min,每工作1 h休息0.5 h,球磨0~18 h (2号罐每间隔2 h取样测定取代度),取出样品用无水乙醇和去离子水交替反复离心洗涤(转速5 000 r/min,时间5 min)至离心上层清液呈中性,以除去溶剂 DMF和未反应的试剂。
1.2.3 纳米纤丝化纤维素制备
取球磨时间为12 h的样品悬浊液,用蒸馏水稀释浓度至0.5%~1.0%之间,将悬浊液依次在20,40,60,80,100和120 MPa的均质压力下循环均质20次,得到纳米纤丝化纤维素水溶胶。
1.2.4 取代度测定
采用滴定法测定改性纳米纤维素的取代度[12-13]。具体方法如下:样品经冷冻干燥后,放入烘箱中105℃条件下再干燥2 h,准确称量0.100 0 g样品于锥形瓶中,加入40 mL 75%乙醇并置于超声波清洗器中超声分散10 min。为使纳米纤维素进一步润胀,将其放入60℃水浴锅里保温30 min。然后准确加入20 mL 0.5 mol/L NaOH溶液,60℃磁力搅拌15 min,室温下静置48 h。过量的NaOH以酚酞为指示剂用0.5 mol/L HCl 溶液滴定。采用公式(1)计算纤维素取代度(DS):
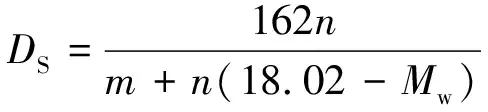
n=VNaOH×CNaOH-VHCl×CHCl
(1)
式中:DS表示纤维素取代度,162为纤维素无水葡萄糖单元摩尔质量,g/mol ;Mw为一个取代基取代的无水葡萄糖单元摩尔质量的净增值,g/mol ;m为试样的绝干质量,g;n为试样中所含酯基的物质的量,mol;VNaOH=20 mL;VHCl为到达滴定终点时消耗HCl标准溶液的体积,mL;CNaOH为NaOH标准溶液的浓度,mol/L;CHCl为HCl标准溶液的浓度,mol/L。
1.3 产物的表征
1.3.1 原子力显微镜(AFM)
将m-NFC分散于水中,形成浓度为0.01%~0.05%的胶体溶液,滴于硅片上,室温下自然晾干,使用原子力显微镜在轻敲模式下观察[14]。
1.3.2 红外光谱(FTIR)分析
m-NFC胶体溶液经逐级脱水后置于真空冷冻干燥机中干燥,取少量m-NFC粉末状固体KBr压片,扫描范围500~4 000 cm-1。使用IS10型傅里叶变换红外光谱仪以全反射的模式对其进行特征官能团分析。
1.3.3 X射线衍射(XRD)分析
m-NFC胶体溶液经逐级脱水后置于真空冷冻干燥机中干燥,干燥后的粉末压成薄片,辐射源为铜靶,扫描范围2θ=10°~50°,步长0.010°,进行X射线衍射分析。根据Turley计算样品的结晶度:
XC=(I002-Iam)/I002×100%
(2)
式中:XC为结晶度指数,%;I002为002面峰的强度,%,即结晶区的衍射强度;Iam为2θ=18°时峰的强度,即无定型区的衍射强度,%。
2 结果与分析
2.1 傅里叶红外光谱(FTIR)和取代度分析

图1 不同反应时间的m-NFC红外光谱图Fig. 1 The FTIR spectra of m-NFC with different reaction time
球磨时间对m-NFC取代度的影响见图2。随反应时间的延长,改性产物的取代度逐渐增加。反应初始阶段增加速度较快,当反应时间达8 h时,取代度增加速度变缓;当反应时间达12 h时,取代度趋于稳定,约为2.07。反应后期取代度随时间延长增加不明显,是因为该反应产物除生成纤维素酯外,同时也产生了盐酸,盐酸中的H+可使酯键发生水解,使反应达到一个平衡状态。

图2 球磨时间对m-NFC取代度的影响Fig. 2 Effect of ball milling time on substitution degree of m-NFC
本实验在不加催化剂的条件下即可生产较高取代产物有两方面原因:一方面是丁酰氯在此亲核反应中具有极高的反应活性,在所有与醇发生亲核反应生产酯的试剂中,酰氯的反应活性最大,远远高于羧酸、酸酐等试剂,在不加催化剂的常温体系中即可发生反应;另一方面,球磨过程产生的机械力与酰基化溶剂体系产生机械力化学作用[15]。
2.2 均质压力对纤维尺寸的影响
不同均质压力对纤维尺寸的影响见图3。当均质压力较小时,得到的纤维素尺寸较大,随均质压力的增大,纤维素的平均长度逐渐减小。当均质压力达80 MPa后,继续升高压力,纤维尺寸减小趋势不明显。较高的压力会增加生产能耗,同时对均质设备的损害程度也将增加,因此,选择80 MPa的均质压力较为合适。

图3 不同均质压力下m-NFC的平均长度Fig. 3 Average length of m-NFC under different homogeneous pressure
当均质压力达到80 MPa时循环处理20次时制备的m-NFC激光粒度分析见图4。图中出现两个峰,第二个峰对应的纤维长度较大,但所占比例较小,这是因为在高压均质过程中部分物料受力不均匀而出现的较大纤维。从表1可知,80 MPa循环20次得到的m-NFC微纤丝平均长度为316.9 nm,分布范围为100~1 000 nm。
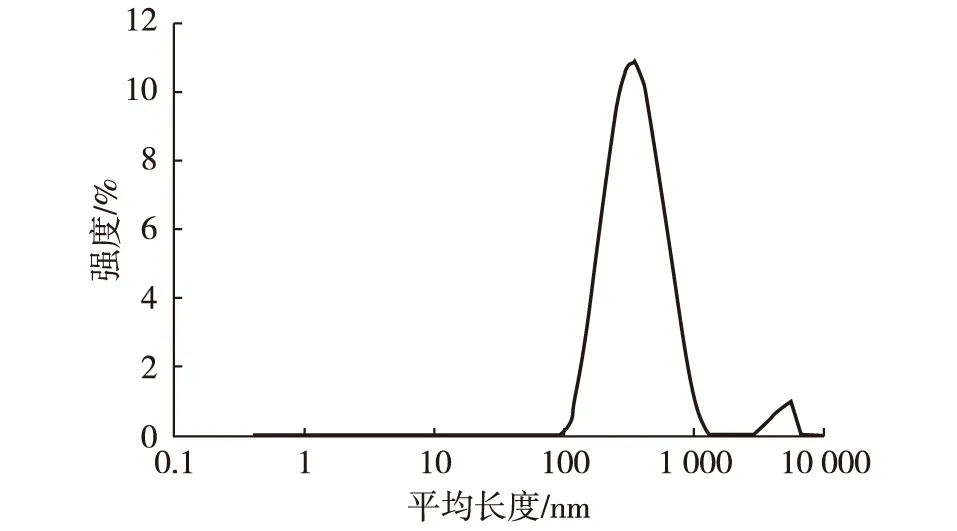
图4 80 MPa均质压力处理20次制备的m-NFC激光粒度分析Fig. 4 m-NFC particle size analysis with 80 MPa for 20 cycles

名称平均长度/nm长度/nm强度/%分布宽度/nmm⁃NFC31693770966187745860348345
2.3 不同处理阶段纤维素形貌和尺寸
经纤维质量分析仪检测,提纯α-纤维素平均长度为1.94 mm,宽度为25.7 μm;球磨处理12 h后,纤维平均长度减小为0.338 mm,宽度为16.2 μm。通过光学显微镜对提纯α-纤维素、球磨12 h后的纤维形态进行观察(图5a和5b),对比可以发现,纤维素大分子链在球磨剪切力的作用下被切断,长度明显减小,球磨处理12 h的纤维表面出现分丝扫化现象,说明球磨预处理使组成纤维的微纤丝之间的氢键结合下降,微纤丝层间变得松散,有效减小了纤维尺寸[16]。

图5 球磨处理对竹浆纤维尺寸和形貌的影响Fig. 5 Effect of ball milling on bamboo pulp fiber size and shape
在高压均质压力为80 MPa时循环处理20次制得的m-NFC原子力显微镜照片见图6,m-NFC直径为25~80 nm,长度达数微米。另外,在图6中可以发现少量白色团状物质,这可能是由于在制样过程中,m-NFC在硅片上发生部分絮聚而形成的团状颗粒,可能会导致测试结果偏大。
2.4 X射线衍射分析
X射线衍射分析如图7所示,曲线a、b和c分别为提纯α-纤维素、球磨12 h后的纤维和m-NFC的X射线衍射曲线。图中曲线a在2θ=16.5°和22°附近出现明显的强吸收峰,呈现出典型的纤维素I结构,通过公式(2)计算其结晶度为58.34%。曲线b和c与曲线a呈现出较大不同,经球磨和高压均质等机械力化学过程后,物质的尖峰特征衍射峰基本消失,变成馒头峰,说明此机械力化学过程使晶体的有序化程度降低,无定型化程度增强,结晶度降低,m-NFC的晶体结构发生了变化[17]。

图6 m-NCF的原子力照片Fig. 6 Atomic force photo of m-NFC

图7 不同处理阶段物质的XRD图Fig. 7 The XRD diagram of cellulose materials in different processing stages
2.5 分散性能分析
将在80 MPa均质压力下循环20次制备的NFC分散于水中,可以观察到其产生的显著的丁达尔效应,表明其分散良好,形成了质量分数为1%的相对稳定的水相胶体溶液(图8);而将它分散在弱极性溶剂丙酮中静置2 d后发生明显团聚沉降在容器底部(图9a),此团聚现象与杨振钰等[18]研究的乙酰化改性纳米纤维素在不同极性的溶剂体系中的分散行为相似;而取代度为2.07的m-NFC因表面羟基部分被丁酰基基团取代,极性下降,分散在低极性体系丙酮中2 d后仍可以稳定悬浮(图9b)。

图8 分散于水中的质量分数为1%未改性NFC水溶胶(a)及其产生的丁达尔效应(b)Fig. 8 The 1% (m/V) NFC solution dispersed in water(a) and its Tyndall effect(b)

图9 未改性NFC(a)和改性m-NFC(b)在丙酮中的分散情况Fig. 9 Dispersion of unmodified NFC (a) and modified m-NFC (b) in acetone
3 结 论
1)FTIR分析结果表明,使用丁酰氯为酰基化试剂,以N,N-二甲基甲酰胺(DMF)为分散剂,在球磨中对提纯后的竹浆纤维进行常温改性处理,纤维表面成功完成酰基化反应;随球磨时间的延长,取代度增加,最高可达2.07。
2)激光粒度分析仪和AFM分析结果表明,球磨疏水改性后的纤维素纤维经高压均质机均质处理,制备的改性纳米丝化纤维素(m-NFC),直径分布在25~80 nm范围, 平均长度为316.9 nm。强烈的机械力过程使纤维晶体的有序化程度降低,无定型化程度增强,结晶度降低。
3)未经改性的NFC在水分散中可以形成相对稳定的胶体溶液,但在弱极性改性低极性溶剂丙酮中易于团聚;改性后m-NFC却在丙酮中具有良好的分散性能。使用丁酰氯和N,N-二甲基甲酰胺体系,结合机械力作用在常温可以对NFC进行良好改性,可制备在低极性溶剂中分散良好的m-NFC,为其应用于高分子生物基质材料制备提供了较好手段。
[1]SUN B, ZHANG M, HOU Q X, et al. Further characterization of cellulose nanocrystal (CNC) preparation from sulfuric acid hydrolysis of cotton fibers[J]. Cellulose, 2016, 23(1):439-450.
[2]SATYAMURTHY P, JAIN P, BALASUBRAMANYA R H,et al. Preparation and characterization of cellulose nanowhiskers from cottonbres by controlled microbial hydrolysis[J]. Carbohydrate Polymers, 2011, 83(1):122-129.
[4]TIAN C, YI J, WU Y, et al. Preparation of highly charged cellulose nanofibrils using high-pressure homogenization coupled with strong acid hydrolysis pretreatments[J]. Carbohydrate Polymers, 2016, 136:485-492.
[5]AMIN K N, ANNAMALAI P K, MORROW I C, et al. Production of cellulose nanocrystals via a scalable mechanical method[J]. RSC Advances, 2015, 5(70):57133-57140.
[6]SVAGAN A J, SAMIR M A S A, BERGLUND L A. Biomimetic polysacchafide nanocomposites of highcellulose contentand high toughness[J]. Biomacromolecules, 2007, 8(8):2556-2563.
[7]NISHINO T, TAKANO K, NAKAMAE K. Elastic-modulus of the crystalline regions of cellulose polymorphs[J]. Journal of Polymer Science Part B—Polymer Physics, 1995, 33(11):1647-1651.
[8]NISHINO T, MATSUDA I, HIRAO K. All-cellulose composite[J]. Macromolecules, 2004, 37(20):7683-7687.
[9]AKSOY E A, AKATA B, BAC N, et al. Preparation and characterization of zeolite beta-polyurethane composite membranes[J]. Journal of Applied Polymer Science, 2007, 104(5):3378-3387.
[10]MA X, CHANG P R, YU J. Properties of biodegradable thermoplastic pea starch/carboxymethyl celluloseand pea starch/microcrystalline cellulose composites[J]. Carbohydrate Polymers, 2008, 72(3):369-375.
[11]何文, 张齐生, 蒋身学, 等. 慈竹纳米纤维素的制备及特征分析[J]. 林业科技开发, 2013, 27(4):23-27. HE W, ZHANG Q S, JIANG S X, et al. Preparation and characterstics analysis of nanocellulose fromBambusaemeiensis[J]. China Forestry Science and Technology, 2013, 27(4):23-27.
[12]KIM D Y, NISHIYAMA Y, KUGA S. Surface acetylation of bacterial cellulose[J]. Cellulose, 2002, 9(3/4):361-367.
[13]FREIRE C, SILVESTRE A, NETO C, et al. An efficient method for determination of the degree of substitution of cellulose esters of long chain aliphatic acids[J]. Cellulose, 2005, 12(5):449-458.
[14]WAGNER R, ROBERT J, RAMAN A, et al. Mechanical properties of cellulose nanomaterials studied by contact resonance atomic force microscopy[J]. Cellulose, 2016(23):1031-1041.
[15]PETERS K. Mechanochemische reaktionen[J]. Symposion Zerkleinern, 1962, 43(5):78-98.
[16]徐媚, 徐梦蝶, 戴红旗, 等. 球磨和PFI磨预处理对纸浆纤维结构及形态的影响[J]. 纤维素科学与技术, 2013, 21(2):46-52. XU M, XU M D, DAI H Q, et al. The effects of ball milling and PFI pretreatment on the cellulose structure and fiber morphology[J]. Journal of Cellulose Science and Technology, 2013, 21(2):46-52.
[17]JONOOBI M, HARUN J, MATHEW A P, et al. Preparation of cellulose nanofibers with hydrophobic surface characteristics[J]. Cellulose, 2010, 17(2):299-307.
[18]杨振钰, 王文俊, 邵自强, 等. 纳米纤维素晶须的表面醋酸酯化改性及复合材料的力学性能[J]. 高等学校化学学报, 2013, 34(4):1021-1026. YANG Z Y, WANG W J, SHAO Z Q, et al. Surface acetylation of cellulose nanowhiskers and its reinforcing function in cellulose acetate[J]. Chemical Journal of Chinese Universities, 2013, 34(4):1021-1026.
Preparation and characterization of hydrophobic nanofibrillatedcellulose fiber from bleached bamboo pulp
ZHOU Jing1, SHEN Kuizhong1,2*, FANG Guigan1,2, LI Man1, LIN Yan1,2, DENG Yongjun1,2
(1. Key Lab. of Biomass Energy and Material, Jiangsu Province; Key and Open Lab. of Forest Chemical Engineering, SFA; National Engineering Lab. for Biomass Chemical Utilization; Institute of Chemical Industry of Forestry Products, CAF, Nanjing 210042, China; 2. Collaborative Innovation Center for High Efficient Processing and Utilization of Forestry Resources, Nanjing Forestry University, Nanjing 210037, China)
Nanofibrillated cellulose can be chemically modified for special properties. Hydrophobic nanofibrillated cellulose (m-NFC) was prepared by pretreating bleached bamboo pulp using butyl chloride as a modification reagent and DMF as a dispersant in planetary ball mill for a period of time. Subsequently, the obtained microfiber with surface substitution degree of 2.07 was passed through a high-pressure homogenizer. The modified NFC was characterized with atomic force microscopy (AFM), Fourier transform infrared spectroscopy (FTIR) and X-ray diffraction (XRD). The m-NFC obtained from 20 passed of the homogenizer with maximum pressure of 80 MPa had an average length of 316.9 nm and average diameters between 25 nm and 80 nm. The results of XRD showed that the degrees of crystallinity of m-NFC were changed as a result of the severe mechanical treatment. The m-NFC showed good dispersion stability in a low polar solvent of acetone. Hydrophobic modification of nanofibrillated cellulose has great development potential in hydrophobic substrate material.
nanofibrillated cellulose fiber; nanofibrillated cellulose fiber modification; degree of substitution; dispersion
2016-08-15
2016-09-17
“十二五”国家科技支撑计划项目(2014BAD02B02);江苏省生物质能源与材料重点实验室基金(JSBEM-S-201510)。
周静,女,研究方向为生物质化学转化。通信作者:沈葵忠,男,研究员。E-mail:shenkuizhong@yahoo.com.cn
TQ351.3
A
2096-1359(2017)02-0101-06
