胸中上段食管癌同中心上下半野调强放射治疗(IMRT)的物理剂量分布优化分析及研究
2017-04-20朱万里张红智吴楚楚邱艳艳
程 杭 杨 昕 朱万里 张红智 张 毅 吴楚楚 邱艳艳 吕 翠
胸中上段食管癌同中心上下半野调强放射治疗(IMRT)的物理剂量分布优化分析及研究
程 杭①杨 昕①朱万里①张红智①张 毅①吴楚楚①邱艳艳①吕 翠①
目的:探讨胸中上段食管癌患者同中心上下半野调强放射治疗(IMRT)在各个层面的剂量分布,为临床应用提供参考。方法:选取20例确诊为胸中上段食管癌患者,上下半段靶区分别对应设计制作上、下半野IMRT计划。通过胶片剂量仪进行衔接层面的相对剂量验证、指形电离室及适配模体对中心点剂量验证,以及通过二维矩阵电离室Mapcheck进行冠状面的相对剂量验证,对同中心上下进行2个半野IMRT不同层面的剂量分布统计分析。结果:上下分野衔接层面的胶片验证结果<5%,无剂量冷热点出现,符合剂量验证;中心点剂量验证结果为偏差度均<3%;冠状面的相对剂量验证在3 mm/3%条件下通过率>98.04%,4 mm/4%条件下通过率>98.77%。结果表明,所有患者的照射野剂量通过率均高于98%。结论:同中心上下半野IMRT技术在各个层面的剂量分布均能够通过验证要求,符合临床治疗需要。
同中心上下半野技术;调强放射治疗;胸中上段食道癌;剂量验证
程杭,男,(1982- ),硕士,工程师。金华市中心医院放疗科,研究方向:肿瘤放射治疗物理剂量学及优化研究,肿瘤放疗物理质量控制与管理。
胸中上段食管癌患者因其靶区长度及深度较易改变,在放射治疗过程中容易引起靶区层面剂量分布不一[1-2]。为有效改善患者靶区的剂量分布和靶区的适形度,目前临床上主要采用调强放射治疗(intensity modulated radiation therapy,IMRT)技术,但该术不免存在肺组织受到过度低剂量照射等劣势[3-6]。若能实施同中心上下半野技术,上下半段靶区通过各上下半野IMRT,不仅可以有效改善患者靶区的适形度以及剂量,同时还可以避免肺组织遭受过度低剂量放射。因此,本研究通过对20例胸中上段食管癌患者同中心上下半野IMRT在不同层面的剂量优化分布的分析,以期为临床应用提供参考。
1 资料与方法
1.1 一般资料
选取金华市中心医院2014年1月至2016年6月确诊的20例胸中上段食管癌患者,回顾性分析并采用随机数字表法进行随机化分组,其中男性15例,女性5例;年龄38~75岁,平均年龄(55.05±5.91)岁。本研究内容已经医院医学伦理委员会批准,且所有患者均自愿签署知情同意书。
1.2 纳入与排除标准
(1)纳入标准:①患者年龄>18岁;②通过病理证实为胸中上段食管癌。
(2)排除标准:①伴有严重心血管疾病者;②严重肝肾功能不全者;③伴有精神性疾病,且无法进行有效沟通者。
1.3 仪器设备
采用Primus Plus直线加速器(德国西门子公司);治疗计划系统(TPS)为XIO 4.62(美国CMS公司);SIEMENS SOMATOM Sprit螺旋CT模拟定位机(德国西门子公司);Mapcheck 1175二维矩阵电离室(美国Sun Nuclear公司)。
1.4 方法
1.4.1 方法选择
对所有患者实施同中心上下半野技术,上半段靶区进行上半野调强放射,靶区下半段进行下半野调强放射。为能够符合临床要求,通过测量Primus Plus加速器多叶准直器(multi-leaf collimator,MLC)0位时的欠位或过位区,避免加速器MLC运动时带来的机械误差。
1.4.2 同中心上下半野照射图组成
本研究实施的是同中心上下半野技术,故仅有1个放射治疗中心点。上下半野在中心点处进行衔接,上半野准直器铅门Y2和下半野Y1均为0 cm,较常规的IMRT,同中心上下2个半野调强的准直器和MLC运动面积会遭受一定干扰,故在半野IMRT过程中,MLC以及独立准直器应禁止自动伴随,另一半的Y级铅门位于0位处。
1.4.3 调强计划设计与制作
在CT定位机下,均制作热塑体膜固定20例患者体位,并实施胸部CT扫描,通过网络传输CT扫描的影像,由高年资放射治疗医生进行肿瘤靶区的勾画。并在CMS XIO 4.62 TPS上设计制作IMRT计划,能量选择10 MV的X射线。针对每一病例设计一种同中心上下2个半野调强方案。调强计划均采用静态步进(Step&Shoot)方式,对放射剂量的计算则使用超级迭代算法(Superposition),剂量计算格栅为2.0 mm,3野和5野方法均进行等均分野[7-8]。肿瘤计划靶区(planing target volume,PTV)处方剂量全部是60 Gy/30次。PTV100﹪处方剂量体积应≥95﹪,PTV110﹪处方剂量体积应<10﹪,靶区外的任一区域处方剂量的体积不能出现>110﹪;脊髓最大剂量<42 Gy,双肺的V20<28﹪;食管壁上不出现热点,而PTV内不出现冷点。
1.4.4 衔接层面相对剂量验证方式
应用IBA固体水体模开展衔接层面相对剂量的测量验证。将EDR2胶片放在固体水体模中,并置于等中心处,与射线束中心轴成90o角,源片距定在90处。对称光野开至25 cm×25 cm后,把其中铅门Y1开至0.2 cm处。利用半野曝光,并调整曝光跳数到105 MU。接着在上述条件25 cm×25 cm开野下,另一铅门Y2开至0 cm处,亦是半野曝光,并调整曝光跳数到105 MU。之后通过另一张EDR2胶片,在上述条件下进行全开野透视。透视结束时对胶片进行冲洗,同时采取林格曼黑度计测出胶片黑度。
1.4.5 中心点剂量验证方式
通过CT扫描固体水体模,并在其电离室适配孔中将PTW0.6cc电离室置入,同时利用CT Sim网络系统,把固体水体模的CT图像传送到放射治疗计划系统(treatment planning system,TPS)。通过TPS软件功能描绘外围轮廓Body,同时勾画电离室灵敏体积,并将其取名为TD。将20例患者的同中心上下半野照射的IMRT计划按实际射野角度移植到固体水体模中,并将方案取名为Program YP。电离室灵敏体积的中心即是直线加速器的等中心,接着在TPS上得出剂量值,并将其存在一个YP方案中,测量等中心点的剂量值。
1.4.6 冠状面相对剂量验证方式
通过Sun Nuclear Mapcheck1175开展冠状面相对剂量的验证。Mapcheck1175共有445个半导体探测器,射野范围为22 cm×22 cm,含有调强治疗全过程剂量验证和质量保证的应用软件,进行自动比对分析测量调强计划数据的剂量。
1.5 观察与评价指标
观察衔接层面的相对剂量、中心点剂量及冠状面相对剂量的验证情况的指标。其评价指标为:①衔接层面相对剂量的变化情况。由于EDR2胶片上的所有点均在一样的物理条件下放射而获得,亦在相同的冲洗方式上给出胶片黑度的变化情况;②中心点剂量。利用剂量体积直方图(dose volume histograms,DVH)记录TD的平均值Mean,获取必须验证的计划中心点的剂量值;③冠状面相对剂量。通过比较Mapcheck1175二维矩阵实时得出的分布图和TPS的IMRT冠状面剂量分布图,并进行不同的数据统计分析公式,最终获取客观的剂量偏差值。
1.6 统计学方法
利用Mapcheck自带的剂量分布软件进行剂量偏差数据的计算,结果通过SPSS 21.0统计学软件进行数据处理和分析。
2 结果
20例胸中上段食管癌患者的同中心上下半野照射的剂量符合验证要求,且均达到临床的标准。所有Plan的同中心上下半野照射的衔接层面胶片验证结果均<5﹪,表明剂量分布均匀,尚无出现热点(>10﹪)或冷点(<10﹪),均能够通过验证;中心点剂量验证结果表明,偏差度均<3﹪,达到临床需要,亦能够通过验证,见表1。冠状面的相对剂量验证结果表明,所有患者的照射野剂量通过率均>98﹪,符合试验之初给定的标准(Mapcheck验证通过率>95﹪,即为符合),见表2。以上所有剂量验证方式均反映出同中心上下半野技术能够达到验证要求。

表1 20例患者中心点的绝对剂量偏差
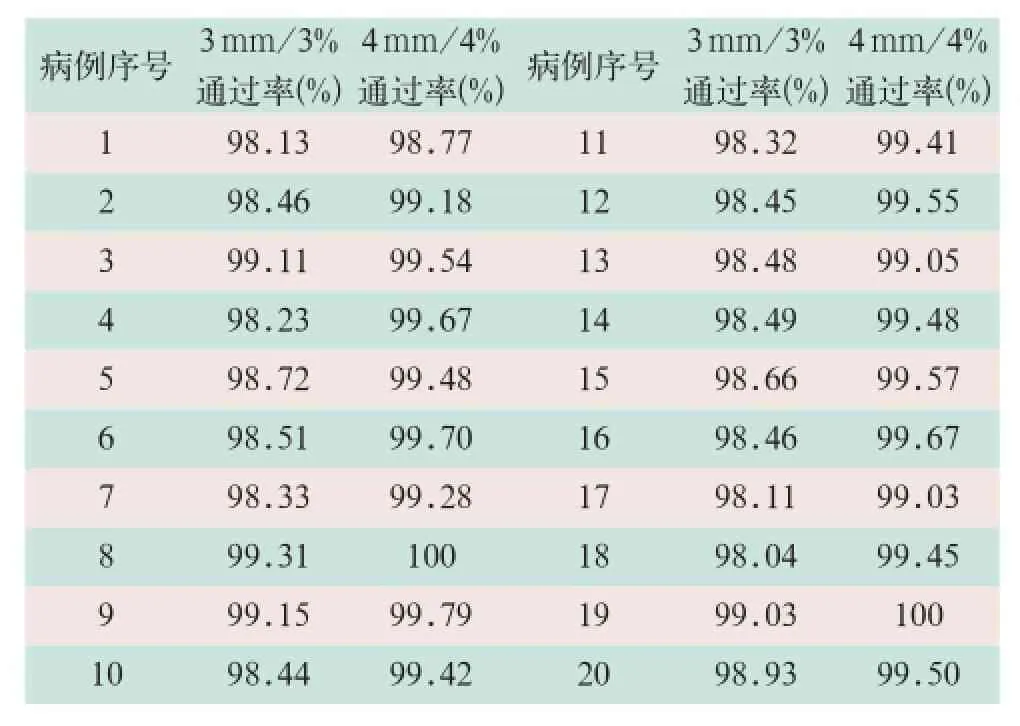
表2 20例患者冠状面的相对剂量通过率
3 讨论
同中心上下半野IMRT技术与常规IMRT进行对比,二者之间均仅有一个治疗中心,仅进行进机房1次摆位,即均不会延长放射治疗物理师及技术员的工作时间和胸中上段食管癌患者的治疗时间[9-10]。然而,同中心上下半野IMRT较常规IMRT更有助于改善患者靶区的剂量分布,降低肺低剂量照射区域,增强对正常气管的保护能力,因此,同中心上下半野IMRT可作为一种临床上可行性较强的放射治疗技术应用[11-13]。
放射治疗剂量的准确性是确保一项放射治疗技术能够广泛应用开展的关键因素,对同中心上下半野调强放射剂量精度造成干扰主要因素有:患者的摆位误差、半野调强中子野放射剂量的精确度、子野照射进行时多叶光栅叶片的位置准确性、加速器跳数的剂量线性以及上下半野衔接层面剂量的准确性等。以上因素均在一定程度上引起放射治疗方案测出的剂量分布与患者真正照射时的实时剂量分布产生误差[14-15]。临床中,一旦验证误差差别过大,则设计的放射治疗调强计划方案将不能予以使用,而应及时寻求差别过大的原因并进行解决,待反复验证符合要求后,才能进行放射治疗。因此,剂量分布符合验证标准,尤其是衔接层面的剂量分布验证是确保同中心上下2个半野IMRT技术得以准确应用到胸中上段食管癌患者放射治疗的关键步骤。
本研究结果显示,20例胸中上段食管癌患者的同中心上下2个半野放射方案的剂量均符合验证要求,均达到临床的标准。所有剂量验证方式均反映出同中心上下半野技术能够达到剂量验证要求。在此基础上可进一步利用热释光片对仿真人体模型的衔接层面进行绝对剂量的验证。然而,因为试验条件有限,缺乏热释光剂量仪,而且热释光的校准较难以进行,故尚未实施该项工作。本次研究在进行衔接层面剂量的验证过程中,因试验基础受限,缺乏非冲洗的ISP胶片,亦尚未通过Film QA Pro软件以处理胶片剂量数据,在一定程度上可能会对试验结果产生误差。
同中心上下半野IMRT技术在各个层面的剂量分布均能够通过验证要求,符合临床治疗需要。
[1] 曾彪.同中心上下半野照射在胸中上段食道癌放疗中的应用[D].北京:清华大学,2013.
[2]白文文.颈段食道癌三维适形放疗与调强放疗的剂量学及临床对比研究[D].石家庄:河北医科大学,2014.
[3]徐珊.食道癌调强放疗临床研究[D].石家庄:河北医科大学,2014.
[4]Nomura M,Kodaira T,Furutani K,et al.Predictive factors for radiation pneumonitis in oesophageal cancer patients treated with chemoradiotherapy without prophylactic nodal irradiation[J].Br J Radiol,2012,85(1014):813-818.
[5]程蒙蒙.颈、胸上段食道癌不同照射技术的剂量学对比研究[D].合肥:安徽医科大学,2014.
[6]曾彪,张九堂,席许平,等.单中心上下半野技术在胸中上段食道癌放射治疗中的剂量学分布[J].中国医学物理学杂志,2015,32(3):357-360.
[7]李润霄.调强放射治疗计划系统的物理统计分析[D].石家庄:河北科技大学,2014.
[8]胡俊,刘海,王晓萍,等.EPID在颈、胸上段食道癌调强放疗中的应用价值[J].中国医疗设备,2012,27(6): 164-166.
[9]尚凯.胸段食道癌图像引导放射治疗中摆位和剂量误差及治疗分次内动度对靶区剂量的影响[D].石家庄:河北医科大学,2013.
[10]郦守国.胸中段食道癌适形放疗和调强放疗剂量学研究[D].福州:福建医科大学,2012.
[11]陈明芬.食道癌调强放射治疗在治疗过程中靶区变化的相关研究[D].福州:福建医科大学,2013.
[12]范华.胸中下段食道癌放疗中运动规律及剂量学研究[D].泸州:泸州医学院,2013.
[13]李鸣鹤,马庭炜.食管内超声对食道癌术前诊断和临床分期的应用价值[J].中国医学装备,2015,12(9):79-82.
[14]赵一虹,许卫东,张富利.TOMOX方案联合三维适形放射治疗中晚期食道癌的近期疗效及不良反应观察[J].中国医学装备,2016,13(10):61-64.
[15]Wang D,Shi J,Liang S,et al.Dose-volume histogram parameters for predicting radiation pneumonitis using receiver operating characteristic curve[J].Clinical and Translation Oncology,2013,15(5):364-369.
The optimal analysis and research of dose distribution at various aspects of the monoisocenter irradiation technique in IMRT for the treatment of patients with upper and mid esophagus cancer
CHENG Hang, YANG Xin, ZHU Wan-li, et al//
China Medical Equipment,2017,14(4):61-64.
Objective: To discuss dose distribution at various aspects of the mono-isocenter irradiation technique in intensity-modulated radiation therapy (IMRT) for the treatment of patients with upper and mid esophagus cancer in order to provide reference value for clinical application. Methods: 20 cases diagnosed as upper and mid esophagus cancer were selected from our hospital during 2014-2016, and the first target used half field IMRT in the up area while the second target used half field IMRT in the down area. One was the relative dose verification of interface slice used with the film dosimeter; the another was the center point dose verification used with the ionization chamber and adapter module; the third one was the relative dose verification of the coronal plane used with the two dimensional matrix Mapcheck dosimeter; and the dose verification results of IMRT used with the mono-isocenter irradiation technique were statistical analyzed. Results: The film verification indicated that didn't have cold-hot point and the results accorded with verification; the center point dose verification results indicated that the degree of deviation was less than 3%; the relative dose verification of the coronal plane showed that passing rate was above 98.04% under 3 mm/3%; and was above 98.77% under 4 mm/4%. These results indicated the dose passing rate of radiation field of all patients were above 98%. Conclusion: The dose distribution at various aspects of the monoisocenter IMRT can pass the verification requirements, which accord with the demands of clinical treatment and is worthy for application and promotion.
The mono-isocenter irradiation technique; Intensity modulated radiation therapy; Upper and mid esophagus cancer; Dose verification
10.3969/J.ISSN.1672-8270.2017.04.016
1672-8270(2017)04-0061-04
R816
A

2016-12-28
①金华市中心医院放疗科 浙江 金华 321000
[First-author’s address] Department of Radiotherapy, Jinhua Central Hospital, Jinhua 321000, China.
