嵌合抗原受体构建与肿瘤治疗的研究进展
2017-04-17钱昱臻张明睿任刚邹伟
钱昱臻,张明睿,任刚,邹伟
1.辽宁师范大学 生命科学学院,辽宁 大连 116081;2.辽宁省生物技术与分子药物研发重点实验室,辽宁 大连 116081;3.中国医学科学院 医药生物技术研究所,北京 100050
嵌合抗原受体构建与肿瘤治疗的研究进展
钱昱臻1,2,张明睿1,2,任刚3,邹伟1,2
1.辽宁师范大学 生命科学学院,辽宁 大连 116081;2.辽宁省生物技术与分子药物研发重点实验室,辽宁 大连 116081;3.中国医学科学院 医药生物技术研究所,北京 100050
多年来,癌症治疗一直是困扰人类的难题之一,常规的治疗手段都各有局限。随着基因转移和细胞培养技术的更新换代,细胞免疫治疗逐渐走入公众视线。嵌合抗原受体(chimeric antigen receptor,CAR)修饰的T淋巴细胞(CAR-T)治疗是几年来肿瘤过继免疫治疗的新方法,能特异性识别靶抗原,并杀伤肿瘤细胞。我们将CAR-T细胞在肿瘤治疗中的应用及构建CAR-T细胞的策略做简要综述。
嵌合抗原受体;T淋巴细胞;肿瘤治疗
多年来,肿瘤治疗一直是困扰人类的最大难题之一,常规治疗手段都各有局限。随着基因转移和细胞培养技术的更新换代,细胞免疫治疗逐渐引起人们的重视。1989年,Gross及Goverman等[1-2]提出了一个新的想法,引入细胞毒性T细胞杂交瘤细胞作为基因材料用以构建一种抗体识别抗原的模型。1991年,Romeo和Irving等构建了与信号分子相连的编码CD4或CD25的嵌合受体,证实了单一的多肽链的确能够复制大部分T细胞受体(T cell receptor,TCR)的定位特征[3-4]。上述基础研究共同证明了重组T细胞不依赖MHC限制性,在特异性地定位靶抗原,对抗人类肿瘤上是具有可能性的。近年来,嵌合抗原受体T细胞(chimeric antigen receptor T cell,CAR-T)作为一种新的免疫细胞治疗方式,在肿瘤临床治疗,尤其是在血液癌等非固态瘤的癌症治疗中,取得了突破性进展。2016年初,《The Guardian》报道,美国弗雷德·哈钦森癌症研究中心发现CAR-T可作为特定白血病的治疗新方法,在不同国家进行的早期临床试验效果明显,超过90%的病人症状完全消失。在此,我们简要综述了嵌合抗原受体(chimeric antigen receptors,CARs)结构、CAR-T细胞在肿瘤治疗中的应用及局限性,以及目前构建CAR-T细胞的策略,旨在为临床研究应用提供依据。
1 嵌合抗原受体的结构
利用基因工程方法将能与肿瘤抗原特异性结合的受体、细胞跨膜的部分和细胞内信号转导的部分结合起来,构成新的结构,称为CARs。用之修饰T细胞,赋予其特异性的肿瘤杀伤能力即为CAR-T细胞。简单来说,CARs最基本的结构由单链可变区(single chain fragment variable,scFv)的胞外配体结合域通过跨膜结构域与胞内信号域连接组成(图1)[5]。细胞外的配体结合域一般为单链抗体,决定了CARs的特异性;胞内信号域最初为T细胞活化基序,即免疫受体酪氨酸活化基序(immunoreceptor tyrosine-based activa⁃ tion motif,ITAM),起到激活T细胞的作用,通常为CD3ζ和FcεRIγ。这种模式化的结构方式从第一代CARs(仅有一个CD3ζ结构域)开始一直沿用至今,只有形式上的改进,从未有结构上的颠覆。但是,仅仅由ITAM发出的激活信号只能引起T细胞的短暂分裂和较低水平的细胞因子分泌,不能提供大量的单克隆扩增和长时间的抗肿瘤效应[6-7]。因此,根据T细胞活化双信号学说,在第一代CARs的基础上,加入了新的单一或更多的共刺激分子(costimulatory molecule,CM),第二、三代CARs应运而生(图1)。与第一代CAR-T细胞相比,第二、三代CAR-T细胞毒性、增殖活性、存活时间、细胞因子释放等均显著增加[8-11]。而Pegram等[12]以第二代CARs为基础,以CD19为靶抗原,构建了一种能分泌IL-12的新型CAR-T细胞,提出了第四代CARs的新构想。这种新型CAR-T细胞在未用环磷酰胺预处理的情况下,具有抗CD19+肿瘤的作用。这就说明新型四代CARs可以不借助强毒副作用的放化疗药物,具有扩展CAR-T细胞的临床应用范围,减少患者所受伤害的可能性。
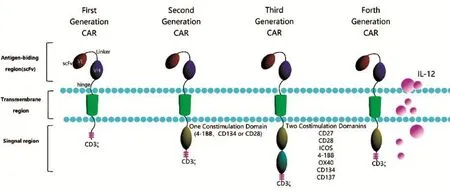
图1 癌症免疫疗法——CAR-T疗法的细胞结构示意图
2 CAR-T细胞在肿瘤治疗中的应用及局限性
2.1 CAR-T细胞在肿瘤治疗中的应用
早在2006年便首次公开报道了将CAR-T细胞技术应用于临床试验的相关研究[13-14],其后越来越多的文章相继发表,提出了很多有价值的见解[15-19]。Porter等在《New England Journal of Med⁃icine》上报道了关于CAR-T细胞成功治疗慢性淋巴细胞白血病(chronic lymphocytic leukemia,CLL)的临床研究,3例CLL患者经过CD19-CART细胞靶向治疗后,检测发现CAR-T细胞能在体内扩增1000倍以上,可维持6个月的治疗周期,而其中2例患者的病情完全得到缓解[15]。Till等,用逆转录病毒构建出第三代CAR-T细胞(CD20-CD28-CD137-CD3ζ),用于治疗非霍奇金淋巴瘤。临床结果显示,第三代CAR-T细胞在体内存活时间超过12个月[17],较第二代CAR-T细胞6个月的存活周期相比具有更强的效用时间。
B细胞抗原CD19是典型的CARs抗原,其表达于正常B细胞与多数B细胞恶性肿瘤,而在其他组织和尚未发育完全的B细胞中不表达,因此CD19可以作为一个CAR-T细胞持续作用的生物标志物。CD19是已知最好的,也是最常用的靶向分子。宾夕法尼亚大学以抗CD19嵌合抗原受体T细胞为基础,开发出第一个针对特定癌症(急性B细胞恶性肿瘤)的个性化细胞治疗方式——CTL019。2014年美国食品和药物管理局授予CTL019“突破疗法”称号。截至2015年底,已有100多个患者接受抗CD19基因重组T细胞治疗,并且越来越多的关于该疗法的初步临床试验结果被发表。目前,还有一些针对顽固恶性实体瘤的实验在积极进行中,目的是完善CAR-T细胞疗法,使其不仅仅局限于B细胞恶性肿瘤的治疗。
截止于2016年3月,CAR-T细胞在淋巴瘤、白血病临床治疗中已获得了令人瞩目的成绩,全球范围内有记录可查的CAR-T研发及临床试验已有百余项,而在中国,CAR-T细胞在卵巢癌、恶性胶质瘤、肝癌和乳腺癌等研究中也取得了一定的突破(表1)。
2.2 CAR-T细胞肿瘤治疗中的局限性
临床应用中CAR-T治疗高潜力、快发展的背后同样存在制约,例如不能特异性识别肿瘤抗原、过度激活大量释放炎症因子等现象。不能特异性识别肿瘤抗原即脱靶效应(与抗原受体特异性和抗原分子拟态相关),主要原因是缺少肿瘤的特异性抗原(tumor specific antigen,TSA)[20-21],这就很可能发生肿瘤逃逸,或造成对正常细胞的杀伤。实体瘤中,若CAR-T细胞不能准确归巢到正确的肿瘤位置,由于脱靶效应,反而会和靶点表达较少的正常细胞结合,杀伤正常细胞,造成致命危害。因此,可以说脱靶效应是CAR-T细胞治疗面临的重大挑战。目前,研究者在努力寻找肿瘤新型表位的同时[22],也在积极探索能消除或沉默CAR-T细胞来控制脱靶效应的新方法,如引入“自杀基因”等[23]。
CAR-T细胞与有效抗原结合后,能激活相关细胞因子的产生和释放。其活化T细胞产物,释放IFN-γ、IL-2和其他多种细胞因子,使得它们转而激活其他免疫细胞,包括巨噬细胞等,从而形成免疫细胞间的联合杀伤。若CAR-T细胞过度激活或在疾病根除后仍在患者体内大量存活,就会导致细胞因子过度释放,这是十分危险的[24]。目前,临床上通过抗细胞因子疗法控制其危害。抗细胞因子疗法能直接靶向次级介体,反应迅速,无毒,不影响T细胞移植[25]。然而,抗细胞因子疗法的前提是必须明确过度激活的细胞因子,才能针对性消除,这使得新型CAR-T细胞产品用于人体时,很难分辨这一新型产品的临床毒性。
3 CARs构建的基本原理及研究进展
CARs基础结构的构建与分子生物学的基因工程免疫受体有关。简单来说,就是将一个来自某一抗体的轻链和重链序列的多肽结构,连接于受体上的信号传导装置,如经典的T细胞受体——ζ链,通过对其三大区域(配体结合域、跨膜结构域与胞内信号域)基本设计上的不断改进,从而提高其效能。
3.1 构建CARs信号域
CARs传输一个信号到细胞内的T细胞需要通过一个信号域,经典的信号域为CD3ζ链,也有人使用来自Fcγ受体的信号域[14]。第二、三代CARs在初代CARs信号域CD3的基础上引入新的信号域,如CD28、4-1BB或OX40,以期产生共同刺激,使TCR更易被抗原递呈细胞(APC)识别,完全激活T细胞生理活性[26-27]。事实证明,引入共刺激信号分子这种方式能增加细胞因子的产量及促进CAR-T细胞体外增殖,第二代CD19特异性的CARs能携带CD28或4-1BB信号集团,且在临床前模型和B细胞恶性肿瘤的临床试验中已经证明其具有体内抗肿瘤活性[19,25-35]。
目前常用的共刺激分子包括CD27、CD28、CD134(OX40)、CD137(4-1BB)、CD244和ICOS等,将其合并在一起能增加ζ链信号,从而增强T细胞的增殖和存活[36-41]。CD28是第一个用于构造CARs的共刺激分子,显著增加了IL-2的产物和细胞毒性[9,42],加入共刺激分子CD28后,通过调节T细胞能增加CARs对细胞毒性的抗性[43]。临床前实验发现与CD28共刺激CARs相比,CD137的引入更能改善CARs的体内存活,增强其抗肿瘤活性[36]。而ICOS信号域过表达能使人T细胞转化为Th17表型,并且在某些情况下与CD28共刺激的Th17细胞会产生更高一级的抗肿瘤功效[43-45]。已清楚地发现引入单一共刺激分子能赋予CART细胞更高的存活或其他一些T细胞功能,而较单一共刺激分子相比,增加更多的共刺激分子的确增加了CAR-T细胞的特性[11,46]。
3.2 CARs跨膜域构建

表1 CAR-T技术在中国的临床试验
配体结合域通过铰链区与跨膜域相连,通常来源于CD8和IgG4分子。铰链对于细胞表面的CARs表达非常重要。铰链区影响scFv的韧性,从而影响其与配基的相互作用。而铰链区的长度会影响T细胞和标靶间的相互作用(取决于目标抗原标位的位置),例如,CD22靠近细胞膜表位较远端表位相比会引起更溶胞作用[47]。同样,越长的连接区域越能增强CARs识别NCAM和5T4等膜近端表位的能力,还有可能增加其适应性[48-49]。这一发现很可能揭示了CARs修饰的细胞和靶向细胞最佳的距离。
3.3 CARs结合域构建
研究表明,CAR-T细胞能识别和清除相当于自身100倍的靶向抗原[50],如果提高CAR-T细胞的特异性,会降低其激活的条件,扩大其治疗窗[51]。所以说,作为与靶标结合的至关重要的特异性区域,CARs配体结合域的构建尤为重要。其构建的关键在于如何能只特异性地与靶向细胞结合而不影响其他组织器官。目前大多数已确定的肿瘤特异性抗原是那些在早期胚胎发育期正常表达,而在恶性肿瘤中被异常表达的自身抗原,例如NY-ESO1和MAGE家族抗原。
近期发表在《Cell》的一项研究中,提出提高CAR-T细胞靶向特异性和准确性的一种有效方法是改造它们,使其识别组合抗原,而Kole等利用基因工程技术改造了一种需要组合激活的T细胞回路(T cell circuit)。在这一回路中,改造后的T细胞需要识别2个抗原,一种合成Notch受体能识别其中一个抗原,被激活后能够诱导对应第二个抗原的CAR表达,只有在肿瘤细胞同时表达2种抗原的情况下,改造后的T细胞才会被激活,研究者将这种T细胞命名为dual-receptor AND-gate T cells。体内实验中,这些T细胞展现出精准的识别与治疗,能够区分出只拥有单个抗原的非目标肿瘤,且有效清除携带组合抗原的肿瘤[52]。
不同的临床情况需要不同的scFv、铰链、跨膜区、刺激和共刺激域。事实上,迄今仍没有一个公认最佳的方式来构建CARs。关于CARs的最佳设计仍然需要更多的调查和对不同恶性肿瘤的临床评估。我们也许可以运用一些简单的克隆技术替换或改进其不同组件,以便于评估和完善CARs模块化设计。虽然CARs最优设计仍未得到根本解决,但可喜的是,关于CARs设计的新思路却层出不穷,以其为基础的新型靶向免疫治疗技术日新月异,如T细胞受体工程T细胞(T cell receptor-engineered T cells,TCR-T)、双特异性T细胞衔接器(bispecific T-cell engagers,BiTE)和嵌合抗原受体NK细胞(chimeric antigen recep⁃tor NK cells,CAR-NK)等。这意味着CARs领域的发展将比经典的新型分子药物更为迅捷,是目前肿瘤免疫治疗中炙手可热的新贵。
4 结语
癌症免疫疗法是继细胞毒药物化疗和靶向药物治疗之后新兴的癌症治疗策略。作为免疫疗法的重要代表,嵌合抗原受体T细胞免疫疗法在临床白血病的治疗中实现了治愈[34]。目前,该治疗策略还存在一些问题,包括CAR-T细胞识别癌细胞时可能发生脱靶效应,以及病人在CAR-T治疗后会面临“细胞因子风暴(细胞因子释放综合征)”的风险。解决这些问题可能要依赖于基因工程手段,或配合使用其他类型的治疗药物。这些手段将有助于增加CAR-T疗法的安全性、有效性,以及对更多种类癌症治疗的适用性,从而挽救更多患者的生命。
[1]Gross G,Waks T,Eshhar Z.Expression of immuno⁃globulin-T-cell receptor chimeric molecules as func⁃tional receptors with antibody-type specificity[J].Proc Natl Acad Sci USA,1989,86(24):10024-10028.
[2]Goverman J,Gomez S M,Segesman K D,et al.Chi⁃meric immunoglobulin-T cell receptor proteins form functional receptors:implications for T cell receptor complex formation and activation[J].Cell,1990,60(6): 929-939.
[3]Romeo C,Seed B.Cellular immunity to HIV activated by CD4 fused to T cell or Fc receptor polypeptides [J].Cell,1991,64(5):1037-1046.
[4]Irving B A,Weiss A.The cytoplasmic domain of the T cell receptor 6 chain is sufficient to couple to sig⁃nal transduction pathways[J].Cell,1991,64(5):891-901. [5]Cheadle E J,Gornall H,Baldan V,et al.CAR-T cells:driving the road from the laboratory to the clinic [J].Immunol Rev,2014,257(1):91-106.
[6]Jensen M C,Popplewell L,Cooper L J,et al.Anti⁃transgene rejection responses contribute to attenuated persistence of adoptively transferred CD20/CD19-specif⁃ic chimeric antigen receptor redirected T cells in hu⁃mans[J].Biol Blood Marrow Transplant,2010,16(9): 1245-1256.
[7]Pule M A,Savoldo B,Myers G D,et al.Virus-specif⁃ic T cells engineered to coexpress tumor-specific re⁃ceptors:persistence and antitumor activity in individu⁃als with neuroblastoma[J].Nat Med,2008,14(11):1264-12670.
[8]Brentjens R J,Latouche J B,Santos E,et al.Eradica⁃tion of systemic B-cell tumors by genetically targeted human T lymphocytes co-stimulated by CD80 and in⁃terleukin-15[J].Nat Med,2003,9(3):279-286.
[9]Maher J,Brentjens R J,Gunset G,et al.Human T-lymphocyte cytotoxicity and proliferation directed by a single chimeric TCRzeta/CD28 receptor[J].Nat Biotech⁃nol,2002,20(1):70-75.
[10]Zhao Y,Wang Q J,Yang S,et al.A herceptin-based chimeric antigen receptor with modified signaling do⁃mains leads to enhanced survival of transduced T lym⁃phocytes and antitumor activity[J].Immunology,2009, 183(9):5563-5574.
[11]Carpenito C,Milone M C,Hassan R,et al.Control of large,established tumor xenografts with genetically re⁃targeted human T cells containing CD28 and CD137 domains[J].Proc Natl Acad Sci USA,2009,106(9): 3360-3365.
[12]Pegram H J,Lee J C,Hayman E G,et al.Tumor-tar⁃geted T cells modified to secrete IL-12 eradicate sys⁃temic tumors without need for prior conditioning[J]. Blood,2012,119(18):4133-4141.
[13]Lamers C H J,Sleijfer S,Vulto A G,et al.Treat⁃ment of metastatic renal cell carcinoma with autolo⁃gous T-lymphocytes genetically retargeted against car⁃bonic anhydrase IX:first clinical experience[J].J Cli⁃ni Oncol,2006,24(13):20-22.
[14]Kershaw M H,Westwood J A,Parker L L,et al.A phase I study on adoptive immunotherapy using genemodified T cells for ovarian cancer[J].Clin Cancer Res,2006,12(20 Pt1):6106-6115.
[15]Porter D L,Levine B L,Kalos M,et al.Chimeric an⁃tigen receptor-modified T cells in chronic lymphoid leukemia[J].N Engl J Med,2011,365(8):725-733.
[16]Monjezi R,Miskey C,Gogishvili T,et al.Enhanced CAR T-cell engineering using non-viral Sleeping Beauty transposition from minicircle vectors[J].Leuke⁃mia,2016,doi:10.1038/leu.2016.180.
[17]Till B G,Jensen M C,Wang J,et al.Adoptive immu⁃notherapy forindolent non-Hodgkin lymphoma and man⁃tlecell lymphoma using genetically modifiedautologous CD20-specific T cells[J].Blood,2008,112(6):2261-2271.
[18]Long A H,Highfill S L,Cui Y,et al.Reduction of MDSCs with all-trans retinoic acid improves CAR therapy efficacy for sarcomas[J].Cancer Immunol Res, 2016,4(10):869-880.
[19]Turtle C J,Hanafi L A,Berger C,et al.Immunothera⁃py of non-Hodgkin's lymphoma with a defined ratio of CD8+and CD4+CD19-specific chimeric antigen receptor-modified T cells[J].Sci Transl Med,2016,8 (355):355ra116.
[20]Lamers C H,Sleijfer S,van Steenbergen S,et al. Treatment of metastatic renal cell CARscinoma with CAIX CARS-engineered T-cells:clinical evaluation and management of on-target toxicity[J].Mol Ther, 2013,21(4):904-912.
[21]Morgan R A,Yang J C,Kitano M,et al.Case report of a serious adverseevent following the administration of T-cells transduced with a chimeric antigen recep⁃tor recognizing ERBB2[J].Mol Ther,2010,18(4):843-851.
[22]Marcela V.Designing CAR T cells for glioblastoma[J]. Oncoimmunology,2015,4(12):e1048956.
[23]Philip B,Kokalaki E,Mekkaoui L,et al.A highly compact epitope-based marker/suicide gene for easier and safer T-cell therapy[J].Blood,2014,124(8):1277-1287.
[24]Lee D W,Gardner R,Porter D L,et al.Current con⁃cepts in the diagnosis and management of cytokine re⁃lease syndrome[J].Blood,2014,124(2):188-195.
[25]Davila M L,Riviere I,Wang X,et al.Efficacy and toxicity management of 19-28z CARS T-cell therapy in B cell acute lymphoblastic leukemia[J].Sci Transl Med,2014,6(224):268-276.
[26]Kochenderfer J N,W ilson W H,Janik J E,et al. Eradication of B-lineage cells and regression of lym⁃phoma in a patient treated with autologous T cells ge⁃netically engineered to recognize CD19[J].Blood,2010, 116(20):4099-4102.
[27]Porter D L,Levine B L,Kalos M,et al.Chimeric an⁃tigen receptor-modified T cells in chronic lymphoid leukemia[J].N Engl J Med,2011,365(8):725-733.
[28]Long A H,Haso W M,Shern J F,et al.4-1BB co⁃stimulation ameliorates T cell exhaustion induced by tonic signaling of chimeric antigen receptors[J].Nat Med,2015,21(6):581-590.
[29]Li W,Guo L,Rathi P,et al.Redirecting T cells to glypican-3 with 4-1BB zeta chimeric antigen recep⁃tors results in Th1 polarization and potent antitumor activity[J].Hum Gene Ther,2016,doi:10.1089/hum. 2016.025.
[30]Savoldo B,Ramos C A,Liu E,et al.CD28 costimula⁃tion improves expansion and persistence of chimeric antigen receptor-modified T cells in lymphoma patients [J].J Clin Invest,2011,121(5):1822-1826.
[31]Brentjens R J,Davila M L,Riviere I, et al.CD19-targeted T cells rapidly induce molecular remissions in adults with chemotherapy-refractory acute lympho⁃blastic leukem ia[J].Sci Transl Med,2013,5(177):638-643.
[32]Chen R,Song X T,Chen B.CD19 chimeric antigen receptor T cell therapy for the treatment of B cell lin⁃eage acute lymphoblastic leukemia.[J].Discovery Med, 2015,20(110):185-190.
[33]Chen F,Fan C M,Gu X Z,et al.Construction of an⁃ti-CD20 single-chain antibody-CD28-CD137-TCRzeta recombinant genetic modified T cells and its treat⁃ment effect on B cell lymphoma[J].Med Sci Monit, 2015,21:2110-2115.
[34]Maude S L,Frey N,Shaw P A,et al.Chimeric anti⁃gen receptor T cells for sustained remissions in leuke⁃mia[J].N Engl J Med,2014,371(16):1507-1517.
[35]Lee D W,Kochenderfer J N,Stetler-Stevenson M,et al.T cells expressing CD19 chimeric antigen recep⁃tors for acute lymphoblastic leukaemia in children and young adults:a Phase 1 dose-escalation trial[J]. Lancet,2015,385(9967):517-528.
[36]Milone M C,Fish J D,Carpenito C,et al.Chimeric receptors containing CD137 signal transduction do⁃ mains mediate enhanced survival of T cells and in⁃creased antileukemic efficacy in vivo[J].Mol Ther, 2009,17(8):1453-1464.
[37]Sanchez-Paulete A R,Labiano S,Rodriguez-Ruiz M E,et al.Deciphering cd137(4-1BB)signaling in T-cell costimulation for translation into successful can⁃cer immunotherapy[J].Eur J Immunol,2016,46(3):513-522.
[38]Hombach A A,Heiders J,Foppe M,et al.OX40 co⁃stimulation by a chimeric antigen receptor abrogates CD28 and IL-2 induced IL-10 secretion by redirect⁃ed CD4+T cells[J].Oncoimmunology,2012,1(4):458-466.
[39]Altvater B,Landmeier S,Pscherer S,et al.2B4 (CD244)signaling via chimeric receptors costimulates tumor-antigen specific proliferation and in vitro expan⁃sion of human T cells[J].Cancer Immunol Immunoth⁃er,2009,58(12):1991-2001.
[40]Song D G,Ye Q,Poussin M,et al.CD27 costimula⁃tion augments the survival and antitumor activity of re⁃directed human T cells in vivo[J].Blood,2012,119(3): 696-706.
[41]Guedan S,Chen X,Madar A,et al.ICOS-based chi⁃meric antigen receptors program bipolar TH17/TH1 cells[J].Blood,2014,124(7):1070-1080.
[42]Mittal P,St Rose M C,Wang X,et al.Tumor-unrelat⁃ed CD4 T cell help augments CD134 plus CD137 du⁃al costimulation tumor therapy[J].J Immunol,2015,195 (12):5816-5826.
[43]Loskog A,Giandomenico V,Rossig C,et al.Addition of the CD28 signaling domain to chimeric T-cell re⁃ceptors enhances chimeric T-cell resistance to T regu⁃latory cells[J].Leukemia,2006,20(10):1819-1828.
[44]Paulos C M,Carpenito C,Plesa G,et al.The induc⁃ible costimulatory(ICOS)is critical for the develop⁃ment of human T(H)17 cells[J].Sci Transl Med,2010, 2(55):7444-7451.
[45]Savoldo B,Ramos C A,Liu E,et al.Brief report CD28 costimulation improves expansion and persis⁃tence of chimeric antigen receptor-modified T cells in lymphoma patients[J].J Clin Invest,2011,121(5):1822-1826.
[46]Zhong X-S,Matsushita M,Plotkin J et al.Chimeric antigen receptors combining 4-1BB and CD28 signal⁃ing domains augment PI3kinase/AKT/Bcl-XL activa⁃tion and CD8&plus,T cell-mediated tumor eradica⁃tion[J].Mol Ther,2010,18(2):413-420.
[47]James S E,Greenberg P D,Jensen M C,et al.Anti⁃gen sensitivity of CD22-specific chimeric TCR is mod⁃ulated by target epitope distance from the cell mem⁃brane[J].J Immunol,2008,180(10):7028-7038.
[48]Guest R D,Hawkins R E,Kirillova N,et al.The role of extracellular spacer regions in the optimal de⁃sign of chimeric immune receptors:evaluation of four different scFvs and antigens[J].J Immunother,2005,28 (3):203-211.
[49]Haso W,Lee D W,Shah N N,et al.Anti-CD22-chi⁃meric antigen receptors targeting B-cell precursor acute lymphoblastic leukemia[J].Blood,2013,121(7): 1165-1174.
[50]Watanabe K,Terakura S,Martens A C,et al.Target antigen density governs the efficacy of anti-CD20-CD28-CD3ζ chimeric antigen receptor-modified effec⁃tor CD8+T-cells[J].J Immunol,2015,194(3):911-920.
[51]Song D G,Ye Q,Poussin M,et al.A fully human chimeric antigen receptor with potent activity against cancer cells but reduced risk for offtumor toxicity[J]. Oncotarget,2015,6(25):21533-21546.
[52]Roybal K T,Rupp L J,Morsut L,et al.Precision tu⁃mor recognition by T cells with combinatorial antigensensing circuits[J].Cell,2016,164(4):770-779.
Progress of Engineering Chimeric Antigen Receptor in Tu⁃mor Therapy
QIAN Yu-Zhen1,2,ZHANG Ming-Rui1,2,REN Gang3,ZOU Wei1,2*
1.College of Life Science,Liaoning Normal University,Dalian 116081;2.Liaoning Key Laboratories of Biotechnol⁃ogy and Molecular Drug Research and Development,Dalian 116081;3.Institute of Medicinal Biotechnology,Chi⁃nese Academy of Medical Sciences,Beijing 100050;China
How to treat cancer has always been one of the biggest problems that afflict humanity for years be⁃cause conventional treatment has its limitations.As the development of gene transfer and cell culture technology, cellular immunotherapy gradually come to public attention.Chimeric antigen receptor T-cell(CAR-T)immunothera⁃py is a new adoptive tumor immunotherapy approach that can target antigen specificity recognition and kill tumor cells.Therefore,this review summarizes the application of CAR-T in oncotherapy and the strategy of building CAR-T cells.
chimeric antigen receptors;T lymphocyte;oncotherapy
R392.1
A
1009-0002(2017)02-0188-08
10.3969/j.issn.1009-0002.2017.02.025
2016-09-19
钱昱臻(1990-),男,硕士研究生
邹伟,(E-mail)weizou60@126.com
*Corresponding anthor,E-mail:weizou60@126.com
