胆维丁原料中共晶与游离态维生素D3和胆固醇含量的定量分析
2017-04-14戴健姜玲孙宁云
戴健+姜玲+孙宁云
摘 要 通过差示扫描量热分析 (DSC)、拉曼光谱及粉末X射线衍射(PXRD)发现胆维丁原料中存在共晶现象,并对其进行表征。采用粉末X-射线衍射(PXRD)建立了共晶与游离态维生素D3和胆固醇含量的定量分析方法。
关键词 胆维丁 拉曼光谱 粉末X射线衍射法
中图分类号:R917; R977.24 文献标识码:A 文章编号:1006-1533(2017)05-0071-04
Quantitative analysis of the content of the eutectic and free vitamin D3 and cholesterol in cholecalciferol cholesterol compound by powder X-ray diffraction method
DAI Jian*, JIANG Ling, SUN Ningyun
(Institute of Medicine, Shanghai Xinyi Pharmaceutical Co. Ltd., Shanghai 201206, China)
ABSTRACT Eutectic structure existed in cholecalciferol cholesterol compound was found by Raman spectroscopy, differential scanning calorimetry (DSC) and powder X-ray diffraction (PXRD) and characterized. A quantitative analysis method for the determination of content of eutectic and free vitamin D3 and cholesterol in cholecalciferol cholesterol compound was established by powder X-ray diffraction.
KEY WORDS cholecalciferol cholesterol compound; Raman spectroscopy; powder X-ray diffraction
藥物共晶是指在常温下共晶形成物与药物活性成分通过氢键等非共价键的形式结合形成的晶体[1]。药物共晶是一种新的药物固体形态,共晶具有改良药物原有理化特性的优势,且新的药物共晶可获得知识产权保护,因此可延长原有药物的上市周期,具有广阔的研发及应用前景,近年来开始获得广泛关注[2-3] 。
胆维丁片或乳剂是维生素D3与胆固醇的等摩尔分子加成物,其作用与肌肉注射维生素D的效果相当,具有促进钙、磷吸收和利用,促进骨正常钙化的作用,是预防和治疗佝偻病的安全有效的临床常用药物[4-10]。胆维丁原料为晶体,仅有少数文献报道其由维生素D3与胆固醇通过氢键结合形成等摩尔分子加成物[11],但并未对其结构进行深入研究,目前尚未见胆维丁和胆固醇、维生素D3的混合物进行区分的报道,也没有对游离的胆固醇和维生素D3建立分析方法。本文根据文献提供的共晶表征方法[12-15],对胆维丁原料晶体进行了研究。通过差示扫描量热分析 (DSC)、拉曼光谱及粉末X-射线衍射(PXRD)发现该晶体中存在共晶现象,并对其进行表征。采用PXRD建立了共晶与游离态维生素D3和胆固醇含量的定量分析方法。对提高此类难溶性药物共晶形成工艺条件及质量控制方法的研究具有重要的参考价值。
1 材料和方法
1.1 仪器与试药
i-Raman Plus型高性能拉曼光谱仪(必达泰克公司);DSC 204F1型差示热量仪(德国Netzsch公司);D8 Advance X-射线衍射仪(德国Bruker AXS 仪器有限公司)。胆维丁对照品购自中国药品生物制品检定所,胆维丁样品为本公司自制,胆固醇样品购自南京新百药业有限公司,维生素D3购自四川玉鑫药业有限公司。
1.2 方法
1.2.1 拉曼光谱的测定
测定条件:激光源780 nm,激光功率 100 mW,曝光时间 15 s,曝光次数10次。分别精密称取胆维丁对照品、企业自制胆维丁、维生素D3和胆固醇各100 mg,在200~2 700 cm-1位移范围内分别进行扫描。
1.2.2 DSC的测定
分别精密称取样品各5 mg进行差示扫描量热分析。扫描温度范围 20~300 ℃,升温速率10 ℃/min 。
1.2.3 粉末X-射线衍射法测定胆维丁
取相同质量的胆固醇和维生素D3混合均匀,制成胆固醇-维生素D3=1∶1的混合物。按制剂混合规则,将胆维丁与混合物配制成胆维丁含量分别为1.6%、3.1%、6.2%、12.5%、25.0%、50.0%、75.0%、87.5%、93.8%、96.9%、98.4%的混合样品。样品研磨过100目筛,称取过筛后的样品50 mg进行粉末X射线衍射测定,读取2θ≈4.0°处的衍射峰峰高值,乘以仪器校正因子后代入线性回归方程:Y=20 435x-23.87,即x=(Y+23.87)/20 435,计算待测样品中胆维丁含量,每个待测样品平行测定2次,取平均值。
1.2.4 精密度和准确度试验
配制适量胆维丁含量为25%(低含量)、50%(中含量)、75%(高含量)的样品,从中各取6份样品进行XRPD测定。
1.2.5 稳定性试验
配制胆维丁含量为95%的样品1份,取50 mg,于室温放置0、3、6、12和24 h时进行XRPD实验。
1.2.6 回收率试验
平行配制胆维丁含量为20%、75%、90%的样品各5份,每份各取50 mg的样品进行测试。
2 结果
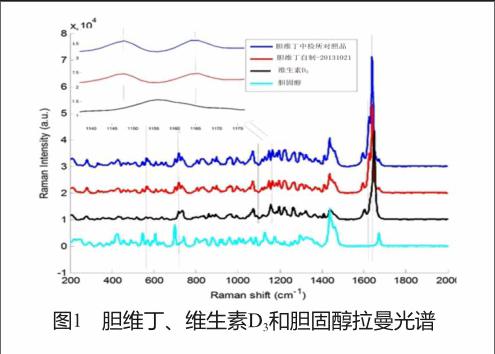
2.1 拉曼光谱区分胆维丁与维生素D3和胆固醇
拉曼光谱扫描结果表明,单独的维生素D3与胆固醇在1 130 cm-1与1 175 cm-1处衍射峰与共晶的胆维丁明显不同。胆维丁在1 640 cm-1处有特征衍射峰,可用来判断是否存在胆维丁(图1)。
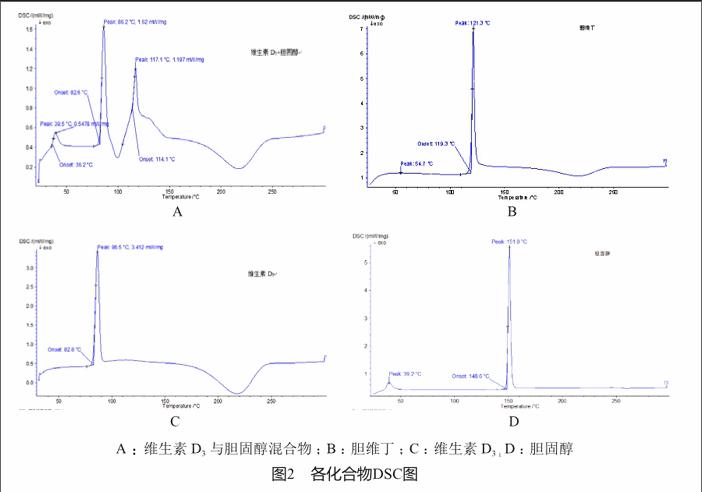
2.2 DSC可区分胆维丁与维生素D3和胆固醇
由DSC检测发现,维生素D3在86.5 ℃有明显吸收峰,胆固醇在151.0 ℃有明显吸收峰。维生素D3与胆固醇单纯的混合物为多处吸收峰,而共晶的胆维丁在121.3℃有单一吸收峰。可以认为胆维丁与维生素D3和胆固醇混合物的DSC明显不同(图2)。
2.3 XRPD测定条件
2.3.1 XRPD样品前处理的确定
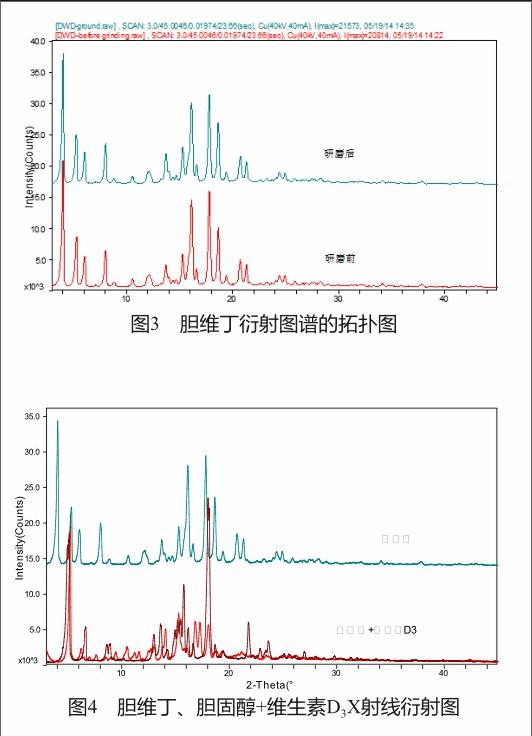
XRPD定量分析要求样品颗粒尽可能细小、均匀,从而尽可能避免由于择优取向的影响而产生的偏差,同时样品在研磨处理过程中也可能导致样品晶型发生改变,故需对样品研磨处理前后的衍射图谱进行考察。
胆维丁样品在研磨处理前后的衍射图谱的拓扑图形、衍射角位置均基本一致,晶型未发生改变(图3)。故可将上述胆维丁样品研磨过100目筛。
2.3.2 衍射峰的选择
将胆维丁、胆固醇、维生素D3的XRPD图谱放在一起进行比较(图4),结果发现,胆维丁的衍射峰中未与胆固醇、维生素D3的衍射峰发生重叠的衍射峰主要有2θ≈4.0°和2θ≈8.0°的二个衍射峰,且2θ≈4.0°的衍射峰为胆维丁的最强衍射峰,2θ≈8.0°的衍射峰为胆维丁的较强衍射峰,故初步选择2θ≈4.0°和2θ≈8.0°的衍射峰作为胆维丁的特征衍射峰,并对其进行含量分析。

2.3.3 XRPD分析测试参数的筛选
分别以胆维丁含量为横坐标(X),2θ≈4.0 °的衍射峰峰高度(Y)为纵坐标进行线性回归,得方程A:Y=20 435X-23.879;以胆维丁含量为横坐标(X),2θ≈4.0 °的衍射峰峰面积(Y)为纵坐标进行线性回归,得方程B:Y=225 838X-9 313;以胆维丁含量为横坐标(X),2θ≈8.0 °的衍射峰峰高度(Y)为纵坐标进行线性回归,得方程C:Y=6 100.2X-390.3;以胆维丁含量为横坐标(X),2θ≈8.0 °的衍射峰峰面积(Y)为纵坐标进行线性回归,得方程D:Y=78 982X-3 476.2。
经比较发现,方程A的线性相关系數为R2=0.997,为四个方程中最优,方程C的线性相关系数为R2=0.991为4个方程中最差。在精密度、准确度方面,方程A和方程C的RSD值最大值均小于4%,而方程B和D的RSD值最大值分别为4.23%和8.31%。稳定性方面,4个方程的RSD值均小于2%。综上所述,最终采用方程A对混合样品中胆维丁含量进行分析。
2.4 精密度和准确度测定
精密度和准确度测定结果表明,它们的RSD均小于4%(表1)。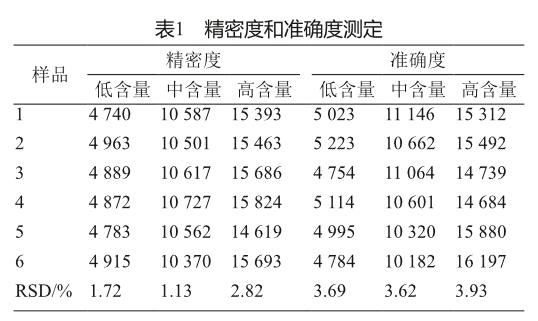
2.5 稳定性和回收率
含量为95%的胆维丁样品在室温放置0、3、6、12和24 h时测定的含量分别是95.13%、94.44%、94.64%、96.20%、94.60%,RSD=0.76%,小于2%,表明样品在室温放置24 h稳定。
3种含量的胆维丁样品各5份测定的回收率表明,同一含量的RSD值均小于5%(表2)。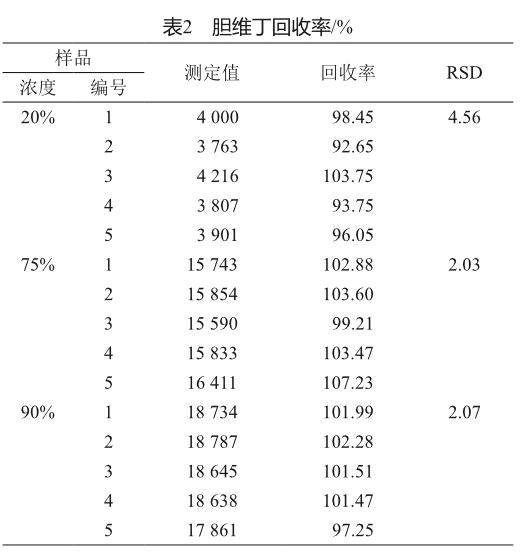
3 讨论
用PXRD建立的定量分析方法能准确测定出胆维丁中维生素D3和胆固醇通过氢键形式形成共晶的含量多少,有效区别了胆维丁中维生素D3和胆固醇的共晶态和物理混合态。而常规含量测定的液相色谱方法则无法识别出形成共晶的还是处于游离态的维生素D3和胆固醇,也就无法针对性的对共晶进行含量检测,从而不能区分固体制剂中原料药的晶型和成分。用PXRD建立的定量分析方法可确保证制剂质量的稳定性。
由于X-射线衍仪器精度不高,所以PXRD建立的定量分析方法测定的精确度较低,目前只能保证RSD不超过4%,这是本分析方法不足之处。PXRD建立的定量分析方法也可用于制剂研究,如有共晶现象的原料药在制剂工艺中的稳定性及制剂成品的质量控制和稳定性考察等。
参考文献
[1] 高缘, 祖卉, 张建军. 药物共晶研究进展[J]. 化学进展, 2010, 22(5): 829-836.
[2] 马坤. 药物共晶的筛选技术及热力学研究进展[J]. 药学进展, 2010, 34(12): 529-534.
[3] 闻聪, 金方. 药物共晶在药学中的应用[J]. 中国新药杂志, 2007, 16(15): 1167-1177.
[4] 斯琴, 陈月华.胆维丁乳液治疗小儿佝偻病的临床疗效观察[J]. 中外医疗, 2008, 27(21): 121.
[5] 王义成, 冯成亮, 杨素勤, 等. 药物共晶的最新研究进展[J]. 药学进展, 2013, 37(3): 120-121.
[6] 唐业忠. 胆维丁乳与维生素D丸治疗佝偻病活动期的疗效对比[J]. 上海医药, 1994, 15(5): 15-16.
[7] 秦平, 翟玉华, 生敏, 等. 英康利(胆维丁乳)治疗小儿佝偻病100例疗效观察[J]. 上海医药, 1994, 15(6): 17.
[8] 林秀芳, 汤通如. 胆维丁乳剂与维生素D3针剂治疗小儿佝偻病的比较[J]. 新药与临床, 1997, 16(2): 128.
[9] 张婕,杨威. 佝偻病儿口服胆维丁乳后骨源性碱性磷酸酶活性测定[J]. 河南预防医学杂志, 2002, 13(6): 378-379.
[10] 胡忠梅, 焦喜涛, 宫宏宇. 胆维丁乳治疗早期佝偻病的临床疗效观察[J]. 河南职工医学院学报, 2007, 19(3): 254-255.
[11] 何丹, 杨林. HPLC法测定胆维丁原料药的含量和有关物质[J]. 中国药房, 2012, 23(21): 1999-2002.
[12] 张晓明, 卢晓娥, 李静. 药物共晶制备及表征方法研究进展[J]. 广东化工, 2013, 40(7): 79-80.
[13] 王小兵, 黄世铭, 廖静怡, 等. 氯噻嗪药物共晶的制备、表征及量化计算[J]. 江西师范大学学报(自然科学版), 2015, 39(3): 240-245.
[14] 弋东旭, 洪鸣凰, 徐军, 等. 药物共晶研究进展及应用[J].中国抗生素杂志, 2011, 36(8): 561-565, 575.
[15] 毛会林. 药物共晶的制备与分析研究[D]. 天津: 天津大学, 2009.
