自制盐酸二甲双胍缓释片与原研药格华止XR的体外释放一致性研究
2017-04-14杨继荣朱颖
杨继荣+朱颖

摘 要 目的:比较自制盐酸二甲双胍缓释片与原研药格华止XR(Glucophage XR, 500 mg/片)的体外释放一致性。方法:使用羟丙甲纤维素和羧甲基纤维素钠为缓释材料,先将盐酸二甲双胍与羧甲基纤维素钠混匀,加入润湿剂80%乙醇溶液,制粒,过20目筛,干燥,整粒。再将干燥后的颗粒与羟丙甲纤维素等混匀,加入硬脂酸镁,压制成片。比较制得的盐酸二甲双胍亲水凝胶缓释骨架片与默克-雪兰诺公司生产的格华止XR的片剂性质,并分别采用使用pH介质的中国药典桨法和使用生物相关介质的美国药典往复筒法进行体外释放度的检测与比较。结果与结论:使用羟丙甲纤维素和羧甲基纤维素钠制备的盐酸二甲双胍缓释片与格华止XR的片剂物理性质和体外释放行为极其相似。
关键词 盐酸二甲双胍缓释片 羟丙甲纤维素 羧甲基纤维素钠 亲水凝胶缓释骨架片
中图分类号:R927.11 文献标识码:A 文章编号:1006-1533(2017)05-0007-04
Study on in vitro drug release consistency between homemade metformin hydrochloride extended release tablet and its reference listed drug Glucophage XR
YANG Jirong*, ZHU Ying
(Department of Technique, Shanghai Colorcon Co. Ltd., Shanghai 201108, China)
ABSTRACT Objective: To compare the in-vitro drug release consistency between homemade metformin hydrochloride extended release tablet and its reference listed drug Glucophage XR (500 mg). Methods: Metformin hydrochloride extended release tablets were manufactured by taking hydroxypropyl methylcellulose (HPMC, Methocel K100M) and sodium carboxymethyl cellulose (CMC-Na) as drug dissolution rate control polymers and 80% alcohol as a wet agent by granulation, screening and drying, then by blending the dried granule with HPMC and MCC-Na until uniform and finally by adding magnesium stearate and pressing tablets. The properties of tablets were compared between homemade metformin hydrochloride extended release tablet and Glucophage XR and the drug release profiles were also compared by paddle method in four different pH media and USP III method with bio-relative media. Results & Conclusion: The in vitro drug release behavior of homemade metformin hydrochloride extended release tablet is very close to that of Glucophage XR.
KEY WORDS metformin hydrochloride extended release tablet; hydroxypropyl methylcellulose; sodium carboxymethyl cellulose; hydrophilic matrix
盐酸二甲双胍是双胍类降血糖药物,是2型糖尿病的常用治疗药物,其缓释片的临床应用已趋普遍。盐酸二甲双胍在生物药剂学分类系统(biopharmaceutical classification system, BCS)中属Ⅲ类药物,在人体内呈高溶解性、低渗透性,具有被动扩散吸收和主动转运载体介导的肠吸收机制,主要在小肠中上部的十二指肠和空肠被吸收,跨膜速度随胃肠道pH增加而逐渐降低,平均绝对生物利用度约为55%。患者服用盐酸二甲双胍普通片后的血藥浓度波动大,而盐酸二甲双胍缓释片具有一定的胃滞留效应,可提高药物在胃内停留的时间、提高药物的生物利用度、降低血药浓度的波动幅度、降低药物的不良反应,并可减少用药次数、方便患者用药[1- 3]。
本实验的目的是比较自制的盐酸二甲双胍缓释片与默克-雪兰诺公司的原研药格华止XR(Glucophage XR, 500 mg/片)的体外释放度。根据国家食品药品监督管理总局2015年663号文附件《普通口服固体制剂溶出曲线测定与比较的指导原则》,于不同溶出检测条件下对上述两种片剂进行体外释放一致性评价,为自制盐酸二甲双胍缓释片的生物等效性临床评价提供参考依据。
1 仪器与试药
1.1 仪器
RCZ- 8M型溶出试验仪(天津天大天发科技有限公司);RZQ- 8C溶出度自动取样器(天津天大天发科技有限公司);Biodis溶出仪(美国VanKel公司);安捷伦1260 Infinity系列高效液相色谱仪(美国安捷伦公司);岛津UV- 1800紫外-可见分光光度仪(日本岛津公司);Sartorius BP- 121S分析天平(北京赛多利斯科学仪器公司);Rimek mini press-ⅡSF旋转式压片机(印度Rimek公司);Pharma Test硬度检测仪(德国Pharma Test公司);电子数显千分尺(0~25 mm。桂林广陆数字测控股份有限公司)。
1.2 试药
盐酸二甲双胍原料药(石家庄普力制药有限公司);格华止XR(美国默克-雪兰诺公司);羟丙甲纤维素(美多秀K100M。美国陶氏化学公司);羧甲基纤维素钠(Walocel CRT 10000PA。美国陶氏化学公司);微晶纤维素(PH101、PH102。美国FMC公司);硬脂酸镁(湖州展望药业股份有限公司);安素营养液(Ensure Plus。美国雅培公司);胆酸钠等(均为分析纯)。
2 方法
2.1 自制盐酸二甲双胍缓释片的制备
将盐酸二甲双胍原料药与羧甲基纤维素钠混匀,加入80%乙醇溶液制粒。使湿颗粒过20目筛,于60 ℃下干燥。干燥后的颗粒再过20目筛,整粒。将干燥后的颗粒与微晶纤维素和羟丙甲纤维素混匀,加入硬脂酸镁后再混匀,压片,即得自制盐酸二甲双胍缓释片[4]。
2.2 自制鹽酸二甲双胍缓释片与格华止XR片剂物理性质的比较
检测并记录两种片剂的长、宽、高以及片重、硬度。
2.3 药物片剂体外释放度的检测
2.3.1 中国药典桨法
按2015年版中国药典(二部)中的“溶出度与释放度检测法”第二法(桨法)操作,按国家食品药品监督管理总局2015年663号文附件《普通口服固体制剂溶出曲线测定与比较的指导原则》中的溶出介质配制组成分别配制pH为1. 2、4. 0、6. 8的溶出介质,采用紫外-可见分光光度法,以盐酸二甲双胍原料药为对照,于波长233 nm和转速50、75、100 r/ min条件下分别检测两种片剂在1 000 ml上述3种溶出介质和水中的药物累积释放度[5- 6]。
2.3.2 美国药典往复筒法
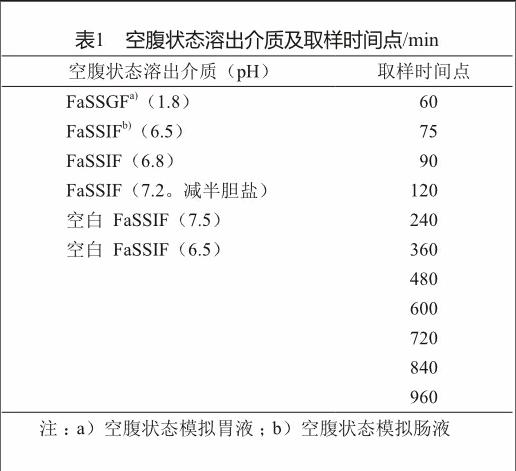
按美国药典收载的USP Ⅲ法(往复筒法)操作,以生物相关介质模拟空腹和饱腹状态的胃肠液,每个溶出介质的体积为220 ml,片剂浸入频率为10次/min。取样完成后,采用高效液相色谱法于波长233 nm处对样品进行检测[7],完成后计算药物累积释放度。生物相关介质及取样时间点见表1、2。
3 结果
3.1 片剂物理性质比较结果
检测自制盐酸二甲双胍缓释片与格华止XR的片剂性质,结果见表3。从表3可以看出,两种片剂的物理性质非常相似。
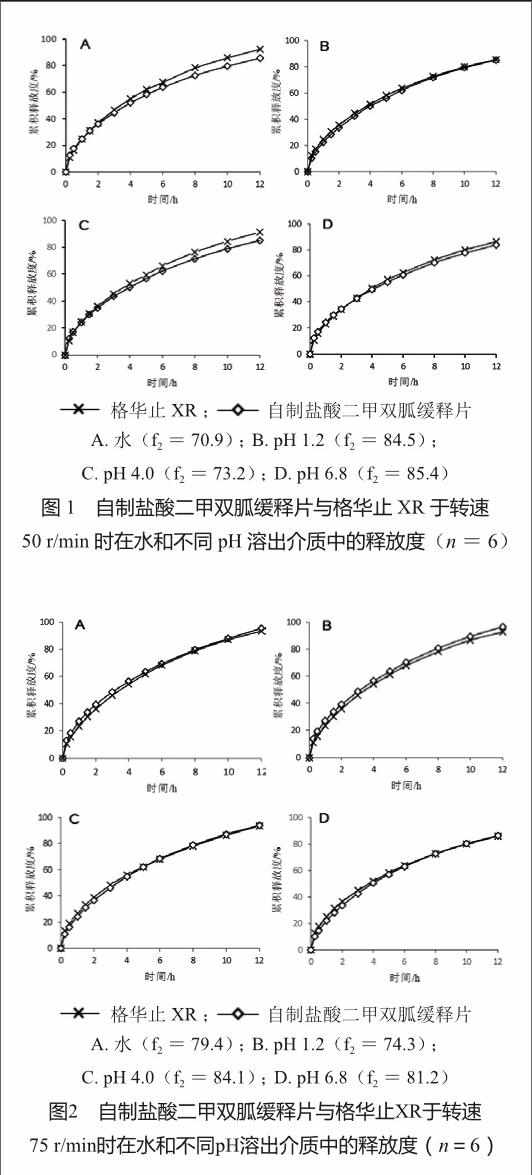
3.2 桨法所测释放度比较结果
采用桨法于不同转速条件下检测自制盐酸二甲双胍缓释片与格华止XR在水和3种不同pH溶出介质中的释放度,结果见图1~3。从图1~3可以看出,两种片剂在不同检测条件下的释放行为非常相似(相似因子f2>70)。
3.3 往复筒法所测释放度比较结果
采用往复筒法检测自制盐酸二甲双胍缓释片与格华止XR在生物相关介质模拟的空腹和饱腹状态胃肠液中的药物累积释放度,结果见图4。从图4可以看出,两种片剂在模拟空腹和饱腹状态胃肠液中的释放行为极其相似(相似因子f2>90)。自制盐酸二甲双胍缓释片与格华止XR在溶出检测完成后的片剂外观也非常相似。
4 讨论
仿制药的质量一致性评价是目前许多药品生产企业非常关注的内容。盐酸二甲双胍在BCS中属Ⅲ类即高溶解性、低渗透性药物。目前市场上的国产盐酸二甲双胍缓释片在片剂的重量、大小、性质以及药物释放行为方面均与原研药存在一定程度的差异[5],这会影响国产药的生物等效性[8]。
本实验结果表明,我们的自制盐酸二甲双胍缓释片与原研药格华止XR的片剂物理性质非常相似,在水和3种不同pH溶出介质以及3种不同转速条件下的药物释放曲线均非常相似(相似因子f2>70),使用生物相关介质和往复筒法检测的药物释放曲线也极其相似(相似因子f2>90),且溶出检测完成后的片剂外观亦非常相似。这些数据表明,我们的自制盐酸二甲双胍缓释片配方的生物不等效性风险较低,为随后开展生物等效性试验提供了充分的依据。
致谢:感谢卡乐康公司美国总部的同事Manish、Sandra和Maureen在应用美国药典往复筒法检测方面给予的帮助。
参考文献
[1] 李娟, 范铭, 庄伟. 盐酸二甲双胍口服肠吸收机制及凝胶骨架片的处方优化[J]. 药学与临床研究, 2009, 17(3): 215-220.
[2] 张永春, 左立, 马毅, 等. 盐酸二甲双胍缓释片的制备工艺及体外释放度研究[J]. 山东轻工业学院学报:自然科学版, 2006, 20(1): 20-24.
[3] Graham GG, Punt J, Arora M, et al. Clinical pharmacokinetics of metformin [J]. Clin Pharmacokinet, 2011, 50(2): 81-98.
[4] Peter T, Andrew BD, Kiren AV, et al. Method of use of a biphasic controlled release delivery system for high solubility pharmaceuticals and method: US, 6660300B1 [P/ OL]. [2016-11-13]. http:/ / www.freepatentsonline.com/ 6660300.html.
[5] 吴燕, 张春全, 徐荣. 不同厂家盐酸二甲双胍缓释片体外释放度考察[J]. 安徽医药, 2014, 18(6): 1050-1052.
[6] 梅勇, 李兴东. 国产盐酸二甲双胍缓释片与美国fortamet?缓释片体外释放度的对比研究[J]. 临床合理用药杂志, 2012, 5(15): 18-19.
[7] Klein S. The use of biorelevant dissolution media to forecast the in vivo performance of a drug [J]. AAPS J, 2010, 12(3): 397-406.
[8] 韩静, 张丹, 刘会臣. 仿制药的生物不等效风险与质量一致性评价[J]. 中国新药杂志, 2014, 23(24): 2897-2901.