惟变所出 万变不从
2017-04-14庄山任慧吴频庆
庄山+任慧+吴频庆
摘要:运用U型管、半封闭式U型管、具支U型管制作实验装置,并将装置应用于人教版义务教育教科书《化学》(九年级上、下册)燃烧条件、空气中氧气含量测定、活性炭吸附实验、Na2CO3或NaHCO3与盐酸反应等多个实验中,取得了很好的效果。
关键词:U型管;半封闭式U型管;具支U型管;创新实验
文章编号:1008-0546(2017)04-0090-03 中图分类号:G633.8 文献标识码:B
doi:10.3969/j.issn.1008-0546.2017.04.031
一、研究缘起
“Chemistry”拆分为“Chem is try”,强调研究化学是一个不断尝试、不断创新、不断实验的过程。我国化学家和教育家傅鹰先生也说过:“化学是实验的科学,只有实验才是最高法庭。”义务教育化学课程标准(2011版)明确指出:“应该根据学校的实际情况合理地选择实验形式,有条件的学校尽可能多地为学生提供动手做实验的机会;条件有限的学校,可采取教师演示实验、家庭小实验等”[1]。因此设计、改进、创新化学实验在化学教学中显得尤为重要。为此,我们利用化学实验室常见的仪器及药品制作了U型管、半封闭式U型管和具支U型管等实验装置,并将这些实验装置应用于人教版义务教育教科书《化学》(九年级上、下册)多个实验中。
二、半封闭式U型管的制作
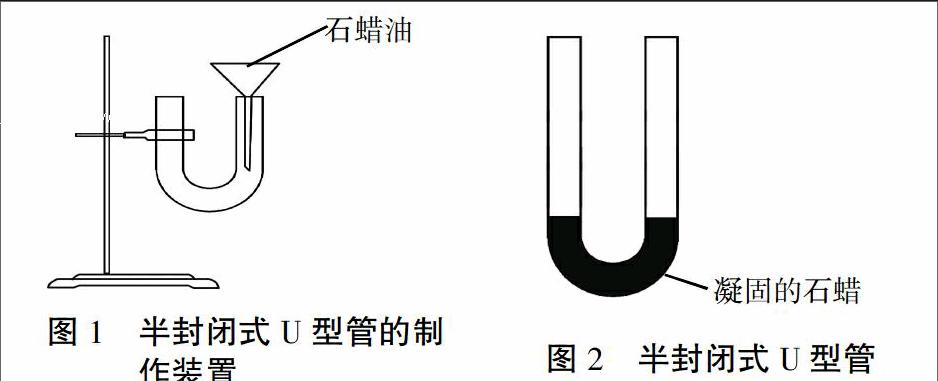
将石蜡放在烧杯中加热融化,将U型管管口朝上固定在铁架台上,在U型管的一端管口放上漏斗,将融化的石蜡倒入其中,如图1[2]。取走漏斗(注意:不要让石蜡遗留在U型管的管壁上)让其在空气中自然冷却凝固,制成半封闭U型管。实验如图2所示。它最大的优点就是在没有通风设备的条件下,可以形成密闭装置,并且能消除污染。
三、U型管、半封闭式U型管和具支U型管的创新应用
以人教版义务教科书《化学》(九年级上、下册)实验内容为例,介绍U型管、半封闭式U型管和具支U型管在实验中的创新应用。
1. 燃烧条件的实验
(1)教材上的实验内容
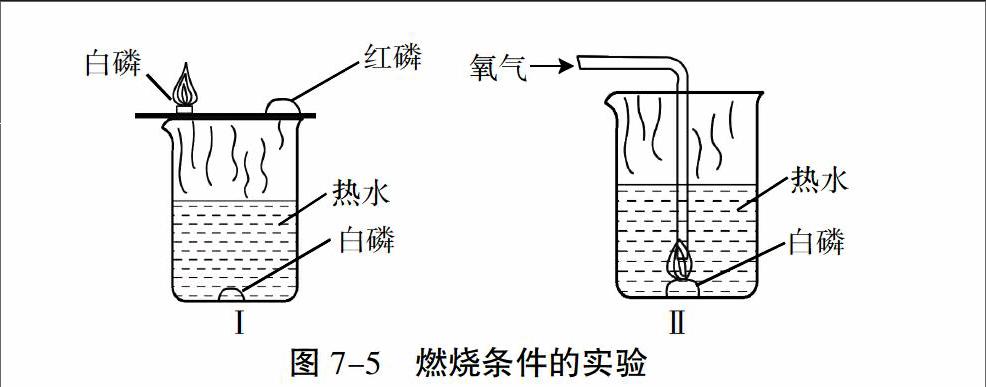
在500mL烧杯中加入300mL热水,并放入硬纸圈圈住的一小块白磷。在烧杯上盖一片薄铜片,铜片上一端放一小堆干燥的红磷,另一端放一小块已用滤纸吸去表面上水的白磷,观察现象。
用导管对准上述烧杯中的白磷,通入少量氧气(或空气)观察现象。
(2)教材中该实验的不足
“燃烧条件”实验装置是非密闭的,常会因为白磷和红磷是在开放体系中燃烧,产生的白烟(P2O5)会污染环境,因此教材特别注明了实验需在通风橱或抽风设备下进行。事实上很多化学教师通常都在普通教室里演示该实验,很多学校实验室中也没有通风橱或抽风设备。由于白磷或红磷燃烧产生的污染问题没能得到很好的处理,因而有不少化学教师对该实验往往采用“黑板上讲实验”或“多媒体播实验”的方式处理,因而也弱化了这一经典实验的教学功能。
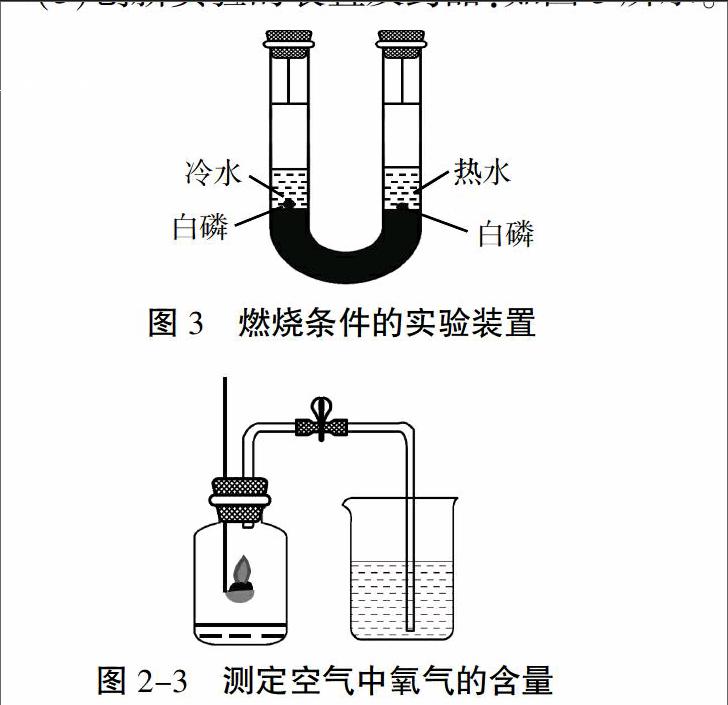
(3)创新实验的装置及药品:如图3所示。
(4)创新实验的操作及现象解释
①在半封闭式U型管的两端分别加入等体积的冷水和热水。
②在冷水和热水中分别加入两块大小相同的白磷,然后迅速塞上橡皮塞(橡皮塞上带有铜丝绕成隔板),观察U型管内两块白磷都不燃烧。说明燃烧的条件之一是可燃物与氧气或空气接触。
③将U型管倒置,观察到热水中的白磷燃烧而冷水中的白磷不燃烧,说明燃烧的条件之一是温度必须达到可燃物的着火点。
④实验完毕后,再将U型管倒置,振荡,迅速消除P2O5的污染。
(5)创新实验的优点
①使用的实验药品种类少(没有使用红磷)、操作简便。
②实验重复性好、实用性强,有利于推广和普及。
③在封闭体系中进行实验,药品使用量少,绿色、环保、无污染。
④作為教师演示实验效果良好,也比较适合在教师指导下的学生分组探究实验。
2. 空气中氧气含量的测定
(1)教材上的实验内容
在集气瓶内加入少量的水,并将水上方的空间分为5等份。用弹簧夹夹紧橡皮管。点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧,观察红磷燃烧的现象。待红磷熄灭并冷却后,打开弹簧夹,观察实验现象及水面的变化情况。
(2)教材中该实验的不足
①在塞橡皮塞之前,燃烧产生大量的白烟已弥散在空气中,危害师生健康。
②点燃红磷伸入到集气瓶的过程中,无论动作多么迅速,都不可避免地使集气瓶内的空气受热膨胀而外逸,最终导致测量结果偏大。
③实验结束后导管内留存的部分应倒吸入集气瓶中的水,导致测量结果偏小。若实验多次,就会出现测量结果时而偏大、时而偏小的情况,教师即使把失误的原因分析得头头是道,并从各个角度加以阐述和论证也难以让学生信服,更会影响教学任务的完成。
(3)创新实验的装置及药品:如图4所示。
(4)创新实验操作及现象解释
①在U型管的左侧放置一个铜丝绕成的隔板,隔板表面做成凹槽状。
②将U型管固定在铁架台上,从U型管的左侧管口加入少量热水到第一格刻度线处,将水面以上空间平均分成五等份(如图4所示),用镊子夹取一小块用滤纸吸干表面水的白磷放入隔板凹槽中。
③塞上橡胶塞观察实验现象,几秒钟后白磷燃烧产生大量白烟,左侧液面下降右侧液面上升,一段时间后白磷熄灭。等冷却后,右侧液面下降左侧液面上升,最终上升到液面以上空间的五分之一处。说明空气中的氧气被消耗,消耗的氧气约占空气体积的1/5。
④实验完毕后,倾斜U型管,迅速消除P2O5的污染。
(5)创新实验的优点
①实验装置简单,操作简便,便于观察水位上升的现象。
②利用铜丝的导热性,使实验操作简单化,消除了点燃红磷后能否快速伸入的影响。
③在封闭体系中进行实验,药品使用量少,无污染,并且实验结果一致性高。
④作为教师演示实验效果良好,也可安全地进行学生分组实验,并且有利于实验推广和普及。
3. 活性炭的吸附实验
(1)教材上的实验内容
①第四单元水的净化中,虽然没有具体要求进行活性炭吸附,但是大部分老师为了完整的进行水的净化实验,都进行活性炭的吸附实验。
②向盛有半瓶水的小锥形瓶里,加入一滴红墨水,使水略显红色。投入几块烘烤过的木炭(或活性炭),轻轻振荡锥形瓶,观察现象。
(2)教材中此类实验的不足
在第四单元课题2讲到利用活性炭除去水中有色有味杂质时,缺乏实验支持学生不易理解。在第六单元第1课时介绍木炭及活性炭具有吸附性实验时安排了演示实验,但由于实验是将木炭或活性炭投入一瓶有红色水的锥形瓶里,炭的黑色干扰了现象的观察,学生对活性炭的吸附色素和气味的性质仍有疑问,如果再加入过滤实验则耗时过长影响课堂效率。
(3)创新实验装置及药品:如图5所示。
(4)创新实验操作及现象解释
①在U型管中装入1/3体积的活性炭,两端用棉花堵住,用玻璃棒压实。
②将该装置固定在铁架台上,从U型管的一侧倒入10mL果粒橙(倒入之前上下振荡)。
③约1分钟后观察到从U型管的另一侧流出澄清透明的溶液,对比两边溶液发现不仅除去了果粒橙的颜色而且除去了气味。
④取下U型管,将无色溶液倒出发现U型管的另一侧留有果粒,说明活性炭层不仅能够吸附可溶性的色素和气味还能过滤不溶性杂质果粒。
(5)创新实验的优点
①实验装置取材容易、制作简单、操作简便,便于吸附前后的实验对比。
②将生活中的果粒橙变成清澈的液体实验现象非常明显,时间短。
③结合生活中的实验,教学效果非常好,还可以进行学生的分组实验。
4. 碳酸钠、碳酸氢钠与盐酸反应的实验
(1)教材上的实验内容及问题
向盛有0.5g碳酸钠的试管里加入2mL盐酸,迅速用带导管的橡胶塞塞紧试管口,并将导管一端通入盛有澄清石灰水的试管中,观察现象。
用碳酸氢钠代替碳酸钠进行上述实验,并分析现象。
(2)教材中该实验的不足
①课本设计的实验只能探究两者是否都能与盐酸反应产生二氧化碳,对于两者现象差异学生无法直观感受,所以记录实验现象时,都是以教师告知为主。
②最重要的是:该实验无法解决等质量碳酸钠、碳酸氢钠粉末与盐酸反应的快慢、生成二氧化碳多少的问题。也不能很好地与高中知识进行衔接。
因此,为了很好地进行初高中衔接也为学生更好地理解碳酸钠、碳酸氢钠的化学性质提供直观的实验平台,为此我们进行了如下的创新设计。
(3)创新实验装置及药品:如图6所示
(4)创新实验操作及现象解释
①在半封闭式具支U型管的两侧分别加入同浓度的3mL盐酸。
②将两个各装0.3gNa2CO3或NaHCO3粉末的小气球分别套在U型管的管口(U型管管口事前粘涂雙面胶防止气压变大气球弹出)。
③将气球内的Na2CO3或NaHCO3粉末同时倒入U型管中,观察到NaHCO3粉末这边反应更快,气球最先鼓起。
④反应结束后往外拉动注射器,拔下注射器并安装金属针头将注射器内的气体注入盛有澄清石灰水的小试管中,观察到澄清石灰水变浑浊,证明有二氧化碳生成。
(5)创新实验的优点
①该实验很好地控制了变量,做到了等量、同时。
②该实验的实验现象明显,通过气球变化的不同很容易得到实验结论。
③该实验作为教师演示实验效果良好,也比较适合进行学生分组实验。
④两个实验,可以一人同时操作,对比性强,因此渗透了“比较学习法”。
四、结束语
宋朝吕本中在《官箴》中写道:“惟变所出,万变不从”。意思是惟有变化才能推陈出新,否则教条主义没有出路。而“惟变所出,万变不从。”还有另一层意思就是尽管形式上变化多端,其本质或目的应该保持不变。化学教学中课本实验的创新正应如此,我们可以利用创新实验使操作变得简单,现象变得更加明显,使实验更加安全、环保;不变的是目的:更好地激发学生学习化学的兴趣、培养学生的科学探究能力从而提升学生的化学学科素养。化学实验创新永无止境,我们在实验创新的路上不断前行。
参考文献
[1] 中华人民共和国教育部制定. 义务教育化学课程标准(2011版)[M].北京:北京师范大学出版社,2012
[2] 谢丹敏,汤中华.封闭式U型管在对比实验中的应用[J].化学教学,2016(4)
